腔镜治疗小儿肺隔离症65例
苏 芸 武玉睿
(首都儿科研究所附属儿童医院胸部及肿瘤外科,北京 100020)
小儿肺隔离症(pulmonary sequestration,PS)是一种先天性肺发育畸形,隔离的肺组织与气管、支气管树相通或不相通,由体循环异常动脉供血。隔离肺分为叶内型和叶外型。叶内型隔离肺的术前诊断比较容易,但手术方式选择多样。叶外型隔离肺种类多,术前诊断有时容易混淆。我科2017年1月~2019年12月诊断小儿肺隔离症65例,均采用腔镜治疗,61例为胸腔镜,4例为腹腔镜。现结合文献,对叶内型隔离肺的手术方式和叶外型隔离肺的术前诊断进行总结分析,帮助临床医师更好地进行诊断和手术治疗。
1 临床资料与方法
1.1 一般资料
本组65例,男40例,女25例。年龄21天~13岁半,中位年龄9个月,其中3个月内1例,4~6个月17例,7~12个月25例,1~2岁11例,2~5岁8例,>8岁3例。体重4.3~56 kg,中位数9.5 kg。左侧50例,右侧15例(其中1例为双侧,先处理右侧)。
59例(90.8%)产前超声异常,肺部或胸腔内占位56例,腹膜后占位3例,其中50例孕17~30周发现,平均孕24周,9例孕周不详;6例产前超声未发现。50例(76.9%)入院前无明显症状;15例有症状,包括10例肺炎,2例咳嗽发热,3例支气管炎。
65例术前均完善胸部及上腹部增强CT及大血管重建,CT诊断肺隔离症59例(90.8%)(图1),其中4例为腹腔内隔离肺(图2)。其余6例诊断,1例为膈下腹主动脉前见迂曲血管团,腹腔异常强化灶,1例纵隔神经源性肿瘤,1例肺不张,1例气管囊肿,1例先天性肺气道畸形,1例纵隔囊肿。

图1 增强CT提示右肺下叶叶内型隔离肺:A.右肺下叶增强病变;B.有主动脉分支供血,血管直径3.4 mm;C.主动脉血管重建,可见来源于主动脉的异常分支 图2 上腹增强CT提示左肾上腺区增强包块,诊断左侧腹膜后隔离肺 图3 术中见膈膨升合并叶外型隔离肺图4 术中见隔离肺的异常动脉
25例术前行胸部或腹部超声,考虑肺隔离症18例,肾上腺区囊实性包块1例,先天性肺气道畸形1例,5例未见明显异常。
2例术前行MRI检查。1例胸部MRI,左肺下叶后基底段脊柱旁可见混杂信号包块影,其内见血流信号,印象:结合CT检查,符合先天性肺隔离症。1例腹部MRI,左侧腰椎旁、脾、胃之间见包块影,类似椭圆形,等T1长T2信号,内见管状低信号影,印象:左侧腹膜后包块,性质待定(可能为隔离肺叶外型)。
14例(21.5%)合并先天畸形,包括左侧膈膨升3例(图3),先天性心脏病2例(卵圆孔未闭1例,动脉导管未闭1例),左侧纵隔囊肿1例,胃重复畸形1例,肠旋转不良1例,先天性漏斗胸1例,脑血管畸形1例,双侧肾囊肿1例,双侧先天性肺气道畸形1例,左颈总动脉起源于头臂干1例,左弓右降主动脉、左侧主支气管受压1例。
1.2 手术方法
1.2.1 胸腔镜手术 全麻,单腔气管插管,健侧单肺通气,健侧卧位,根据病变位置建立1个观察孔,2个操作孔。
叶内型隔离肺,术前仔细阅读胸部及上腹部增强CT,明确病变肺叶,本组均为下叶,找到异常体循环分支(图4),病变静脉回流血管。观察孔远离病变,取腋中线第6肋间为观察孔,腋后线第8肋间、肩胛线第7肋间为操作孔。①初期行隔离肺肺叶切除术,先找到异常动脉分支,夹闭后切断,逐一仔细分离病变肺叶的静脉及支气管,分别夹闭后切断,将病变肺叶完整切除。②后期行隔离肺肺段切除术,先找到异常动脉分支,夹闭后切断。病变肺叶可见缺血线,以电钩标记病变范围。逐一仔细分离病变肺段的静脉及段支气管,分别夹闭后切断,沿缺血线将病变肺段完整切除。
位于胸腔的叶外型隔离肺,取腋中线第5肋间为观察孔,腋后线第8肋间、肩胛线第7肋间为操作孔,行异常肺叶切除术。术中可见病变肺叶有独立的脏层胸膜,有体循环分支动脉供血。先将异常动脉结扎切断,再将异常肺叶切除。
2例混合型隔离肺,1例行隔离肺肺叶切除+异常隔离肺切除,1例行隔离肺肺段切除+异常肺叶切除术。
1例腹腔内隔离肺术前诊断合并左侧膈膨升,故在胸腔镜下打开膈肌,行肠粘连松解、隔离肺切除、膈肌修补、膈肌折叠术。
1.2.2 腹腔镜手术 5例腹腔内隔离肺,根据产前超声、术前增强CT及MRI、腹部超声,4例选择腹腔镜手术。全麻气管插管,双肺通气,平卧位,患侧垫高70°。脐部为观察孔,剑突下、左侧肋缘下分别为操作孔。4例均位于左侧腹膜后,左肾上腺区。充分游离脾脏及结肠脾曲,利用重力作用,将左侧肾上腺区充分暴露。1例有1支体循环分支供血,血供不丰富;3例有多支体循环分支供血,血供丰富。先将异常动脉夹闭切断,再仔细分离病变肺组织,将其完整切除。
2 结果
65例均顺利完成手术,术中诊断叶内型34例,叶外型29例,混合型2例。胸腔镜61例,其中1例术中见隔离肺位于膈肌内,中转开胸行隔离肺切除+膈肌修补术;4例腹腔镜手术。65例均无术中输血。术式和手术指标见表1。叶内型34例均位于下叶,左侧20例,右侧14例。叶外型29例中左侧28例,右侧1例。24例为胸腔内隔离肺,其中23例位于下肺韧带的后方,1例位于左侧膈肌内;5例为腹腔内隔离肺。2例混合型隔离肺,均为左侧,1例为左下肺叶、左后胸壁,1例为左下肺后基底段、左下肺韧带后方。
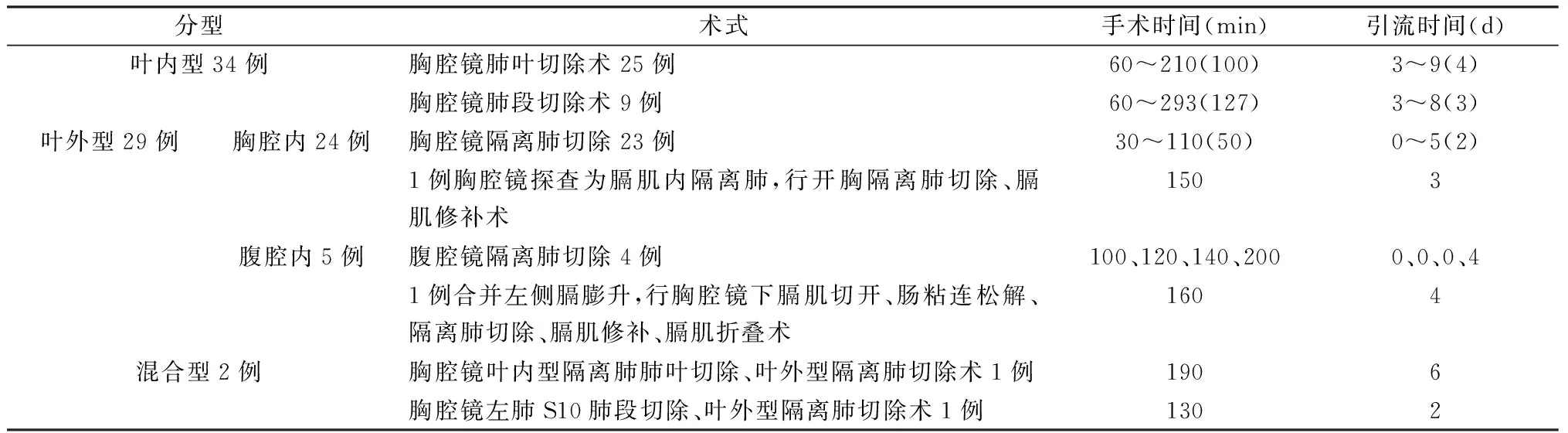
表1 65例肺隔离症的术式和手术指标
1例为双侧隔离肺,产前超声发现右肺占位,术前增强CT右侧为叶内型外基底段隔离肺,左侧叶外型隔离肺。第一次行胸腔镜右侧外基底段切除术,3个月后行胸腔镜左侧叶外型隔离肺切除术。
异常体循环血管1支49例,2支4例,3支2例,4支及以上10例。来源于降主动脉、胸主动脉、腹主动脉及分支、胸廓内动脉、胃左动脉、锁骨下动脉、胸壁动脉。
1例术后拔除气管插管后,持续鼻导管吸氧时经皮血氧饱和度维持在70%左右,转入ICU 1天,余64例病情平稳回病房。11例术后未放置引流管,54例放置引流管,其中53例为胸腔闭式引流管,放置1~9 d,平均4 d,1例为腹膜后引流管,放置4 d。术后气胸2例,纵隔积气2例,胸腔积液2例,均保守治疗治愈。住院时间6~25 d,平均11 d;术后住院时间2~19 d,平均6 d。病理诊断均为肺隔离症。
56例术后1、3个月复查胸片,均未见明显异常。52例术后6~12个月复查胸部CT,1例左肺下叶S9+10肺段切除术后可见左肺下叶基底段局部小囊腔,1例左肺下叶切除术后左肺容积小,肺血管纤细,其余50例未见异常。
3 讨论
小儿肺隔离症是一种罕见的先天性肺发育畸形,本组病例男女比1.6∶1,男性略多于女性,同文献报道[1,2]。隔离肺的确切病因及发病机制尚未明确,命名最终扩展为“肺隔离症及相关先天性支气管肺血管畸形”[3]。根据是否有独立的脏层胸膜,分为叶外型肺隔离症(extralobar sequestration,ELS)和叶内型肺隔离症(intralobar equestration,ILS),也有混合型。叶内型约60%以上位于左肺下叶的后基底段,约35%位于右肺下叶[4]。叶外型分为胸腔内、腹腔内两种,胸内型64%~77%位于左侧,与食管相邻,常位于膈肌与下叶之间,也可见于心包、纵隔及膈肌实质内[5]。胸腔内肺隔离症有一种特殊类型,病变完全位于膈肌内,左侧为主。膈肌内的隔离肺胸部及上腹部增强CT及三维重建可见实性或囊实性包块,新月形或椭圆形,膈肌包裹病灶,局部膨隆,可见体循环的供血动脉,病变无钙化[6]。腹腔内肺隔离症通常在腹膜后。
随着产前超声的普及,越来越多的肺隔离症在孕期发现[7]。孕期16周即可发现,超声可以探及胎儿胸腔内或腹腔内强回声或稍强回声包块,呈三角形或叶状,内部均匀,边界清,有体循环分支的动脉供血[8]。本组59例(90.8%)产前发现,其中50例孕17~30周发现,平均孕24周。术前完善胸部及上腹部增强CT及血管重建,可以看到胸腔或腹膜后包块,明显强化,无钙化,有来源于体循环的动脉供血。本组25例术前行胸部或腹部超声,20例有异常发现,探查到胸腔或腹膜后强回声包块,部分可以探及来源于体循环的动脉供血。因为肺部气体的影响,需要有一定经验的超声医师仔细探查才能发现,对腹腔内的肺隔离症,超声有一定帮助。
肺隔离症诊断明确后,均需要进一步治疗。目前的治疗方式以手术切除为主,也有采用介入栓塞治疗。手术时机选择在肺隔离症感染前[9]。如果合并感染,建议感染控制1~2个月后择期手术[10]。产前超声发现的无明显症状的肺隔离症可以选择在3~6月龄手术[11]。有人认为无症状的叶外型隔离肺可以观察[9]。我院均采用胸腔镜或腹腔镜手术,建议出生后6个月左右手术,但大多数家长倾向于1岁左右手术。根据产前超声和术前检查,确定病变位置,位于胸腔内的使用胸腔镜[12],位于腹腔内的使用腹腔镜。
胸腔镜探查叶内型肺隔离症均位于下叶,左侧居多,以后基底段为多。我院早期均行胸腔镜下肺叶切除,随着手术经验的积累和技术的提高,后期行胸腔镜下解剖性肺段切除术,以保留更多的肺组织。术前需充分阅片,确定病变范围,了解病变肺段异常血管供应,动脉、静脉、段支气管走行。术中一般先处理异常动脉,多位于增厚的下肺韧带附近,故处理下肺韧带时需仔细辨别异常动脉,大部分有1支,有时也会有多支[13]。我院采用胸腔镜下Hem-o-lok或可吸收夹夹闭血管远近端,中间以超声刀或剪刀横断,处理异常动脉时均无明显出血。叶内型肺隔离症处理完异常动脉后,再分别处理动脉、静脉及支气管[1]。
胸腔内叶外型肺隔离症大部分位于下肺韧带近膈面附近,也有小的病灶位于壁层胸膜,有时探查可以发现多个病灶。胸腔内叶外型肺隔离症手术完成前,充分膨肺排气后,可以不放置胸腔闭式引流管[7]。叶内型肺隔离症放置胸腔闭式引流管,引流液<50 ml/d夹闭6 h后复查胸片,无明显气胸、积液后拔除。叶内型肺隔离症也可以合并叶外型,故术中需要仔细探查,避免遗漏术前检查未发现的微小病灶。本组1例为双侧肺隔离症,我院的处理方式是:先做右侧(叶内型外基底段隔离肺),行胸腔镜下外基底段隔离肺切除术,术后3个月后,患儿恢复良好,再做左侧(叶外型胸腔内),行胸腔镜下叶外型隔离肺切除术,术后病理证实均为肺隔离症。
膈肌内的肺隔离症术前需要仔细阅片,定位病变位置是关键[14]。必要时需要完善胸部MRI,区分膈肌内病变[8]。如术前不能定位,只能判断病变在胸腔,需胸腔镜下仔细探查。本组1例膈肌内隔离肺,术前定位是胸腔,在胸腔镜下仔细探查,均未发现病灶,膈肌表面局部稍隆起,决定打开隆起的膈肌探查。中转开胸,打开后外侧膈肌,可见与膈肌粘连明显的包块,有来源于膈下的异常动脉供血,将异常动脉以Hem-o-lok夹闭,超声刀横断。病变完全位于膈肌内,未突破膈肌进入腹腔。以超声刀将病变完全切除,缝合膈肌。
腹腔内的肺隔离症一般位于腹膜后肾上腺区,位置比较隐蔽,左侧居多[15]。术前超声检查为低回声软组织包块影,增强CT可见增强的软组织包块影,边界清楚,有的可见体循环供血血管,血管1支或多支,比较纤细。上腹部MRI也可以清楚地显示病变位置及大小。此型肺隔离症与腹膜后肿瘤不易区分,术前检查不能完全鉴别,需要术中探查明确,而且手术操作困难[15]。血管纤细可以用超声刀离断,如果血管稍粗大,可以用Hem-o-lok夹闭血管近端,远端超声刀横断。包块与周围组织粘连明显,操作时需要仔细分离。我们初期做腹腔内肺隔离症时,经常定位困难,探查不容易找到病灶,需结合术前影像学检查寻找,操作特别困难时应中转开腹。1例膈下隔离肺,因合并左侧膈膨升,所以在胸腔镜下操作。
综上所述,小儿肺隔离症的诊断需要综合产前超声、出生后增强CT及三维重建明确,必要时完善MRI。明确诊断后,均需要手术治疗,建议出生后6个月左右手术,腔镜微创手术是首选方式。叶内型隔离肺可以选择解剖性肺段切除术,以保留更多的肺组织。

