HPLC 测定葡萄糖酸锌口服液中山梨酸钾的含量
张 蔚,邝嘉颖,吉 薇,龙慧静,周秀春
(广东第二师范学院生物与食品工程学院,广东广州 510225)
山梨酸钾是经由山梨酸与碳酸钾发生中和反应而生成的,拥有山梨酸基本的性能[1],作为常用的防腐剂,其价格低廉、毒性小,在防腐过程中可以保持食品原本的色、香、味且营养物质不改变。虽然山梨酸钾毒性小,但使用时仍存有一些不良反应,如皮肤刺激性反应、过敏性或者超敏性反应等,并且部分食品添加剂会超标。因此,控制山梨酸钾的使用含量,保证其使用安全性具有重要的意义[2]。检测山梨酸钾含量的方法有拉曼光谱法、荧光光谱法、高效液相色谱法等,其适用范围仅限于调味品、饮料、果酱、口服液等食品与药品。
口服液剂内含糖、蛋白质等营养物,容易长出霉菌而发霉,为了保障口服液的质量,某些厂家会向产品中添加一定量的山梨酸钾,达到防腐保质的目的。此前,也有很多关于口服液中山梨酸含量测定的文献,大多数是研究中药口服液中的多种防腐剂,但未出现过葡萄糖酸锌口服液山梨酸含量测定的研究,而葡萄糖酸锌口服液并非中药制剂,并且国家并未出台相关的检测标准测定葡萄糖酸锌口服液中山梨酸钾的含量。试验参考有关资料[3-8],确定了最适合葡萄糖酸锌口服液的流动相及系统配置,相比起其他检测口服液中防腐剂的研究,该方法提高了专属性、简化了操作,为葡萄糖酸锌口服液中的山梨酸钾含量测定提供一种简单、高效、便捷、准确度高的新方法。
1 仪器与试剂
1.1 仪器
岛津LC-20A 型四元低压液相色谱仪及配套色谱工作站、KQ-300DE 型数控超声波清洗器、赛多利斯BSA224S 型十万分之一电子天平、瑞士梅特勒托利多百万分之一电子天平等。
1.2 试剂
山梨酸钾标准品(批号:101075-201602,含量100.0%),中国食品药品检定研究院提供;随机在市面上购买的葡萄糖酸锌口服液(批号:20180105,18060727,17092531,170601);乙腈、甲醇,均为色谱纯;水,为超纯水;其他溶液均为分析纯。
2 试验方法
2.1 色谱条件
色谱柱:岛津C18型柱(250 mm×4.6 mm,5 μm),流动相:0.02 mol/L 磷酸二氢钠溶液∶乙腈(75%∶25%),柱温40 ℃,进样量20 μL,流速1 mL/min,检测波长为262 nm。
2.2 溶液的配制
2.2.1 标准品储备液
精密称取山梨酸钾标准品约20 mg,置其于100 mL 容量瓶中,加入一部分水溶解,放入超声波清洗仪中超声溶解,超声完毕冷却到室温后加水稀释至刻度,摇匀,贴上标签,作为标准品储备液。
2.2.2 样品溶液
精密量取样品5 mL,置于25 mL 容量瓶中,加入一部分水溶解,放入超声波清洗仪中超声溶解,超声完毕冷却到室温后加水稀释至刻度,摇匀,贴上标签,作为样品溶液。
2.2.3 标准品辅助液
精密称取山梨酸钾标准品10 mg,置于100 mL容量瓶中,加入一部分水溶解,放入超声波清洗仪中超声溶解,超声完毕冷却到室温后加水稀释至刻度,摇匀,贴上标签,作为标准品辅助液。
3 结果与分析
3.1 色谱条件的优化
主要对流动相的类型与比例、柱温、进样量进行比较筛选,而流速与检测波长不作为条件筛选,流速过大会对液相色谱仪造成压力,1 mL/min 是最合适的流速;检测波长是因为该方法只研究一种防腐剂,不需要同时测定几种不同的防腐剂在口服液中的含量,参考相关学者的研究[9-10],最后选择波长为262 nm。理论塔板数(按山梨酸钾峰计) 不低于4 000,山梨酸钾与相邻峰分离度符合要求。
3.1.1 流动相的选择
以A 组(甲醇∶乙酸铵溶液= 5%∶95%)、B 组(乙腈∶水= 40%∶60%)、C 组(0.02 mol/L 磷酸二氢钠溶液∶乙腈= 80%∶20%) 为流动相进行进样。
不同流动相的液相色谱图见图1。
由图1 可知,B 组流动相组合峰形既不美观也不对称,而且出峰时间也过早,A 组流动相组合峰形相较C 组流动相组合而言也不够美观,C 组流动相组合出峰时间合适,峰形也美观对称,故选择C 组:0.02 mol/L 磷酸二氢钠溶液∶乙腈= 80%∶20%作为流动相。
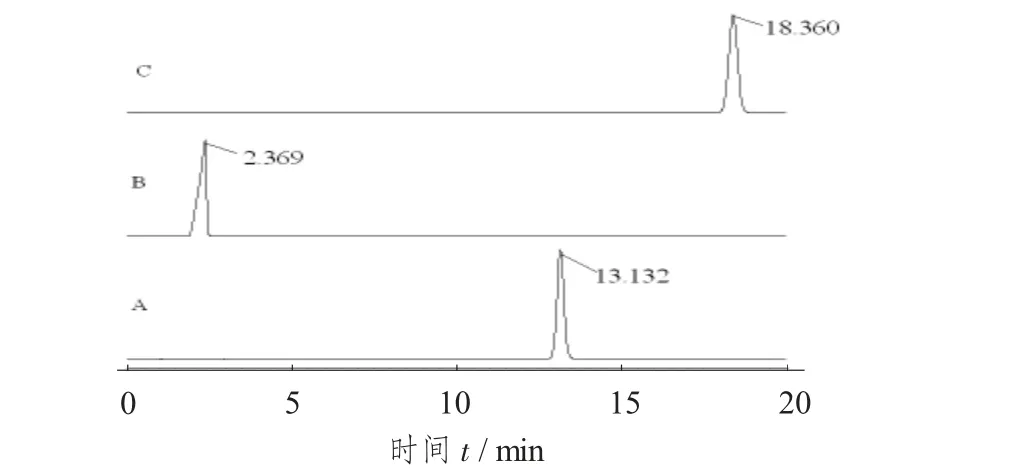
图1 不同流动相的液相色谱图
3.1.2 流动相比例
确定流动相的组成后,用山梨酸钾标准品制成质量浓度为0.04 mg/mL 的山梨酸钾对照品溶液,在柱温40 ℃,进样量20 μL,流速1 mL/min,波长262 nm 的条件下,以±5%进行流动相比例调整以达到更佳的峰形和更合适的出峰时间,发现75%∶25%已经能够达到比较理想的效果。
不同比例的0.02 mol/L 磷酸二氢钠溶液与乙腈为流动相时的液相色谱图见图2。

图2 不同比例的0.02 mol/L 磷酸二氢钠溶液与乙腈为流动相时的液相色谱图
3.1.3 柱温
确定流动相的组成和比例后,用山梨酸钾标准品制成质量浓度为0.04 mg/mL 的山梨酸钾对照品溶液,波长262 nm,流速1 mL/min,进样量20 μL 时,分别在柱温为40,30 ℃条件下进样。40 ℃的峰形更加尖细,出峰时间也相较30 ℃的更合适。
3.1.4 进样量
用山梨酸钾标准品制成质量浓度为0.04 mg/mL的山梨酸钾对照品溶液,固定波长262 nm,流速1 mL/min 不变,分别在进样量为20,10 μL 的条件下进样,记录色谱图。20 μL 的进样量相较10 μL 的更加合适,峰形也比10 μL 的美观。
3.2 方法学验证
3.2.1 线性范围
配制质量浓度为0.008,0.016,0.032,0.040,0.048,0.064,0.080 mg/mL 的梯度溶液,以质量浓度(X) 为横坐标,峰面积(Y) 为纵坐标绘制标准曲线。据图3 可知,山梨酸钾的线性回归方程为Y=206 812 000X+49 078,R2=0.999 8。结果说明,山梨酸钾在质量浓度为8.136~81.360 μg/mL 内线性关系良好。
线性回归方程见图3。
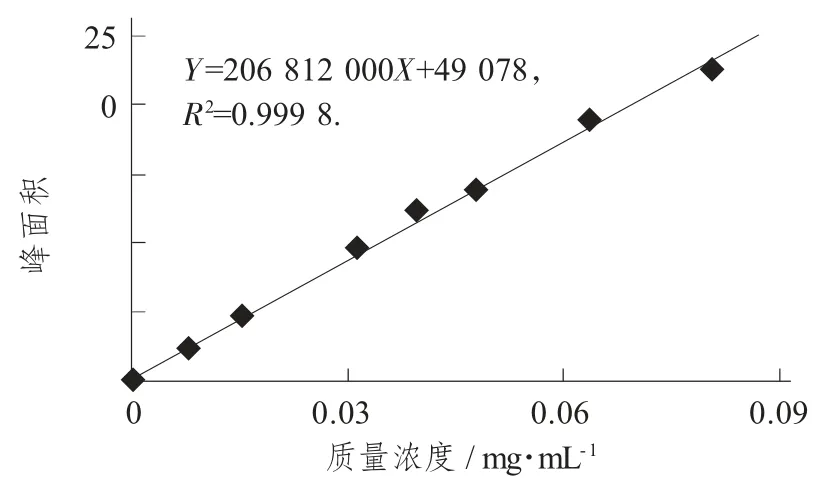
图3 线性回归方程
3.2.2 专属性验证
专属性验证指的是如果样品除了待测成分以外还存在其他成分时,如辅料、杂质、降解产物等,采用的方法可以正确地测定被测物的能力。按2.2.1的方法得到标准品储备液,按2.2.2 的方法得到样品(批号17092531) 溶液和阴性样品(批号20180105)溶液对照,记录出峰时间及峰面积。
专属性验证色谱图见图4。
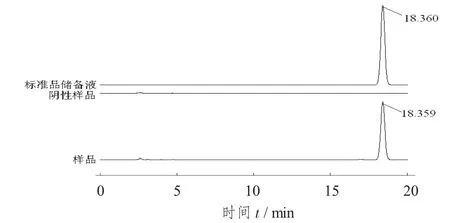
图4 专属性验证色谱图
由图4 可见,山梨酸钾峰周围并无杂质峰,标准品储备液与样品出峰时间在误差范围内,且同一时间阴性样品并未出现色谱峰。证明该方法专属于山梨酸钾峰的检出。
3.2.3 精密度验证
按2.2.1 的方法得到标准品储备液,连续在液相色谱仪中进样6 次,记录峰面积。精密度要在规定的条件之下,同1 份样品多次取样测得结果之间接近程度,经计算得出山梨酸钾峰面积的RSD 为0.27%(n=6),表明该液相色谱仪的精密度良好,经该液相色谱仪的试验数据真实、可靠、准确。
3.2.4 重复性验证
按2.2.2 的方法制备样品(批号17092531) 溶液,分别在室温条件下放置0,1,2,4,6,8 h 后进行测定,记录峰面积。该结果测得山梨酸钾含量的RSD 为0.60%,表明该方法的重复性良好,多次操作结果都在误差范围内,该方法所得出的试验数据真实可信。
3.2.5 稳定性验证
按2.2.2 的方法制备样品(批号17092531) 溶液,分别在室温条件下放置0,1,2,4,6,8 h 后进行测定,记录峰面积。试验结果测得山梨酸钾峰面积RSD 为0.52%(n=6),说明样品溶液在8 h 内稳定性良好,在8 h 内样品性质未发生改变,可以用于试验操作,放置8 h 后试验结果仍然准确可靠。
3.2.6 加样回收率
准备9 个50 mL 容量瓶,将这9 个容量瓶分成3 组,每组3 个,分组名为“1∶0.8”“1∶1.0”“1∶1.2”;各加入已知含量的样品(批号17092531)5 mL,再分别加入标准品储备液,“1∶0.8”组中加入6 mL 标准品辅助液,“1∶1.0”组中加入8 mL标准品辅助液,“1∶1.2”组中加入10 mL 标准品辅助液。加入一部分水溶解,放入超声波清洗仪中超声溶解,超声完毕冷却到室温后加水稀释至刻度,摇匀,贴上标签,进行测定,记录测得的峰面积。根据线性回归方程进行含量计算及另外进行加样回收率的计算。加样回收率一般用于测定方法的准确度,即该方法测定出来的结果跟参考值或者真实值接近程度,该方法中的山梨酸钾加样回收率为98.21%,RSD 为0.53% (n=9),说明该方法准确度良好。
3.2.7 耐用性验证
分别改变柱温、流动相pH 值,其他条件不变,记录峰面积并进行计算。分别改变柱温、流动相pH 值,其他条件不变时,测定结果不受影响,可以为建立的日常检验新方法提供依据。
3.3 样品含量测定
按2.2.2 的方法制备样品(批号18060727)、样品(批号17092531)、样品(批号170601),进行测定,记录峰面积,按所得出的线性回归方程进行含量计算。
样品中山梨酸钾含量测定结果见表1。
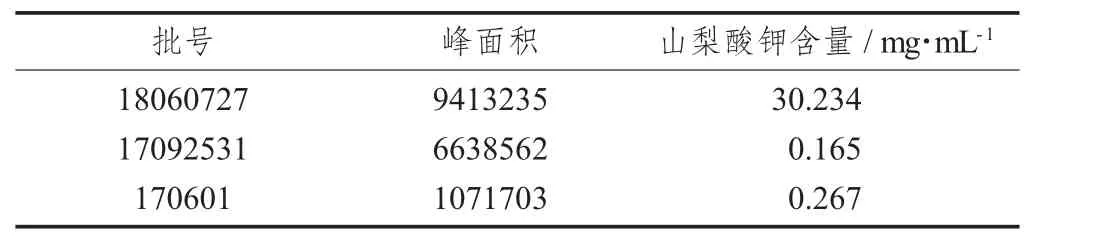
表1 样品中山梨酸钾含量测定结果
4 结论
研究得出最适合测定葡萄糖酸锌口服液中山梨酸钾含量的高效液相色谱条件为流动相0.02 mol/L,磷酸二氢钠溶液∶乙腈(75%∶25%),柱温40 ℃,进样量20 μL,流速1 mL/min,检测波长262 nm。该方法灵敏度高、可信度高、操作简便,目前我国尚未有明确的山梨酸钾添加在药品中的限量标准,因此研究可以为葡萄糖酸锌口服液中山梨酸钾的含量检测提供参考。

