心脏磁共振评估儿童慢性肾脏病1期早期亚临床心功能障碍
侯瑞来,谢林均,傅航,张露,郭应坤
(四川大学华西第二医院放射科·出生缺陷与相关妇儿疾病教育部重点实验室,四川 成都 610041)
慢性肾脏病(coronary kidney disease,CKD)指存在影响健康的肾脏损伤指标异常(如蛋白尿、组织学或解剖学异常)或估算肾小球滤过率(estimated glomerular filtration rate,eGFR)<60 mL/(min/1.73 m2)超过3个月的疾病。目前,临床根据eGFR下降程度将CKD分成5期,eGFR正常[≥90 mL/(min/1.73 m2)]为G1期[1]。儿童CKD总体发病率约(3.0~17.5)/100万[2]。心血管疾病(cardiovascular disease,CVD)是CKD儿童常见并发症,CKD患儿被美国心脏协会的指南列为发病风险最高的儿童群体之一[3]。CVD是CKD儿童,尤其是终末期肾病(end stage renal disease,EDRD)儿童最主要的死亡原因。在肾功能严重下降之前是识别和干预心血管系统早期损伤的最佳时期[4],但CKD G1儿童心血管系统是否受累目前仍缺乏影像学研究证据。心脏磁共振(cardiac magnetic resonance,CMR)有无创、无电离辐射、可重复性高、多参数多序列成像等优点,可以全面评价CKD儿童的心脏早期损伤。本研究通过CMR组织追踪技术分析CKD1期(G1)儿童左心室心功能及心肌应变,借以探讨CKD G1儿童是否存在早期亚临床心功能障碍,并分析左心室早期改变与临床指标的相关性。
1 资料与方法
1.1 一般资料
选取2019年4月至2021年5月四川大学华西第二医院临床确诊的35例CKD G1儿童及18名健康儿童为研究对象,并分别设为CKD G1儿童组和对照组。CKD G1儿童组中,男性16例,女性19例;年龄6~14岁,平均11.5岁。对照组中,男性8例,女性10例;年龄6~14岁,平均10.5岁。本研究获四川大学医学伦理委员会批准,儿童及健康志愿者均签署知情同意书,两组儿童年龄、性别、体表面积、心率、收缩压及舒张压比较,差异无统计学意义(P>0.05),CKD G1儿童组体质量指数(body mass index,BMI)高于对照组(P<0.05)。见表1。
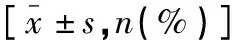
表1 两组儿童一般资料比较
纳入标准:(1)年龄<18周岁且临床诊断为CKD G1的儿童,诊断标准依据国际肾脏病组织“改善全球肾脏病预后组织”2012年修订后指南标准;(2)所有儿童均能够配合完成CMR电影序列检查。排除标准:(1)患有其他心血管系统疾病,如先天性心脏病、心律失常等;(2)体内有金属植入物或有严重的幽闭恐惧症的儿童;(3)图像质量不满足诊断要求。根据上述纳入及排除标准,共计35例儿童纳入研究。其中男性16例,女性19例;年龄6~14岁,平均11.5岁。同时收集性别、年龄匹配的健康对照18例,对照组儿童均无心血管及肾脏相关病史,其中男性8例,女性10例,年龄6~14岁,平均10.5岁。
1.2 方法
1.2.1 实验室数据收集 收集所有CKD G1儿童的肾功能数据,包括同期的尿蛋白定性、肾功能生化检查、尿蛋白持续异常时间等,作为综合评估肾功能的指标。尿蛋白定性是记录小便常规中尿白蛋白“+”的数量,阴性记为“0”,“±”记为“0.5”;尿蛋白持续异常时间的计算方法:统计发病日期后儿童所有小便常规结果,累加尿蛋白连续异常的时间,若中途尿蛋白转阴,则自此次转阴日期至下一次复发日期时间间隔不计入,时间单位为月。
1.2.2 非增强磁共振扫描 采用西门子skyra 3.0T磁共振扫描仪进行心脏扫描,取头先进仰卧位,使用专用胸前导联与心脏扫描专用双相门控线圈(包括心电门控和呼吸门控)进行扫描。电影序列使用稳态自由进动序列(steady-state free-precession,SSFP)进行扫描,短轴位电影序列扫描范围覆盖左心房及左心室(层数8~12层,层厚8 mm,层间距2 mm,重复时间(TR)37.66 ms,回波时间(TE)1.2 ms,翻转角度39°),并扫描长轴二腔、三腔、四腔电影序列(TR/TE 35.77/1.3 ms,翻转角度40°,视场280 mm×373 mm,基体尺寸146 mm×280 mm)。
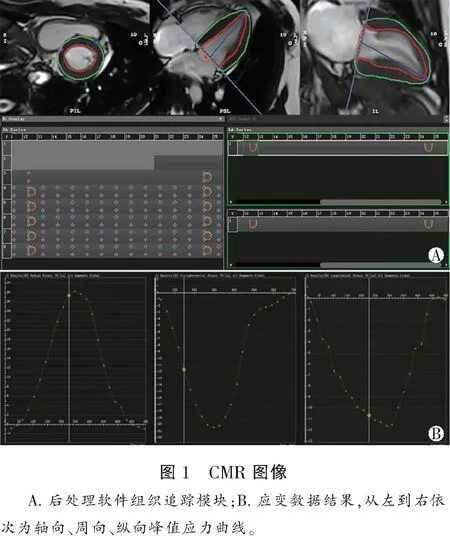
1.2.3 图像分析 使用专用心血管后处理软件(Cvi42;Circle Cardiovascular Imaging,Inc.,Calgary,Canada)进行CMR图像分析,均由1名有3年磁共振诊断经验的放射科医生独立完成。在短轴功能(SAX-function)模块中载入短轴位层面电影图像,软件自动勾画出基底到心尖每个层面舒张末期和收缩末期左心室心内膜、心外膜轮廓线,经手动矫正边缘后测量出左心室舒张末期容积(left ventricular end-diastolic volume,LVEDV)、左心室收缩末期容积(left ventricular end-systolic volume,LVESV)、每搏输出量(stroke volume,SV)、左心室舒张末期质量(left ventricular end-diastolic mass,LVEDM)和左心室射血分数(left ventricular ejection fraction,LVEF)、左心室向心性重构指数(left ventricular concentricity index,LVCI)、左心室的最大收缩速率(peak ejection rate,PER)与最大充盈速率(peak filling rate,PFR)等常规心功能参数。随后,将长轴二腔、四腔和短轴电影序列载入组织追踪模块,软件自动勾画所有载入序列的舒张末期和收缩末期的每个层面的心内膜和心外膜轮廓,手动矫正仔细排除乳头肌后,由软件自动分析处理获得左心室整体、心尖段、中间段及基底段心肌应变参数,包括心肌轴向、周向、和纵向峰值应力(peak strain,PS)。见图1。
1.3 统计学分析
2 结果
2.1 两组儿童左心室心功能参数比较
两组儿童左心室心功能比较,差异无统计学意义(P>0.05)。见表2。
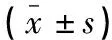
表2 两组儿童左心室心功能参数比较
2.2 两组儿童左心室3D整体及节段峰值应力比较
两组3D应变参数均取绝对值后分析显示,CKD G1儿童组左心室左心室整体纵向PS低于对照组(P<0.05),且以心尖段纵向PS减低为主(P<0.05)(图2);左室整体轴向及周向PS、心底段、心中段纵向PS、各段周向及轴向PS与对照组比较,差异无统计学意义(P>0.05)。见表3及图2。
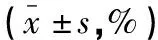
表3 两组儿童左心室3D整体及节段峰值应力比较
2.3 CKD G1儿童组左心室构型及功能参数与临床指标的相关性
相关性分析显示,同期尿蛋白定性与LVEF、左心室整体轴向及周向PS呈负相关(P<0.05),与LVCI呈正相关(P<0.05);尿蛋白持续异常时间与LVCI呈正相关(P<0.05)。BMI与LVEF、左室整体轴向及周向PS呈负相关(P<0.05),与LVCI呈正相关(P<0.05)。此外,BMI与尿蛋白定性、尿蛋白持续异常时间呈正相关(P<0.05);尿蛋白定性与尿蛋白持续异常时间无相关性(P>0.05)。见表4。
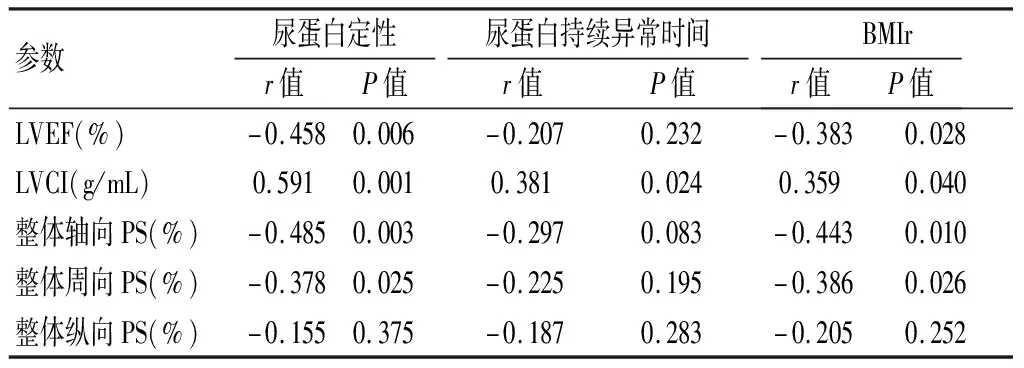
表4 CKD G1儿童组左心室构型及功能参数与临床指标的相关性
3 讨论
CKD 导致CVD的机制较为复杂,高血压、肥胖、血脂异常等传统危险因素及肾素-血管紧张素系统的激活、血管内皮功能障碍、氧化应激反应等肾性因素可能共同参与了这一过程[5]。CKD儿童存在的心血管改变包括左心室收缩及舒张功能障碍、左心室肥厚(left ventricular hypertrophy,LVH)、心肌纤维化、动脉内膜厚度增加、冠状动脉钙化等,可最终导致心肌病、心力衰竭、冠状动脉粥样硬化性心脏病等,甚至导致心源性猝死[4,6-8]。识别CKD儿童的早期心血管损伤,对于预防与治疗CKD心血管并发症及改善儿童预后有重要意义。既往有大量针对中晚期CKD儿童心血管系统病变的研究,但少见针对早期CKD儿童的研究,本研究重点关注CKD G1儿童心肌的亚临床功能障碍,望为早期监测、早期干预提供新的影像学指标。
本研究发现,即使CKD G1儿童LVEF还在正常范围内,也已发生左心室整体及心尖段纵向PS明显降低。关于 G2~G5期CKD儿童的超声和CMR研究均发现在儿童LVEF保留时已经发生心肌应力的降低[9-11]。另外,有大量关于中晚期CKD儿童以及关于ESRD儿童的研究[6,12-14]发现,儿童LVEF均维持正常水平,但存在明显的LVH,并且肥厚程度随着肾功能的下降而加重。超声研究[15]报道,eGFR轻度降低的CKD患者即出现LVEF的明显下降。本研究关于CKD G1儿童LVEF与左心室应力的结果与既往绝大部分的研究结果一致,但LCMI与LVCI无明显增高,说明CKD G1儿童尚未发生明显的左心室重构。CKD G1儿童左室壁整体及心尖段纵向PS早于周向、轴向PS发生降低,与此前关于CKD G2~G5患者的超声心动图研究[10,15]结果一致,推测可能是左心室前、后负荷增加时导致心肌肥厚与心肌纤维化,心内膜下心肌需氧量增加;同时CKD血管内皮功能受损可导致早期冠状动脉微循环障碍[7,16],因此心内膜下心肌率先出现损伤。3D心肌应力模型中,纵向PS主要反映心内膜下心肌功能,而周向PS主要反映心外膜下心肌功能,轴向PS能够反映短轴方向上肌层厚薄变化,这与肌壁内外层不同心肌纤维走行方向有关[17]。CKD G1儿童左心室整体及心尖段纵向PS的降低,可能反映了CKD G1儿童心内膜下心肌早期异常的存在。因此,PS对于早期发现CKD患者的心血管损伤有一定意义。
相关性分析显示,尿蛋白定性及BMI与左心室整体轴向PS及周向PS呈负相关,与LVEF呈负相关。尿蛋白是常用的预测CKD患者心血管系统预后的早期肾损伤的指标[18],是CKD 患者发生LVH的独立相关因素[19],即使不伴eGFR下降的微量尿白蛋白也会使CKD患者的CVD风险增加2~4倍[20]。同时,BMI是公认的CVD独立风险因素,有研究表明肥胖的儿童较正常儿童更易发生显著的心室重塑与左心室功能障碍[21]。本研究结果提示尿蛋白或BMI的异常增高将可能导致CKD G1儿童左心室早期收缩功能的异常。另外,LVCI与尿蛋白、BMI的相关性在没有发生LVH的CKD G1期已经展现,说明尿蛋白及BMI对心脏的影响或许可以追溯到疾病初期。值得注意的是,我们发现儿童BMI与蛋白尿严重程度及持续异常时间呈显著相关,这可能由于CKD的激素治疗药物副作用,以及肥胖加速肾功能下降共同导致[22-23]。儿童尿蛋白及BMI之间存在密切的关系,其与左心室心功能及应变参数的相关性或许是二者综合作用的结果,未来还需要更深入的研究。本研究不足之处在于:(1)样本量较小,需要后续扩大样本量进一步证实研究结果;(2)纳入的CKD儿童原发疾病多样,未排除原发疾病可能存在的其他心血管风险因素,在未来进一步研究中,需要消除不同疾病间的存在的差异;(3)尿蛋白持续异常时间为人为估算,过去的研究中也没有明确的计算方法,在未来研究中可能需要改进与完善。
综上,CKD G1儿童左心室整体PS较对照组降低,且以心尖段纵向PS降低为主。CMR组织追踪技术是早期反映左心室亚临床心功能障碍的无创、敏感、有效的检查方法。另外,CKD G1早期左心室重构及收缩功能障碍与尿蛋白定性、尿蛋白异常持续时间、BMI可能存在一定相关性。

