守恒法在高中化学解题中的应用
朱 岩
(江苏省连云港市厉庄高级中学 222121)
守恒解题就是利用化学反应和变化中的某些因素之间守恒联系,推算习题解答.通过开始与结束之间的守恒关系理念,可以简化题目,构建对应的公式完成答题,有助于提高学生的化学答题效率.
一、守恒法与化学题
例1在KOH固体中含有7.2%的K2CO3以及2.8%的水,将1g该样品放入到25mL浓度是2mol/L的HCl中,同时把剩下的HCl和30.0mL的KOH溶液进行中和,而KOH溶液的浓度为1.0mol/L,此时将中和之后的溶液进行加热并蒸干,求蒸干后固体的质量.
解题对题目进行审题可以发现,KOH和K2CO3都能与盐酸反应生成KCl,剩下的盐酸再和KOH溶液进行中和又生成KCl,所以蒸干的固体为KCl,根据元素守恒定律可以得到公式为:n(HCl)=n(KCl)=2mol/L×0.025L=0.05mol,再根据m(KCl)=0.05mol×74.5g/mol=3.725g,计算出KCl的质量为3.725g.
例2鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小东和小军同学进行了如图1所示的实验,相关实验数据如下所示:

图1
(1)小东根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为( ).
(2)小军根据“反应过程中减少的质量”也求得了蛋壳中碳酸钙的质量分数,请你写出小军的计算过程和结果.
(3)小东和小军经过反复实验得出该鸡蛋壳中碳酸钙的质量分数与小军结果吻合,请分析小东开始所得结果出现误差的可能原因.

物料守恒是指原子个数在溶解前后不会有变化,例如硫氢化钠溶液中Na和S的原子个数相同,那么硫氢化钠在溶解后Na和S这两种原子个数是不会发生变化的,即n(Na)=n(S),S原子等于HS-、S2-和H2S之和,在同时除以硫氢化钠的溶液体积,可得出硫氢化钠的物料守恒公式:c(Na+)=c(HS-)+c(S2-)+c(H2S).

A.2n个 B.3n个 C.6n个 D.8n个
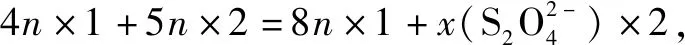
例4某混合溶液中MgCl2的浓度为2mol/L,AlCl3的浓度为3mol/L,将200mL此溶液中的Mg2+完全沉淀(氢氧化铝恰好溶解),需加入1.6mol/L的为____.
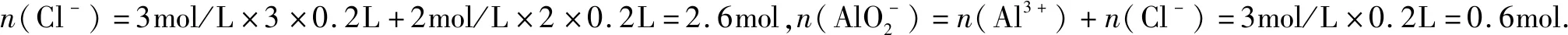
例5现有9.4 g CaCO3和K2CO3的固体混合物,测得其中含有氧元素的质量是3.6 g,将该混合物与100 g稀盐酸混合,恰好完全反应.则最后所得不饱和溶液的质量为( ).
A.105g B. 108.3g C.106g D. 106.1g

二、总结
在解题中借助守恒法则,帮助学生更快更有效的掌握到解笞问题的关键信息,快速提升学生处理分析化学问题的能力,增强学生对化学知识的深度专研的信心和动力,鼓励学生掌握不同技巧和方法来解答化学题目,提升学生学习知识能力和提高考试中的解题能力,不断提升学生自主学习的能力和养成积极思考的习惯.

