产前应用低分子肝素对胎儿生长受限的临床疗效及安全性分析
魏美兰
(广东省惠州市第六人民医院 产科,广东 惠州 516211)
0 引言
作为产科临床常见的一类并发症,胎儿生长受限(Fetal growth restriction,FGR)在欧洲地区的发生率约为10%,而发展中国家的发生率高达55%[1]。目前,关于国内FGR 发病率的报道数据存在一定的区域特点,对胎儿的正常发育影响颇为明显,甚至可能导致围生儿死亡[2]。既往,针对FGR 的干预以药物治疗为主,如葡萄糖、丹参注射液以及维生素等,然而临床效果欠佳[3]。故此,寻求一种更为积极有效的治疗方式显得尤为重要,亦是目前临床研究的热点。随着近年来相关研究的日益深入,越来越多的学者发现治疗FGR 的重中之重在于调节孕期血液高凝状态,对胎盘血液循环进行改善,从而促使其为胎儿的生长发育提供充足保障[4]。低分子肝素作为新型抗凝剂之一,具有显著的抗凝作用,可有效抑制Xa 的活性,故此应用于FGR 的治疗中可能获得较为理想的效果[5]。鉴于此,本文通过研究产前应用低分子肝素对FGR 的临床疗效及安全性,旨在为临床FGR 的治疗提供科学有效的方案,现作以下报道。
1 资料与方法
1.1 一般资料
将医院自2017 年1 月至2020 年1 月收治的FGR产妇91 纳入研究。将其按照随机数字表法分作研究组45 例和常规组46 例。研究组年龄21~38 岁,平 均(29.15±4.02)岁;孕 周26~34 周,平 均(31.44±2.10)周;孕次1~4 次,平均(2.25±0.71)次。常规组年龄21~39 岁,平均(29.20±4.03)岁;孕周26~34 周,平均(31.50±2.12)周;孕次1~4 次,平均(2.27±0.72)次。两组年龄、孕周及孕次比较,差异无统计学意义(P>0.05),均衡可比。入选标准:①所有入选对象均和《妇产科学》第8 版[6]中所制定的胎儿宫内生长受限相关诊断标准相符;②均经产检、B 超等确诊;③均为单胎妊娠;④孕妇年龄≥20 岁。剔除标准:①合并其他组织或(和)器官病变者;②对本研究相关药物过敏者;③因其他原因引起的FGR;④神志异常或合并神经系统疾病者;⑤正参与其他研究者。所有入选对象及其家属知情并在同意书上签字,且经伦理委员会批准。
1.2 治疗方式
所有受试者均开展基本治疗,内容如下:①营养支持;②低流量吸氧;③补充微量元素;④氨基酸+林格静脉滴注。研究组同时加用低分子肝素(河北常山生化药业股份有限公司,批准文号:国药准字H20063910)治疗。通过皮下注射给药,选择前外侧/后侧腹壁皮下组织作为注射部位,给药剂量0.4mL/次,1 次/d。所有受试者均开展2 周的治疗。
1.3 观察指标
分析两组临床疗效,治疗前后脐动脉血流参数水平,新生儿出生情况,不良妊娠结局发生情况等方面的差异。临床疗效评价主要是通过治疗前后各项生长发育参数实现,主要生长发育参数涵盖头围(HC)、腹围(AC)、双顶径(BPD)以及胫骨长径(FL)。检测时间为治疗前1d 以及治疗结束后1d,检测仪器为Philips IU22 超声诊断仪,具体操作遵循仪器说明书完成。脐动脉血流参数主要涵盖搏动指数(PI)、阻力指数(RI)以及收缩期血液流速高值(S)/舒张晚期血液流速高值(D)。检测时间为治疗前1d以及治疗结束后1d,检测仪器为Philips IU22 超声诊断仪,具体操作遵循仪器说明书完成。新生儿出生情况主要指标包括出生胎龄、出生体质量、身长。不良妊娠结局主要囊括早产儿、新生儿窒息、急性胎儿窘迫以及足月低体重儿。
1.4 统计学处理
数据处理软件为SPSS 22.0,计数/计量资料以%/()表示,开展χ2/t检验。差异有统计学意义的标准即P<0.05。
2 结果
2.1 治疗前后两组各项生长发育参数评价
治疗后研究组HC、AC、BPD、FL 均高于常规组(均P<0.05),见表1。
表1 治疗前后两组各项生长发育参数评价(cm,)
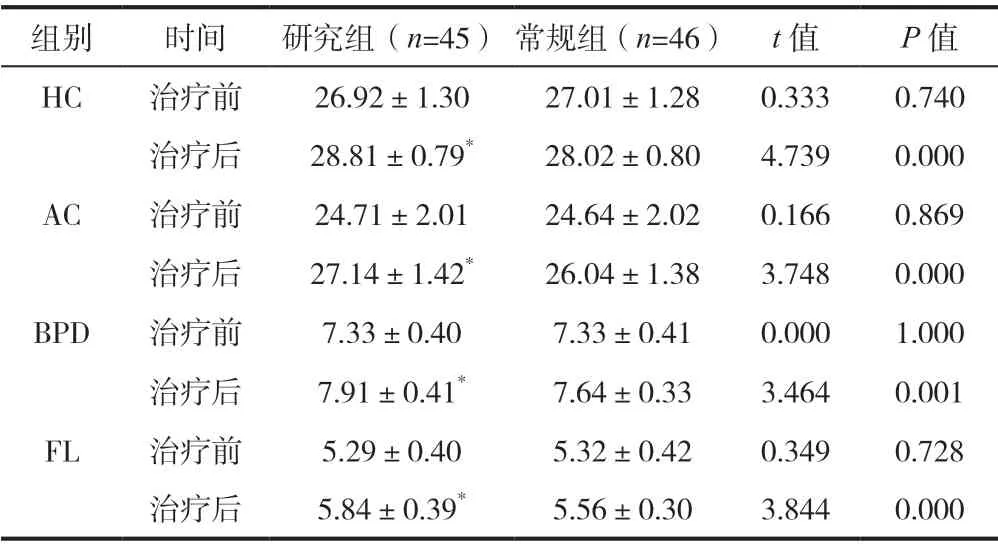
表1 治疗前后两组各项生长发育参数评价(cm,)
注:与常规组相比,*P<0.05
2.2 治疗前后两组脐动脉血流参数评价
治疗后研究组PI、RI、S/D 均低于常规组(均P<0.05),见表2。
表2 治疗前后两组脐动脉血流参数评价( )
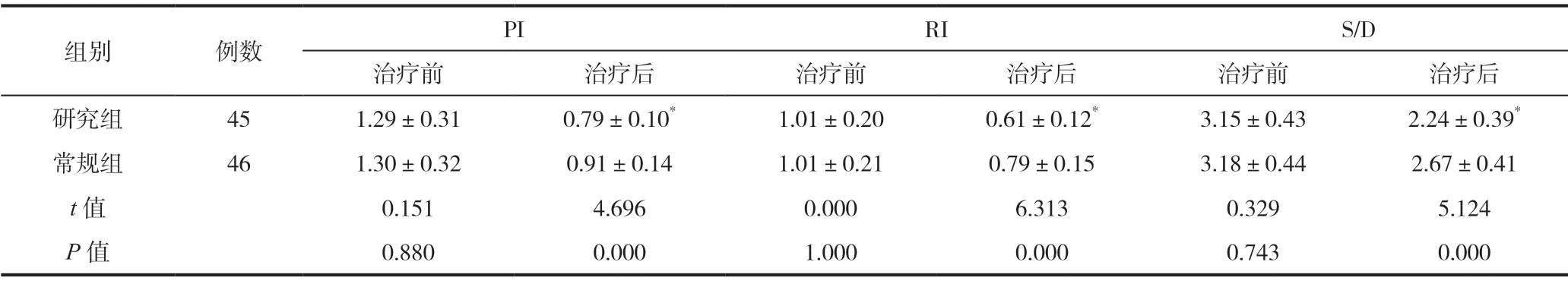
表2 治疗前后两组脐动脉血流参数评价( )
注:与常规组相比,*P<0.05
2.3 两组新生儿出生情况评价
研究组新生儿出生胎龄、出生体质量、身长均高于常规组(均P<0.05),见表3。
表3 两组新生儿出生情况评价( )
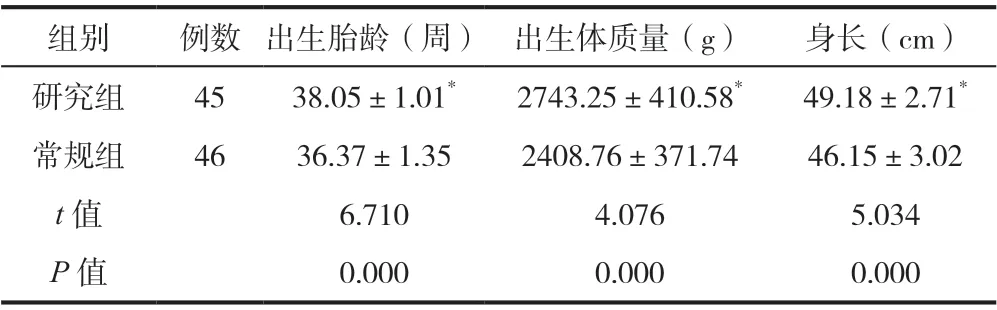
表3 两组新生儿出生情况评价( )
注:与常规组相比,*P<0.05
2.4 两组不良妊娠结局发生情况评价
研究组各项不良妊娠结局发生率均低于常规组(均P<0.05),见表4。
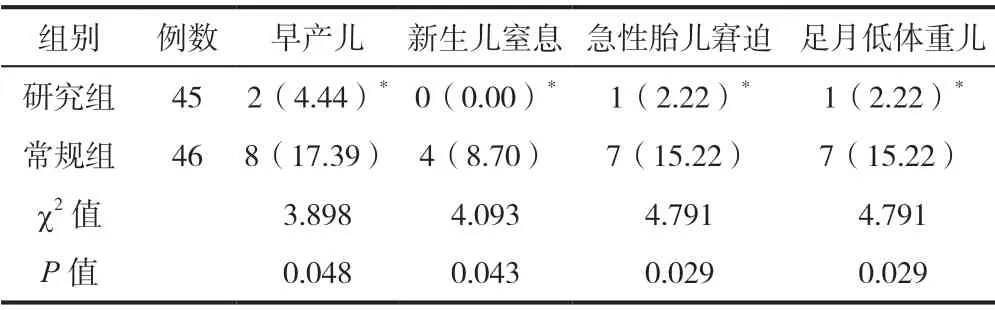
表4 两组不良妊娠结局发生情况评价[(n)%]
3 讨论
FGR 的发生主要是因孕妇胎盘螺旋小动脉导致纤维蛋白原沉着、血栓以及血管硬化等异常情况,继而引起营养物质输送至血管阻塞,进一步促使绒毛间质血管物质传输受阻,最终引发FGR[7-9]。目前,临床医师主要是采用常规治疗方案实现对FGR 孕妇的治疗,然而大量研究报道证实,常规治疗FGR 的临床疗效欠佳,新生儿胎龄延长并不显著,且出生体质量偏低[10-12]。因此,寻求一种更为安全有效的治疗手段成为产科医生共同关注的热点。相关研究发现,低分子肝素有利于改善高凝血液状态,促使孕妇胎盘血供明显增加,继而促进了物质之间的交换,进一步改善胎盘血灌注不足以及孕妇子宫环境,从而为胎儿的正常生长发育起到积极促进作用[13-15]。
本研究发现,治疗后研究组HC、AC、BPD、FL均高于常规组。这在王俊虎等[16]的研究报道中得以佐证:低分子肝素治疗组宫内生长受限胎儿治疗后 的HC、AC、BPD、FL 分 别 为(28.65±0.78)、(27.12±1.46)、(7.87±0.42)、(5.82±0.35),均明显高于常规治疗组的(28.05±0.82)、(26.24±1.52)、(7.62±0.36)、(5.54±0.28)。这提示了产前应用低分子肝素对FGR 的临床疗效显著,有助于促进胎儿的正常生长发育。考虑原因可能在于:低分子肝素的应用可有效阻断纤维蛋白沉积在胎盘血管基底膜,进一步促使血管阻力的下降,继而有助于血液循环,改善胎盘微循环,从而实现为胎儿提供一系列营养物质的作用。且在和常规治疗药物联合应用时,可通过差异性作用机制改善胎盘功能,为胎儿的生长发育提供良好的环境基础。此外,低分子肝素可有效改善胎儿脐动脉血流参数。考虑原因可能在于:低分子肝素可通过和抗凝血酶Ⅲ结合形成复合物,从而抑制血小板的凝聚,有助于凝血系统的激活,促进血栓溶解,最终改善胎盘血供[17-18]。同时,该药可发挥保护血管内皮细胞的作用以及局部抗炎功效,有利于子宫内环境的改善,起到促进胎儿生长发育的作用。在和常规药物联合应用时可加快血液循环,增加胎盘以及胎儿的血液灌注量,从而促进胎盘营养物的获取,最终达到改善胎儿血流参数的目的。另外,研究组新生儿出生胎龄、出生体质量、身长均高于常规组。低分子肝素进入人体后的主要作用之一是干扰纤维蛋白原的转变,减少或避免纤维蛋白原大量沉积于胎盘血管基膜表层,有益于血管局部血液循环改善,从而为胎儿的生长发育创造一个有利的环境,最终可改善围生儿结局[19-20]。本研究还发现了研究组不良妊娠结局发生率均低于常规组,具有较好的安全性。考虑原因可能是低分子肝素不会通过胎盘屏障吸收,因此不会对胎儿的造成不利影响,十分安全有效,同时可改善胎盘微循环。
综上所述,产前应用低分子肝素对FGR 的临床疗效较为理想,且可获得较为理想的安全性,具有较高的临床推广应用价值。

