高倍率铌基氧化物负极材料的研究进展
叶一桦,巴德良,刘帅磊,陈颍霖,李园园,刘金平
(1.武汉理工大学化学化工与生命科学学院,武汉430070;2.华中科技大学光学与电子信息学院,武汉430074)
锂离子储能器件如锂离子电池与锂离子混合电容器等因具有自放电小、无记忆效应、工作温度范围宽、使用寿命长等特点,已被广泛应用于各类便携式电子设备,同时也在新能源汽车、智能电网等领域展现出巨大潜力[1].近年来,随着可穿戴电子设备等领域的快速发展,对储能器件的轻量化、安全性和快速充放电能力提出了越来越高的要求[2].因此,储能器件不仅要具有高的能量密度和循环寿命,而且还应该提供高的功率密度,并且在快充情况下保障良好的运行安全性[3].当前,在增强能量密度的同时,开发快速充电(20 min内达到80%的充电状态)的锂离子储能器件至关重要[4].传统的锂离子负极材料(如石墨与硅)虽然具有较低的成本与高的理论容量(Si约为4200 mA·h/g,石墨约为372 mA·h/g)[5],但是其倍率性能已无法满足当前储能设备对快充负极材料的要求;并且,由于其较低的嵌锂电位,在快速充放电的过程中易导致锂金属的沉积与枝晶的生成,产生安全隐患.因此,为了优化锂离子储能器件的倍率性能以满足日益增长的需求,寻找新型安全、高倍率负极材料迫在眉睫[6~8].
钛基材料如TiO2与Li4Ti5O12材料(LTO)在约1.55 V的高氧化还原平台发生嵌/脱锂反应,有效地避免了固体电解质界面膜(SEI)与锂枝晶的形成[9],具有较高的安全性.此外,LTO在充放电过程中体积的“零应变”特性使其具有优异的循环稳定性.但LTO的理论容量(175 mA·h/g)低,电导率(10−13S/cm)差,以及锂离子扩散系数较小,严重限制了其高倍率性能与商业化进程.
铌基氧化物包括Nb2O5[10~12]和TiNbxO2+2.5x[13,14]等化合物.因其独特的结构优势(如用于锂离子传输的准2D网络,开放且稳定的Wadsley-Roth剪切晶体结构,反应过程中微小的体积膨胀)与多电子氧化还原反应(Nb5+/Nb4+与Nb4+/Nb3+),可提供快速的离子传输通道、较长的循环寿命与较高的理论容量(200~400 mA·h/g).此外,铌基氧化物大多表现出高工作电压(>1.0 Vvs.Li+/Li),可有效避免SEI和锂枝晶的形成,具有比石墨材料更高的安全性[10].并且,不同于非本征赝电容材料在特定的尺寸或形貌下才具备赝电容行为,铌基氧化物作为独特的本征赝电容材料有望实现锂离子快速储能研究领域的进一步突破,并已在多类电化学储能系统中获得应用[13].
然而,固有的导电性差等缺点阻碍了铌基氧化物在电化学储能领域的应用.尽管已有部分研究总结了合成方法与形貌等条件对铌基氧化物电化学性能的影响[9~14],但鲜有聚焦于高倍率铌基氧化物负极材料改性研究方面最新进展的综合评述.要获得高倍率特性,需要对电极材料的电子/晶体结构、微观尺寸/形貌、缺陷和电荷传输路径等进行有效调控[15].本文系统总结了高倍率铌基氧化物负极材料在锂离子储能器件领域的应用,概述了各种性能优化策略,以及先进的表征与计算方法.Scheme 1与表1总结了铌基氧化物常见的改性手段,包括形貌调控、导电材料复合、阵列/自支撑结构设计与异质离子掺杂等,用以提升其倍率性能、比容量与循环寿命[16~59].此外,还展望了铌基氧化物在未来研究和商业应用的前景与挑战(Scheme 2).
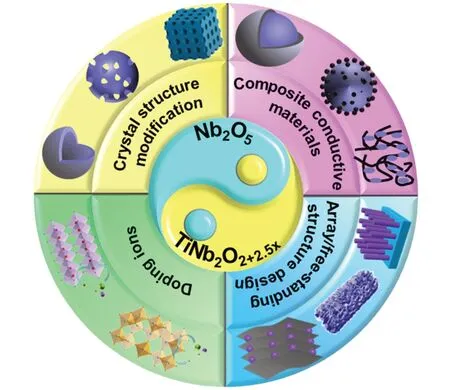
Scheme 1 Schematic of different modification methods of Nb2O5 and TiNb2O2+2.5x
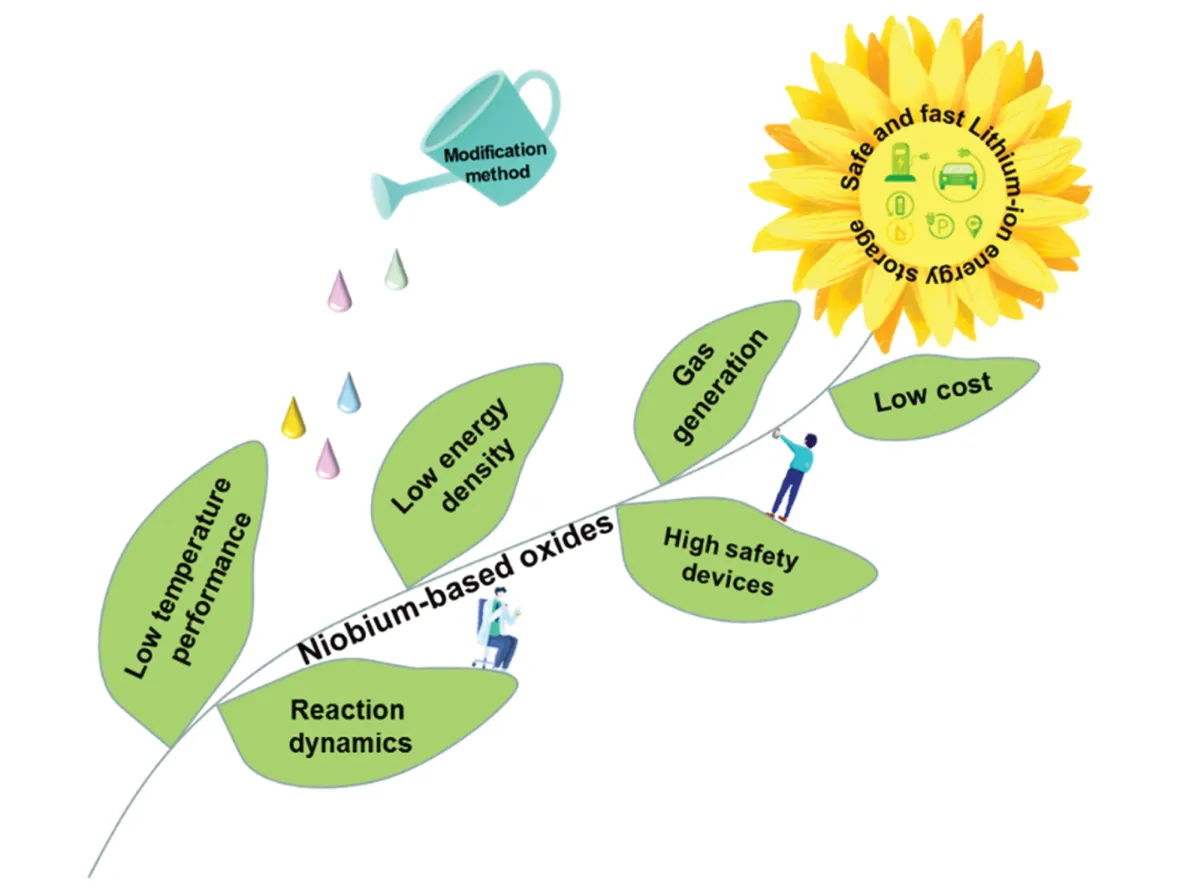
Scheme 2 Schematic illustration of various challenges faced by niobium⁃based oxides to achieve safe and fast energy storage
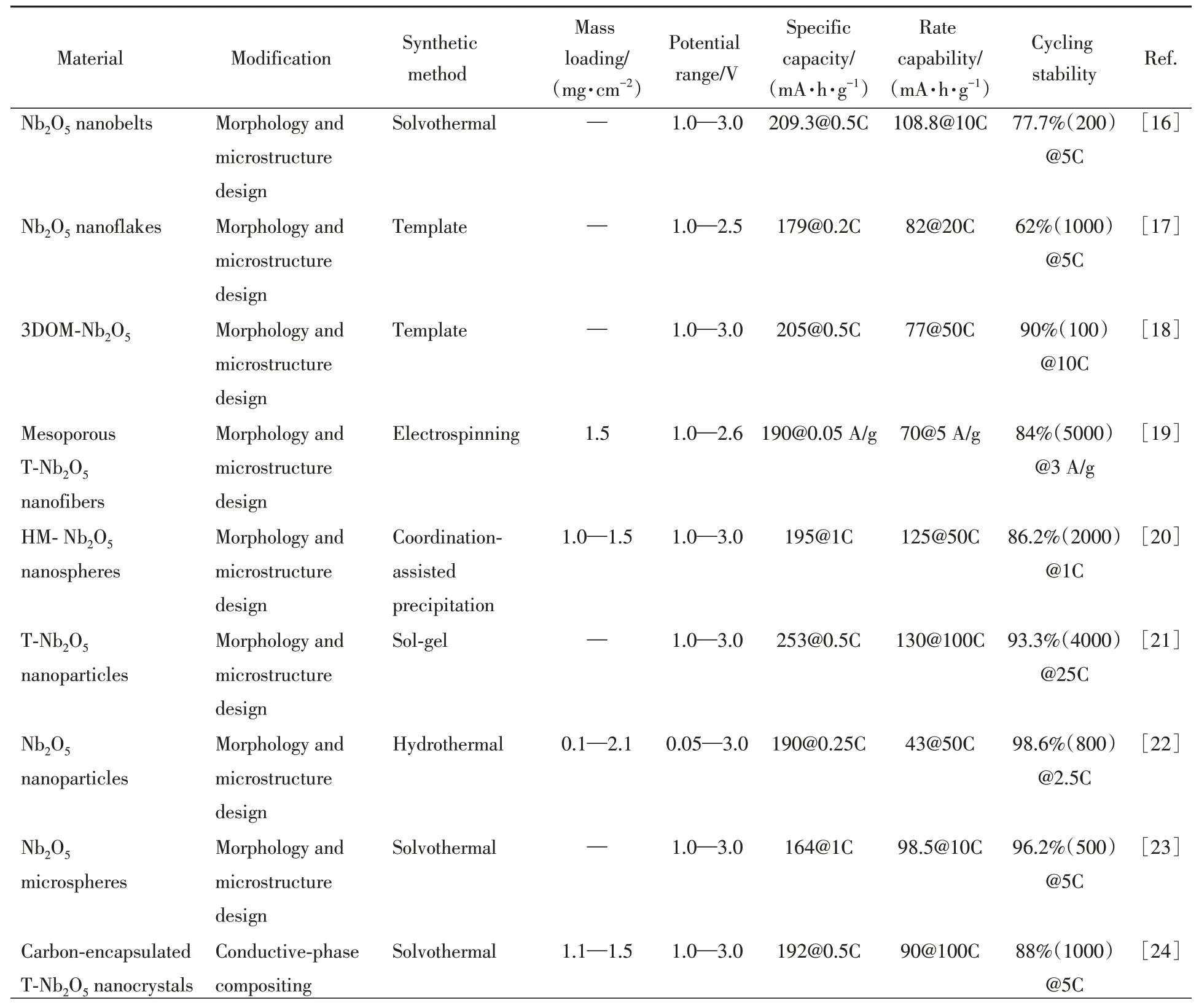
Table 1 Electrochemical performance of niobium-based oxide materials with various modifications
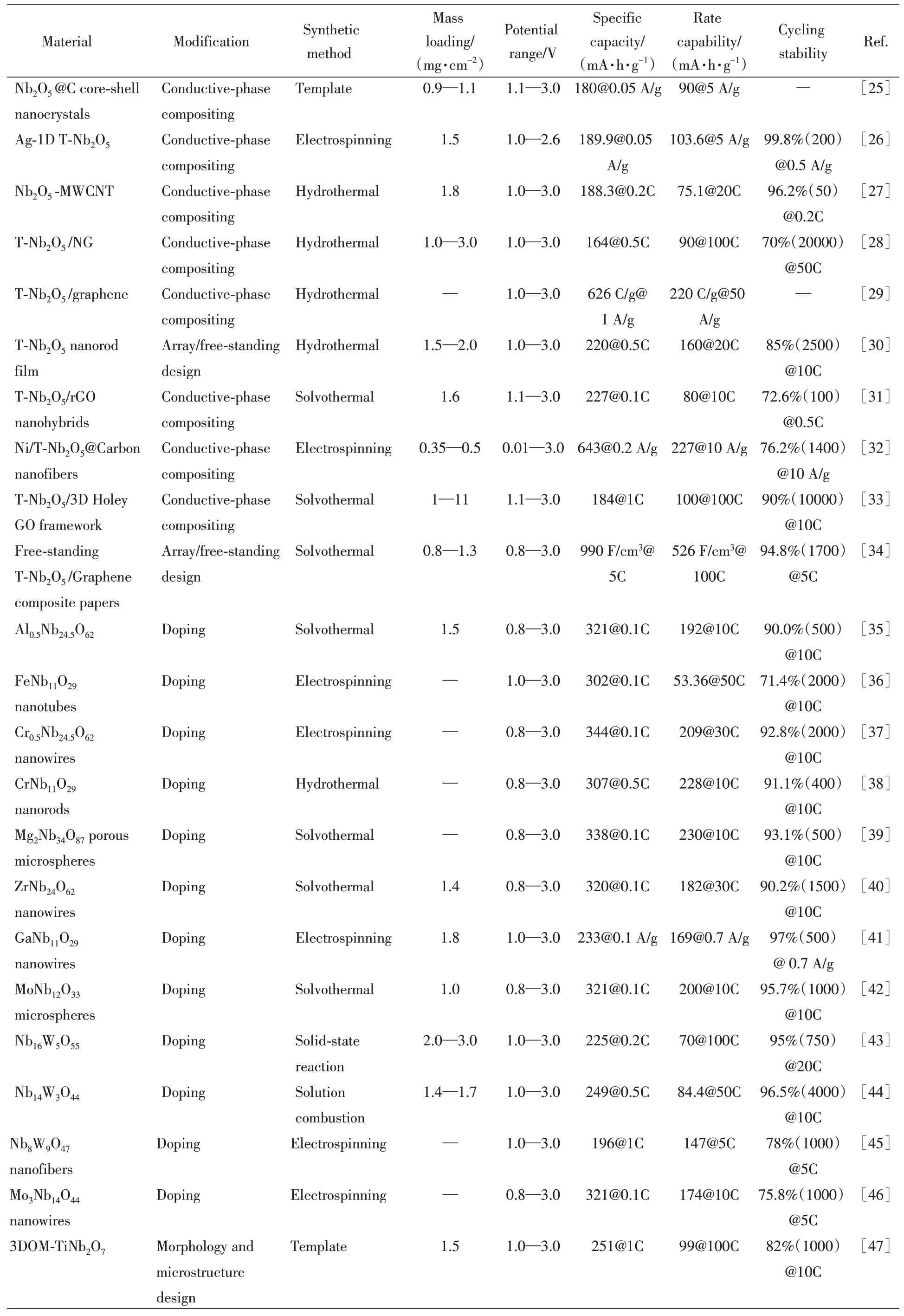
Continued
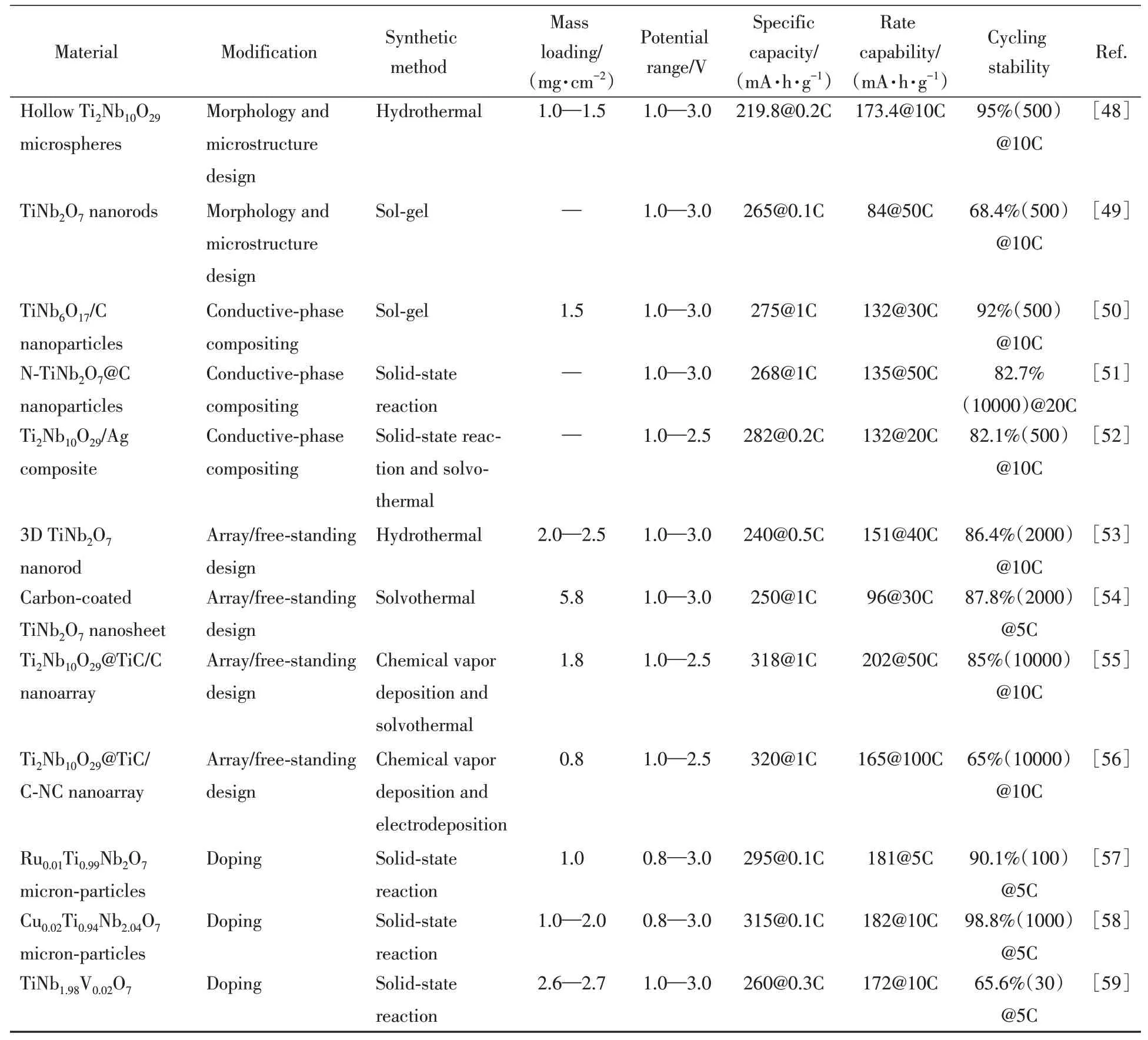
Continued
1 Nb2O5
源于铌元素自身的多化学价态特性,铌氧化物的种类较多,包括NbO(+2价),Nb2O3(+3价),NbO2(+4价)和Nb2O5(+5价).这些氧化铌材料在光催化、金属冶炼和锂离子负极材料领域中具有广阔的应用前景[10,60~63].其中Nb2O5是最常见、最稳定、性能最优的储能氧化铌材料,其在锂离子负极材料领域中的研究也最为广泛.下面将重点介绍Nb2O5的储锂机理与改性方法.
1.1 晶体结构类型与储锂机理
Nb2O5是一种宽禁带半导体材料,具有3.4 eV的禁带宽度,被广泛应用于光催化与电化学储能领域.Nb2O5具有典型的ReO3构型,其独特的层状结构为锂离子的嵌入脱出提供了非常有利的通道;锂离子的快速嵌脱还可在Nb2O5颗粒的表面与内部同时进行.此外,该结构在嵌脱锂的过程中仅伴随微弱的体积变化,因此具有较好的倍率性能与循环稳定性[64,65].
Nb2O5在经过不同温度的热处理后具有不同的晶体结构,随着处理温度的提高,Nb2O5会依次发生以下顺序的晶型变化:TT-Nb2O5(赝六方晶系),T-Nb2O5(正交晶系),M-Nb2O5(四方晶系),H-Nb2O5(单斜晶系)[62,66].不同的晶体结构直接导致了各相Nb2O5储能过程中储锂机制的差异[64].图1展示了3种晶相的Nb2O5晶体结构示意图.T-Nb2O5具有pbam空间群,T-Nb2O5中每个铌原子与6或7个氧原子相邻,NbO6与NbO7多面体通过共角沿c轴排列,构成交替的层间距为0.39 nm的层状结构.M-Nb2O5由4×4块体组成,内部由共享角的八面体连接,边缘由共享边的块体连接.H-Nb2O5的空间群为P2/m,由角共享的NbO6八面体的角堆叠而成,属于具有(3×4)1与(3×5)∞ReO3类八面体的Wadsley Roth晶体剪切构型.晶体内的层板相互偏移(1/2)b,层间距为0.383 nm.在各种晶型中,T-Nb2O5表现出优异的电化学性能,也是目前被广泛研究的Nb2O5电极材料[67~70].
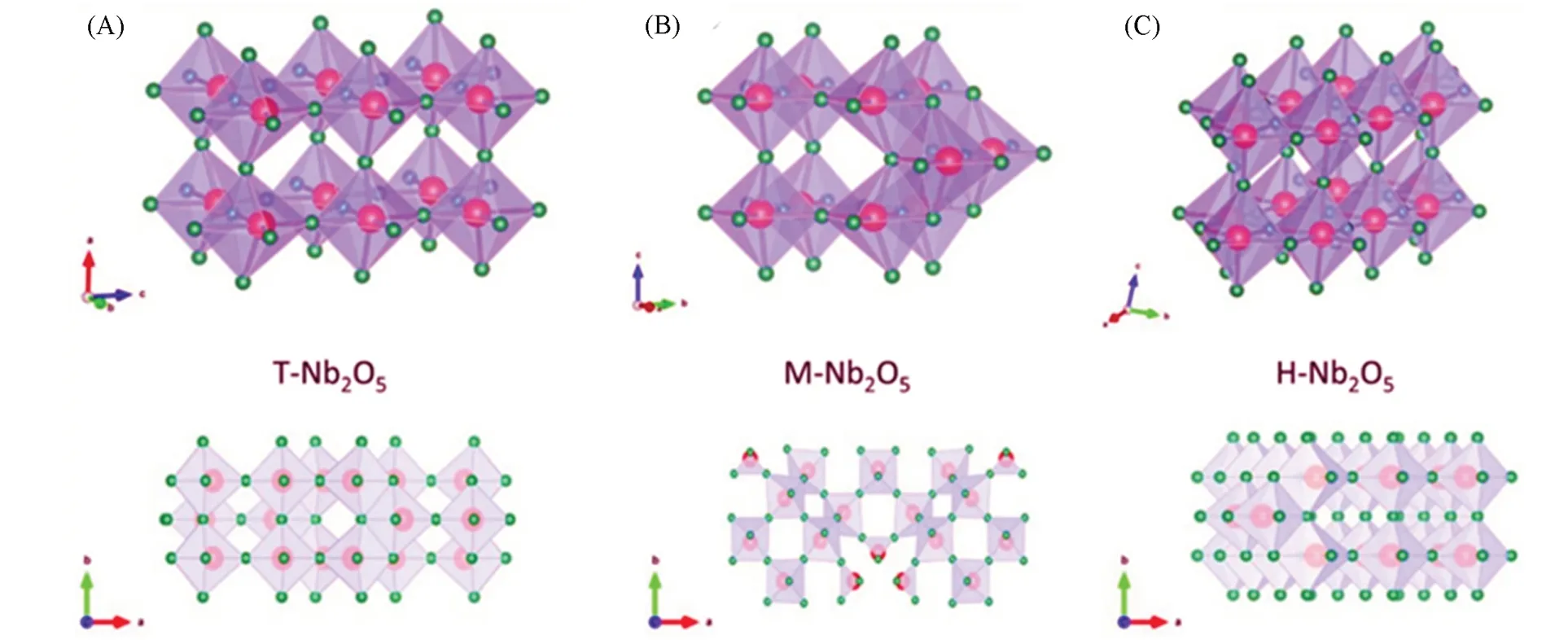
Fig.1 Crystal phase diagrams and the corresponding crystallographic plan views along the c⁃axis[64]
以T-Nb2O5的晶体结构为例,Li+在Nb2O5晶体内的输运与存储机理可以作以下描述.T-Nb2O5是由不规则排布的NbO6与NbO7多面体组成,如图2所示交替的双层晶体结构(4g与4h层).从c轴方向观察,4h层是相对刚性的Nb与O−间隔排列层,4g则是相对松散的O−离子层.随着Li+进入4g层,当Li+位于两个4h层中O−正下方时,会与O−形成桥键.此时,该位置被称为桥接位点[71].理论计算结果也表明,Li+嵌入在桥接点时的吸附能低于非桥接点.此外,拉曼光谱的变化也证明了Li+嵌入/脱出的过程高度可逆[72].Li+在4g层中的扩散路径可分为两种类型:NbOx多面体边共享的路径A与角共享的路径B.两条路径中的低Li+迁移能垒(0.25~0.33 eV)更有利于锂离子扩散.Li+在T-Nb2O5中的快速输运有以下几点优势:(1)0.39 nm的层间距更有利于Li+的传输;(2)桥接位点的存在保证了Li+嵌入后的稳定性;(3)4g层形成的2D传输通道中无阳离子,减少了阳离子对于Li+的静电排斥,加速了其迁移速率[11,71~73].

Fig.2 Lithium storage mechanism diagram of T⁃Nb2O5[71]
1.2 改性策略
虽然Nb2O5独特的结构在锂离子传输中拥有一定优势,但较长的扩散路径、较低的电子电导率(3×10−6S/cm)等在一定程度上阻碍了材料的高倍率性能.通常,高倍率性能与锂离子传输动力学、电子电导率以及电极与电解质界面问题紧密相关.目前已提出大量优化策略解决上述问题,并可归纳为以下几个主要方向.
1.2.1 材料的形貌调控对于传统的微米级Nb2O5材料,锂离子的扩散路径较长,无法满足快速储能的需求.而纳米尺度的电极材料具备更短的离子扩散距离和更大的电化学反应面积,有利于提升锂嵌入/脱出的速率、增加比容量.此外,三维特殊微纳结构的设计也可在保证短的离子路径和高的接触面积的同时,避免纳米材料的团聚,提高电极的振实密度.
均匀分散的纳米颗粒是较为常见的高倍率纳米电极材料.如Liu等[21]通过溶胶-凝胶法合成了兼具超高倍率与循环稳定性的T-Nb2O5−x纳米颗粒.T-Nb2O5−x在0.5C倍率下表现出253 mA·h/g的高比容量,当倍率增加到100C时依然保持130 mA·h/g的比容量,在25C倍率下循环4000次仍具有187 mA·h/g的高可逆容量.另外,一维纳米纤维独特的纵横比则可为Li+传输提供定向的快速路径,从而提升倍率性能.Cheong等[19]制备了直径为200 nm的T-Nb2O5纳米纤维.该纳米纤维具有超长的循环保持率(500 mA/g电流密度下循环2000次后仍有160 mA·h/g的容量)与优异的倍率能力(5000 mA/g时容量约为70 mA·h/g).Shi等[74]则使用软模板法获得了长度50~100 nm与直径25~40 nm的一维Nb2O5纳米棒,展现优异的倍率性能,即便在5000 mA/g电流密度下仍具有120 mA·h/g的容量.与一维纳米结构类似,二维纳米结构可为电子、离子的快速传输与扩散提供连续的载体.此外,二维结构在开放的形貌边缘具有更多存储Li+的位点,提升倍率能力的同时提供更高的比容量.Liu等[16]采用溶剂热法制备了Nb2O5纳米带,所得纳米带在10C倍率下可提供104 mA·h/g的容量.此外,Nb2O5纳米带在5C倍率下循环200次,可逆容量仍为95.8 mA·h/g.Liu等[75]使用水热法合成了结晶性良好的二维Nb2O5纳米片.矩形的互连片层提供了巨大的表面积,扩大了电极和电解质之间的接触,并加速了反应速率,从而获得了良好的倍率性能,在2C和5C倍率下分别提供130和90 mA·h/g的比容量.
大量研究表明,纳米结构设计很大程度提高了Nb2O5电极的电化学性能[10~14].然而,在充放电过程中,常规的纳米电极材料面临着不可控的团聚等关键问题.三维多孔结构则可以在增加界面接触的同时有效避免活性物质的随机团聚,从而获得更理想的性能,有望成为未来超高倍率铌基氧化物的重要发展趋势.Shen等[17]采用膨化大米碳为模板制备由大量交联纳米片组成的三维分层多孔PL-Nb2O5,独特的形貌结构使PL-Nb2O5兼具高比表面积、高离子扩散系数与结构稳定性.在5C和10C倍率下仍分别具有126和103 mA·h/g的高比容量.Lou等[18]则使用聚苯乙烯(PS)微球为模板,通过毛细作用使NbCl5的醇溶液自发地渗透进紧密排列的相邻PS球间的空隙中,去除模板后得到如图3所示的三维有序大孔T-Nb2O5(3DOM-T-Nb2O5).该材料去除PS微球后不仅保持了60~130 nm多孔结构,还获得了因反应过程中气体产生释放所致的直径约为7.6 nm的介孔.独特的形貌与丰富的孔洞使3DOM-T-Nb2O5即便在20C与50C的高倍率下仍具有106与77 mA·h/g的可逆容量.
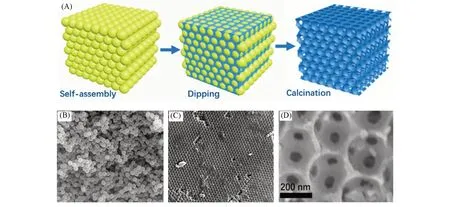
Fig.3 Synthesis route and morphology analysis of 3DOM T⁃Nb2O5[18]
1.2.2 导电材料复合Nb2O5材料的低电子电导率一直是制约其应用的一大难题,尽管有许多的优化策略可提高Nb2O5材料的电子导电性,但相邻Nb2O5颗粒间的电子连通性差仍是快速储能应用中无法避免的关键问题[15].复合导电材料如碳基材料或金属材料等则是较为有效的解决方案,不仅可以提升电导率,同时还可缓解充放电过程中材料的体积变化.
通常,在水热合成过程中加入有机碳源,进行后续热处理即可获得Nb2O5原位复合碳材料.如Yang等[76]通过微波辅助溶剂热法制备了T-Nb2O5@C纳米线,并以此为负极,商用活性炭为正极构建了锂离子混合电容器,能量密度高达60.6 W·h/kg,功率密度为8.5 kW/kg.此外,有机碳源还可以在前驱体合成中发挥诸多作用,包括作为表面活性剂,促进晶体沿择优方向生长与避免纳米材料的自聚集等.Han等[24]通过氯化铌与溶剂苯乙酮的两个单独的缩合反应生成紧密且均匀的氧化铌与1,3,5-三苯基苯(TPB)混合物,并可以通过调节Nb2O5/TPB的比例与加入添加剂来优化退火后的Nb2O5/C复合电极电化学性能(图4,NP-X为Nb2O5/C纳米粒子,NS-X为纳米微球,X代表碳含量).性能最优的NP-10在100C的倍率下比容量约为90 mA·h/g.Lim等[25]通过一种软模板法获得了均匀分散的Nb2O5@C核-壳纳米材料(Nb2O5@CNCs).添加的软模板剂不仅可以有效防止合成过程中Nb2O5颗粒的不可控团聚,还可在后续惰性气氛中热处理后形成碳涂层包覆Nb2O5.碳涂层的包覆提升了材料的倍率能力,在5000 mA/g的电流密度下容量仍达初始容量的50%.
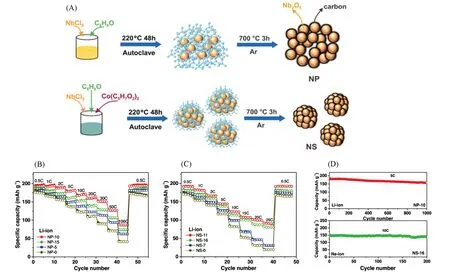
Fig.4 Synthesis diagram and electrochemical performance of NP and NS[24]
石墨烯与碳纳米管(CNT)等也是性能极佳的导电碳材料,Nb2O5材料与石墨烯和CNT复合可构建更有利的电荷传输网络,显著提升其导电性进而优化倍率性能[27~29].Kong等[34]通过水热法获得了T-Nb2O5/rGO复合材料;其中,T-Nb2O5纳米粒子均匀地分散在rGO上.得益于丰富的导电网络和更短的电荷传输路径,制得的T-Nb2O5/rGO复合材料表现出优异的高倍率性能.在1和50 A/g电流密度下,复合材料分别具有626和220 C/g的比容量,显著优于T-Nb2O5材料.Gao等[27]合成的Nb2O5/多壁碳纳米管(MWCNT)复合材料也具有优异的倍率性能,其锂离子迁移率高出纯Nb2O5材料一个数量级,即便在20C倍率下仍保持75 mA·h/g的容量.
除了复合碳材料外,Nb2O5材料还可与导电金属复合以提升导电能力.如Dien等[77]通过静电纺丝法将纳米金粒子分散在Nb2O5纤维上.相比于未改性的Nb2O5纤维,金元素的复合显著提升了材料的电导率与倍率性能.10C倍率下复合金的Nb2O5纤维的容量(132 mA·h/g)远优于纯Nb2O5纤维(53 mA·h/g).类似地,Cheong等[26]也通过静电纺丝法在纳米纤维上复合纳米银来提升Nb2O5材料的倍率性能.
1.2.3 阵列/自支撑结构的设计传统电极通常是将活性物质粉末、导电剂(导电炭黑、乙炔黑等)、黏结剂(聚偏氟乙烯等)混合后涂敷在各类集流体(铜/铝箔)上而成.然而,由于黏结剂不具备电化学活性,对电子的输运会产生一定的阻碍作用.此外,导电剂与黏结剂还占据了电极的体积与质量,降低了器件的能量密度[78].而采用无黏结剂的三维阵列电极材料则可以带来如下优势.(1)阵列电极采用阵列与基底间强有力的化学作用力替代传统电极中不良的接触界面,显著降低了接触电阻,在电极上进行高效的电子与离子传输,为高能量密度与功率密度的器件提供了合理的解决方案;(2)阵列材料存在有序与丰富的孔结构与间隙,更有利于电解液与活性材料充分接触并缓解充放电过程中结构的体积变化,从而提升电极的比容量与循环性能;(3)阵列结构还可以搭配柔性基底适应各种形变,避免传统电极在形变过程中产生的龟裂脱落[79].
2018年,我们课题组[30]通过简易水热法,以氯化铌改性后的碳布为载体制备了不含黏合剂和导电剂的T-Nb2O5纳米棒薄膜,并以此搭配活性炭正极组装了锂离子混合电容器(图5).独特的阵列结构提供了电子传输的直接通道并缩短了离子扩散距离,展现出优异的倍率能力.此外,碳布的可弯折性能赋予了器件柔性,即便在各种角度弯折仍可以正常工作.该柔性器件的能量密度和功率密度分别为95.55 W·h/kg和5350.9 W/kg.Kong等[34]采用溶剂热法合成了一种T-Nb2O5/石墨烯复合自支撑材料,进一步通过真空过滤与热处理实现石墨烯层与层的交错堆叠,获得具有均匀纳米孔道、无黏结剂与导电剂的T-Nb2O5/石墨烯自支撑电极.该自支撑电极不仅在100C的高倍率下仍具有526 F/cm2的高比容量,同时拥有一定的柔韧性与良好的循环寿命(5C倍率下循环2000次仍有93%的容量保持率).
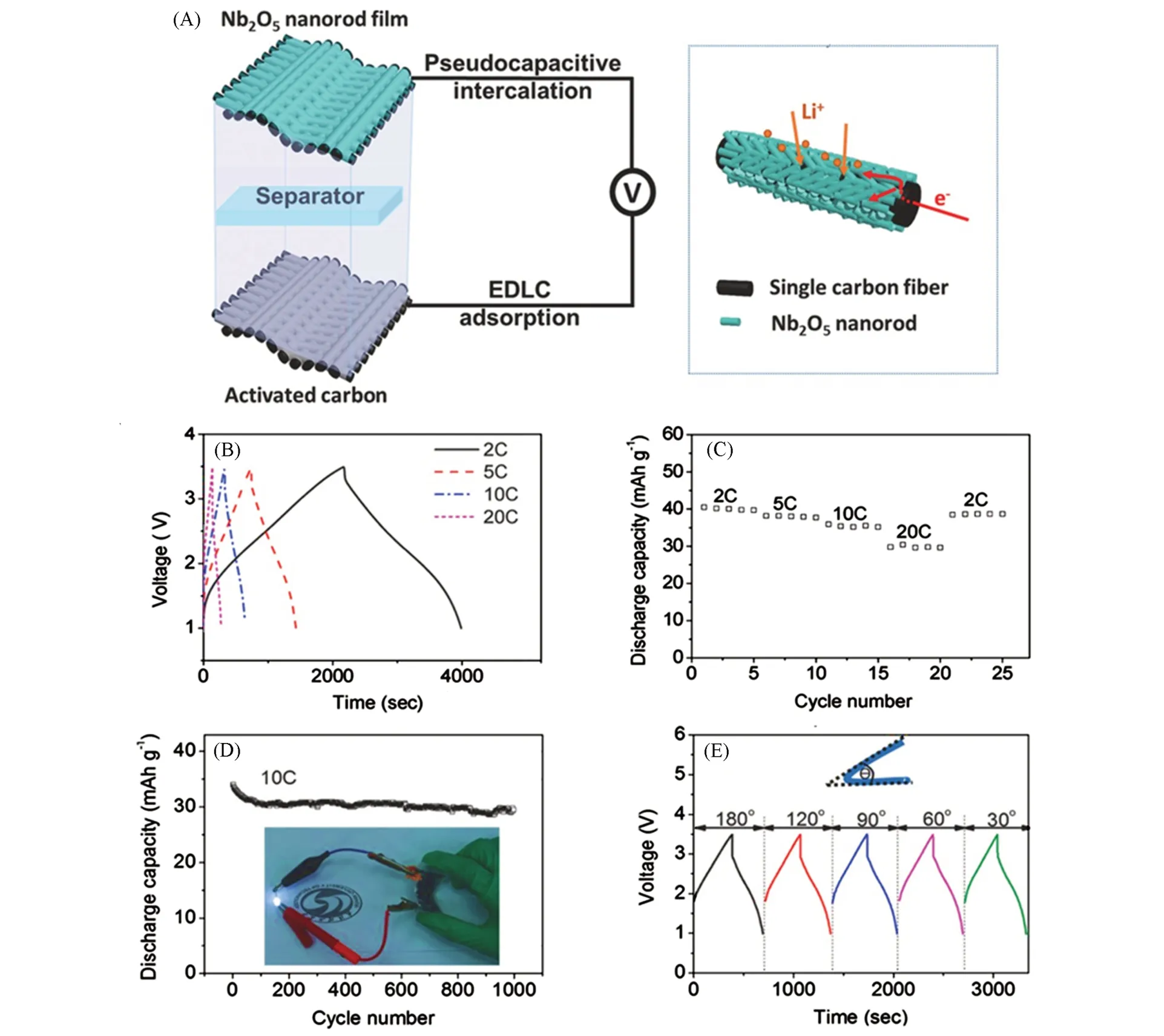
Fig.5 Schematic illustration of device configuration and electrochemical performance of Nb2O5 nanorod films[30]
1.2.4 异质离子的掺杂Nb2O5具有ReO3剪切晶体结构,该晶体结构是开放与稳定的,可在Nb2O5晶体中掺杂异质离子以提升其性能.首先,部分被掺杂的离子具有更轻的原子质量或多价态的氧化还原反应,可提升材料的理论容量.其次,掺杂可以将具有未配对电子的离子引入晶体,从而提高电导率优化倍率性能.此外,还可引入离子尺寸更大的掺杂离子,从而提升晶胞体积并在晶格中产生更宽裕的锂离子扩散路径以优化倍率性能.
目前已经有多种异质离子掺杂在高倍率氧化铌锂离子储能领域的研究[35~46],如Al-Nb-O,Cr-Nb-O,Fe-Nb-O,W-Nb-O等.Al是一种经济且原子质量低的元素,当Al原子部分替代Nb原子时不仅可以降低整体电极的原料成本,更可显著提高Nb2O5的理论容量,同时Al—O键的超高键能(511 kJ/mol)增强了Al-Nb-O材料的结构稳定性并提升了其循环性能[35].Fu等[35]使用溶剂热法合成了多孔微球状的Al0.5Nb24.5O62-P(ANO-P).微量Al元素的掺杂使得ANO-P材料在0.1C倍率时的比容量提升至321 mA·h/g,并提高了材料的锂离子扩散系数与结构稳定性,展示出卓越的倍率性能和循环稳定性[图6(A)~(C)].ANO-P即便在10C倍率下仍有192 mA·h/g高比容量且循环500次后容量保持率为90%.

Fig.6 Crystal structure,SEM image and rate performance of various M⁃Nb⁃O
同样,选择经济且环保的金属掺杂元素,Zheng等[36]使用静电纺丝法制备了Fe掺杂的FeNb11O29(FNO)中空纳米管[图6(D)~(F)].FNO在1C与10C的倍率下循环2000次容量仍为175.8 mA·h/g(单次循环的损失率仅为0.012%)与101.3 mA·h/g.得益于Fe元素掺杂与中空纳米管结构的协同效应,FNO材料的锂离子扩散系数优于传统Nb2O5材料几个数量级,高达2.51×10−12cm2/s.Zheng等[36]也从晶体结构的角度对FNO储锂过程进行了分析.如图6(D)所示,在充电过程中,FNO的晶体结构经历了从类型Ⅰ至Ⅳ的变化,结合原位XRD测试分析,FNO在完全充电时材料体积变化仅为6.9%,并可在充电过程中观察到相反的相变,表明FNO在电化学过程中具有高度可逆的晶体结构.Lou等[80]则报道了在引入3.8%的氧空位后制备的FeNb11O27.9具有比FeNb11O29更大的单位晶胞体积,更有利于锂离子在晶体结构中的运输.
为了进一步提升M-Nb-O材料的电导率,掺杂含未配对电子的Cr3+的研究也被广泛报道[37,38].如Guo等[37]通过静电纺丝法在Nb2O5中掺杂Cr3+,制备了电导率高达3.6×102S/cm的Cr0.5Nb24.5O62纳米线[图6(G)~(I)].Cr3+掺杂不仅带来高可逆容量(0.1C倍率时为344 mA·h/g)与出色的循环稳定性(10C倍率下1000次循环后仍有92.8%的容量保持率),更提升了Cr0.5Nb24.5O62材料的导电性与高倍率能力(倍率提升至30C,仍具有209 mA·h/g的高容量).其它Cr-Nb-O材料也具有较好的电化学性能,如高导电CrNb11O29纳米棒在0.1C和10C的倍率下分别具有344和228 mA·h/g的高可逆容量[38].
掺杂半径大的离子,则有利于提升晶胞体积、提供更宽裕的锂离子扩散路径以优化倍率能力.Mg2+的离子半径为0.072 nm,显著大于Fe3+和Cr3+等离子,因此Mg2Nb34O87具有更大的晶胞体积与锂离子扩散系数.可在0.1C与10C倍率下提供338与230 mA·h/g的高可逆容量,即便10C倍率下循环500次仍有93%的容量保持率.通过分析其循环伏安曲线,计算出在1.1 mV/s的扫描速率下,掺杂Mg2+的Mg2Nb34O87赝电容行为贡献率高达87.7%[39].Zr4+与Mg2+离子半径相近,ZrNb24O62也作为一种理想的锂离子储能材料受到关注.Yang等[40]报道了一种Zr4+掺杂的多孔ZrNb24O62纳米线材料展示出优异的倍率特性(30C倍率下为182 mA·h/g)与循环稳定性(10C倍率下循环1500次容量保持率为90%).除了上述M-Nb-O电极,其它掺杂元素如Ga,Mo,Cu,Zn,Mn,V等也在提升铌基氧化物倍率性能方面展现出良好的效果[81~83].
倍率性能与材料微观结构密切相关.通常,大的颗粒尺寸会延长锂离子扩散的距离进而影响电极材料的倍率性能.然而,Grey等[43]在微米尺度的铌基氧化物高倍率锂离子储能领域仍取得重大突破,他们报道的两种微米级W-Nb-O(Nb16W5O55与Nb18W16O93)均具有卓越的电化学性能,其原因可归纳为以下几点:(1)W6+到W4+的多电子氧化还原反应带来的高理论容量;(2)晶体中心的锂离子传输通道的密度较高,锂离子在中心的扩散速度比边缘位置的扩散速度更快;(3)金属离子与氧离子的三维连接结构提供了有效的电子通道,因而具有出色的导电性.这些优势使得即便是微米尺寸的W-Nb-O材料,仍具有出色的高倍率能力.Nb16W5O55材料在20C与100C的超高倍率下仍分别具有148与70 mA·h/g的高比容量;在10C倍率下循环250次后容量保持率为95%,而后在20C的倍率下循环750次也具有95%的容量保持率[43].
Grey等[84]使用第一性原理密度泛函理论计算并分析了3种W-Nb-O材料(Nb12WO33,Nb12W3O44与Nb16W5O55)的储能机理.晶体剪切相导致内部电子局部化,从而限制了嵌段结构对电子的影响,从而展示出良好的电子传导性.此外,通过消除Li+嵌入过程中的八面体畸变,可以缓冲整体体积的膨胀.因此,即使是微米级的铌钨氧化物,也具有良好的循环稳定性与倍率性能.此后,通过简易的溶液燃烧法,Yang等[44]合成的微米尺寸的Nb14W3O44表现出优越的循环性能和倍率能力(10C倍率下循环4000次比容量仍达130 mA·h/g).Shu等[85~88]则通过静电纺丝法合成了一系列的Nb-W-O材料(如Nb8W9O47,Nd10W22O81,Nb12WO33,Nb18W16O93,Nb60WO153等),均展现出良好的电化学性能与应用潜力.
2 TiNbxO2+2.5x
Ti的原子半径为0.2 nm,与Nb(0.208 nm)十分相近,将氧化铌与氧化钛粉末按比例混合后,高温煅烧即可制备TiNbxO2+2.5x.TiNbxO2+2.5x系列材料也具有较高的工作电压,可抑制SEI膜与锂枝晶的形成,确保电池具有优异的安全性能.TiNb2O7(TNO)(x=2)属于单斜晶系(空间群C2/m;晶胞参数a=2.0351 nm,b=0.3801 nm,c=1.1882 nm,β=120.19°).在NbO6与TiO6八面体共享角与边缘的单斜结构中,位于八面体中心位置的钛与铌原子随机分布,而层状结构中存在的2D间隙则为每个单元式提供多达5个锂离子的存储空间.TNO的5电子电化学反应(Ti4+/Ti3+,Nb5+/Nb4+和Nb4+/Nb3+)赋予材料高达388 mA·h/g的理论容量.与TNO类似,Ti2Nb10O29(x=10)和Ti2Nb24O62(x=24)的理论容量也分别可以达396和401 mA·h/g.
早在1952年,TiNbxO2+2.5x便作为核工程应用的难熔氧化物被首次报道,但其首次作为锂离子储能材料被报道却在30年后的贝尔实验室[14].1983年,Cava等[89]首次研究了TNO中锂的嵌入与脱出,并报道了其在1.4~3.0 V电压范围内的电化学锂化行为.结果发现,在锂嵌入和提取的电化学过程中,晶体结构保留完好(体积变化仅为3.6%).受到当时尖晶石Li4Ti5O12研究与层状嵌入式二硫化物等材料研究的影响,TiNbxO2+2.5x材料在锂离子储能领域的进展罕有报道.在TiNbxO2+2.5x电化学储能研究中断近30年后,Goodenough与其团队[90]于2011年重新点燃了TiNbxO2+2.5x锂离子储能研究的热潮.
2.1 储锂机理
以TNO为例,其锂化机理如图7所示[91].在嵌锂过程中,外部Li+首先逐渐占据4i(1)和4i(2)位置.当这两种八面体位置被完全占据时,形成Li0.88TiNb2O7,该反应为固溶反应.在4i(1)和4i(2)位点被锂离子完全占据后,会发生两相转变.进行第2步时,已占据4i(1)位点的Li+不断移动到4i(3)和4i(4)位点.与此同时,后续嵌入的外部Li+通过4i(1)位点后占据4i(3)和4i(4)位点,最后逐渐占据4i(1)位点.在第3步中,一旦4i(1)位点再次被锂离子完全占据,处于4i(1)和4i(2)位点的Li+同时转移到4i(5)位点,随后更多的外部Li+被嵌入到4i(1)和4i(2)位点.同时,4i(3)位点的Li+迁移到8j位点.完全锂化后得到的最终产物为Li4TiNb2O7.

Fig.7 Lithiation process of TiNb2O7 during discharging[91]
2.2 改性策略
虽然TiNbxO2+2.5x有许多优点,但由于Ti4+和Nb5+离子都处于最高价态,不含自由的3d/4d电子,所以TiNbxO2+2.5x是一种绝缘体.此外,TiNbxO2+2.5x较低的锂离子扩散系数也很大程度限制了其在高倍率下的应用.因此,提高TiNbxO2+2.5x的电子与离子传输速率对于实际高倍率应用是非常必要的.迄今,TiNbxO2+2.5x的大部分研究也集中在通过各种方法去优化其倍率性能上,包括形貌结构控制、导电材料复合、阵列/自支撑电极设计以及异质离子掺杂等.旨在提高TiNbxO2+2.5x材料的比容量、安全性、循环稳定性和倍率性能,从而满足储能领域的高能量密度、高安全性、长循环寿命和高功率密度4项关键要求.
2.2.1 形貌调控三维多孔结构具有更大的比表面积、快捷的离子输运通道,同时可有效避免活性物质的随机团聚,从而有望获得更理想的倍率性能.Lou等[47]使用去模板法合成了高度有序的三维大孔TiNb2O7(3DOM-TNO),该材料具有均匀、连续的蜂窝结构,提供了离子快速输运通道.独特的结构特性使3DOM-TNO在20C,50C和100C倍率下分别展现出135,120和99 mA·h/g的比容量,同时在10C的高倍率下循环1000次仍具有82.3%的容量保持率.Sun等[48]通过改进的模板辅助水热法,在聚合物微球的形成过程与后续的热解过程中原位截留了Ti与Nb,从而合成了高度均匀的Ti2Nb10O29空心微球.中空且多孔的结构更有利于电解液渗透电极材料,并提供了更高的电化学反应面积.Ti2Nb10O29空心微球在0.2C倍率时,首次库伦效率高达95.3%,并拥有250.8 mA·h/g的比容量,显著高于同等条件下实心微球的213.9 mA·h/g;在50C倍率下比容量为103.7 mA·h/g,在10C倍率下循环500次仍有95%的容量保持率.
Ise等[92]分别合成了H-TiNb2O7(H-TNO)与S-TiNb2O7(S-TNO),并使用X射线吸收精细结构谱(XAFS)对两种材料进行了分析(图8).两种TNO电极Ti和Nb的XANES结果显示,随着充放电过程中锂的嵌入,晶体结构并未发生改变.同时Ti和Nb的边缘能量随着锂插入量的增加而同时移动,这些结果均与以前的报道[90]吻合.但H-TNO电极在单位TNO锂嵌入量大于4.0的范围内同时发生Ti和Nb的线性边缘漂移,这是由于当锂嵌入量大于4.0时,H-TNO中Li+离子含量的增加从而表现出电荷补偿.该结果表明,H-TNO的附加容量是基于锂插入TNO晶体位点引起的氧化还原反应.

Fig.8 Electrochemical performance and XANES spectra of H⁃TNO and S⁃HTO[92]
2.2.2 导电材料复合TiNbxO2+2.5x材料导电性差的缺点显著限制了其倍率性能.采用导电材料进行复合可合理改善其导电性,优化倍率性能.Sun等[50]制备了原位无定型碳包覆的TiNb6O17/C纳米晶,并与纯TiNb6O17进行比较.结果表明,原位生成的无定型碳可增加电子电导率并将材料粒径从约100 nm减小至约50 nm.在高倍率电流密度下的性能表现更是显著提升,30C的高倍率下TiNb6O17/C的比容量仍高达132 mA·h/g,约为无碳包覆的TiNb6O17材料的两倍.而在10C的高倍率下循环保持率也远超无碳包覆的TiNb6O17材料,次均容量衰减率仅为0.016%.通过将固相合成的TiNb2O7包覆双氰胺后退火,Gao等[51]制备了高性能的表面氮化碳包覆TiNb2O7(N-TNO@C).碳涂层的包覆形成了良好的导电网路,改善了TNO粒子间的接触界面,N掺杂的引入则通过还原Nb5+形成了带有未成对电子的Nb4+,显著提升了复合材料的电子电导率;与此同时,碳包覆还改善了TNO的结构稳定性.最终,N-TNO@C电极在50C的超高倍率下展现出135 mA·h/g的比容量,并在10C的倍率下循环1000次仍有82.7%的容量保持率.
除了常见的包覆碳材料,修饰导电金属(如Ag等)也可大幅提升材料的整体性能.最近,Mao等[52]通过将少量硝酸银与Ti2Nb10O29颗粒混合后进行溶剂热反应,制备了银纳米粒子均匀分布在TNO表面的Ti2Nb10O29@Ag.与未复合Ag的Ti2Nb10O29材料相比,Ti2Nb10O29@Ag具有更出色的倍率能力与循环稳定性,在10C的高倍率下提供173 mA·h/g的高容量,同时在10C倍率下循环500次后依然保留142 mA·h/g的容量,约为纯Ti2Nb10O29材料的两倍(68 mA·h/g).
2.2.3 阵列/自支撑结构阵列/自支撑结构不仅优化了活性物质与集流体的接触界面,提供了直接的电子输运通道,同时也能有效地缩短离子的扩散路径.最近,我们[53,54]报道了多种TNO阵列电极在柔性快速锂离子储能器件领域的研究,其中一种柔性自支撑纳米片TiNb2O7阵列(TNO NSAs)载量最高可达10 mg/cm2[图9(A)和(B)].使用活性物质载量为5.8 mg/cm2的TNO NSAs阵列电极搭配锂金属电极进行半电池测试时,10C的高倍率下仍具有189 mA·h/g的比容量,5C倍率下循环2000次仍有87.8%的容量保持率.与高电压LiNi0.5Mn1.5O4正极搭配组装成的3 V柔性全电池器件即便在各种角度的弯折情况下仍可以正常工作,并展现高达229 W·h/kg的能量密度和1860 W/kg的功率密度[54].
2018年,Yao等[55]采用化学气相沉积法在Ti6Al4V网上制备了TiC/C核壳阵列,然后利用溶剂热与氩气高温退火法将Ti2Nb10O29纳米颗粒沉积在TiC/C骨架上得到了Ti2Nb10O29@TiC/C,最后将Ti2Nb10O29@TiC/C浸泡盐酸多巴胺溶液后于氮气中高温退火成功包覆了氮掺杂的碳层,获得了NCTi2Nb10O29@TiC/C核壳阵列[图9(C)~(F)].TiC/C骨架与NC涂层协同构成的全方位导电网络极大地促进了阵列电极的电子运输与结构稳定,同时通过理论计算也证明氮元素的掺杂降低了锂离子运输的能垒.该阵列电极在50C倍率下仍具有202 mA·h/g的超高比容量,在10C倍率下循环10000次后容量保持率达85%,同时NC-Ti2Nb10O29@TiC/C//LiFePO4全电池展现出2 kW/kg的高功率密度.
采用类似的合成方法,Yao等[56]于2020年报道了一种氧空位协同氮掺杂优化的阵列Ti2Nb10O29@TiC/C-NC.Ti2Nb10O29中的氧空位与氮掺杂可以起到减小带隙与扩大晶格的作用,同时提高了电子与离子传输速率.这种内外协同策略共同加速了反应动力学,实现了半电池测试下的超长循环寿命与卓越的高倍率能力(液态半电池100C的超高倍率下容量为108 mA·h/g,固态半电池40C倍率下容量达108 mA·h/g).最后,还分别在液态电解质与固态电解质中搭配LiFePO4正极材料进行了器件展示.液态器件在20C倍率下循环2000次仍有约100 mA·h/g的比容量,固态器件在50C的高倍率下比容量仍保持91 mA·h/g.此研究为高倍率锂离子储能器件的设计提供了参考,同时阵列与固态电解质复合设计的策略也为解决固态电池的界面问题提供了新的思路[56].但该阵列结构复杂的合成过程增加了制备成本,一定程度限制了其未来商业化的发展.
2.2.4 异质离子掺杂2011,Goodenough等[90]报道了通过溶胶-凝胶法合成的TNO与固相合成的n型掺杂的并且通过在氩气中退火蔗糖包覆的材料合成了碳包覆的C-TNO与C-DTNO.他们使用10%的Nb(IV)替代了Ti(IV),将导电性差的TNO转变为导电良好的DTNO.并验证了碳的包覆不仅提高了复合材料的电导率,也有利于稳定Nb(IV)的价态.C-DTNO还具有不对称的电化学行为,半电池对称充电/放电循环测试的倍率性能可达4C/4C,而不对称循环(快充慢放)测试的倍率性能则高达100C/2C.此后,不断有阳离子掺杂如Ru4+,Mo6+,V5+,Cu2+,以及阴离子掺杂如氮掺杂等研究被报道[56~59].
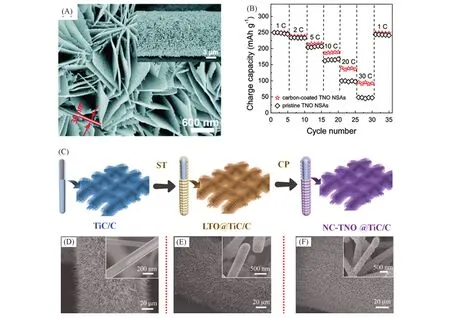
Fig.9 SEM image and rate performance of TNO arrays,synthesis route and morphology analysis of NC⁃TNO@TiC/C
掺杂异质离子通常可以改变材料的电子电导率和/或锂离子扩散速率,甚至调控颗粒尺寸与形貌.Lin等[57]通过在TiNbxO2+2.5x晶格中引入导电的Ru4+离子首次合成了高电导率的Ru0.01Ti0.99Nb2O7(RTNO),其中1%的Ti4+被Ru4+取代.第一性原理的计算结果表明,来自Ru4+的4d电子显著缩小了能带间隙,将RTNO的电子电导率提高至1.01×10−7S/cm.此外,1%的Ru4+掺杂不仅增加了单位晶胞体积、提升了粒子的扩散速率,还有效阻碍了高温过程中的晶粒成长,从而使平均粒径降低了24%,提高了RTNO的倍率性能.RTNO不仅在0.1C倍率时具有295 mA·h/g的容量,即便在5C倍率下仍有181 mA·h/g的容量.Zhao等[93]通过掺杂Mo6+固相合成了MoxTi1−xNb2O7+y,该材料在6 A/g(约40C)的高倍率下仍展现出141.2 mA·h/g的高比容量,搭配LiNi0.5Mn1.5O4正极材料组装的全电池器件拥有高体积能量密度(1338 W·h/L)和功率密度(31200 W/L).
2.3 产业化进展
钛酸锂负极材料凭借其使用寿命长与安全性高等优点,在早年便被商业化生产并投入使用.如日本东芝公司在2008年便推出使用寿命高达15000次的钛酸锂负极制造超级快充锂离子电池产品,但其大规模商业化应用却一直受到钛酸锂负极能量密度较低、产气等缺陷的限制[94].
与钛酸锂材料相比,TiNbxO2+2.5x材料具有更高的比容量,有望在商业高倍率锂离子储能领域中取代石墨与钛酸锂负极[92,94~96].2018年,东芝公司生产了一款额定容量为49 A·h的TNO//LiNi0.6Co0.2Mn0.2O2(NCM)软包电池[96].虽然其体积能量密度(350 W·h/L)与质量能量密度(138 W·h/kg)低于目前最先进的石墨//NCM电池,但TNO//NCM动力电池被设计应用于更高的电流密度与更严苛的温度条件下工作.TNO的高倍率性能导致电池即便在10C的倍率下容量仍保持0.2C倍率时的93%.此外,由于低温下石墨负极缓慢的离子扩散与更易形成锂枝晶等问题,低温环境对于石墨负极是非常大的挑战,这也是目前商用锂离子电池在低温环境中性能不佳的原因之一.但TNO材料在充放电过程中不生成SEI膜与锂枝晶,可以有效解决低温环境带来的问题,即便在−30℃的低温下,TNO//NCM电池的容量保持率仍达室温环境的63%,该研究为商用低温锂离子储能器件的发展奠定了科学基础.
3 总结与展望
铌基氧化物具有高可逆容量、高安全性、高循环稳定性和优异的倍率性能,有望被应用于高倍率和高安全的锂离子储能领域,如城市轨道交通用动力电池和启停备用电源等.理论计算与实验结果也证明,锂离子在大部分铌基氧化物中的嵌入主要受赝电容机制控制,并仅伴随着不明显的相变与轻微的体积膨胀.但是,大部分铌基氧化物的电子电导率很低,这阻碍了其在实际中的应用.为提高其倍率性能,从形貌与结构调控、掺杂等角度研究了诸多性能优化策略.但目前铌基氧化物高倍率锂离子负极材料的研究仍处于初级阶段,若要实现大规模应用,一些关键的问题与挑战仍需进一步探索.
(1)质量能量密度不高.铌基氧化物的高工作电位虽然确保了高安全性,但是牺牲了整个电池的能量密度.尽管目前已有使用高电压的正极材料搭配铌基氧化物以提升整体能量密度的思路,其质量能量密度仍低于以石墨为负极的锂离子储能器件.但值得注意的是,铌基氧化物的密度约为石墨的1.5~2倍.因此,铌基氧化物具有较高的体积比容量,相信未来可在高体积能量密度需求的场景(如微小型储能器件)中得到应用.
(2)电化学反应动力学的控制因素尚不明确.铌基氧化物中,T-Nb2O5表现出无相变的快速锂存储动力学性能,被认为是一种典型的赝电容材料.而其它具有Wadsley-Roth结构的铌基氧化物提供快速的锂存储动力学,却伴随相变与可逆的结构应变.目前尚还不明确铌基氧化物电化学反应动力学的本质控制因素,部分铌基氧化物展示出更高的锂离子扩散系数,颗粒尺寸即便在微米量级也可表现出高速率性能.因此,未来仍然需要继续研究铌基氧化物独特电化学行为的内在机理.
(3)低温性能的研究.温度的变化将对电池性能产生重大的影响,低温时容量大幅降低,Li+的扩散阻抗增加且负极更易形成锂枝晶.而铌基氧化物可避免生成锂枝晶,部分铌基氧化物还具有较高的锂离子扩散系数,可适应低温下急剧增加的Li+扩散阻抗.关于TNO低温性能的研究已有报道[96],但目前鲜有关于其它铌基氧化物在低温环境下的研究,同时其低温储锂机理尚不明确.相信对其低温性能的进一步研究,将对开发宽温域特别是低温环境下的锂离子电池有重大意义.
(4)更高安全性器件的研究.虽然铌基氧化物具有高安全性,但目前大部分锂离子电池使用的都是有机电解液,电解液本身是易燃物,易产生安全隐患.为了进一步提升电池的安全性能,目前已有部分研究采用“盐包水”电解液或固态电解质构建高安全水系或固态锂离子储能器件[97,98].开发更经济与更高安全性的锂离子储能器件仍然是未来的重要挑战之一.
(5)产气问题.铌基氧化物的高工作电压虽提升了安全性,但也一定程度引发了其它问题.高的工作电位避免在活性物质表面生成SEI膜,却也使活性物质表面在充放电过程中与电解液接触,导致电解液与微量水在活性材料表面被还原分解产生H2,CO2和CH4等气体[99].虽然关于铌基氧化物胀气因素与解决方法的研究不断被报道,但是其胀气问题仍未被完全解决.因此,铌基氧化物电化学过程中产气的机理和应对策略仍需进一步探索,以确保铌基氧化物未来能真正大规模应用于储能领域.
(6)更经济的合成路径探索.铌的价格远高于石墨,昂贵的生产成本限制了其商业化的进展.尽管得益于高工作电压,放电过程中集流体铝箔与锂在低电位下发生合金化反应的过程可以有效避免,部分研究已采用铝箔代替铜箔在一定程度上降低了电池的整体生产成本,但仍无法大幅降低铌基氧化物本身的资源成本.因此,探索更廉价的铌源与更绿色经济的合成方法是铌基氧化物未来商业化进程中的重要方向.

