盐析辅助水蒸气蒸馏法提取肉豆蔻精油及其抗氧化和清除亚硝酸盐作用研究
席小辉,宋欠欠,江雨彤,杨晓宇,税 清,秦宇仙,张能飞,李 诚,胡 滨
(四川农业大学食品学院,四川 雅安 625014)
肉豆蔻属于肉豆蔻科,是一种天然香料,主要产自于印度尼西亚、马来西亚等地,我国主要分布在云南等地[1]。肉豆蔻精油是从干燥的成熟肉豆蔻种仁中提取的一种挥发油,含量为5%~8%;其主要成分为萜烯类化合物,如γ-松油烯等;肉豆蔻精油具有抗炎[2]、抗氧化[3]、镇痛、抑菌、保肝、抗癌[4]等多种功效。目前,肉豆蔻精油常作为抑菌剂和天然抗氧化剂被广泛应用于调味品、烘焙食品、肉制品及饮料等食品加工工业中[5]。
精油提取方法包括压榨法、水蒸气蒸馏法、有机溶剂提取法、超临界流体萃取法、微波萃取法、超声波萃取法等。付聪等利用水蒸气蒸馏法提取朝鲜崖柏枝精油,当液料比6.9 mL·g-1、蒸馏时间2.7 h、NaCl质量分数2.6%时,精油得率为4.3%[6]。吴晓菊等利用有机溶剂法提取青金桔籽精油,当以正己烷为提取溶剂,提取时间4 h、提取温度50℃、料液比1:15(g·mL-1)条件下,神香草精油得率为1.093%[7]。Xiong等利用超临界CO2萃取法提取陈皮挥发油,当提取温度45℃、萃取压力14 MPa、萃取时间147 min时,挥发油得率为1.34%[8]。上述方法虽常用于精油提取,但压榨法虽然操作简单,但得率较低,杂质较多,易变质;超临界流体萃取法操作复杂,成本高;有机溶液提取法极易残留有机溶剂等,导致传统方法无法大规模应用。水蒸气蒸馏法是将原料与水共同加热,通过水蒸气带出易挥发油,冷凝回流收集精油,操作简单、设备简易、成本低廉,还可防止精油分解或变质,降低成分馏出温度[9]。研究表明,一定浓度NaCl溶液可提高精油得率[10]。目前,利用盐析辅助水蒸气蒸馏法提取肉豆蔻精油未见报道。
本试验通过单因素试验和响应面试验优化提取工艺,测定肉豆蔻精油基础理化指标、成分分析、结构表征、热力学性质、抗氧化及清除亚硝酸盐能力,以期为肉豆蔻精油进一步开发利用提供参考。
1 材料与方法
1.1 试验材料与试剂
肉豆蔻:购自于广西玉林宏鑫土特产公司,经真空干燥粉碎,过40目筛后密封置于4℃冰箱中备用。
无水硫酸钠、DPPH(1,1-二苯基-2-苦肼基)、无水乙醇、维生素E、酚酞指示剂、TPTZ(2,4,6-三吡啶基三嗪)、氢氧化钾、醋酸盐缓冲液、氯化钠、盐酸、水杨酸-乙醇溶液、冰乙酸、H2O2、三氯甲烷、FeSO4、碘化钾、硫代硫酸钠等试剂,均为分析纯。
1.2 主要仪器与设备
挥发油测定器,上海臻浔金属制品有限公司;电子天平(TE412-L),诸暨市超泽衡器设备有限公司;电热套(20002),上海贝仑仪器设备有限公司;气相色谱-质谱联用仪(7890A-5975C),安捷伦科技有限公司;中草药粉碎机(FW135),天津市泰斯特仪器有限公司;差示扫描量热仪(Q200M DSC),美国TA公司。
1.3 试验方法
1.3.1 水蒸气蒸馏法提取肉豆蔻精油
按照《中国药典》I部(2010年)附录XD方法[11],将20 g肉豆蔻粉末置于500 mL圆底烧瓶,加入300 mL蒸馏水,连接挥发油提取装置,电热套加热沸腾蒸馏5 h后,记录精油体积,按照下式计算精油得率。

式中,V-精油体积(mL);ρ-相对密度(g·mL-1);m-肉豆蔻粉末质量(g)。
1.3.2 盐析辅助水蒸气蒸馏法提取肉豆蔻精油
将20 g肉豆蔻粉末置于500 mL圆底烧瓶,按一定质量比加入氯化钠溶液,连接挥发油提取装置,电热套加热沸腾后蒸馏提取,记录精油体积,按照上式计算精油得率。
1.3.2.1 单因素试验
①液料比对精油得率的影响。设定NaCl浓度为4%,提取时间为3.5 h,测定不同液料比(8:1、10:1、12:1、14:1、16:1 mL·g-1)对得率的影响。
②提取时间对精油得率的影响。设定液料比为12:1,NaCl浓度为4%,测定不同提取时间(2.5、3、3.5、4、4.5 h)对得率的影响。
③NaCl浓度对精油得率的影响。设定液料比为12:1,提取时间3.5 h,测定不同NaCl浓度(2%、3%、4%、5%、6%)对得率的影响。
1.3.2.2响应面优化试验
依据单因素试验结果,选取各因素中肉豆蔻精油得率最高的3个水平,开展响应面试验,优化肉豆蔻精油提取条件。
1.3.3 肉豆蔻精油理化指标测定
测定两种方法提取的肉豆蔻精油理化指标,其中肉豆蔻精油试样准备、相对密度、蒸发后残留物含量、酯值、过氧化值、酸值分别按照GB/T 14454.1-2008《香料试样准备》[12]、GB/T 11540-2008《香料相对密度测定》[13]、GB/T 14454.6-2008《香料蒸发后残留物含量评估》[14]、GB/T 14455.6-2008《香料酯值或含酯量的测定》[15]、GB/T 33918-2017《香料过氧化值的测定》[16]、GB/T 14455.5-2008《香料酸值或含酸量的测定》[17]等标准测定。
1.3.4 肉豆蔻精油成分分析及表征
1.3.4.1 GC-MS分析
将两种方法提取的肉豆蔻精油作GC-MS分析。参考Wang等方法稍作修改[18]。色谱柱HP-5MS毛细管柱(30 m×0.25 mm×0.25 μm),He为载气,流速为1 mL·min-1。起始温度设定为50℃并保持2 min,然后以10℃·min-1速度增至300℃并保持3 min。喷射器和检测器温度分别设置为250和280℃。分流比60:1,进样量1 μL,电离方式EI,电离电压70 eV,离子源温度260℃,扫描质量范围40~800 amu,全扫描。通过检索NIST11数据库阐明肉豆蔻精油化学成分。
1.3.4.2 DSC(差示扫描量热法)分析
将两种方法提取的肉豆蔻精油作DSC分析。称取适量微胶囊于铝坩埚中,盖上坩埚盖,放入样品室,以空坩埚为空白对照,扫描温度范围为100~300℃,程序升温速率为10℃·min-1,氮气流速为10 mL·min-1。
1.3.5 肉豆蔻精油抗氧化性能测定
1.3.5.1 总抗氧化能力测定
参考李嘉欣等方法[19]。取不同质量浓度FeSO4溶液0.1 mL,各加入2.9 mL TPTZ工作液,37℃下反应10 min,测定其在波长为593 nm处吸光度。以吸光度为纵坐标,FeSO4质量浓度为横坐标绘制标准曲线。
分别取0.2 mL不同质量浓度精油溶液于5 mL离心管中,加入3.8 mL TPTZ工作液(0.3 mol·L-1醋酸盐缓冲液,10 mmol·L-1TPTZ溶液,20 mmol·L-1FeCl3溶液以V(醋酸盐缓冲液):V(TPTZ溶液):V(FeCl3溶液)=10:1:1混合,现用现配),37℃下反应10 min,测定其在波长为593 nm处吸光度,以等浓度VE为对照。
1.3.5.2 DPPH·清除率测定
参考Cui等方法[20],利用无水乙醇配制浓度为2、4、6、8和10 mg·mL-1精油溶液,避光保存。取2 mL 0.02 mg·mL-1DPPH-无水乙醇溶液与2 mL精油溶液置于具塞试管中,充分反应,在517 nm处测定吸光度为A,2 mL无水乙醇与2 mL DPPH-无水乙醇溶液吸光度为B,精油与无水乙醇吸光度为C,以上体系均避光反应0.5 h,以VE作为阳性对照。DPPH·清除率按下式计算。
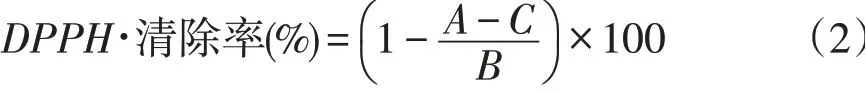
1.3.5.3 羟基自由基清除率测定
参考苏瑾等方法[21]。利用无水乙醇配制浓度为2、4、6、8和10 mg·mL-1精油溶液,取2 mL精油溶液、0.2 mL 8.8 mmol·L-1H2O2溶液、1 mL 9 mmol·L-1水杨酸-乙醇溶液和1 mL 9 mmol·L-1FeSO4溶液,充分混匀,在37℃下水浴30 min,乙醇溶液调零,在510 nm下测定吸光值为A,将精油溶液用无水乙醇代替测定吸光度为B,将H2O2用蒸馏水代替测定吸光度为C。用VE作为阳性对照。羟基自由基清除率按下式计算。
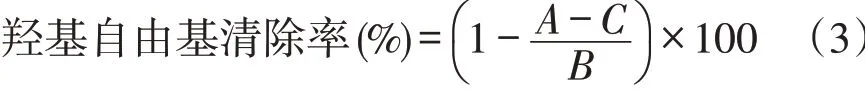
1.3.6 肉豆蔻精油清除亚硝酸盐能力测定
将5 mL 0.5 mol·L-1、pH 3柠檬酸钠-盐酸缓冲液置于10 mL容量瓶中,加入1.0 mL 100 mg·L-1NaNO2溶液,再分别加入0、100、200、300、400、500 μL肉豆蔻精油,定容至刻度,37℃反应1 h。吸取0.4 μL反应液于10 mL容量瓶中,加入0.4 mL 0.4%对氨基苯磺酸溶液,0.2 mL 0.2%盐酸萘乙二胺溶液酸盐,摇匀后放置15 min,用分光光度计在538 nm处测吸光度值,按照下式计算亚硝酸盐清除率:

式中,A-未加精油空白试验吸光值;B-添加不同精油反应液吸光值。
1.3.7 数据处理与分析
每组试验重复3次,试验结果取平均值,运用Microsoft Excel(2010)初步整理数据,响应面设计及结果用Design-Expert 10.0软件处理,SPSS 21.0作显著性分析,采用Origin 9.0绘图。
2 结果与分析
2.1 单因素试验结果与分析
2.1.1 液料比对得率的影响
液料比对得率影响结果如图1所示。

图1 液料比对得率的影响Fig.1 Effect of liquid-solid ratio on the yield
由图1可知,精油得率随液料比增加而呈先升后降趋势,当液料比为12:1时,精油得率最大,为12.35%。液料比为8:1~12:1,得率随液料比增加而增加,可能是因蒸馏水增加导致其与原料接触面积增大,渗入植物细胞中,加热蒸馏水可使植物细胞快速破裂,不断释放精油[22]。此外,传质速率及分子扩散也随液料比增加而不断提高,使提取率增加[23]。当液料比继续增加时,得率下降,可能因溶剂过多,精油在水中溶解度增加,导致得率减小。因此,选择液料比为12:1较适宜。
2.1.2 提取时间对得率的影响
提取时间对得率影响结果如图2所示。

图2 提取时间对得率的影响Fig.2 Effect of extraction time on the yield
由图2可知,随提取时间增加,得率呈先增后减趋势。在提取时间2.5~3.5 h范围内,得率随提取时间增加而升高,因蒸馏水浸润肉豆蔻粉末过程中,精油不断蒸出,得率提高。当提取时间为3.5 h时,得率最大。随提取时间继续增加,得率则显著降低,可能因精油长时间暴露于高温导致某些有效成分损失[24]。此外,原料中精油随时间增加而逐渐减少,且精油易挥发,提取后期挥发损失速率高于出油率,导致得率降低。因此,选择提取时间3.5 h较为适宜。
2.1.3 NaCl浓度对得率的影响
NaCl浓度对得率影响结果如图3所示。
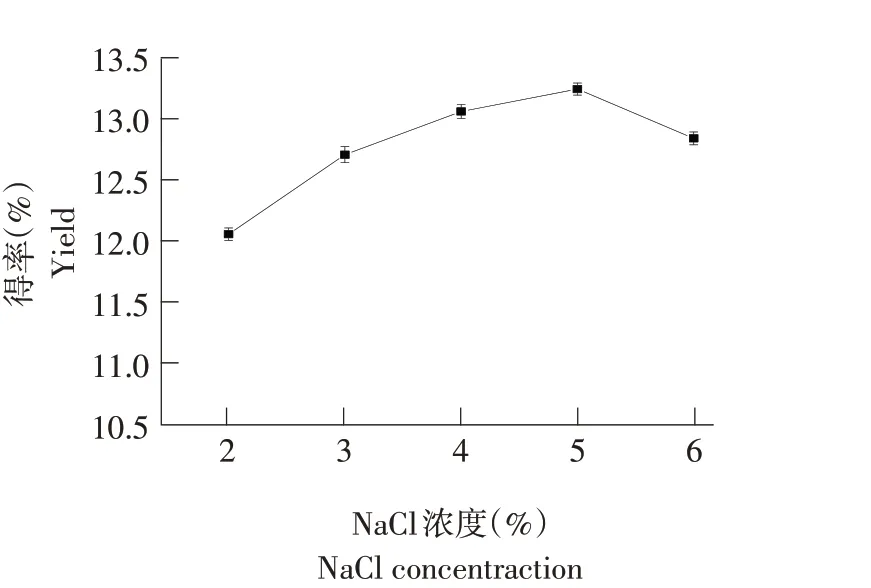
图3 NaCl浓度对得率的影响Fig.3 Effect of NaCl concentration on the yield
由图3可知,随NaCl浓度增加,得率先增后减。在蒸馏水中加入适量NaCl可提高精油得率,因NaCl可增加原料组织细胞内外渗透压,使油脂类物质更易渗出[25],NaCl浓度为2%~5%,得率随NaCl浓度升高而增加;NaCl浓度为5%时,得率最高,达13.26%;NaCl浓度高于5%时,得率呈下降趋势,可能因过高NaCl浓度使精油在蒸馏水中溶解度降低,随水蒸气蒸馏出精油量减少,得率降低。此外,过量NaCl更易引起爆沸,精油中挥发性强成分损失增加,导致得率下降[26]。
2.2 响应面试验结果与分析
2.2.1 响应面模型建立
根据单因素试验结果,建立响应面模型,以A(液料比)、B(提取时间)及C(NaCl浓度)3个因素为自变量,以得率为响应值,按照Design-Expert 10.0软件中Box-Behnken Design(BBD)设计响应面试验(Response surface methodology,RSM),各因素具体取值和RSM结果见表1。

表1 BBD设计及结果Table 1 Experiment design and results of BBD
采用Design-Expert 10.0软件分析表1试验结果,得出得率与液料比、提取时间和NaCl浓度二次回归方程模型:
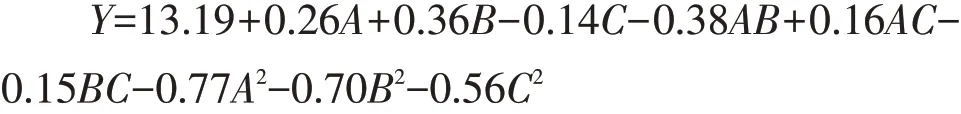
2.2.2 响应面模型显著性检验
对二次回归方程模型作方差分析,结果见表2。P值表示自变量对响应值显著程度的影响,P值越大,显著性越小;反之,则显著性越大。
由表2可知,该模型中R2为0.9958,R2Adj为0.9905,均接近于1,表明该模型拟合度较高。对回归方程系数进一步显著检验可知,A、B、AB、A2、B2、C2对试验结果影响极显著(P<0.01),C、AC、BC对试验结果影响显著(P<0.05),说明试验因素对响应面影响为二次抛物线关系,存在最大值。因此,该模型可用于预测肉豆蔻精油得率。

表2 回归方程方差分析Table 2 Variance analysis of regression equation
2.2.3 各因素间交互作用响应面分析
各因素间交互作用响应面结果如图4所示。

图4 两因子交互作用对得率影响响应面Fig.4 Response surface of the effects of interaction of two factors on yield
由图4a可知,当NaCl浓度固定在中心点,提取时间一定时,得率随料液比增加先增后减。当料液比一定时,得率随提取时间增加先升后降。因此,料液比和提取时间对得率存在极显著交互作用。
由图4b可知,当提取时间固定在中心点,NaCl浓度一定时,得率随料液比增加先增后减。当料液比一定时,得率随NaCl浓度增加先升后降。因此,料液比和NaCl浓度对得率存在显著交互作用。
由图4c可知,当料液比固定在中心点,NaCl浓度一定时,得率随提取时间增加先增后减。当提取时间一定时,得率随NaCl浓度增加先升后小幅降低。因此,提取时间和NaCl浓度对得率存在显著交互作用。
2.2.4 验证试验
采用Design-Expert 10.0软件预测回归方程模型,获得较优肉豆蔻精油提取工艺为:液料比12.19:1、提取时间3.62 h、NaCl浓度2.85%,理论得率为13.25%。考虑到试验可操作性,将精油提取工艺修正为:液料比12:1、提取时间3.6 h、NaCl浓度3%,对修正后条件作3次试验,平均得率为13.27%,与预测值接近,说明该模型可预测试验结果,具有较好应用价值。
2.3 两种提取方法提取肉豆蔻精油得率的比较
两种提取方法提取肉豆蔻精油得率比较如表3所示。
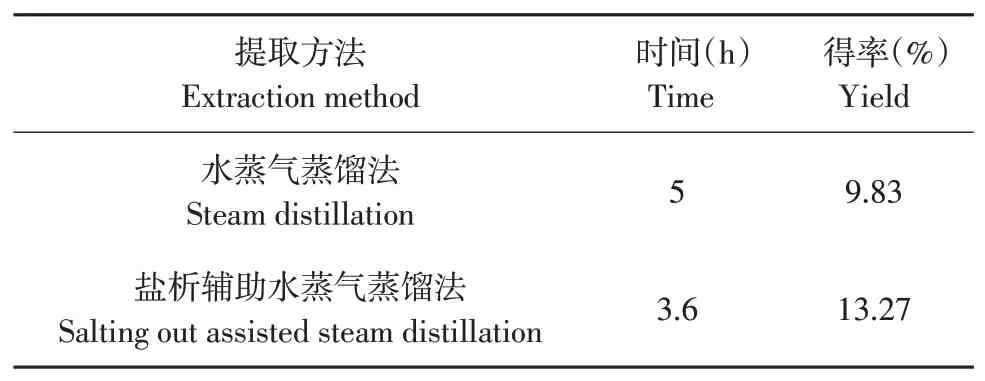
表3 两种提取方法提取肉豆蔻精油得率比较Table 3 Comparison of yield of nutmeg essential oil by two extraction methods
由表3可知,水蒸气蒸馏法提取肉豆蔻精油5 h,得率达9.83%;盐析辅助水蒸气蒸馏法提取肉豆蔻精油3.6 h,得率达13.27%,表明盐析辅助水蒸气蒸馏法可有效提高肉豆蔻精油得率,缩短提取时间,有效节约成本。因此,盐析辅助水蒸气蒸馏法具有较好适用性。
2.4 肉豆蔻精油理化特性分析
由表4可知,水蒸气蒸馏法和盐析辅助水蒸气蒸馏法提取肉豆蔻精油基础理化指标相似,表明盐析辅助水蒸气蒸馏法未对肉豆蔻精油产生影响。肉豆蔻精油感官品质较好,无色透明,具有典型肉豆蔻香辛料味;在20℃时,密度约在0.9,处于正常范围;蒸发后残留物约1.6%,表明肉豆蔻精油挥发性强;酸值可反应精油抗氧化能力和质量,酸值越高,精油质量越差,抗氧化能力越低,肉豆蔻精油酸值均<1.2 mg KOH·g-1,具有良好抗氧化性;肉豆蔻精油过氧化值较低,表明精油质量较好。

表4 肉豆蔻精油理化指标及感官品质Table 4 Physical and chemical indices and sensory quality of nutmeg essential oil
2.5 肉豆蔻精油成分分析及表征
2.5.1 GC-MS分析
利用气质联用仪对肉豆蔻作成分分析,总离子流图见图5。
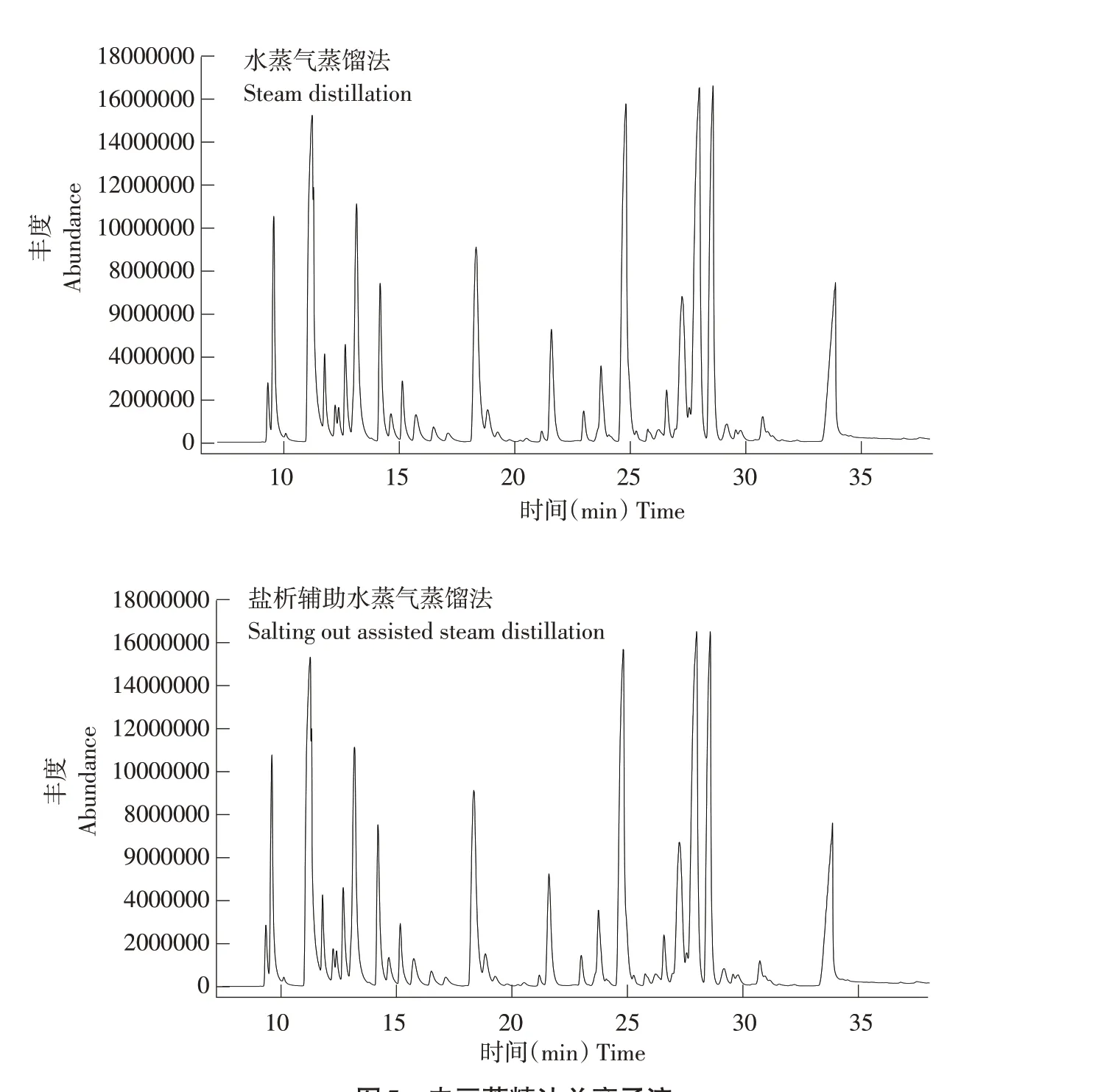
图5 肉豆蔻精油总离子流Fig.5 Total ion flow diagram of nutmeg essential oil
按峰面积归一化法计算各组分质量分数,经NITS11谱图库检索对比,同时参考相关文献,确定肉豆蔻精油组成成分,检索结果见图5和表5。水蒸气蒸馏法提取肉豆蔻精油检出30种化合物,盐析辅助水蒸气蒸馏法提取肉豆蔻精油共检出33种化合物,两种方法提取肉豆蔻精油主要成分相同,为肉豆蔻醚、皮蝇磷、甲基丁香酚、榄香素等。肉豆蔻精油主要由烯类、醇类、酯类、醚类、酸类及酚类等物质组成,约占总成分93%。Dupuy等[27]在对肉豆蔻精油成分分析中也得出一致结论,说明盐析辅助水蒸气蒸馏法提取对肉豆蔻精油主要组成成分无影响,可用于精油提取。

表5 肉豆蔻精油成分分析Table 5 Composition analysis of nutmeg essential oil extracted
2.5.2 DSC分析
肉豆蔻精油DSC分析如图6所示。两种方法提取肉豆蔻精油吸热和放热曲线、峰型均相似,说明盐析辅助水蒸气蒸馏法在提取过程中未对肉豆蔻精油物理性质造成破坏。DSC分析图中出现一个主要吸热峰,峰值约在200℃,是由于精油中醛类、酮类挥发性物质吸热汽化导致。
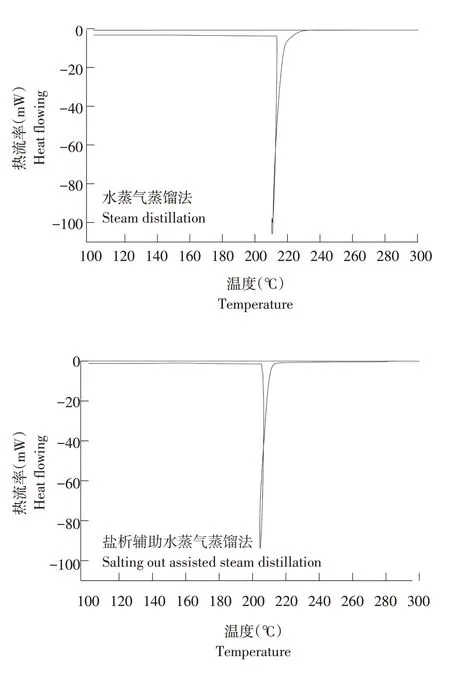
图6 肉豆蔻精油DSC分析Fig.6 DSC analysis of nutmeg essential oil
2.6 抗氧化能力
2.6.1 总抗氧化能力
由图7可知,肉豆蔻精油和VE的FRAP(铁离子还原能力)值均随浓度增加而提高,但VE的FRAP值高于肉豆蔻精油FRAP值,且水蒸气蒸馏法提取肉豆蔻精油与盐析辅助水蒸气蒸馏法提取肉豆蔻精油的FRAP值相近,表明不同提取方法未对肉豆蔻精油总抗氧化能力产生影响。当精油浓度为0.2~0.6 mg·mL-1,随精油浓度升高,FRAP值小幅上升;浓度0.6~1.0 mg·mL-1时,FRAP值大幅升高,而VE的FRAP值随浓度增加始终保持大幅提高。其中水蒸气蒸馏法提取肉豆蔻精油最大FRAP值为0.173 mmol·L-1,盐析辅助水蒸气蒸馏法提取肉豆蔻精油最大FRAP值为0.175 mmol·L-1,可见,两种方法提取肉豆蔻精油总抗氧化能力相近;而VE最大FRAP值为0.711 mmol·L-1,高于肉豆蔻精油,可见VE具有较好抗氧化性能。
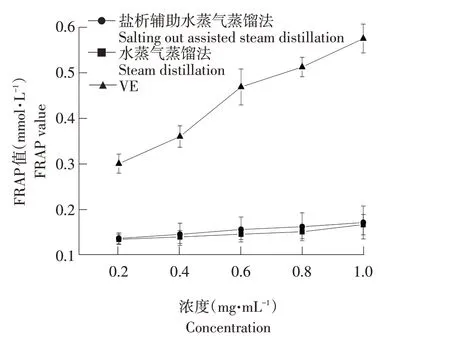
图7 肉豆蔻精油总抗氧化能力Fig.7 Total antioxidant capacity of nutmeg essential oil
2.6.2 DPPH自由基清除能力
由图8可知,肉豆蔻精油对DPPH自由基清除能力与浓度呈正相关。当精油浓度为0.2~0.6 mg·mL-1时,随精油浓度升高,DPPH自由基清除率大幅增加;精油浓度超过0.6 mg·mL-1后,即使精油浓度增加,DPPH·清除率提高不明显;VE浓度为0.2~1.0 mg·mL-1时,对DPPH自由基清除率始终大于90%,且远高于肉豆蔻精油。其中水蒸气蒸馏法提取肉豆蔻精油的IC50为1.03 mg·mL-1,盐析辅助水蒸气蒸馏法提取肉豆蔻精油的IC50为0.97 mg·mL-1,VE的IC50为0.026 mg·mL-1,可见,水蒸气蒸馏法提取肉豆蔻精油与盐析辅助水蒸气蒸馏法提取肉豆蔻精油对DPPH·清除能力相似,表明不同提取方法对肉豆蔻精油DPPH·清除能力无影响。

图8 肉豆蔻精油对DPPH自由基清除能力Fig.8 DPPH radical scavenging ability of nutmeg essential oil
2.6.3 羟基自由基清除率
由图9可知,随浓度增加,肉豆蔻精油和VE对羟基自由基清除率均呈上升趋势。浓度为0.2~1.0 mg·mL-1时,两种方法提取肉豆蔻精油对羟基自由基清除率呈大幅增加趋势,其中水蒸气蒸馏法提取肉豆蔻精油的IC50为0.586 mg·mL-1,盐析辅助水蒸气蒸馏法提取肉豆蔻精油的IC50为0.485 mg·mL-1,可见水蒸气蒸馏法提取肉豆蔻精油对羟基自由基清除能力较盐析辅助水蒸气蒸馏法低。研究表明,酚类物质是具有高氢/电子贡献活性、抗自由基和抗氧化潜力的主要成分[28],盐析辅助水蒸气蒸馏法提取肉豆蔻精油中酚类物质占11.56%,甲基丁香酚占10.84%;水蒸气蒸馏法提取肉豆蔻精油中酚类物质占8.18%,甲基丁香酚占7.9%,导致盐析辅助水蒸气蒸馏法提取肉豆蔻精油对羟基自由基清除能力高于水蒸气蒸馏法。而VE对羟基自由基清除率增长较缓慢,始终大于90%,IC50为0.117 mg·mL-1,远高于肉豆蔻精油对羟基自由基清除率。
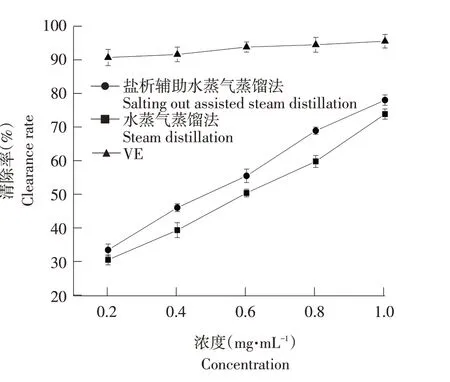
图9 肉豆蔻精油对羟基自由基清除能力Fig.9 Hydroxyl radical scavenging ability of nutmeg essential oil
2.7 亚硝酸盐清除率
由图10可知,随浓度不断升高,肉豆蔻精油对亚硝酸盐清除率呈增长趋势,但水蒸气蒸馏法提取肉豆蔻精油对亚硝酸盐清除能力低于盐析辅助水蒸气蒸馏法。当浓度为100~400 μL时,清除率缓慢增加;浓度继续增加,清除率增长加快;当肉豆蔻精油浓度为500 μL时,两种方法提取肉豆蔻精油清除率分别达53.29%和68.12%。肉豆蔻精油对亚硝酸盐清除作用与其含有萜烯类化合物有关[29]。研究表明,精油对亚硝酸盐清除为动态平衡过程[30],但清除机理需进一步研究。
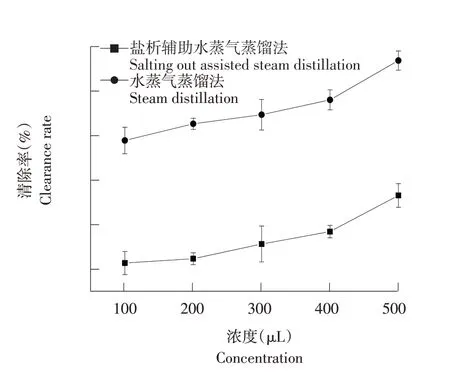
图10 肉豆蔻精油对亚硝酸盐清除能力Fig.10 Nitrite scavenging ability of nutmeg essential oil
3 讨论与结论
李荣等利用微波辅助蒸馏提取肉豆蔻精油,结果表明,当料液比1:10,提取时间56 min时,肉豆蔻精油得率达6.94%[31];郑福平等采用无溶剂聚焦微波提取肉豆蔻精油,得率达8.23%[32]。本试验采用盐析辅助水蒸气蒸馏法提取肉豆蔻精油得率为13.27%,远高于微波辅助蒸馏法和无溶剂聚焦微波提取法。超临界萃取法具有试验条件温和、萃取速度快、无溶剂残留、工艺简单等优点,但因成本高、设备清洗困难而限制其在工业中应用。水蒸气蒸馏法是一种传统提取方法,操作简单、成本较低,但提取时间过长且提取率较低。饶建平等采用NaCl溶液辅助水蒸气蒸馏提取柚子花精油时发现,NaCl可有效提高精油提取率,其机理可能是NaCl不仅促进柚子花与水的水溶作用,使其充分接触,从而加速精油从细胞壁中渗出[33];NaCl还可降低精油在水中溶解度,保证从柚子花中提取出来的精油不溶解在水中。潘晓梅也认为盐属于强电解质,在溶液中电解成离子,从而产生电场;在电场作用下,水分子易与盐离子缔合成分子,使精油在水中溶解度降低,提高提取率[34]。盐析辅助水蒸气蒸馏法操作简单,缩短提取时间,提高提取得率,成本降低。后续试验可针对无机盐提高精油得率展开研究。
与VE相比,肉豆蔻精油抗氧化能力和清除亚硝酸盐能力较低,但随着肉豆蔻精油浓度升高,对DPPH自由基、羟基自由基和亚硝酸盐清除率逐渐增加,也可说明肉豆蔻精油生产价值。后续将研究不同提取方法对肉豆蔻精油抗氧化性能和清除亚硝酸盐能力的影响。
本试验利用响应面优化提取工艺,最优提取工艺为:液料比12.19:1(mL·g-1)、提取时间3.62 h、NaCl浓度2.85%,肉豆蔻精油得率为13.27%。盐析辅助水蒸气蒸馏法提高精油得率,且对肉豆蔻精油理化性质和热力学性质无影响。肉豆蔻精油对DPPH自由基、羟基自由基及亚硝酸盐具有一定清除能力,但均低于VE。以上试验结果为进一步研究肉豆蔻精油提供参考。

