Bi/石墨毡电极对铁铬液流电池性能的影响
倪思青,陈 杰,张 欢,白 林,曲博文
(辽宁科技大学 材料与冶金学院,辽宁 鞍山 114051)
发展风能、太阳能等可再生能源发电是应对气候变化的重要举措。然而,由于可再生能源具有间歇性,可再生能源发电直接并网可能会破坏电网的稳定。配备固定电化学储能装置能够有效整合出可持续电能[1],但安装和维护成本仍然是电化学装置在电网中普及的主要障碍[2]。因此,近年来提出利用液流电池来解决可再生能源的持续发电问题。液流电池的基本结构包括:储液罐、电化学反应电堆和流动系统。该结构可进行灵活的模块化设计和规模化控制,而且维护成本适度,循环寿命长,具有解耦效率和容量的独特能力。在众多液流电池体系中,铁铬液流电池采用低成本、环境友好的铁/铬盐酸溶液分别作为阴极和阳极,有望在储能应用中得到广泛应用[3-5]。
自1974年NASA开发出铁铬液流电池以来,限制铁铬液流电池商业化发展的问题主要在于电解液失活[6]、Cr3+/Cr2+动力学迟缓[7]以及析氢副反应[8]。铁铬液流电池的运行温度通常在55~65℃,该温度范围有利于保持电解液中Cr(H2O)5Cl2+的活性[5,9]。为了提高Cr3+/Cr2+活性,一些催化剂被引入到负极,如Au[10]、Pb[11]、Bi[12]、ZrP[13]、SiO2[14]。其中,Pb、Bi也被用于抑制负极析氢副反应,进而提高电池的寿命、稳定性及安全性[8,15]。近年来,采用低成本、高导电性的Bi增强电极电化学活性的研究受到了广泛关注[16]。目前石墨毡是液流电池的首选电极材料,而Bi增强石墨毡电极材料在铁铬液流电池中的应用参数并不完善[12,17]。本文将金属Bi以离子形式引入到电解液中,借助铁铬液流电池的充放电过程在石墨毡电极上形成Bi颗粒,并通过循环伏安法(CV)、电化学阻抗谱(EIS)和充放电试验,考察Bi/石墨毡电极对铁铬液流电池性能的催化作用。
1 实验材料及表征
1.1 石墨毡的活化
聚丙烯腈基石墨毡购于甘肃郝氏炭纤维有限公司,厚度为5 mm。石墨毡置于马弗炉中,以15℃/min的升温速度升至500℃,保温5 h,随炉降温,取出备用,记作TGF。
1.2 电解液的制备
电解液的组成为1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl。由FeCl2·4H2O和CrCl3·6H2O在浓盐酸溶液中溶解,再用去离子水在室温下定容稀释而成。BiCl3分别以浓度为1、5、10、15 mmol/L溶解于电解液中。所有化学试剂均为纯分析试剂,购于国药化学试剂有限公司。
1.3 单电池测试
电堆主要部件为:全氟离子交换膜Nafion 115作为隔膜,切割出交叉形流道的石墨毡作为正负电极,有效面积为9 cm2,石墨板作为双极板。由聚四氟板框控制石墨毡的压缩比为20%,并由硅橡胶垫圈密封。正负极电解液均为50 mL,储存于电堆外部储液罐中,通过磁力循环泵以100 mL/min的速度泵入电堆内循环流动。单电池结构如图1所示。采用充放电试验系统对电池进行监测,经计算可获得单电池的库伦效率(Coulombic efficiency,CE)、电压效率(Voltage efficiency,VE)和能量效率(Energy efficiency,EE),且EE=CE×VE。单电池测试仪型号为CT2001C-5V/2A,购于武汉蓝电电子股份有限公司。测试参数:电流密度为60~120 mA/cm2,截止电压为0.8~1.2 V,电池运行温度控制在65℃。
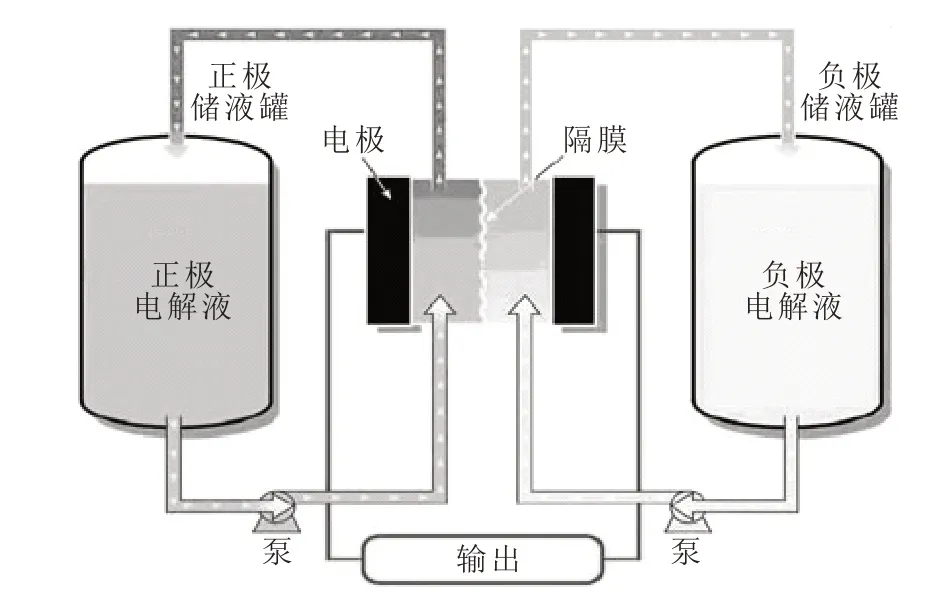
图1 单电池结构示意图Fig.1 Schematic diagram of single cell structure
1.4 形貌分析
采用Zeiss-Σigma-HD场发射扫描电子显微镜观察充放电后石墨毡的形貌。用该仪器对样品中的粒子进行了X射线能量分散谱(EDX)鉴定。采用扫描电子显微镜(SEM)分析石墨毡表面形貌和晶体结构。
1.5 电化学测试
三电极测试体系:以0.3 cm2的圆柱形石墨毡为工作电极,1 cm2的正方形高纯石墨片作为对电极,饱和甘汞电极(SCE)作为参比电极。电化学工作站型号为CS310H CorrTest,购于武汉科思特仪器股份有限公司。电化学工作站连接三电极系统,在室温下进行电化学表征,得到CV曲线和EIS谱图。CV曲线的电化学窗口范围为-1.2~1.2 V。EIS测试的极化电压分别为0.5 V和-0.5 V,交流电压振幅设置为5 mV,频率范围为0.01~100 kHz。
2 结果与讨论
2.1 电池性能
电解液中溶入不同浓度的BiCl3后,电池放电容量的变化如图2所示。其中,正负极电解液均为1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl+x mmol/L BiCl3(x=1,5,10,15)。对比首充后电池放电容量,加入催化剂BiCl3的电池放电容量均低于未加入催化剂的电池,尤其是在BiCl3加入量超过10 mmol/L后,电池首充容量消耗更为显著。这是因为溶入电解液中的Bi离子在石墨毡表面沉积形成Bi颗粒,充放电过程中Bi离子在石墨毡电极表面不断沉积及溶解,消耗一定的电池容量。
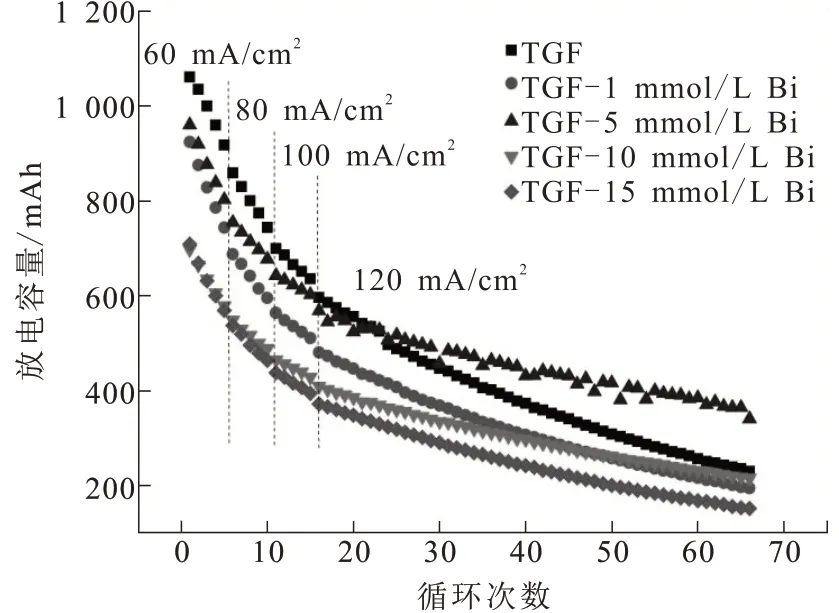
图2 电解液中溶入不同浓度BiCl3后的电池放电容量Fig.2 Discharge capacities of single cells with different BiCl3 contents in electrolyte
经过66次充放电循环后,五种电池容量都大幅度衰减;其中BiCl3加入量为5 mmol/L的电池容量衰减最少,并在15次循环后,剩余电池容量超过其余四种电池。依据负极侧的平衡电势和较慢的Cr氧化还原反应动力学,析氢反应通常比Cr氧化还原反应更容易发生。而Bi不仅可以改善Cr氧化还原反应活性,同时能够抑制析氢反应[4]。所以添加Bi的电池放电容量衰减率得到降低。然而引入Bi也会导致电池容量损耗,因此催化剂的加入量存在一个最优值。
图3为电解液中溶入不同浓度BiCl3后的电池效率。
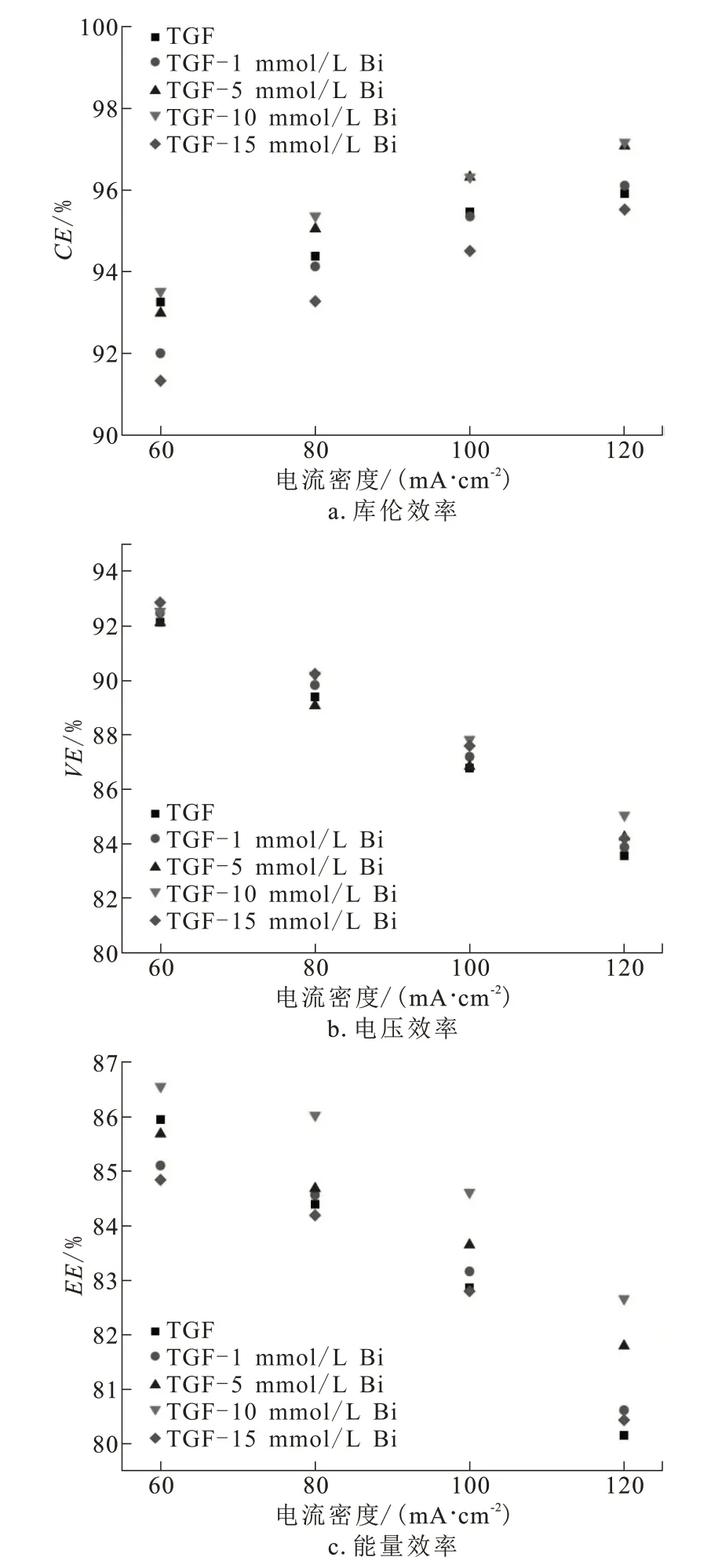
图3 电解液中溶入不同浓度BiCl3后的电池效率Fig.3 Efficiencies of single cells with different BiCl3 contents in electrolyte
随着电流密度的增加,各电池的CE值随之增大。BiCl3浓度为5 mmol/L和10 mmol/L的电池CE值较大,尤其是在电流密度超过80 mA/cm2时,上述浓度对电池CE值影响较为显著。这可能归因于Bi离子对反应活性的贡献,平衡了膜两侧的离子浓度,使得CE值增大。
随着电流密度的增加,各电池的VE值明显减小。在超过100 mA/cm2的较大电流密度条件下,加入BiCl3的电池其VE值全部超过未加入催化剂的电池。在电流密度为120 mA/cm2时,BiCl3浓度为10 mmol/L的电池VE值最大,达到85.07%。VE值可反映电极材料的活化程度[18]。在大电流密度充放电时,电池的极化效应更为凸显,因此Bi对石墨毡电极的活化效果也更为显著。
随着电流密度的增加,各电池的EE值明显减小。BiCl3浓度为10 mmol/L时,电池在各个电流密度下获得的EE值均最大。当电流密度超过80 mA/cm2时,BiCl3浓度为5 mmol/L的电池EE值也较为理想,在120 mA/cm2时EE值达到81.8%。EE值反映的是Bi增强石墨毡电极后对电池CE值和VE值的综合结果。结合电池容量实验结果,认为电解液中BiCl3的最佳浓度为5 mmol/L。
石墨毡内切割流道对电池循环放电容量的影响以及石墨毡内切割流道的实物如图4所示。Cell A电池中石墨毡电极未切流道,Cell B电池中石墨毡电极切宽度为5 mm的交叉形流道,Cell C电池中石墨毡电极切宽度为5 mm的交叉形流道且电解液中加入5 mmol/L的BiCl3。三种电池的效率详见表1。在没有催化剂的情况下,尽管Cell B首次放电容量值最高,但其容量衰减量远高于Cell A。这说明交叉形流道并不利于保持电池容量。但Cell B的效率高于Cell A,这可能是石墨毡内的流道结构增加了电解液的有效流动,降低了浓差极化,从而提高了电池效率,但在缺少催化剂的情况下析氢反应也增多,表现出电池容量衰减快。再进一步对比Cell B和Cell C发现,Cell C的容量衰减量低于Cell B,而两者的效率值差别不大。这说明Bi的引入有利于提高电极反应活性及抑制析氢反应,可以降低电池放电容量衰减量;两种电池效率差距不显著的原因可能是限于电极流道结构相同[19]。
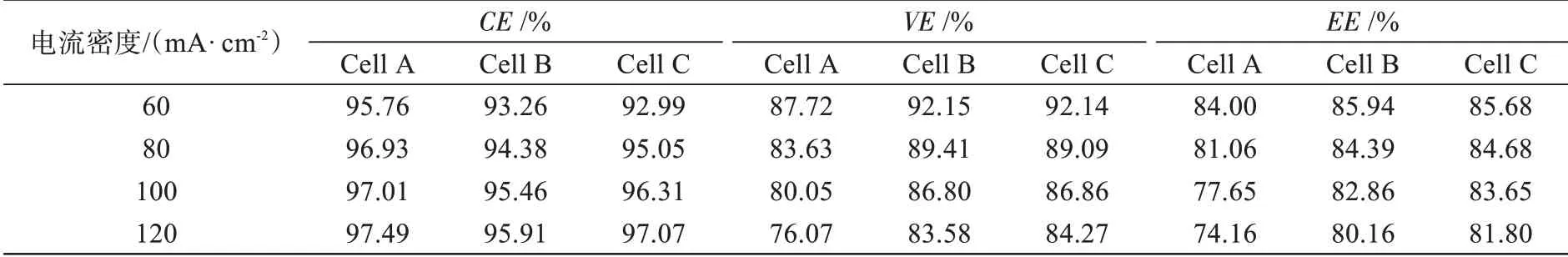
表1 三种电池的效率Tab.1 Efficiencies of three cells
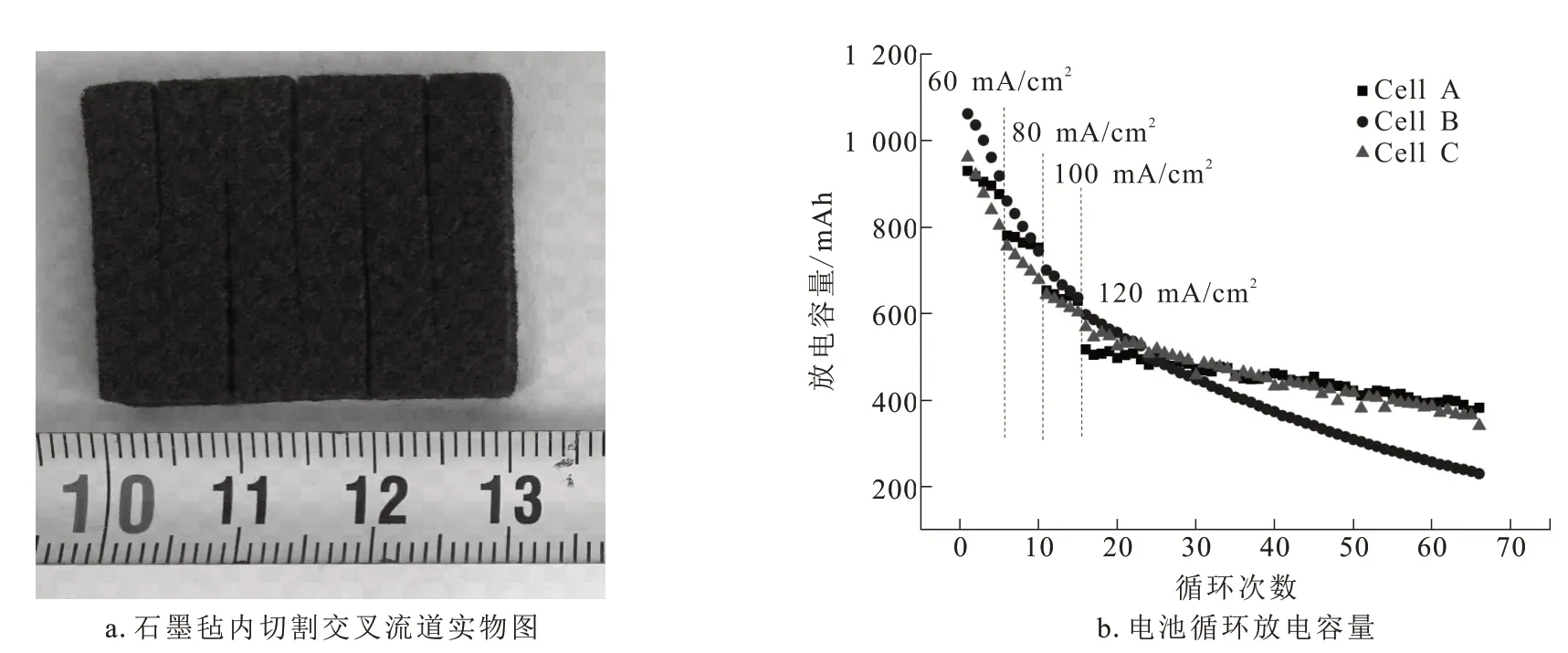
图4 采用交叉流道石墨毡及其电池循环放电容量Fig.4 A graphite felt with crossing flow channels and circulating discharge capacities of ICRFBs using this kind of graphite felt
2.2 Bi/石墨毡电极形貌
采用SEM对电池Cell C完成充放电循环后负极石墨毡电极进行分析,如图5所示。残余的电解液附着在石墨毡电极表面。探测位置内残余电解液的成分主要有O、Cl、Cr、Fe以及Bi元素。图5b~图5g为图5a区域内进行成分面扫的结果。石墨毡的主要成分为C元素,O、Cl、Cr、Fe四种元素主要分布在石墨毡电极外部,但在石墨毡表面和四周都存在Bi元素。可见在截止充放电电压范围内,Cell C完成放电后石墨毡电极表面的Bi颗粒没有完全脱落。即一部分残留在电解液中,而另一部分则保留在电极表面。在充电过程中,Bi颗粒先在负极上沉积,使Cr3+还原为Cr2+;在放电过程中,沉积在石墨毡上的Bi再次被氧化为Bi3+进入到电解液。但在石墨毡上仍残留着一些Bi颗粒,说明Bi的氧化还不完全,这可能是由于Bi的氧化电位还不够高,不足以使Bi颗粒完全氧化所致。

图5 充放电循环后负极石墨毡的SEM和EDX结果Fig.5 SEM images and EDX results of negative graphite felt after charge-discharge cycles
2.3 电化学反应分析
图6为1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl溶液和1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl+5 mmol/L BiCl3溶液中石墨毡电极的CV图,其中图6a的扫描速度为3 mV/s,图6b的扫描速度为1 mV/s。当扫描速度为3 mV/s,Bi使负极Cr3+/Cr2+氧化还原峰的对称性得到了明显改善,峰电流显著增大,峰电位差减小。这说明Bi有助于提高负极Cr3+/Cr2+在石墨毡电极表面的电化学活性。Bi/Bi3+的氧化还原峰分别位于-0.1 V和-0.3 V处,说明Bi的沉积发生在Cr3+/Cr2+反应之前,而Bi的脱落发生在Cr3+/Cr2+反应之后。这导致电池首次充放电时容量消耗较大,并且在放电后仍有部分Bi残留在电极表面。然而,Bi对Fe2+/Fe3+氧化还原峰影响较小,但经过氧化峰和还原峰后的法拉第电流依然较大,说明溶液中的Bi离子在铁离子发生氧化还原反应之后仍能在电极表面产生电流。为了进一步分析Bi对Fe2+/Fe3+的影响,将CV的扫描速度由3 mV/s降至1 mV/s,结果显示,Bi离子的存在使得Fe2+/Fe3+的峰电位差增大,峰电流的比值也偏离1,氧化还原峰的对称性下降,说明Bi不利于改善Fe2+/Fe3+的反应活性。
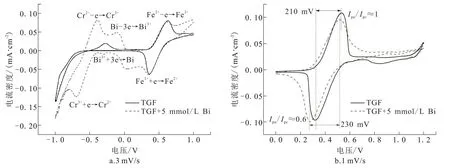
图6 不同扫描速度的CV图Fig.6 CV curves at different scan rates
图7为1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl溶液和1 mol/L FeCl2+1 mol/L CrCl3+3 mol/L HCl+5 mmol/L BiCl3溶液中石墨毡电极的EIS谱图,其中图7a的极化电压为0.5 V,图7b和图7c的极化电压为-0.5 V。EIS谱图均由高频的半圆部分和低频的线性部分组成,半圆曲线反映电极与电解液之间电荷转移电阻,线性部分与离子在溶液中的扩散系数和扩散驱动力有关[20]。
根据图7中的等效电路对各EIS谱图进行拟合,其中Rs表示溶液和电极的欧姆电阻,Rct表示电化学反应的电荷转移电阻,Wo表示扩散电阻,拟合结果列于表2中。当过电位为0.5 V时,Bi离子的引入使得电解液导电性增加,因此Rs值减小,而Bi离子引起Rct和Wo值增加,说明Bi不利于正极反应的电荷转移和离子扩散,该结果与CV图一致。当过电位为-0.5 V时,Bi离子除了使得Rs值减小外,对负极反应的活化作用显著,Rct值大幅度减小,而Bi离子对溶液离子扩散阻碍作用依然使得Wo值增加。说明石墨毡内的流道有利于含Bi电解液的扩散传质。
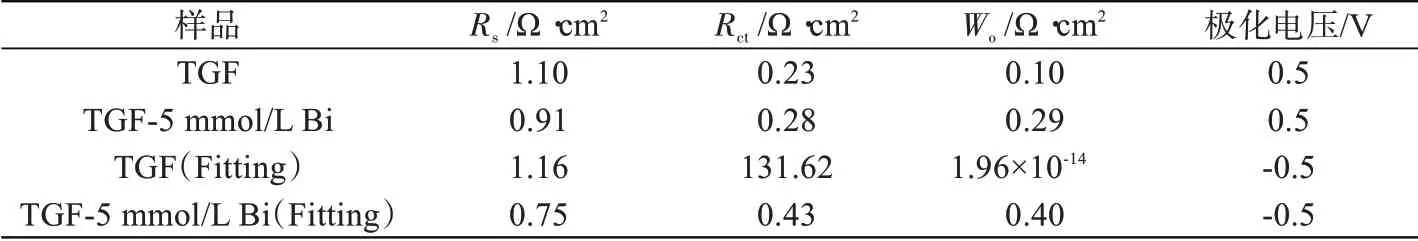
表2 根据等效电路拟合交流阻抗图谱得到的参数Tab.2 Parameters obtained by fitting EIS spectrograms with equivalent circuit
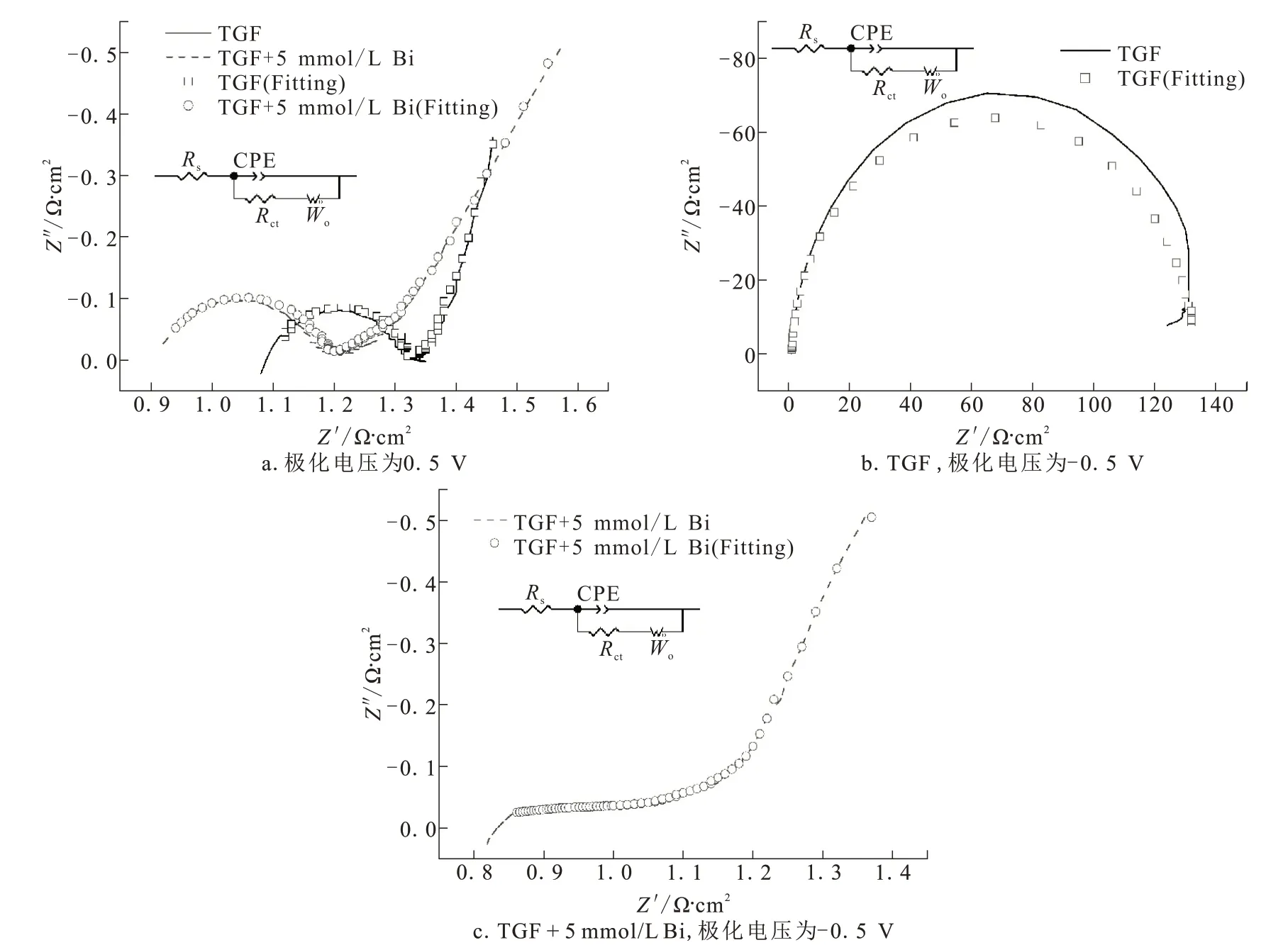
图7 极化电压为0.5 V和-0.5 V的EIS谱图及拟合曲线Fig.7 EIS spectrograms and fitting curves at polarization voltages of 0.5 V and-0.5 V
3 结论
本文通过在电解液中加入BiCl3以及在石墨毡电极内切割交叉形流道来改善铁铬液流电池的循环充放电性能。实验结果表明,电解液中加入BiCl3的最佳浓度为5 mmol/L,该条件下电池每次循环放电容量的平均衰减率不超过1%,电流密度为120 mA/cm2时电池能量效率达到81.8%。在石墨毡内切割交叉形流道可有效提高电解液的流动传质,降低电池容量衰减。然而,BiCl3的引入会消耗一定的电池容量。电池充放电后,Bi元素不仅存在于电解液之中,还残余在石墨毡电极表面。电化学测试结果表明,Bi离子的加入使负极Cr3+/Cr2+活性增强,但不利于正极Fe2+/Fe3+反应。

