废旧锂离子电池中有价金属回收研究现状
邓超群 王海北 周起帆 郑朝振
(矿冶科技集团有限公司,北京100160)
锂电池作为新能源动力电池的典型代表之一,因具有循环寿命长、比能量高、自放电效应小、体积小、工作电压高、无记忆效应、适用温度范围广、绿色环保等优点,被广泛应用于3C及电动车等领域。锂电池使用寿命一般为3~5年,预计到2025年,废旧锂离子电池重量将达64万t。面对如此庞大的废锂电池,如不加以妥善处理,不仅造成巨大的环境污染和安全隐患,还将导致大量镍、钴、锂等金属资源的浪费。
废锂电池由正极、负极、隔膜、集流体、外壳、电解液等组成,其中正极活性材料中的有价金属含量远大于原生矿石,尤其是Ni、Co、Li,分别达到5%~10%、5%~20%、5%~7%[1]。据统计,近年来我国Ni、Co、Li原料对外进口依存度分别均在80%、90%、80%以上[2-4],这意味着这些战略性矿产资源可能随时被掐断,受制于其他国家。将废锂电池作为战略性资源的来源之一,对其处理并建立相应的回收体系是相当的迫切且必要。
对废锂电池有价金属进行资源回收之前,通常需对其进行预处理,得到正极活性材料,再从正极活性材料中回收有价金属。本文主要从预处理及有价金属回收两方面对废锂电池回收进行相关阐述。
1 废锂电池预处理
废锂电池预处理过程主要分为放电、拆解和分离[5]。
放电主要有物理放电和化学放电[6]。物理放电主要在金属粉末介质和石墨粉末介质中进行。其中,金属粉末介质中放电时电池内的温度上升剧烈,有一定的危险性但效率较高;石墨粉末介质中放电较温和,但效率较低[7]。物理放电中还有低温冷冻放电法,因其对设备的要求较高及初始建设成本高,研究的相对较少。尽管对物理放电有一定的研究,但相比化学放电,物理放电效率较低且处理规模较小,难以满足市场上的需求,因而大多数学者主要研究废旧锂离子电池的化学放电。目前的化学放电主要是利用盐溶液(如NaCl、Na2SO4)对废锂电池进行浸泡放电。如FU等[8]将废三元锂电池置于一定浓度的NaCl溶液中浸泡24 h进行放电;LI等[9]使用Na2SO4溶液对对废锂电池进行放电。虽然这几种盐溶液能达到放电的效果,但随着废锂电池的不断增加,其对环境的影响逐渐加大。为了寻找一种环境友好型的盐溶液,YAO等[6]对NaCl、FeSO4和MnSO4溶液进行了相应的研究,得出FeSO4溶液在放电过程中对环境的影响比其他盐溶液更小,且在125 min内能使残留电压减小到1.0 V。
拆解的目的是将正极材料从废锂电池中分离,一般有手动拆解和机械拆解两种方法。正极材料是由Al集流体、正极活性材料及PVDF黏结剂组成。分离Al箔和正极活性材料,一般采取两种方法,一是利用有机溶剂(常用NMP)破坏PVDF的粘结作用[10,11],二是利用NaOH先将Al箔转化为易溶于水的NaAlO2形式,达到Al箔的分离目的[12]。
2 废锂电池有价金属回收利用方法
随着国家对新能源汽车研发及市场普及的重视,新能源汽车在市场上的占有率不断增加。锂电池作为新能源汽车的“心脏”,其装机量也呈现高速增长。据中机中心合格证数据统计,2009—2018年,我国锂电池装机量从0.028 GW·h增加到57.04 GW·h,增长超千倍,年复合增速达233.17%。锂电池的寿命一般为3~5年,今后几年将会有大量废锂电池产生。据统计,2020年我国废锂电池达到50万t以上,预计2025年将达到64万t以上[13]。废锂电池的规模量如此之大,且其含大量有价金属,如Li、Ni、Co、Mn,其品位远高于原矿品位,若对其进行二次开发回收,在很大程度上能缓解我国资源紧张局面。
当前,对废锂电池有价金属回收的方法主要有火法冶金、湿法冶金、火法焙烧—湿法冶金联合法以及其他方法。其中,火法冶金占比26%,湿法冶金占比51%(含火法焙烧—湿法冶金联合法),其他占比23%(如生物冶金、物理回收)[14]。本文重点介绍我国当前使用比较广泛的火法冶金法、湿法冶金法、火法焙烧—湿法冶金联合法,简要介绍生物冶金法。
2.1 火法冶金法
火法冶金法回收废锂电池有价金属主要是利用还原剂对氧的强亲和力,使正极活性材料中的有价金属Ni、Co、Mn还原成单质并形成合金,且可在调整合适渣型条件下,使合金与炉渣较好分离,后续再对合金进行湿法冶金工序,从而实现有价金属的回收。如任国兴[15]研究了无Mn铝壳锂离子电池、无Mn聚合物锂离子电池、含Mn聚合物锂离子电池、含Cr钢壳锂离子电池四种类型壳体材料和正极材料的废旧锂电池的还原熔炼回收工艺,主要回收其有价金属Co、Ni、Cu。在火法熔炼过程中,熔炼温度和氧分压是影响Co、Ni、Cu回收率的关键因素,Al、Mn、Cr是影响氧分压及渣黏度的关键元素。一般熔炼温度在1 450 ℃、氧分压小于10-11,Co、Ni、Cu在合金中的分布率均能达到90 %以上,氧分压过高会使更多的Al、Mn、Cr等元素形成氧化物,导致渣的黏度增加,从而降低Co、Ni、Cu在合金中的分布。袁文辉等[16]利用碳还原熔炼法将废钴酸锂电池在1 600 ℃熔炼1.5 h,实现了Co 78.63%、Cu 81.54%的回收率,并指出Al作为杂质金属同样具有还原性,形成的Al2O3存在于炉渣,可实现Al与主要金属的分离。WANG等[17]通过研究废钴酸锂电池与Al箔集流体的反应,证实了在反应中Al还原剂的存在,LiCoO2在反应后被转化为Li2O、CoO。
火法冶金法充分利用了含铝外壳、负极石墨碳素及隔膜塑料等材料的还原性与蕴含的能量[18],具有对原料适用性强、处理能力大、流程短、效率高,可避免复杂的机械拆解与物理分选,实现正负极及外壳的混合处理特点,但反应过程会产生有毒气体,对温度控制要求严格,且过程需加装烟气净化设备,建设成本高。目前热解/火法冶炼工艺已经工业化运行[19],如比利时Umicore公司、瑞士的BATREC公司、日本Mitsubishi公司[20]。
2.2 湿法冶金法
湿法冶金大多采用无机酸(H2SO4[21]、HNO3[22]、HCl[23,24]或H3PO4[25,26])或有机酸(如柠檬酸[9]、苹果酸[27]、葡萄糖酸[28,29]、抗坏血酸[30]等)对废锂电池有价金属进行酸浸富集,为了增加有价金属的浸出率,会引入还原剂(H2O2[21]、Na2S2O3[31]、Na2SO3[32]或硫酸肼[33])或增加超声波—微波辅助性条件[34],而后采用后续工艺对有价金属进行分离提取或再生制备前驱体,达到对有价金属的充分回收利用。除了酸浸富集法,还有氨浸富集法,该方法因对金属的浸出率较低,且起步较晚,研究的比较少。表1列举了采用湿法冶金回收废锂电池有价金属的主要方法。

表1 采用湿法冶金回收废锂电池有价金属的主要方法Table 1 Main methods of recycling valuable metals from spent lithium-ion batteries by hydrometallurgy
2.2.1 酸浸
由于废锂电池活性正极材料有价金属在酸性溶液中比较容易浸出,一般优先使用酸作为浸出剂。SATTAR等[36]利用H2SO4为浸出剂,H2O2为还原剂,对废三元锂电池正极材料有价金属进行了浸出,探究了矿浆浓度、双氧水、硫酸浓度及温度对有价金属浸出的影响。结果发现,还原剂H2O2的添加对Co、Mn、Ni、Li的浸出有较大促进作用,在矿浆浓度5%、H2SO42 mol/L、H2O24%、温度50 ℃和时间30 min的条件下,Co、Mn、Ni、Li的浸出率均可达到98%以上。为了进一步降低反应温度并增加金属的浸出率,JIANG等[34]利用超声波可产生的微射流、冲击波等力学效应,导致液体微观湍流和固体之间的高速碰撞,从而增强涡流扩散特点,在硫酸酸浸过程中引入超声波,从而促进有价金属的高效浸出。H2SO4为浸出剂虽能实现锂电池有价金属的基本浸出富集,但达不到对个别金属的优先提取,H3PO4的介入可很好地解决这一问题。如CHEN等[37]利用H3PO4为浸出剂,H2O2为还原剂,分别研究了废旧LiCoO2(LCO)、LiMn2O4(LMO)、LiFePO4(LFP)和 LiCo1/3Mn1/3Ni1/3O2(NCM)电池中选择提Li的问题,在最佳条件下,Li的选择提取率分别达到 100%、92.86%、97.57% 和98.94%。
考虑到采用无机酸具有腐蚀性大,且存在反应过程常产生SOx、NOx、Cl2等有毒气体及对有价金属浸出选择性差等问题,许多学者选择温和的有机酸去替代无机酸。如郑莹等[38]选择柠檬酸为酸浸剂,抗坏血酸为还原剂,对废钴酸锂电池正极活性材料有价金属进行还原酸浸。结果表明,在钴酸锂与柠檬酸的摩尔比为1∶3.5、钴酸锂与抗坏血酸的摩尔比为1∶1、固液比(g/L)值为15、温度80 ℃及时间为5 h的条件下,Co和Li的浸出效率可达91%和94%;周涛等[39]采用苹果酸为酸浸剂,双氧水为还原剂,在对废镍钴锰锂电池正极活性材料有价金属进行还原酸浸时发现,在反应时间30 min、反应温度80 ℃ 、苹果酸浓度1.2 mol/L、双氧水体积分数1.5 %及固液比(g/L)值为40 g/L的最佳条件下,Li、Ni、Co、Mn的浸出率分别达到98.9%、94.3%、95.1%和96.4%。
有机酸价格昂贵且量少,单一采用有机酸浸出剂对工业化的推广有一定难度,有学者将有机酸和无机酸联合进行混合酸浸,使酸浸达到最优化。如ZHUANG等[35]采用磷酸和柠檬酸为浸出剂对废三元锂电池正极材料有价金属进行浸出时发现,在磷酸浓度0.2 mol/L、柠檬酸浓度0.4 mol/L、固液比(g/L)值为20、温度90 ℃和反应时间30 min的条件下,Li、Ni、Co、Mn的浸出率分别达到100%、93.38%、91.63%和92.00%,表观活化能分别为45.83、83.01、81.38、92.35 kJ/mol,反应控制阶段为表面化学反应控制。
2.2.2 氨浸
氨浸富集主要是利用氨水—铵盐体系实现对有价金属的富集浸出,过程添加缓冲剂(如碳酸氢铵)、络合剂或还原剂,达到对个别金属选择浸出的目的。该方法较好克服了酸浸富集过程一些固有问题,如产生有毒气体(NO/Cl2)、对设备的强腐蚀性、对有价金属的低选择性等,但反应温度一般较高,且反应时间长,金属的浸出率也低于酸浸法。
郑晓洪[1]开展了利用氨—硫酸铵体系对三元电池正极活性材料有价金属选择性浸出研究,在氨水浓度4 mol/L、硫酸铵浓度1.5 mol/L、亚硫酸钠浓度0.5 mol/L、固液比(g/L)值为10、反应温度353 K和浸出时间300 min的最佳条件下,Li、Ni、Co、Mn的浸出率分别为95.3%、89.8%、80.7%和4.3%。在采用氨—硫酸铵体系进行浸出时,亚硫酸钠的添加很好地促进了锰的沉淀,从而实现了Li、Ni、Co的选择性浸出。WU等[13]对含镍钴电池正极活性材料进行氨—亚硫酸铵选择性浸出时发现,在氨水浓度1.5 mol/L、亚硫酸铵浓度1 mol/L、碳酸氢铵(缓冲剂)浓度1 mol/L、反应温度60 ℃、反应时间180 min条件下,Ni和Cu几乎能被全部浸出,Al几乎不被浸出,Li和Co的浸出率适中。
2.2.3 分离提取/再生前驱体
废电池正极活性材料有价金属经有机酸/无机酸酸浸富集于溶液后,需对其进行分离回收/净化除杂制备前驱体后,方能实现废旧电池的有价回收。酸浸液一般含Ni、Co、Mn、Li等有价金属离子以及Fe、Al、Cu等杂质金属离子。实现有价金属分离常用的方法有化学沉淀、萃取、离子交换、电解沉积等。
陈亮[21]采取图1所示净化工艺流程对废钴酸锂电池正极活性材料进行还原酸浸,实现了钴的分离回收。在最佳的工艺参数条件下,铜的萃取率达99.5%,锰的萃取率>95%,钴的萃取率达95.5%,钴的沉淀率达99.9%。代梦雅等[40]采用溶剂萃取—化学沉淀法从废锂离子电池正极材料中回收硫酸钴、氢氧化镍和氟化锂,并比较了萃取剂P507、Cyanex272对钴、镍的萃取分离性能。结果发现,P507和Cyanex272均能实现从电极材料浸出液中萃取分离钴,萃取率分别为98.21%和99.44%,Cyanex272的萃取效果更好。
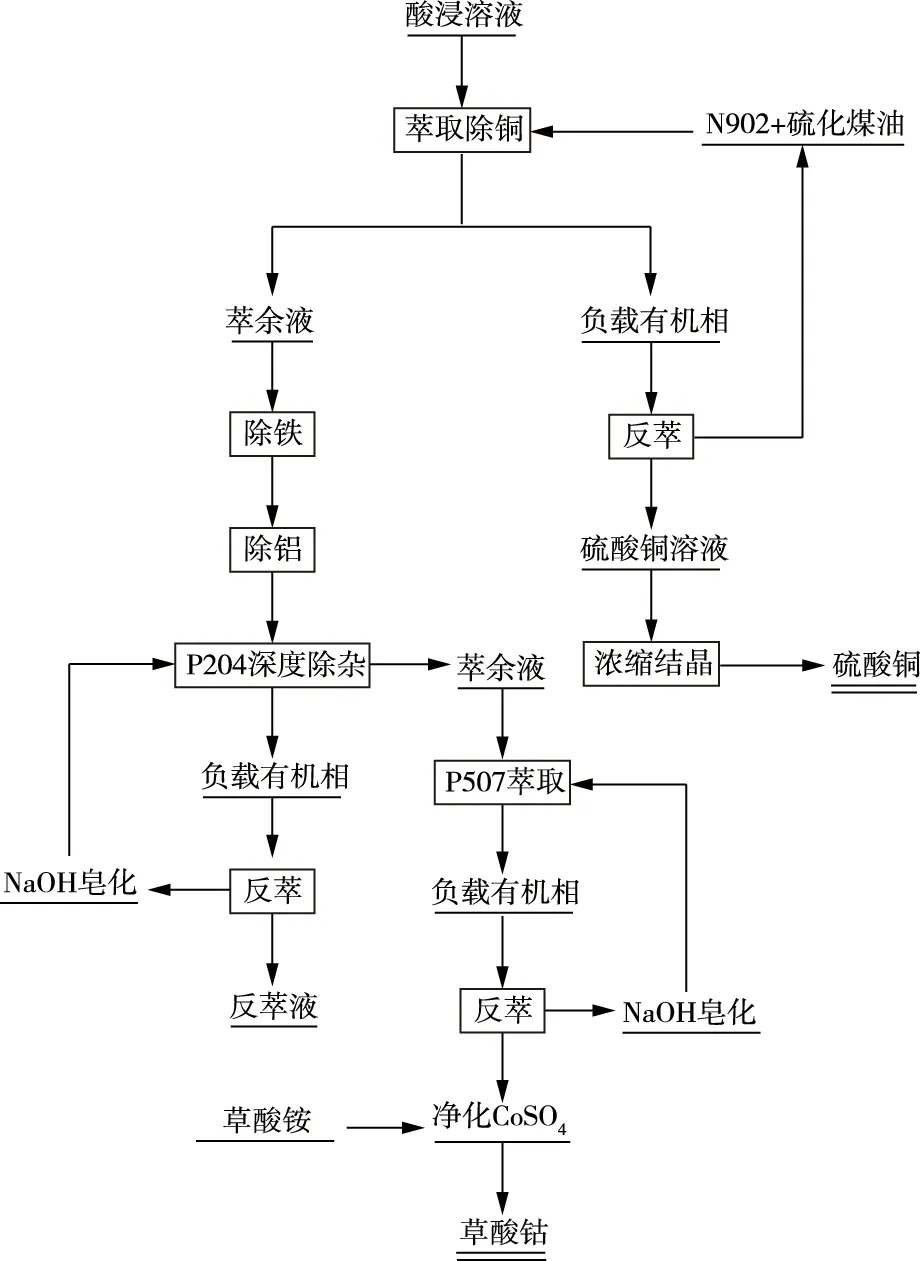
图1 净化工艺流程[21]Fig.1 Flowsheet of purification process[21]
王晓峰等[41]采用离子络合法和离子交换法相结合的方法对电极材料(主要成分为Co2O3,NiO,Al2O3,Al等)中的Ni、Co进行了回收。他们将电极材料有价金属盐酸酸溶富集于溶液之后,利用氨水调节pH值至4,除去杂质Al得到富含Ni、Co的净化液,再向净化液中加入含有一定量NH4Cl的氨水溶液,使Co2+、Ni2+分别转化为[Co(NH3)6]2+,[Ni(NH3)6]2+络合离子,利用[Co(NH3)6]2+在络合离子弱酸性阳离子交换树脂吸附系数比[Ni(NH3)6]2+大得多的特点,利用硫酸氨溶液(2 mol/L以上)和质量分数为5%的硫酸溶液分别将[Ni(NH3)6]2+、[Co(NH3)6]2+脱附,最终达到了分离回收的目的,获得的Ni、Co回收率分别为84.1%、89.9%。
沈勇峰[42]采用硫酸酸浸—电积工艺回收废锂电池中的有价金属钴,也实现了资源的有效回收。他们首先采用硫酸浸出废电极材料,使有价金属富集于溶液,之后向该溶液加入碳酸钠中和剂调节pH值至2~3,除去Al/Cu杂质,最后利用钴始极片为阴极、钛板为阳极对净化后液直接进行电积,在电流密度235 A/m2、电解液温度55~60 ℃下,钴的直收率能达到93%。
对废锂电池有价金属进行分离提取回收,涉及的工艺较长、成本较大且金属损失率较高。若直接对酸浸液进行净化除杂再生前驱体或加入一定碳酸锂煅烧制备正极材料,则不仅能高效回收有价金属,还能对资源进行有效利用,具有很大的经济优势和环境优势。如孔德鹏[43]采用酸浸—再生前驱体制备正极材料的工艺方法对废三元锂电池有价金属进行回收,达到了对资源的回收利用目的。其回收工艺流程为:还原酸浸→净化除杂→共沉淀→煅烧,最终得到了满足电池所需要的三元正极材料。在共沉淀及煅烧步骤中发现,以分步沉淀法、络合剂浓度2 mol/L、pH值8.5、金属离子溶液与沉淀剂并流滴加至NH4HCO3溶液中、煅烧温度900 ℃及混锂比例为1.0的制备条件为最佳,得到的正极材料Ni、Co、Mn元素分散均匀,颗粒尺寸大小均匀,电化学性能稳定,50次循环后,比容量保有率仍有93.4%。张岙[44]利用的络合沉淀剂是氨水和氢氧化钠体系,主要考察了进料速度、陈化时间、反应pH值、络合剂浓度等因素对前驱体形貌与粒径的影响规律。所得最佳工艺条件为:反应温度50 ℃、保护气氛N2、搅拌功率200 W、进料速度0.6 mL/min、陈化时间16 h、反应pH值为11.0±0.2,络合剂浓度0.4 mol/L,在该最佳条件下制备的前驱体球形程度较好、颗粒大小合适。
2.3 火法焙烧—湿法冶金联合法
火法焙烧—湿法冶金联合法是对废锂电池正极活性材料与还原剂/添加剂混匀进行高温焙烧,焙烧后得到的焙砂经过水/酸/碱浸可达到回收有价金属的目的。该方法可实现对个别金属(如Li)的优先提取,减少其在后续工序造成的损失,降低后续酸浸富集其他金属的难度,如不添加还原剂,就可以实现较高的浸出率。方法主要有碳热还原焙烧—水/酸浸、酸化焙烧—酸/水浸等。表2列举了采用火法焙烧—湿法冶金联合法回收废锂电池有价金属的主要方法。
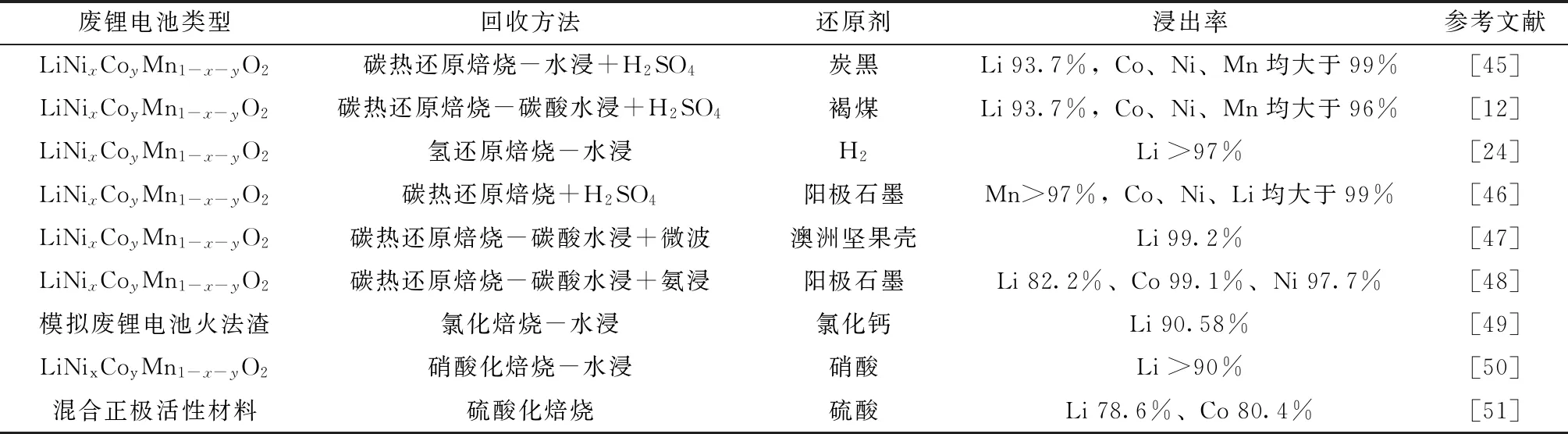
表2 采用火法焙烧—湿法冶金联合法回收废锂电池有价金属的主要方法Table 2 Main methods for recovering valuable metals from spent lithium-ion batteries by united pyro-roasting and hydrometallurgy
2.3.1 碳热还原焙烧—水/酸浸
在碳热还原焙烧过程中,正极活性材料有价金属Ni、Co、Mn以金属或金属氧化物的形式存在,Li以可溶于水的Li2CO3形式存在,对焙烧料依次进行水浸、酸浸,实现Li的优先提取及Ni、Co、Mn的回收。LIU等[45]采取该方法实现了废三元正极活性材料有价金属的分离提取回收,并发现Co、Ni、Mn和Li分别以Co、Ni、NiO、MnO和Li2CO3形式存在。水浸阶段,在液固比30 mL/g、时间90 min、温度25 ℃的条件下,Li的浸出率为93.68%;酸浸阶段,在H2SO4浓度4 mol/L、液固比(mL/g)值10、时间30 min、温度90 ℃的条件下,Co、Mn、Ni的浸出率分别为99.87%、99.9%、99.56%,其酸浸过程均受残留层扩散控制,表观活化能分别为24.00、23.29、29.35 kJ/mol。ZHANG等[12]发现碳热还原焙烧过程中,Co、Ni主要以合金的形式伴生,并从动力学上解释了Li2CO3难于水浸与其活化能较低有关。为改善Li2CO3难浸的问题,向水浸液中通入CO2气体,使其转化为易溶于水的LiHCO3,从而增大Li的选择浸出率。
HU等[52]利用碳还原焙烧—酸浸法将废三元锂电池有价金属浸出至溶液后,对酸浸液分别控制pH值3.5、加入氟盐将Fe、Ca、Mg等杂质去除,之后加入D2EHPA将Mn萃取分离,加入PC88A萃取分离Co、Ni,这样便达到了分离回收各个有价金属的目的。具体的工艺流程见图2。廖财斌等[53]
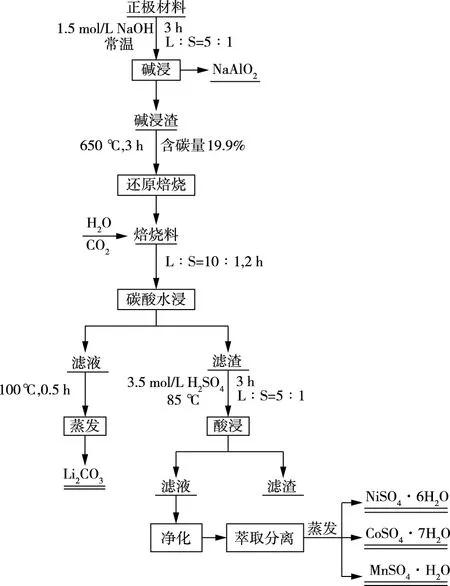
图2 废正极活性材料回收有价金属工艺流程[52]Fig.2 Flowsheet of recovery of valuable metal from spent positive active material[52]
研究了氟和磷杂质对三元正极废粉碳热还原—水浸提锂的影响,得出氟和磷的存在使焙烧料中存在部分的LiF或Li3PO4,从而降低Li的浸出率。在1.3倍于理论量的焦炭用量、焙烧温度800 ℃、焙烧时间60 min的最佳条件下,采用两段水浸,Li的浸出率仅71.62%。
2.3.2 酸化焙烧—酸/水浸
对正极活性材料采取硝酸化焙烧,有价金属转化为硝酸盐,根据分解温度的不同,设定焙烧温度,达到对个别金属的选择回收。如PENG等[50]采用该方法实现了从废三元正极活性材料中优先提锂的目的。对酸化后的物料在不同温度下焙烧,结合XRD分析的结果发现,在焙烧温度250 ℃下,Ni、Co、Mn、Al、Cu等硝酸盐均受热分解成相应的金属氧化物,而LiNO3未分解,仍存在于焙烧料中,对焙烧料进行水浸,实现Li的优先提取。
除硝酸化焙烧外,硫酸化焙烧也能实现对个别金属的优先回收。如PRATIMA等[51]研究发现,对废旧混合正极活性材料进行硫酸化焙烧,之后再对焙烧物料进行水浸,可将将Li和Co有选择地尽量多浸出。在焙烧温度300 ℃、2 mL H2SO4(0.37 mol/L)、焙烧时间30 min、水浸反应温度75 ℃、矿浆浓度25%和反应时间60 min的最佳条件下,大约有78.6%的Li和80.4%的Co被选择浸出,只有15.8%的Ni和12.9%的Mn被部分浸出。为了增加Li、Co的回收率,可选择混酸(H2SO4和HNO3)和葡萄糖体系对浸出渣进行二次浸出。而张贤等[54]采用低温碳还原硫酸熟化工艺回收废三元锂电池正极材料有价金属Ni、Co、Mn时发现,在反应温度250 ℃、反应时间30 min、硫酸和正极黑粉的用量比为0.97 mL/g的最佳工艺条件下,有价金属的回收率均超过了96%。说明碳的加入对硫酸化焙烧的效果有较大促进作用,降低了硫酸化焙烧的反应温度,提高了有价金属的回收率,并简化了反应所需工序。
火法焙烧—湿法冶金联合法的优点主要有:1)低温下就能实现正极活性材料结构的破坏,并使有价金属转化为后续易于浸出的形态;2)在后续水浸/酸浸阶段,不仅能实现个别金属(如Li)的优先提取,还能在不使用还原剂的情况下,达到有价金属的高效浸出。但该法的缺点也比较明显,如正极活性材料含有如氟、磷等杂质,对Li的浸出率有所影响;工序稍微繁琐,需要同时利用火法冶金和湿法冶金工序。
2.4 生物冶金法
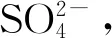
ZENG等[55]利用铁氧化细菌对废钴酸锂电池有价金属进行浸出,添加适量Cu2+催化剂,能显著增加Co的浸出率。原因是Cu2+能进一步降低Fe3+/Fe2+的氧化还原电位,促进Co3+被还原,从而增加Co的浸出率。AHMAD等[56]采用铁氧化细菌、硫氧化细菌混合细菌及两步酸浸法对废锂电池有价金属进行浸出,实现了Li 99.2%、Ni 89.4%、Co 50.4%的浸出率。JOSEPH等[57]通过增加H2SO4及多次补充铁氧化细菌的方式,实现了在100 g/L矿浆浓度情况下Co的高浸出率,在72 h内浸出率达到94%。该方法虽能实现较高的浸出率,但消耗大量的微生物细菌。
生物冶金与火法及湿法冶金相比,不需要消耗大量的试剂,过程不产生有毒烟气,且全过程反应温和,对设备要求不高,相应的投入成本较低,具有很大的环境及经济优势,但其弱点也较明显,整个生产过程对体系的内在要求比较苛刻,且反应周期长,特别是要求矿浆浓度低,严重制约了其在工业上的应用。
3 总结与展望
1)随着电池行业对锂电池需求量的快速增长,每年报废的锂电池量也将日益剧增。废锂电池含有大量有价金属及有毒电解质等,对其进行回收处理,可减少我国有价金属如Ni、Co、Li对外进口的依赖。对资源的循环利用及环境保护等方面均有重大意义。
2)废锂电池有价金属回收方法中,火法冶金耗能高,产生的废气量及渣量大,且只能产出合金中间产品;湿法冶金有酸浸富集及氨浸富集,需要消耗大量的酸/碱,生成的溶液分离纯化步骤繁琐,对设备要求高。氨浸富集能实现对个别金属的优先提取,但金属浸出率普遍不如酸浸富集;生物冶金在废锂电池有价金属回收上具有一定的难度,具体表现在废锂电池含有大量有价金属且含有毒电解质,对微生物活性具有一定的影响;火法焙烧—湿法冶金联合法在低温下就能实现正极活性材料结构的破坏,并使有价金属转化为后续易于浸出的形态;在后续水浸/酸浸阶段,不仅能实现个别金属(如Li)的优先提取,还能在不使用还原剂的情况下,达到有价金属的高效浸出,将来应用前景较好。
3)对于湿法冶金及火法焙烧—湿法冶金联合法得到的酸浸液,采取直接除杂制备前驱体工艺较为合理,一是该工艺所需流程短,成本上具有一定的优势,二是能降低Ni/Co/Mn在萃取分离上的损失率。

