临床药师参与左心室辅助装置植入术后感染治疗的病例分析
李雪 张寒娟 于丽
摘 要 目的:为临床左心室辅助装置植入术后感染患者的治疗提供参考依据与用药经验。方法:临床药师参与1例左心室辅助装置植入术后感染的治疗,协助医师制定给药方案,密切关注药物相互作用,提出个体化用药建议,并对患者进行药学监护。结果:临床药师根据血药浓度监测结果及时调整给药方案,治疗效果显著。结论:临床药师运用专业的药学知识与思维,协助治疗过程,保证了疗效,减少了不良反应的发生,体现了临床药师在多学科诊疗中的积极作用。
关键词 左心室辅助装置 心力衰竭 伏立康唑
中图分类号:R619.3; R654.2 文献标志码:B 文章编号:1006-1533(2021)17-0067-03
Case analysis of clinical pharmacist participating in the treatment of infection after left ventricular assist device implantation
LI Xue, ZHANG Hanjuan, YU Li
(Department of Pharmacy, the Seventh Peoples Hospital of Zhengzhou, Zhengzhou 450016, China)
ABSTRACT Objective: To provide reference basis and medication experience for the treatment of patients with infection after left ventricular assist device implantation. Methods: A clinical pharmacist participated in the consultation treatment of a case of infection after the implantation of the left ventricular assist device, assisted physicians in formulating drug administration plan, proposed individualized medication recommendations, and provided pharmaceutical care for the patient. Results: The therapeutic effect was significant after the administration plan was adjusted in time by the clinical pharmacist according to the results of the monitoring of blood concentrations. Conclusion: Clinical pharmacists use their professional pharmaceutical knowledge and thinking to assist physicians in the treatment process, which can ensure the curative effect, reduce the occurrence of adverse reactions, reflect the positive role of clinical pharmacists in multidisciplinary diagnosis and treatment.
KEy WORDS left ventricular assist devices; heart failure; voriconazole
左心室輔助装置(left ventricular assist device, LVAD)可提高终末期心力衰竭患者的生存率并降低其发病率[1-2]。感染是LVAD植入术后常见的并发症[3]。在过去的几年中,美国LVAD的临床应用呈稳步增长状态,然而在我国,接受LVAD管理的患者人数相对较少,关于LVAD感染的发生率、临床表现和预后的信息有限,且对于其术后抗感染的治疗方法尚未达成共识。因此本文通过临床药师参与的1例左心室辅助装置植入术后感染的病例进行分析,为临床上这一特殊群体的抗感染治疗提供个体化的参考依据。
1 病例资料
患者,男,45岁,体质量78.9 kg。主因“胸憋、气短、四肢末梢凉1 d”入院。患者于6年前无明显诱因出现咳嗽、咳痰,伴呕吐,当地医院诊断为“扩张型心肌病”,期间多次住院治疗,纠正心衰后症状缓解。2021年3月17日以症状加重,胸闷难以缓解于郑州市第七人民医院就诊。查体:双肺呼吸音稍粗,未闻及干湿性啰音,心前区无明显隆起,未触及震颤,心率80次/min,心律齐,心前区可闻及SM2/6级吹风样杂音,P2亢进,未闻及心包摩擦音。双下肢凹陷性水肿。入院诊断:①扩张型心肌病;②二尖瓣关闭不全;③三尖瓣关闭不全;④肺动脉高压;⑤终末期心衰;⑥心功能Ⅳ级。既往史无特殊,否认高血压、糖尿病,药物及食物过敏史。2021年4月21日行全麻体外LVAD植入术,围术期预防用药使用万古霉素、哌拉西林他唑巴坦钠,术后长期口服华法林钠片。因术后出现溶血,4月25日再次行LVAD植入术,术后无尿,行持续CRRT治疗,使用美罗培南预防感染。
2 临床药师介入后的治疗经过
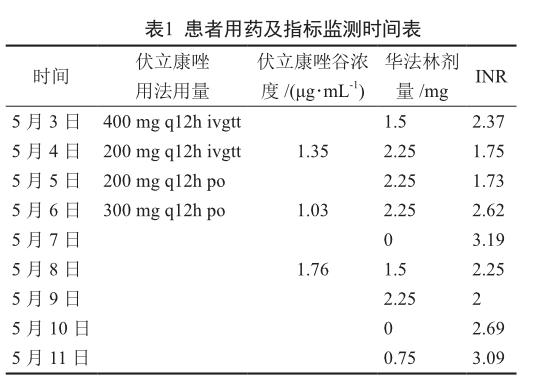
2021年5月2日,患者出现发热伴寒战,体温(T)38 °C,无咳嗽咳痰症状,无尿,继续连续肾脏替代疗法(continuous renal replacement therapy, CRRT)替代治疗。辅助检查:血常规白细胞计数(white blood cell count, WBC)17.9×109/L,N 89.9%;降钙素原(procalcitonin, PCT)0.66 ng/mL;肝肾功能:肌酐(creatinine, Cre)151 μmol/L,总胆红素(total bilirubin, TBil)47.8 μmol/L,转氨酶正常。连续2次G试验(+),GM试验(-);血细菌培养(-)。请临床药师会诊,临床药师建议停用美罗培南,使用米卡芬净100 mg ivgtt qd,同时更换中心静脉置管和CRRT管道并送导管尖端细菌培养,行血病原菌二代基因测序(nextgeneration sequencing, NGS)检查。5月3日,患者最高体温38 ℃,辅助检查:血常规WBC 16.86×109/L,N 87.5%;C反应蛋白(C-reaction protein, CRP) 123.57 mg/L;PCT 1.04 ng/mL;G试验(+)。全院多学科会诊建议将米卡芬净调整为伏立康唑200 mg q12h ivgtt。因为患者术后同时服用华法林,临床药师指出两者合用会增加患者出血风险,因此后续治疗中要加强患者用药监护。5月5日,患者T 37.6°C,血常规WBC 12.49×109/L,N 80.6%;PCT 0.45 ng/mL;各种导管尖端培养均(-);血NGS未检出致病菌。临床药师建议伏立康唑改为200 mg q12h po。5月6日,监测伏立康唑谷浓度1.03 μg/mL,药师建议伏立康唑剂量调整为300 mg q12h po。整个用药期间定期监测肝肾功能、电解质等,随时调整华法林剂量,使国际标准化比值(international normalized ratio, INR)控制在2~3范围内。经上述治疗后,患者无发热,复查血常规正常,PCT正常,G试验(-),于5月11日停用伏立康唑。具体用药和指标监测情况见表1。
3 讨论
3.1 LVAD患者感染治疗方案分析
ISHLT专家共识[4]指出,LVAD术后感染作为患者的主要并发症是患者发病率和死亡率增加的重要原因。5月2日该患者突然出现发热,感染指标升高,临床药师考虑存在术后感染可能。该患者为终末期心衰且心功能Ⅳ级,期间多次住院治疗,入院后分别行2次LVAD植入术,长时间使用广谱抗生素,并且肾功能较差,术后持续进行CRRT。连续两次监测G试验(+)。临床药师对其感染因素进行综合评价,考虑患者为真菌二重感染可能性大。在LVAD真菌感染的患者中,最常见的病原体是白色假丝酵母,约占70%,其病死率为15%~20%[5-6]。有研究表明假丝酵母感染的主要危险因素有全胃肠外营养、留置中心静脉导管、广谱抗菌药物暴露、使用糖皮质激素、腹部大手术等[7]。由于G试验可存在假阳性,连续2次的阳性结果提高了G试验对白色假丝酵母感染诊断的特异度[8]。综合考虑,该患者白色假丝酵母引起血流感染的可能性大。根据相关文献,白色假丝酵母感染血流感染首选棘白菌素类药物治疗[7]。因此,临床药师建议停用美罗培南,给予米卡芬净抗真菌治疗。由于白色假丝酵母易于各种管道定植,因此,建议更换、拔除各种管道,并行导管尖端微生物培养。
患者存在肝肾功能不全,持续CRRT可能会对药物的浓度产生影响,整个治疗过程均由临床药师确定给药剂量。米卡芬净血浆蛋白结合率高,非肾途径清除,CRRT下,不会影响其药物浓度,因此建议给予米卡芬净常规剂量100 mg ivgtt qd。多学科会诊调整米卡芬净为伏立康唑后,药师考虑伏立康唑主要经肝脏代谢清除,肾功能不全和CRRT情況下均无须调整其给药剂量。结合患者肝功能提示胆红素偏高,建议伏立康唑用量200 mg q12h ivgtt,首日24 h给予负荷剂量400 mg q12h以便快速达到稳态浓度,用药期间监测其谷浓度。
3.2 伏立康唑谷浓度测定的意义以及剂型和剂量调整的思考
研究表明,伏立康唑的谷浓度与治疗结果以及肝毒性的发生率具有显著相关性,而并没有证据表明稳态血药浓度与临床结果之间具有相关性[9-10]。因此伏立康唑谷浓度的测定对于临床结局以及不良反应的预测具有重要意义。临床药师在会诊中指出在用药过程中应该密切监测伏立康唑药物谷浓度,同时注意监测肝功能。根据伏立康唑说明书,口服制剂的生物利用度高达96%,在有临床指征时静脉和口服两种给药方式可以互换。中度到重度严重肾功能障碍患者应用静脉制剂时,可发生赋形剂磺丁倍他环糊精钠蓄积,此种患者宜选用口服给药。同时临床药师考虑到患者心功能较差,输入液体量较多,排尿量较少,会增加患者心脏负荷。因此病情控制后,建议患者改为口服伏立康唑片200 mg bid维持剂量。《伏立康唑个体化用药指南》中推荐[11],建议根据中国人群的群体药代动力学进行个体化剂量调整,如果患者伏立康唑谷浓度低于检测下限或者临床效果不佳,则建议增加维持剂量的50%,然后根据血药浓度进行后续调整。监测伏立康唑谷浓度为1.03 μg/mL,接近监测下限1.0μg/mL,同时考虑到患者服用华法林,2种药物竞争相同的代谢底物CYP2C9,因此临床药师建议将伏立康唑剂量调整为300 mg bid po,后复测伏立康唑谷浓度为1.76μg/mL。当患者在调整伏立康唑给药方案后,应及时重复监测伏立康唑药物谷浓度,保证其在目标浓度范围内,从而达到较好的治疗效果。
3.3 伏立康唑与华法林代谢的相互作用
华法林为一种外消旋混合物,由S型和R型两种异构体组成,其中S型的抗凝作用约为R型的5倍。S-华法林主要通过同工酶CYP2C9转化为非活性代谢物,R-华法林则通过CYP1A2、CYP2C19、CYP3A4等代谢。出血为华法林使用过程中最常见的并发症,这与其代谢过程具有密切相关性[12-13]。三唑类抗真菌药物伏立康唑通过CYP2C19、CYP2C9和CYP3A4代谢,同时也是这几种酶的抑制剂。伏立康唑通过抑制CYP2C9的活性而抑制华法林的代谢,从而使华法林血药浓度升高,抗凝作用增加。赵明等[14]的研究结果表明,与单用华法林相比,联用伏立康唑后INR平均升高2.59倍。因此对于华法林联用伏立康唑的患者,需要密切监测INR,及时调整剂量,以降低不良反应的发生率[15]。患者予伏立康唑联用华法林治疗期间,每天监测INR,期间有2次INR低于2,分别为1.75(2021年5月4日)和1.73(2021年5月5日),2次INR高于3,分别为3.19(2021年5月7日)和3.09(2021年5月11日)。临床药师根据INR及时调整华法林剂量,避免了抗凝不足和出血风险。
4 结语
本例患者左心室辅助装置植入术后出现感染症状,虽然没有明确的病原学检查结果,但结合患者的疾病情况及用药史,临床药师判断可能存在真菌感染。协同全院多学科会诊制定出治疗方案,结合治疗药物监测确定个体化给药剂量,获得了显著的治疗效果。同时,在该患者的抗真菌治疗中,临床药师关注伏立康唑与华法林的相互作用,进行严密的药学监护,及时调整华法林的给药剂量。总之,在该患者治疗过程中,临床药师运用药学专业知识和思维,帮助医师调整用药方案,保障了患者的用药安全与用药疗效。
参考文献
[1] Mehra MR, Naka Y, Uriel N, et al. A fully magnetically levitated circulatory pump for advanced heart failure[J]. N Engl J Med, 2016, 376(5): 440.
[2] Son AY, Stein LH, DeAnda A, et al. Impact of chlorhexidine gluconate intolerance on driveline infection during chronic HeartMate II left ventricular assist device support[J]. Int J Artif Organs, 2017, 39(11): 570-574.
[3] Drakos SG, Kfoury AG, Selzman CH, et al. Left ventricular assist device unloading effects on myocardial structure and function: current status of the field and call for action[J]. Curr Opin Cardiol, 2011, 26(3): 245-255.
[4] Kirklin JK, Naftel D, Pagani FD, et al. Seventh INTERMACS annual report: 15 000 patients and counting[J]. J Heart Lung Transplant, 2015, 34(12): 1495-1504.
[5] Riaz T, Nienaber JJC, Baddour LM, et al. Cardiovascular implantable electronic device infections in left ventricular assist device recipients[J]. Pacing Clin Electrophysiol, 2014, 37(2): 225-230.
[6] de By TMMH, Mohacsi P, Gahl B, et al. The European Registry for Patients with Mechanical Circulatory Support(EUROMACS) of the European Association for CardioThoracic Surgery (EACTS): second report[J]. Eur J Cardiothorac Surg, 2018, 53(2): 309-316.
[7] 中国成人念珠菌病诊断与治疗专家共识组. 中国成人念珠菌病诊断与治疗专家共识[J]. 中华内科杂志, 2020, 59(1):5-17.
[8] 周梦兰, 徐英春, 赵玉沛. 侵袭性真菌病血清学检测研究进展[J]. 中国感染与化疗杂志, 2018, 18(1): 118-123.
[9] Gordon RJ, Weinberg AD, Pagani FD, et al. Prospective, multicenter study of ventricular assist device infections[J]. Circulation, 2013, 127(6): 691-702.
[10] Chen K, Zhang X, Ke X, et al. Individualized medication of voriconazole: a practice guideline of the division of therapeutic drug monitoring, Chinese pharmacological society[J]. Ther Drug Monit, 2018, 40(6): 663-674.
[11] 陳恳, 张相林, 克晓燕, 等. 《伏立康唑个体化用药指南》解读[J]. 临床药物治疗杂志, 2019, 17(3): 47-52.
[12] Jin H, Wang T, Falcione BA, et al. Trough concentration of voriconazole and its relationship with efficacy and safety: a systematic review and meta-analysis[J]. J Antimicrob Chemother, 2016, 71(7): 1772-1785.
[13] 刘瑜新, 傅静兰, 夏霄彤, 等. 华法林与唑类抗真菌药物相互作用及其机制研究进展[J]. 中国临床药理学杂志, 2019, 35(13): 1406-1409.
[14] 赵明, 梁良, 张亚同, 等. 唑类抗真菌药物对华法林抗凝活性影响的临床分析和比较[J]. 中国药物警戒, 2016, 13(2): 111-114.
[15] 幸海燕, 邓冬梅, 程彩奕, 等. 1例伏立康唑治疗支气管扩张继发肺曲霉球患者的药学监护[J]. 中国现代应用药学, 2020, 37(23): 2898-2901.

