深低温停循环全弓置换术病人术后出现神经系统并发症的危险因素分析及护理措施
冯蓓娟,黄万珍,李 云
深低温停循环全弓置换术是治疗先天性心脏病、Stanford A型、B型主动脉夹层及主动脉瘤的有效方法,其中深低温停循环能够为手术提供一个相对无血的术野,利于手术的顺利实施;同时低温可在一定程度上减轻谷氨酸的释放所致的神经兴奋毒性,影响钙内流、氧自由基的形成过程,从而起到脑保护的作用[1-2]。但由于深低温停循环手术过程中机体多系统持续处于低温、低血缺氧及炎性反应的内环境中,出现乳酸持续升高、代谢紊乱等微循环障碍,术后极易出现一系列并发症,其中又以神经系统的并发症最为常见且最为严重[3-4]。近年来尽管手术技术及脑保护措施不断发展,但神经系统并发症发病率仍居高不下[5]。神经系统并发症的发生不仅会降低手术治疗效果,不利于病情控制及预后状况,而且会明显增加病人住院时间及治疗费用,加重病人的经济、心理负担,严重影响病人身心健康及生活质量[6-7]。因此,如何预防及减少该类并发症的发生是临床亟需解决的焦点问题。本研究以近年来在我院接受深低温停循环全弓置换术的80例病人为研究对象,分析术后神经系统并发症发生的危险因素及护理措施。
1 对象与方法
1.1 研究对象 选取2018年1月—2020年5月在我院接受深低温停循环全弓置换术的80例病人为研究对象,其中男59例,女21例,年龄22~68(48.12±8.35)岁;体重53~98(75.26±10.08)kg;Stanfor A型主动脉夹层47例,B型主动脉夹层26例,升主动脉瘤7例;出血量15~90(48.40±20.16)mL;基础疾病:合并高血压53例,糖尿病13例,脑梗死5例。
1.2 纳入及排除标准 纳入标准:术前意识清晰,无认知、沟通障碍;术前血流动力学稳定;近3个月内未服用过激素类、神经类药物;无全弓置换术禁忌证;初次相关手术。排除标准:酒精或药物滥用史者;有冠心病病史或肢体功能障碍者;精神系统疾病者;肾上腺病变者;临床资料完善,能完成研究配合者。本研究经医院伦理委员会批准,入组病人均知情并签署知情同意书。
1.3 麻醉、体外循环及手术方法 所有手术均采用静脉及吸入复合麻醉,全身麻醉成功后经右心房、右股动脉或右腋动脉穿刺置管,建立体外循环。转流开始后行全身降温,阻断升主动脉,鼻咽温度降至28 ℃时先完成主动脉近心端的操作;鼻咽温度降至16~22 ℃时,暂停体外循环,阻断头臂血管,降低动脉灌注流量至5~10 mL/(kg·min),经左锁骨下动脉开口远端横行剪开主动脉血管,置入支架型人工血管,完成主动脉弓部、弓降部的手术处理后,经右锁骨下动脉或右腋动脉或颈总动脉行顺行性脑灌注,恢复体外循环并开始复温,待鼻咽温、膀胱温恢复至36.5 ℃以上时,调整血流动力学及体外循环流量,停止体外循环,止血关胸,完成手术。
1.4 术后神经系统并发症的评定 评定标准:术后病人出现嗜睡、昏迷、谵妄、躁动、精神分裂、精神错乱、苏醒延迟等意识障碍;认知及语言障碍;肢体运动障碍;行影像检查无阳性表现。由神经科医生结合以上评定标准进行诊断,并根据术后有无出现神经系统并发症,将其分为并发症组和非并发症组。
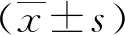
2 结果
2.1 术后神经系统并发症发生情况及单因素分析 术后25例病人出现神经系统并发症,发生率为31.25%;单因素分析显示,两组病人在高血压病史、术前神经系统症状、术前血肌酐水平、术前白细胞计数、手术时间、深低温停循环时间、体外循环时间、术中峰值血糖、术中峰值血乳酸、术中输血量、术后24 h血钠水平相比差异有统计学意义(P<0.05),见表1。
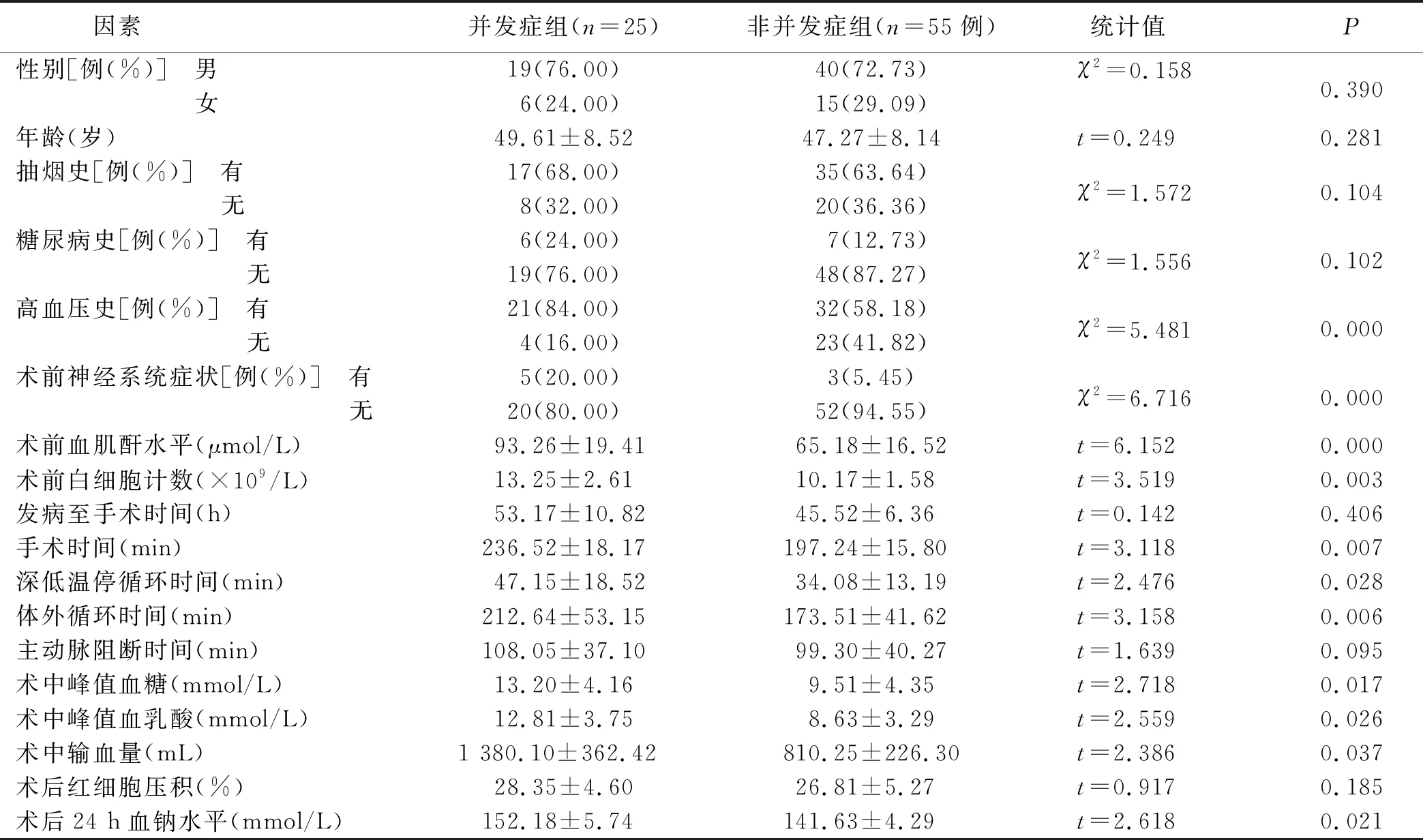
表1 影响术后神经系统并发症发生的单因素分析
2.2 影响术后神经系统并发症发生的多因素Logistic回归分析 以术后发生神经系统并发症为因变量,将单因素分析中P<0.05的因素作为自变量,进行多因素Logistic回归方程分析,结果显示有高血压病史、术前血肌酐值高、术前白细胞值高、深低温停循环时间长、体外循环时间长、术中高血糖是影响病人术后神经系统并发症发生的危险因素(P<0.05),见表2。

表2 影响术后神经系统并发症发生的多因素Logistic回归分析
3 讨论
3.1 影响术后神经系统并发症发生的危险因素分析 国外文献显示,深低温停循环主动脉手术后神经系统并发症发生率为14.1%~45.7%[8]。本研究术后25例病人出现神经系统并发症,发生率为31.25%,与国外文献结果相符。经单因素、多因素Logistic回归分析显示,病人术后神经系统并发症的发生与高血压病史、术前血肌酐水平、术前白细胞计数、深低温停循环时间、体外循环时间、术中峰值血糖等因素密切相关。①有高血压病史是术后神经系统并发症发生的独立危险因素,与宋志强等[9]研究结果一致。高血压病病人对脑血管的自我调节能力及围术期低血压的耐受性降低,易发生血管粥样硬化,导致脑供血不足、术中栓子脱落、栓塞,均可导致神经系统并发症的发生[10-11]。②术前血肌酐高是术后神经系统并发症发生的独立危险因素,原因可能与术前血肌酐值高者,术中出现全身炎性反应、缺血再灌注损伤的风险较大,会导致肾功能进一步恶化,造成体内毒素、代谢产物大量堆积,进而损伤脑神经系统有关[12-13]。③术前白细胞值高是术后神经系统并发症发生的危险因素,与刘红等[14]研究结果一致。究其原因是:术前白细胞值高表明机体处于炎症应激状态,大量炎性物质合成、分泌和表达,损伤自身正常组织,并释放相关炎性因子,进一步加重炎症反应;同时白细胞大量出现会削弱血脑屏障功能,上调内皮细胞黏附分子的表达,使血小板、炎性物质大量聚集,造成微血管堵塞,导致脑供血不足,引起神经细胞缺血性损伤,最终导致神经系统并发症的发生[15-16]。④刘海渊等[17]研究显示,深低温停循环时间>40 min会增加神经系统并发症的发生风险,与本研究结果相符。原因可能与脑动脉内皮细胞可在20 ℃时释放血管物质,引起脑动脉血管收缩、血流灌注减少,导致脑部有效血管灌注不足有关。⑤体外循环时间长是术后神经系统并发症发生的独立危险因素,与汪博闻等[18]研究结果一致,原因可能是:体外循环会引起机体血流动力学变化,降低血液流量,减少血管灌注,导致脑缺血缺氧;随着体外循环过程中血液与体外循环装置的长时间接触,会增加炎性因子释放,加剧脏器缺血-再灌注损伤及脑部细胞组织的破坏;同时体外循环过程中的血液稀释会引起水潴留、脑血流分布不均及携氧能力下降,进一步增加神经系统并发症的发生风险[19-20]。⑥术中高血糖是术后神经系统并发症发生的独立危险因素,原因可能是:术中高血糖会引起天门冬氨酸、谷氨酸的大量释放,增加脑神经兴奋性及脑组织耗氧量,加剧术中脑灌注不足,脑组织出现缺血、缺氧,导致脑神经系统出现缺血缺氧性损伤[21]。
3.2 护理措施
3.2.1 加强术前评估及干预 术前应对病人一般资料、既往病史、血压、血糖、血肌酐、白细胞计数等进行全面评估,加强对影响术后神经功能并发症相关危险因素的管理。对存在高血压病史、术前血肌酐值高、术前白细胞值高的病人给予重点关注并给予相应干预措施。对于术前血压>140/90 mmHg(1 mmHg=0.133 kPa)者应采用扩血管药物硝普钠10 g/(kg·min)微量泵降压,并配合使用β受体阻断剂。降压过程中应严密监测病人血压、心率、意识、血氧饱和度情况,注意控制药量及速度,避免血压、心率剧烈波动,以用药30~60 min达到目标血压、目标心率为宜;对于术前血肌酐值高、术前白细胞值高者应积极给予抗感染治疗,减轻机体炎症状态,降低血肌酐水平及白细胞计数,以防血肌酐水平及白细胞计数过高引起的神经系统并发症[22]。
3.2.2 术中采取脑保护措施 术中尽量缩短体外循环时间及深低温停循环时间,使其控制在安全时限内;术中加强温度管理,待鼻咽温度降至25 ℃时停循环,头部给予冰帽以降低脑细胞代谢需求;复温过程中保持氧供需平衡,可再持续低灌注一段时间,待静脉血氧饱和度>80%时行阶段性复温,以防因复温过快、温差过大引起的代谢不均衡所致的术后神经系统并发症;术中加强对血糖的监测及控制,并采用输注甘露醇、泼尼松、人血白蛋白等方法,减轻脑水肿、全身炎症反应综合征。
3.2.3 加强术后干预 术后应严密监测病人血压、血糖、电解质变化,维持血流动力学稳定。对血压过高者应积极补充血容量,同时使用佩尔地平或硝酸甘油控制血压,将收缩压控制在100~130 mmHg,舒张压60~90 mmHg;对血糖过高者给予生理盐水50 mL联合胰岛素50 U静脉泵入,使血糖维持在6.0~12.0 mmoL;对术后出现神经系统并发症者应及时给予脱水、醒脑、营养脑细胞及脑保护等对症治疗,必要时行高压氧舱治疗,以减轻、控制并发症症状。
综上所述,深低温停循环全弓置换术病人术后神经系统并发症受多种因素影响,围术期应加强其相关危险因素的管理并提前采取干预措施,合理控制术前血肌酐、白细胞、血压及术中血糖水平,尽量缩短体外循环时间、深低温停循环时间,以减少术后神经系统并发症的发生。
——体外循环质量控制的基石

