褐飞虱体内共生菌多样性研究进展
申屠旭萍, 史嘉腾, 宋 阳, 俞晓平
(中国计量大学生命科学学院, 浙江省生物计量及检验检疫技术重点实验室, 杭州 310018)
褐飞虱Nilaparvatalugens属半翅目(Hemiptera)飞虱科(Delphacidae),是一种只以水稻或野生稻韧皮部汁液为食的远距离迁飞性害虫(Xueetal., 2013)。目前,褐飞虱作为亚洲稻区最主要的害虫之一(程家安和祝增荣, 2017),其防治仍然主要依赖于喷施化学农药和种植抗性水稻品种。化学农药能有效控制褐飞虱的发生,但长期以来大量、单一和频繁地使用化学杀虫剂,不仅严重污染了环境,同时也不可避免地造成了褐飞虱对化学杀虫剂产生抗药性。水稻抗虫品种由于其良好的生态效应而备受推崇, 但褐飞虱在与水稻抗虫品种相互作用的过程中,其致害性发生了变异,致使推广的抗虫品种逐渐丧失其原有的抗性(Luetal., 2004; 陈峰等, 2009)。
共生菌在昆虫漫长的进化史中扮演了举足轻重的角色,被誉为昆虫特殊的“多功能器官”(Henryetal., 2015; 杨义婷等, 2016)。与其他刺吸式昆虫相同,褐飞虱体内也含有大量共生菌,主要是以类酵母共生菌(yeast-like symbiont, YLS)为主的共生真菌以及杀雄菌属Arsenophonus和沃尔巴克氏体Wolbachia等为代表的共生细菌(Tangetal., 2010; 唐明等, 2014)。研究表明,种类丰富的共生菌在功能上同样具有多样性,共生菌在褐飞虱的生长、发育、繁殖、营养代谢和免疫等多方面起到至关重要作用(徐红星等, 2014; Juetal., 2020)。另有研究证实,褐飞虱的抗药性以及致害性的发展也与其体内种类繁多的共生菌有着密不可分的联系(Luetal., 2004; 禹海鑫, 2013; 廖逊等, 2019)。褐飞虱内共生菌存在的部位主要为腹部脂肪体和肠道组织。近年来,研究人员在卵巢、唾液腺以及产卵管附近也发现了共生菌的存在,这为共生菌在褐飞虱不同组织之间的扩散机制及功能的研究提供了方向(Zhangetal., 2019)。目前褐飞虱共生菌种类多样性研究主要是采用分子生物学方法和高通量测序技术。本文综述了褐飞虱内共生菌的种类以及它们的功能,期望为进一步阐明褐飞虱内共生菌与宿主间的关系提供参考和思路。
1 褐飞虱体内共生菌概况
1.1 褐飞虱体内共生真菌
早在20世纪60年代,Nasu(1963)就从褐飞虱腹部脂肪体内分离到了一类酵母样的共生真菌即类酵母共生菌(YLS),并对其形态进行了描述。研究证实,褐飞虱共生真菌并非由单一菌株组成,随着分子生物学技术的发展以及高通量测序技术的推广应用,褐飞虱肠道、脂肪体、卵巢等组织中越来越多的共生真菌种类被明确(何林懋, 2018; 王天召等, 2019)。Noda等(1995)首次采用18S rDNA序列作为目的序列,对褐飞虱内共生真菌进行分离鉴定,发现其与子囊菌亚门(Ascomycotina)核菌纲(Pyrenomycetes)麦角菌目(Clavicipitales)的金孢酵母菌Hypomyceschrysospermus亲缘关系最近。后续有关褐飞虱共生菌研究报道中为了突显Noda在这方面做的重大贡献,也简称其为Noda菌。随后Suh等(2001)在其基础上将YLS与其他昆虫病原菌进行比较分析后认为YLS属于真子囊菌纲(Euascomycetes)肉座菌目(Hypocreales)麦角菌科(Clavicipitaceae)。此外,张珏锋等(2009)首次通过卵块分离培养的方法从褐飞虱卵中成功分离到了嗜盐梗孢酵母Sterigmatomyceshalophilus和解脂亚罗酵母Yarrowialipolytica两株类酵母共生菌,而禹海鑫(2013)对褐飞虱腹部脂肪体转录组测序分析表明确实存在这两个属的真菌,这也从侧面证实了褐飞虱类酵母共生菌可经卵垂直传递给下一代。目前,在褐飞虱体内鉴定并报道的共生真菌(测序丰度>0.1%)已有19属(表1),其中Noda菌、毕赤酵母属Pichia、隐球酵母属Cryptococcussp、假丝酵母属Candida和亚罗酵母属Yarrowia为褐飞虱体内的常见共生真菌。
1.2 褐飞虱体内共生细菌
相比于共生真菌,褐飞虱共生细菌的研究起步较晚,但随着近年来肠道微生物多样性研究的兴起,褐飞虱肠道细菌的多样性研究陆续见报道。研究表明,褐飞虱的共生细菌除了存在于肠道,同时在脂肪体、唾液腺以及卵巢中均有分布(唐明等, 2014; Zhangetal., 2019)。早在21世纪初,Wolbachia就被发现存在于褐飞虱体内(甘波谊等, 2000),随后陆续有更多共生细菌从褐飞虱体内被鉴定。但由于褐飞虱内共生细菌多为次级共生菌,共生关系不稳定,因此不同地理位置、取食不同品种水稻的褐飞虱体内共生细菌的种类不尽相同。目前在褐飞虱体内鉴定并报道(测序丰度>0.1%)的共生细菌已有53个属(表2),其中Wolbachia、杀雄菌属Arenophonus、肠杆菌属Enterobacter、不动杆菌属Acinetobacter、芽孢杆菌属Bacillus、沙雷菌属Serratia和醋酸菌属Asaia为褐飞虱体内常见的共生细菌。
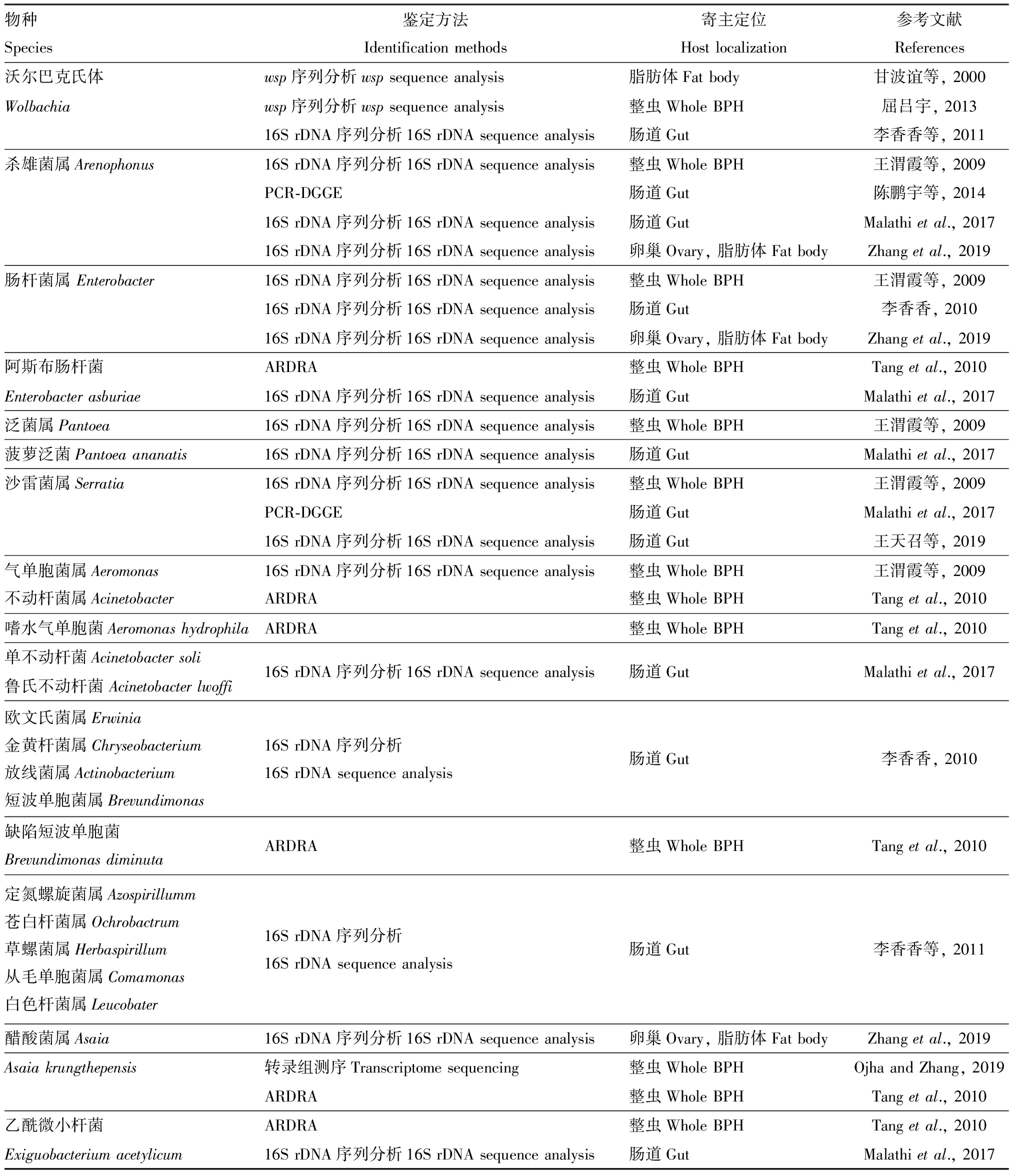
表2 褐飞虱体内共生细菌(测序丰度>0.1%)Table 2 Symbiotic bacteria in Nilaparvata lugens (sequencing abundance>0.1%)

续表2 Table 2 continued
2 褐飞虱体内共生菌的功能
2.1 营养功能
2.1.1合成固醇类物质:褐飞虱与其他昆虫一样无法通过自身从头合成胆固醇,而其单一的食性也使其无法从食物中获取生命活动所必需的胆固醇。研究表明,褐飞虱体内的胆固醇合成与体内共生菌有紧密联系,减菌处理下的飞虱虫体固醇类物质的含量显著降低(Noda and Saito, 1979)。Xue等(2014)在完成褐飞虱全基因组测序分析后发现,褐飞虱基因组与其体内YLS的基因组在固醇类物质合成通路上高度互补。此外YLS基因组中编码C-22脱饱和酶的基因ERG5发生了无义突变,因此YLS无法合成自身所需的麦角固醇,而累积的中间产物麦角甾-5,7,24(28)-三烯则通过褐飞虱以及YLS基因组中发现的7-脱氢胆甾醇还原酶(EC1.3.1.21)和甾醇24-C甲基转移酶(EC2.1.1.41)基因参与合成胆固醇,这恰恰从基因组学上证实了Wetzel等(1992)在飞虱体内检测到胆固醇却检测不到麦角固醇的现象。YLS基因组中合成麦角固醇的基因突变,可能是导致YLS无法正常形成细胞膜从而难以离体培养的重要原因之一(范海伟, 2015)。
2.1.2合成必需氨基酸:褐飞虱同样无法从水稻汁液中获取全部20种氨基酸作为其生命活动的基本营养物质,因此,褐飞虱需要通过自身或者其体内共生菌来合成所需的氨基酸。傅强等(2001)将卵高温减菌处理后发现:孵化出的若虫如果用不添加8种必需氨基酸的营养液饲养,羽化率和对照相比显著降低,说明YLS减少导致8种必需氨基酸合成的量减少,从而影响了褐飞虱的生长发育。王国超(2005)进一步研究发现,必需氨基酸的缺失一定程度上能够促进褐飞虱YLS增殖,从而通过YLS合成必需氨基酸弥补虫体对这些氨基酸的需求。高通量测序结果也显示了褐飞虱本身的基因组注释的基因无法独立合成必需氨基酸,但在其YLS基因组中却发现了完整的氨基酸代谢通路基因,这同样证明了YLS在一定程度上弥补了褐飞虱无法从食物中获取或自身无法合成必需氨基酸的缺陷(Xueetal., 2014)。然而,Zhang等(2019)对褐飞虱脂肪体以及卵巢的共生细菌进行KEGG通路分析发现,氨基酸的代谢以及生物合成是第二丰富的KEGG通路,说明褐飞虱所需的氨基酸合成也与其体内的共生细菌相关,但具体机制尚未阐明,推测共生细菌在这些氨基酸合成通路的辅助因子合成中起重要作用。
氮素循环通路是褐飞虱氨基酸的另一来源。研究表明褐飞虱与YLS在氮素循环路径上具有互补的能力。YLS能与褐飞虱一起对储存在褐飞虱脂肪体细胞中的尿酸进行利用,两者互补具有氮素循环和氨同化通路上的所有基因,两者中任意一个基因的丢失都将导致这个代谢通路终止(范海伟,2015)。另外,Xue等(2014)还发现在其他昆虫基因组中鲜有却存在于褐飞虱基因组中的编码尿酸酶的基因,进化过程中这个基因的保留抑或获得,便于其在尿酸产物不断增长的情况下更好地实现氮素的循环利用。这一发现也合理地解释了在整虫以及分离出的YLS中都能检测到尿酸酶活性的现象(Hongoh and Ishikawa, 1997)。褐飞虱和YLS基因组通过亲密的合作,将尿酸成功地转化为氨,并进一步转化为必需氨基酸合成所需的前体(谷氨酸和谷氨酰胺)。
2.1.3合成维生素:维生素作为一大类营养物质,同样是褐飞虱生命活动所必需的。基因组分析结果显示,褐飞虱脂肪体内杀雄菌属Arenophonus这类共生细菌含有完整的B族维生素合成通路基因,这恰恰也是褐飞虱与YLS基因组中缺失的(Xueetal., 2014)。Ju等(2020)对褐飞虱体内另一常见昆虫共生细菌Wolbachia基因组分析发现其具有完整的维生素B2和B7的生物合成通路基因,并且进一步证明了缺少Wolbachia的褐飞虱体内维生素B2和B7含量显著降低。这说明了Wolbachia与Arenophonus在褐飞虱体内具有类似的功能,均可以为褐飞虱提供B族维生素,与屈吕宇(2013)发现的Wolbachia与Arenophonus在褐飞虱体内具有相似的生态位且互为竞争关系这一结果不谋而合。
褐飞虱体内共生菌营养功能概括如图1。
2.2 抗性发展功能
2.2.1褐飞虱致害性变异:培育抗性水稻作为防治褐飞虱的有效手段,近年来一直面临着褐飞虱致害性变异的困境。研究表明,褐飞虱体内YLS与其致害性变异密切相关(吕仲贤等, 2001; Luetal., 2004)。转录组学分析同样证实了褐飞虱内共生菌与其致害性变异的紧密关系,禹海鑫(2013)发现Mudgo抗性水稻饲养的褐飞虱种群中Wolbachia的许多代谢基因有所上调,并且具有更高的增殖能力,说明Wolbachia在褐飞虱适应Mudgo抗性水稻过程中起关键作用。取食不同抗性水稻品种的褐飞虱肠道共生细菌种类以及丰度存在显著的变化(王天召等, 2019),并且随着褐飞虱对抗性水稻的适应性增强,其后代肠道内的共生细菌多样性变化逐渐趋于稳定,这说明了褐飞虱致害性的变化与其体内共生菌多样性变化有关(Wangetal., 2015; Ojha and Zhang, 2019)。然而共生菌多样性影响褐飞虱致害性的具体机理仍未明确。
2.2.2褐飞虱抗药性发展:使用化学杀虫剂防治褐飞虱是目前最经济、常用的手段,然而不可避免地导致褐飞虱对化学农药产生了较高的抗性。目前,褐飞虱抗药性发展的报道屡见不鲜,但共生菌在其中的作用保持未知。李香香(2010)在取食了杀菌剂处理的水稻苗的褐飞虱肠道中成功分离并采用氟虫腈驯化得到了一株不动杆菌属Acinetobacter细菌,说明了不动杆菌属细菌可能是褐飞虱对氟虫腈产生抗性的原因之一。Malathi等(2018)也在野外具有抗药性的褐飞虱种群的共生细菌基因组中发现了富含解毒功能的基因。然而,Zhang等(2018)对褐飞虱田间抗性种群以及实验室敏感种群肠道共生细菌进行功能分析时发现,这两个种群的解毒和代谢相关的基因表达没有显著差异,说明肠道共生菌并不是直接参与褐飞虱的解毒代谢。唐涛(2019)则用四环素和环丙沙星处理田间褐飞虱种群后,发现其对吡虫啉等杀虫剂敏感性显著增加,而测序和荧光定量PCR分析表明杀菌剂处理后褐飞虱谷胱甘肽S-转移酶和细胞色素P450这些解毒酶活力下调,同时共生菌Arsenophonus和Acinetobacter的拷贝数均显著下降,从侧面印证了褐飞虱的共生菌间接介导了褐飞虱的解毒代谢。而Pang等(2018)则发现S型的Arsenophonus替代原有共生细菌Arsenophonus能够降低褐飞虱对杀虫剂的抗性,转录组以及代谢物的分析结果显示感染S型Arsenophonus的褐飞虱的异质代谢能力显著下降。
2.3 对宿主繁殖的影响
褐飞虱对水稻种植业的危害巨大,与其强大的繁殖能力有着紧密的关系。早在20世纪80年代,Lee和Hou(1987)就通过高温以及溶菌酶处理褐飞虱的卵,结果发现处理后的卵无法孵化。进一步研究发现,在卵减菌的情况下,褐飞虱胚胎发育以及胚后发育所需的某种蛋白无法合成,并且胚胎的腹节分化受阻,从而证明了共生菌能影响褐飞虱的繁殖。后续研究发现,褐飞虱脂肪体内的卵黄原蛋白(vitellogenin, Vg)在其胚胎发育阶段起重要作用,而共生菌的垂直传递与胚胎吸收Vg在时空上具有显著的相关性(南国辉, 2016; 王小龙, 2019)。吕仲贤等(2001)则采用喂食抗性水稻使褐飞虱共生菌数量减少,结果显示,共生菌数量减少的褐飞虱雌成虫在体重、生长速率以及产卵量等指标与取食敏感品系水稻相比均显著下降。此外,研究发现褐飞虱脂肪体内共生细菌Wolbachia能够产生维生素B2和B7,从而直接增加宿主的产卵力(Juetal., 2020)。
3 小结与展望
共生菌在褐飞虱的生命活动中起到了举足轻重的作用。褐飞虱体内的共生菌由种类丰富的共生真菌与共生细菌组成,而不同种类的共生菌发挥着不同的功能,维持着褐飞虱体内的微生态平衡。因此,研究褐飞虱共生菌的多样性,探究其种类组成对了解共生菌与褐飞虱间的关系具有重要的意义。目前,褐飞虱内共生菌多样性的研究已经取得了一定的进展,尤其是随着高通量测序技术的发展,越来越多共生菌的分类地位被明确,但仍然有相当部分共生菌相关的科学问题亟待探究或者解决。
首先,褐飞虱体内到底有多少种共生菌仍未明确。不同翅型、不同发育阶段、不同性别以及不同地理种群或不同抗性种群间的褐飞虱体内共生菌是否存在差异?如果是,又存在哪些差异共生菌,占比有什么变化?要想全盘了解褐飞虱体内的共生菌,需对不同褐飞虱种群的共生菌多样性进行系统研究,从中明确各处理间共生菌的差异,为进一步研究共生菌功能如共生菌是如何介导宿主对化学杀虫剂产生抗药性等奠定基础。
第二,开展某一特定共生菌的功能研究非常困难。迄今针对共生菌功能的研究仍主要停留在整个菌群对褐飞虱的影响,由于褐飞虱YLS的基因组缺失了许多侵染和有性生殖相关的基因,无法脱离宿主独立增殖,因此其与宿主的共生关系更为紧密,难以分离培养。此外,褐飞虱又不能脱离共生菌单独存活,也即实际研究中不可能获得无菌的褐飞虱,这两方面原因导致难以对某一种类共生菌的功能进行单独研究。目前分别有通过抗生素处理除菌和胚胎注射共生菌的方法进行共生菌功能研究(Pangetal., 2018; Juetal., 2020),但这两种方法都存在一定的缺陷。通过抗生素处理除菌并不能单独除去想要研究的单一靶标菌,往往会抑制多种共生菌,所以并不能获得只有靶标菌存在差异的两组褐飞虱种群处理组,也就无法说明褐飞虱各生长特性指标或者各参数变化纯粹是由靶标共生菌引起的。胚胎注射方法本身难度系数极高,因为褐飞虱卵非常小,要在这么小的卵中通过显微注射方法外源加入共生菌,这操作难度系数很大,一不小心就会导致卵破裂;同时想要注射共生菌,那么这共生菌必须能离体培养,而从进化角度分析能离体培养的菌往往和宿主共生关系不紧密,研究这些共生菌(次生共生菌)的功能相比初生共生菌在重要性上就处于劣势;也有学者从不同褐飞虱种群中提取血淋巴注射到另一褐飞虱种群中,但血淋巴中也不仅仅含有要研究的靶标共生菌,注射时也带入了其他共生菌到褐飞虱体内,这对于特定种类共生菌功能的研究也存在缺陷,在后续的共生菌功能研究中需要尝试或者开拓新的方法。
第三,褐飞虱体内不同组织内都含有各种各样的共生菌,但在组织间的扩散途径、扩散的种类和机制尚不清楚。目前已明确YLS在褐飞虱体内以垂直传递的方式进行代次间传播(Cheng and Hou, 2001; Yukuhiroetal., 2014; Nanetal., 2016)。具体传递过程为:脂肪体菌胞中的YLS通过胞吐作用释放到血腔中,血腔中游离的YLS到达卵巢管,靠近包裹着原初卵母细胞的滤泡细胞,通过胞饮作用进入滤泡细胞,进而到达卵巢管的上皮栓,进入卵细胞聚集在成熟卵的后端(Noda, 1977; Cheng and Hou, 2001; Wuetal., 2019)。卵成熟后,在每个卵的后端能清晰地看到一个圆形的菌胞(Noda, 1977)。进一步研究发现YLS进入褐飞虱卵巢和卵黄发生密切相关,并且是由卵黄发生过程引发的(Nanetal., 2016);而隶属丝氨酸蛋白酶家族的褐飞虱凝固酶3(N.lugensproclotting enzyme-3, NlPCE3)则在卵黄发生过程中起到了重要的作用(Wuetal., 2019)。那么YLS从脂肪体到血淋巴是受什么调控,具体的机制又是如何?哪些因素可以影响该过程?是每种共生菌都垂直传递到子代还是部分共生菌发生了垂直传递?不同种群间脂肪体YLS到卵中的种类是否存在差异?这些科学问题都有待后续研究。
第四,既然共生菌和褐飞虱间关系如此紧密,如何充分利用共生菌进行褐飞虱防治?前期我们利用共生菌开展了防治褐飞虱的研究,结果表明以杀菌剂作为杀虫剂的助剂,将杀菌剂和杀虫剂配伍使用,可以达到更好的褐飞虱防治效果,且减少了化学农药的使用量(Shentuetal., 2016)。但是此项研究还有不少科学问题需要阐明,比如:哪种共生菌数量的变化会导致褐飞虱死亡率显著上升,也就是关键共生菌是什么?是共生细菌还是共生真菌数量的减少更能导致褐飞虱死亡呢?杀菌剂和杀虫剂复配制剂中杀菌剂和杀虫剂是如何协同发挥防治褐飞虱的作用?褐飞虱不同阶段施药对防治效果有什么影响,和共生菌之间有什么必然的联系?等等。
褐飞虱体内共生菌种类丰富多样,相信上述科学问题的阐明将丰富褐飞虱和共生菌间的共生关系的内涵,进一步明确共生菌对褐飞虱的作用,同时也可为以“抑菌-治虫”方法开展褐飞虱防治研究奠定理论基础。

