石墨双炔/RDX复合物的热分解性能
曾见有,赵宁宁,张 婷,姚二岗,赵凤起,任莹辉,马海霞
(1.西北大学 化工学院&西安市特种能源材料重点实验室,陕西 西安 710069;2.西安理工大学 理学院,陕西 西安 710048;3.西安近代化学研究所 燃烧与爆炸技术重点实验室,陕西 西安 710065)
引 言
炭材料主要包括木炭、碳纤维、多壁碳纳米管(CNT)、石墨、石墨烯、富勒烯(C60)等。在黑火药中,木炭作为助燃物,燃烧后释放热能并产生大量气体,从而提升火药的性能。石墨是常见的添加剂,石墨片层能嵌入药剂颗粒间作为润滑剂使药剂颗粒更容易滑移,从而增加药剂的装填密度并降低机械感度。石墨烯实际上是单层的石墨,因此石墨烯对含能材料也具有降感和润滑作用[1-2]。由于石墨烯本身优异的力学性能,在含能材料中添加石墨烯能够提高其力学性能[3]。氧化石墨烯(GO)与含能材料复合,既可以降低含能材料感度,又可以提高催化效果[4-5]。碳纳米管具有优良的导电导热性能并且具有中空管道,因此,碳纳米管与含能材料直接混合能有效提高燃烧爆炸性能并降低机械感度与静电感度[6-7]。
这些炭材料从结构上来说,其特点为具备sp3与sp2杂化。然而碳元素还存在sp杂化态,以sp杂化态形成的碳碳三键具有线性结构、无顺反异构体和高共轭等优点,受到了人们的广泛关注。其中一种是γ-石墨双炔(GDY)[8],该物质由我国科学家李玉良院士于2010年首次合成,是由1,3-二炔键将苯环共轭连接形成的二维平面炭材料,其sp与sp2杂化态的成键方式决定了其独特的分子构型。不同于其他炭材料,GDY具有由苯环、C≡C键构成的18个C原子的大三角形环,其孔径大约2.5Å,晶格长度a=b=9.44Å[9]。GDY层与层之间通过范德华力和π-π作用形成层状结构,大三角形环在层状结构中构成了三维孔道结构,这使得GDY具有丰富的碳化学键、高共轭性、均匀分散的孔道构型以及可调控的电子结构。这些优异的性质使得GDY在能源[10]、催化[11]、生物医学[12]以及分离[13]等领域具有重要应用前景。此外,可以通过改变反应条件来精确控制杂原子的引入位置和数量。GDY这些独特的结构性质和制备优势使其具有可观的应用前景。
RDX(环三亚甲基三硝胺,黑索今)常用于固体推进剂的氧化剂,其热分解性能极大地影响固体推进剂的燃烧性能[14]。通常在推进剂中加入少量的燃烧催化剂,可降低热分解温度和表观活化能,从而改善推进剂的燃烧性能。安亭等[15]制备了Ag/CNTs复合材料,结果表明,Ag/CNTs复合材料能够降低RDX的热分解峰温。Lan等[16]制备了一系列不同GO含量的GO/RDX复合材料,结果表明,随着GO含量的增加,RDX的热分解峰温逐渐降低。这些结果表明,炭材料及其复合物的加入能够降低RDX的热分解峰温。然而,将GDY这种新型炭材料用于含能材料还未见报道。
本研究采用液相法制得GDY,通过SEM、TEM、XPS、IR、TG对其进行表征;用物理混合法制得不同质量分数GDY与RDX的复合物,采用DSC测试了各复合物的热行为,采用TG/IR/MS联用仪检测热解产物,分析了热解机理,以期为该炭材料在含能材料中的应用提供参考。
1 实 验
1.1 试剂与仪器
六(三甲基硅基)乙炔基苯(质量分数98%),上海凯瑜琳医药科技有限公司;四氢呋喃(THF)、四丁基氟化铵(TBAF,1.0M的四氢呋喃溶液)、吡啶(Pyridine)、乙酸乙酯、二甲基甲酰胺(DMF),均为AR级,购自阿拉丁公司;铜箔(0.1×100mm),国药集团化学试剂有限公司;无水乙醇(AR),天津市富宇精细化工有限公司;丙酮(AR),成都市科隆化学品有限公司;多壁碳纳米管(CNT),直径10~20nm,长度10~30μm,北京德科岛金公司;石墨烯,自制;富勒烯(C60),苏州恒球科技公司;RDX,平均粒径51.28±21.77μm,研磨后平均粒径为3.43±1.81μm,西安近代化学研究所。
PS-100A型洁康超声波清洗机,东莞市洁康超声波设备有限公司;SHZ-D(III)循环水式多用真空泵旋蒸仪,上海力辰邦西仪器科技有限公司;TG16-WS型台式高速离心机,湖南湘仪离心机仪器有限公司;SIGMA HV型台式SEM,德国蔡司公司;Talos F200X型TEM,美国FEI公司;TA Q600型DSC,美国TA仪器公司;TGA-DSC3/IS10/GSD320型同步热重/红外光谱/质谱联用仪和NEXSA Surface Analysis型XPS,均为美国赛默飞世尔科技公司。
1.2 样品制备
参照文献[8]的方法制得石墨双炔,合成路线如下:
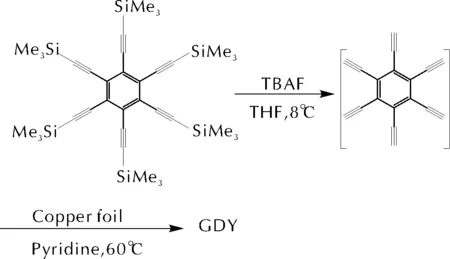
1.2.1 铜片处理
用稀HCl浸泡铜片,超声处理,然后用丙酮和无水乙醇超声洗涤,氩气吹干备用。
1.2.2 六乙炔苯的制备
43.6mg六(三甲基硅基)乙炔基苯溶于20mL四氢呋喃,然后加入0.4mL四丁基氟化铵(1mol/L),在8℃氩气保护条件下,避光,搅拌反应,然后用乙酸乙酯稀释,饱和氯化钠洗涤,无水硫酸镁干燥。旋蒸除去溶剂,将所得固体溶于吡啶中,记为溶液A。
1.2.3 GDY粉末的制备
在三口烧瓶中加入50mL吡啶和处理过的铜片,将溶液A转至恒压滴液漏斗,缓慢加入三口烧瓶中,在60℃氩气保护条件下,避光,搅拌反应3d。反应完成后,用丙酮和DMF轮流洗涤铜片。然后用FeCl3溶液刻蚀铜片,去离子水和乙醇洗涤,离心,真空干燥,得GDY粉末。
1.2.4 GDY与RDX复合样品的制备
取GDY粉末和RDX样品,分别按质量比1∶19、1∶10和1∶1加入研钵,小心研磨,使其充分混合,样品分别记为GDY-RDX119、GDY-RDX110、GDY-RDX11。为了便于对比,RDX在相同条件下研磨相同时间,记为RDXmo。取GDY与RDX质量比为1∶19的样品,不研磨,只简单混合,记为nGDY-RDX119。另外,分别取石墨烯、CNT、C60,按质量比1∶19加入研钵,小心研磨,使其充分混合,样品分别记为G-RDX119、CNT-RDX119、C60-RDX119。
1.3 样品表征及性能测试
采用SEM和TEM对样品的形貌进行表征;采用XPS对样品的元素组成及价态分布进行表征;采用红外光谱仪对样品含有的化学键或官能团进行检测;采用DSC对复合物的热分解行为进行测试,测试气氛为氮气,流量为100mL/min,常压,无孔铝盘;采用热重/红外/质谱(TG/IR/MS)联用仪对热分解产物进行测试,测试气氛为氩气,流量为20mL/min,常压,带孔氧化铝坩埚,升温速率为10℃/min;采用Nano Measurer 1.2软件对样品的粒径分布进行分析并绘图。
2 结果与讨论
2.1 GDY粉末表征结果与分析
不同分辨率下研磨前GDY粉末的SEM、TEM图和粒径分布图如图1所示。
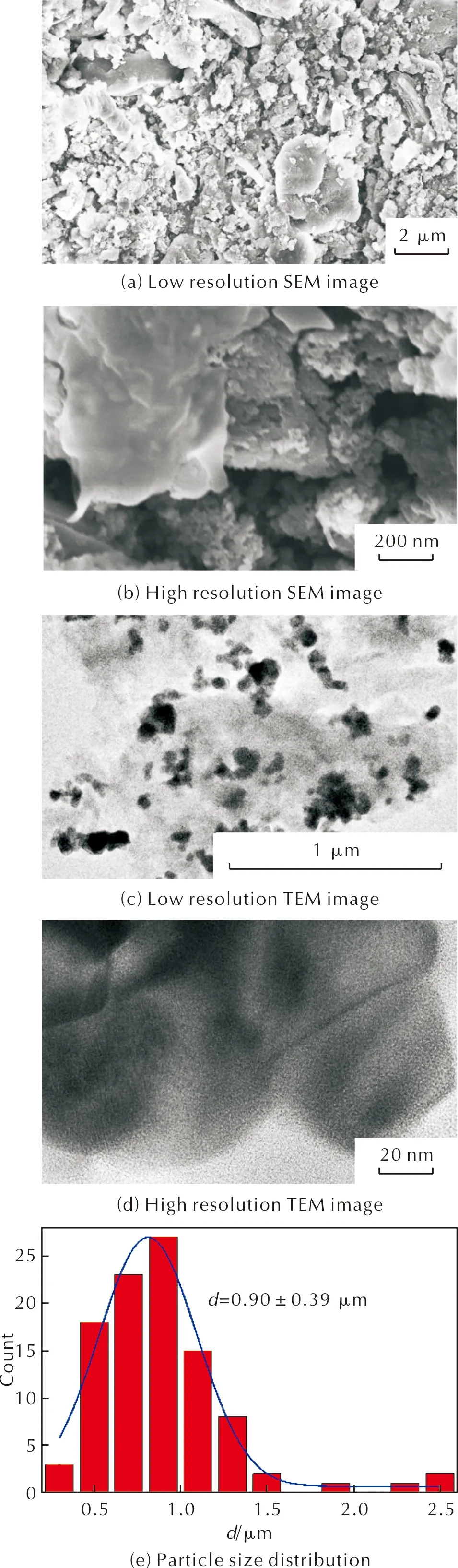
图1 不同分辨率下研磨前GDY的SEM、TEM图和粒径分布图Fig.1 SEM and TEM images of pristine GDY at different resolutions and its particle size distribution
由图1(a)低倍SEM图可见,GDY粉末呈现颗粒状,图1(b)高倍SEM图显示有颗粒也有膜状结构。由图1(c)低倍TEM图可见颗粒状和薄膜状的GDY,图1(d)高倍TEM可见膜状结构。由图1(e)可知,研磨前平均粒径为0.90±0.39μm。
为探究研磨后GDY的形貌是否发生变化,研磨后GDY的SEM、TEM和粒径分布结果如图2所示。由图2(a)SEM图可见,GDY仍呈颗粒状,图2(b)TEM图可见薄膜状结构;由图2(c)可知,研磨后平均粒径为0.65±0.22μm,研磨使得平均粒径略有变小,仍呈颗粒状。

图2 研磨后GDY的SEM、TEM图和粒径分布图Fig.2 SEM, TEM image and particle size distribution of grinding GDY
GDY的XPS全谱、C1s窄谱、TG和IR表征结果,如图3所示。
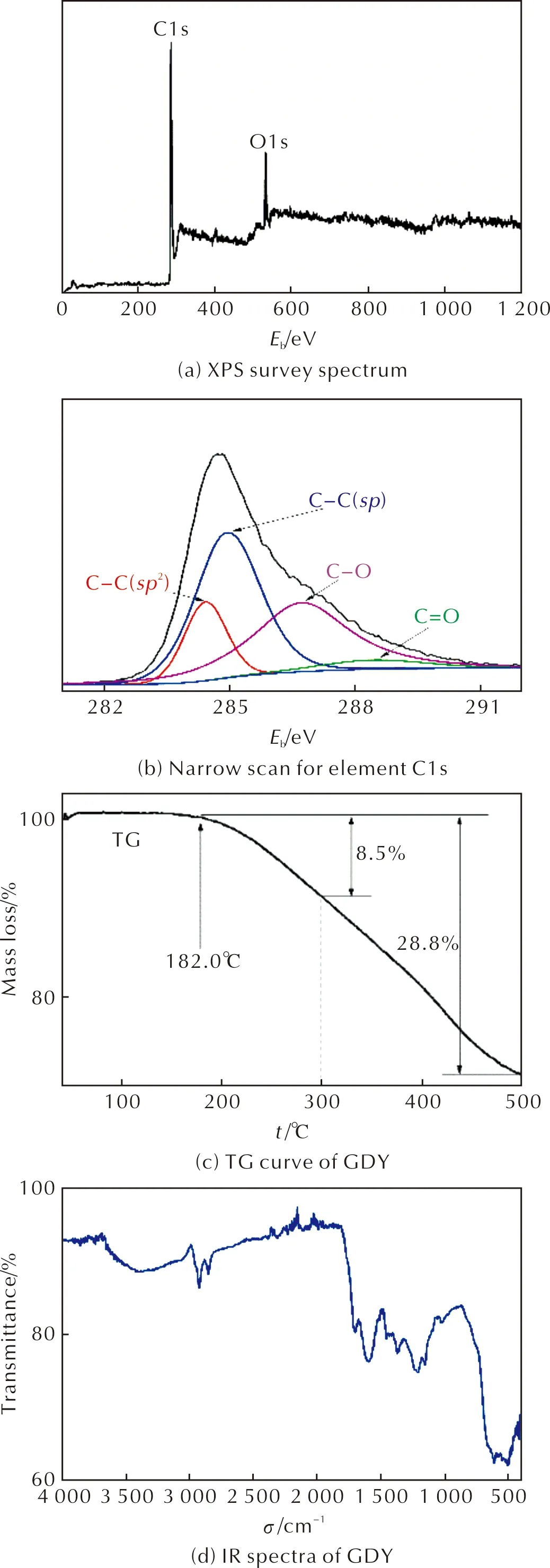
图3 GDY的XPS全谱扫描图、C1s窄谱扫描图、热重曲线和红外光谱图Fig.3 XPS survey scan, narrow scan for element C1s, TG curve and IR spectra of GDY

2.2 GDY与RDX复合物的热重分析
图4为使用带孔的氧化铝坩埚在升温速率为10℃/min所得RDX及GDY-RDX复合物的TG曲线。
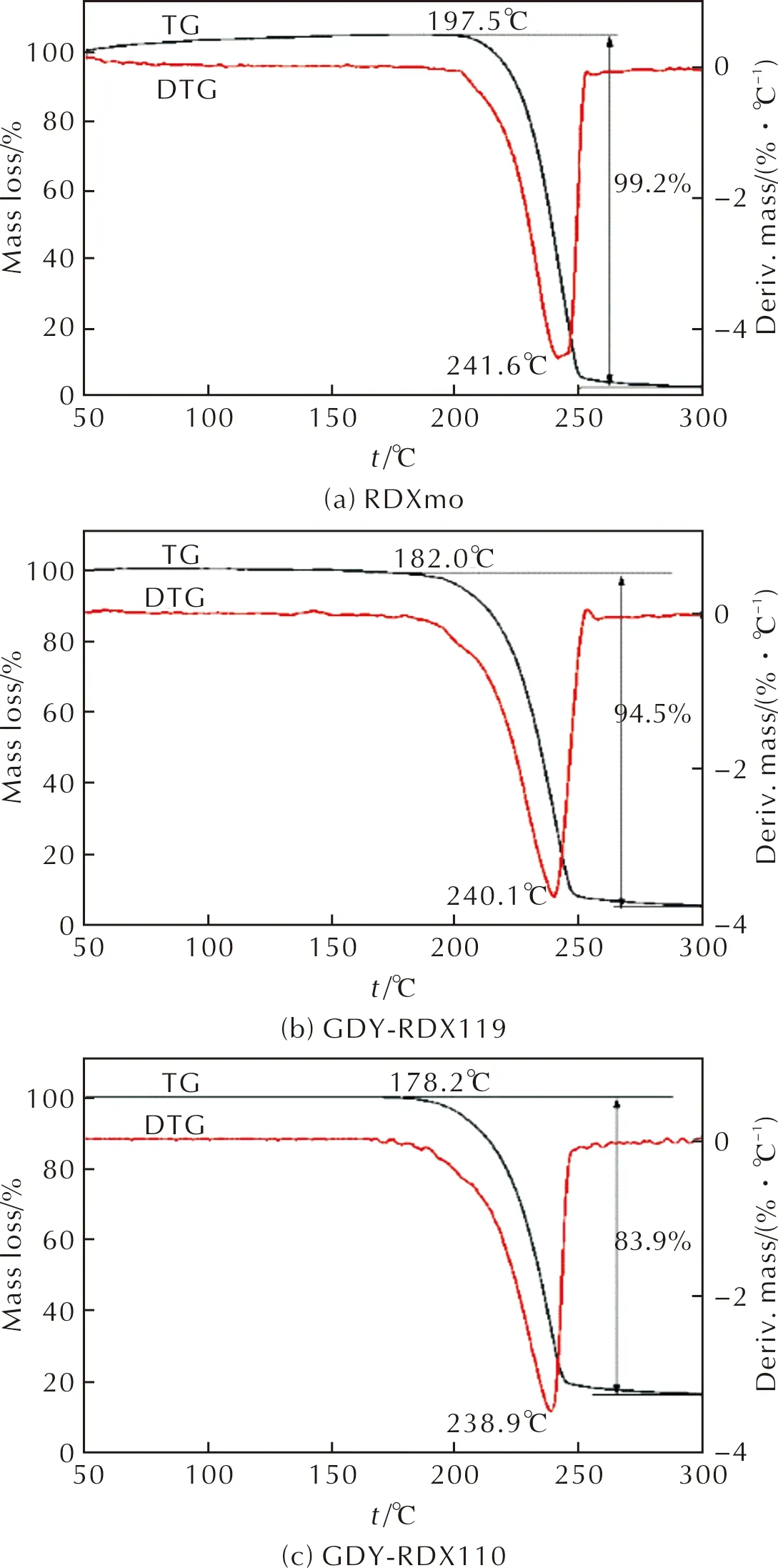
图4 RDXmo、GDY-RDX119和GDY-RDX110的TG-DTG曲线Fig.4 TG-DTG curves of RDXmo, GDY-RDX119 and GDY-RDX110
由图4可知,纯RDX约从197.5℃开始分解,失重速率最快处温度为241.6℃,GDY-RDX119约从182℃开始分解,失重速率最快处温度为240.1℃,GDY-RDX110约从178.2℃开始失重,失重速率最快处温度为238.9℃。结果显示,相比纯RDX,随着GDY加入量的增多,复合样品的起始分解温度和失重速率最快处温度逐渐提前,这表明GDY的加入能够促进RDX的热分解。
2.3 GDY和RDX复合物的动力学研究
为探究GDY对RDX热分解过程表观活化能的影响,对各样品进行不同升温速率的DSC测试,结果见图5,图中的温度为热分解峰温。
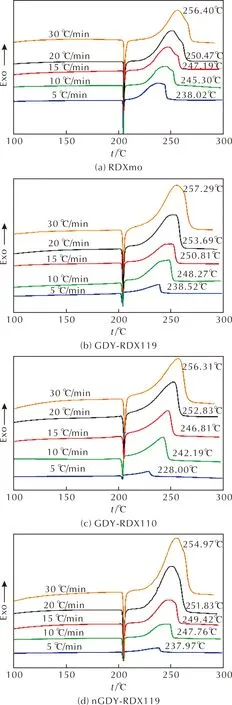
图5 RDXmo、GDY-RDX119、GDY-RDX110和nGDY-RDX119的DSC曲线Fig.5 DSC curves of RDXmo, GDY-RDX119, GDY-RDX110 and nGDY-RDX119
由图5(a)可看到,RDXmo有两个放热峰,一个主放热峰,其后一个肩峰,这与文献[14]类似。相比图5(a)的RDXmo,在相同升温速率时,图5(b)中GDY-RDX119的各分解峰温均推后,峰形有变化,尤其是在升温速率分别为10、15、20℃/min时,均可看到放热峰处一个小平台;图5(c)中GDY-RDX110的各分解峰温基本提前,峰形变尖。峰温和峰形变化的可能原因是,在GDY和RDX质量比为1∶19时,由于GDY的热导率低[19],导致研磨后的样品传热不良,放热峰温滞后;当质量比增加到1∶10时,GDY的催化作用变得明显,使得峰形变尖。另外,在升温速率为10℃/min时,相比纯RDX,质量分数5% GDY的加入使RDX的热分解峰温升高2.97℃。
研磨前复合样品不同升温速率下的DSC曲线见图5(d)。比较图5(b)和图5(d),在相同升温速率下,研磨后样品的热分解峰温略高于不研磨的样品。这可能是由于研磨使颗粒变小,混合更加均匀,但石墨双炔的热导率低[19],导致研磨后的样品传热不良,从而使热分解峰温略有升高。
根据不同升温速率条件下曲线的热分解峰温,采用Kissinger法[式(1)][20]、Ozawa法[式(2)][21]、Kissinger-迭代法[式(3)~式(5)][22-23]和Ozawa-迭代法[式(4)~式(7)][22-23],求得纯RDX和GDY-RDX复合物的非等温热分解表观活化能,分别记为Ek、Eo、Ekd、Eod,结果见表1。
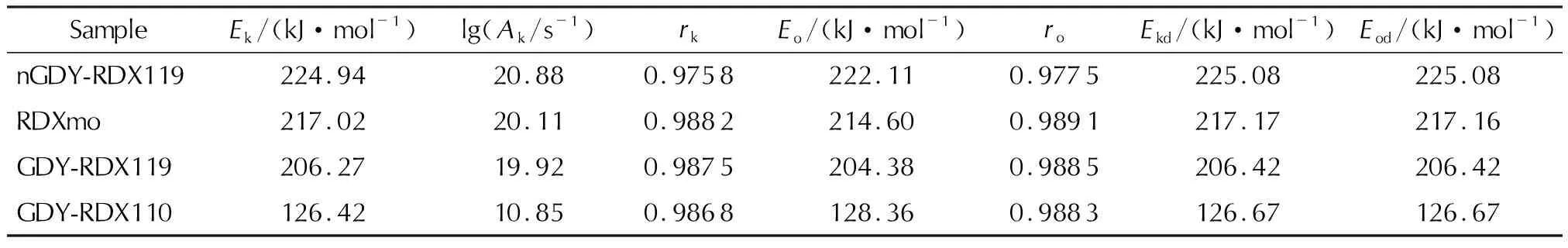
表1 纯RDX和不同含量GDY与RDX复合物的热分解动力学参数Table 1 Kinetic parameters of the thermal decomposition of pure RDX and RDX composites with different contents of GDY
(1)
(2)
(3)
(4)
(5)
(6)
(7)
由表1可知,对同一样品,不同方法计算得到的活化能差值很小,说明计算的数值可信。比较质量比为1∶19的两样品,研磨后GDY-RDX119的活化能比不研磨nGDY-RDX119的活化能低。这可能是由于研磨之后,颗粒变小,混合更充分,在GDY的作用下,反应的活化能降低。对比不同质量比的复合样品,随着GDY含量的增加,活化能逐渐降低。比较Kissinger法计算的活化能,质量分数5% GDY的加入使得RDX的热分解活化能降低了10.75kJ/mol。
2.4 GDY-RDX119的热分解机理
选取质量比为1∶19的样品,对GDY-RDX119进行TG/IR/MS测试,结果如图6所示,分别对应RDX和GDY-RDX119分解产物的红外吸收光谱和质谱图。由图6可知,不同温度时,两样品在667、715、1270~1303、1589~1632、1760~1960、2202~2238、2350、2800、3736cm-1处,吸收强度均发生明显变化。根据物质的特征吸收谱可知,分别对应CO2(667)、HCN(715)、N2O(1270~1303)、H2O(1589~1632)、NO(1760~1960)、N2O(2202~2238)、CO2(2350)、HCHO/HCO(2800)、CO(2185)。在质谱图中,水的强度远大于其他物质的强度,因此,图6(b)和图6(d)中用右侧纵坐标表示水的强度值,用左侧纵坐标表示其他物质的强度值。质谱图中主要气体产物的质荷比分别为17、18、27、28、29、30、44。结合红外图谱和质谱的分析结果,必然有CO2、HCHO、NO、HCN、CO、N2O、H2O。质荷比为17,可能是NH3或OH。质荷比为28,可能是CO,也可能是N2,CO在红外中已检测到。因N2是对称分子,不发生红外吸收,在红外中检测不到,所以N2可能存在于气体产物中。
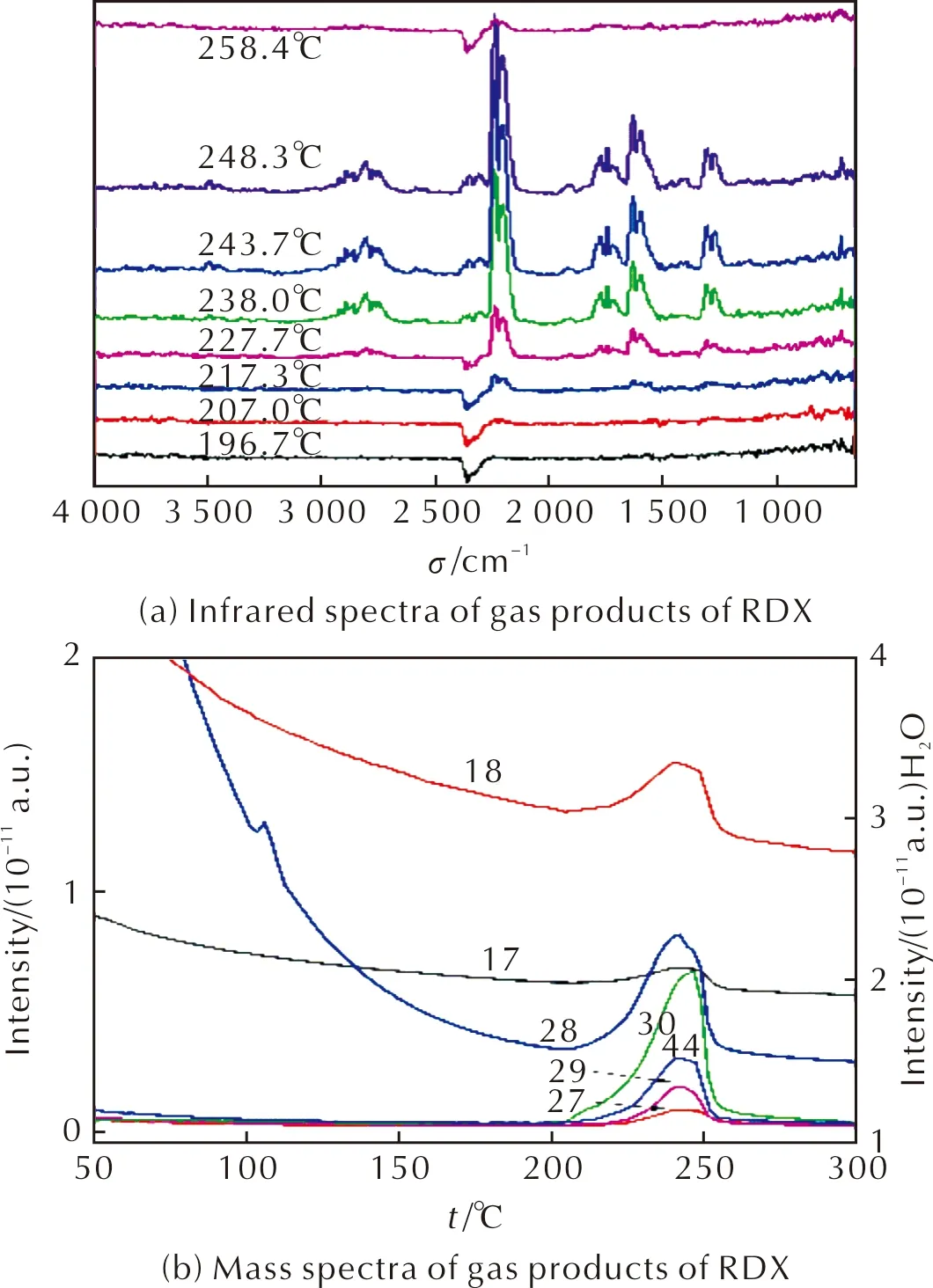
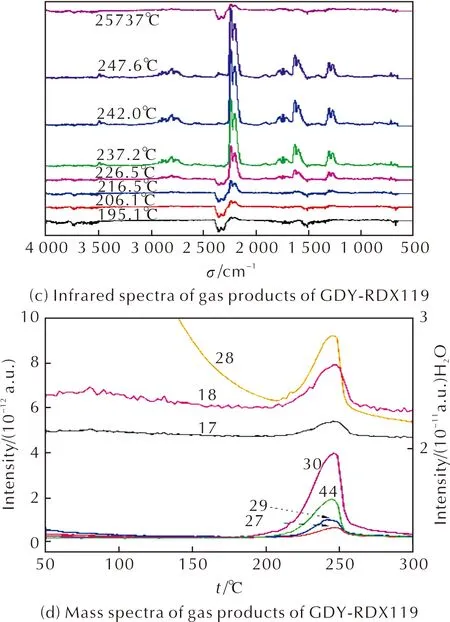
图6 纯RDX和GDY-RDX119分解产物的红外吸收光谱和质谱图Fig.6 Infrared and mass spectra of gas products of RDX and GDY-RDX119
根据质谱结果,将不同质荷比和主要气体产物列于表2。
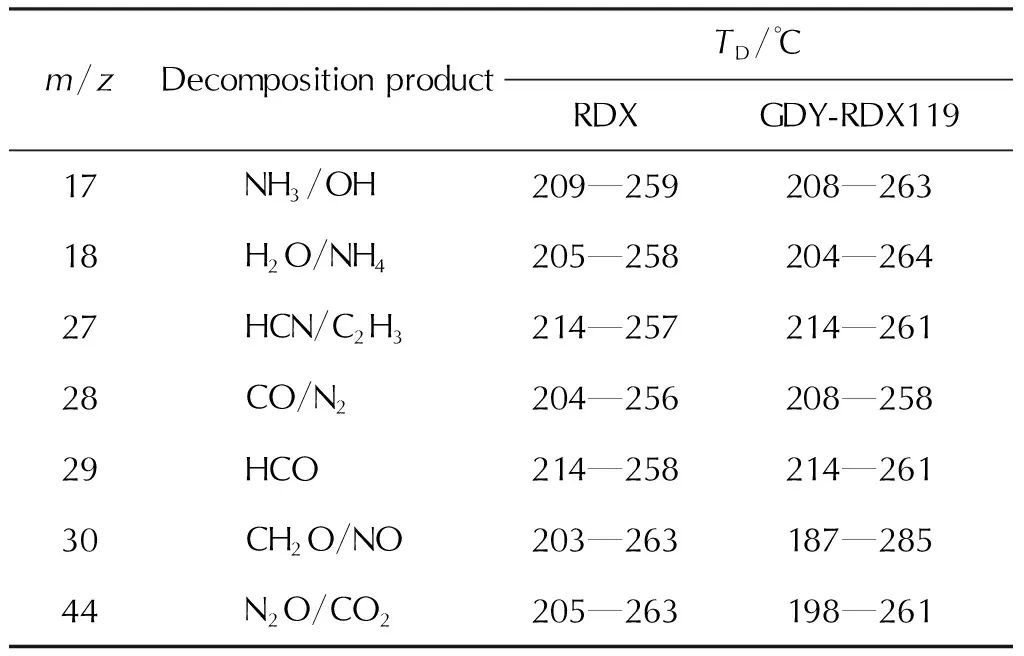
表2 纯RDX和GDY-RDX119的质谱结果和主要气体产物Table 2 Mass spectrum results and main gas products of RDX and GDY-RDX119
由表2可见,相比纯RDX,主要气体产物种类没有发生变化,但是GDY的加入,使得质荷比为30(CH2O/NO)和44(N2O/CO2)的分解产物提前产生。
CH2O、NO、N2O、CO2的红外吸收强度曲线如图7所示。由图7可知,提前产生的物质主要是CH2O和N2O。
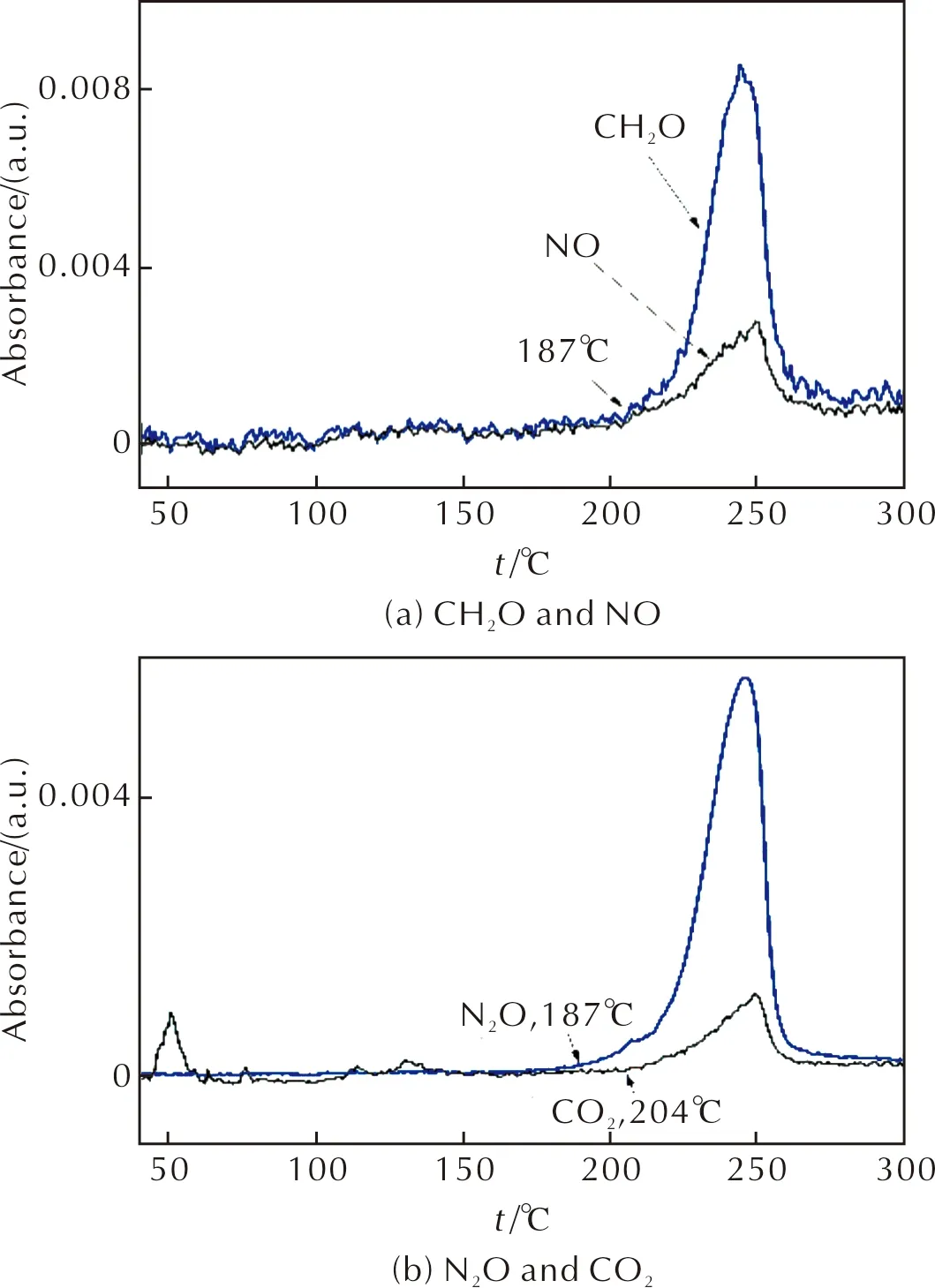
图7 CH2O、NO、N2O和CO2的红外吸收强度曲线Fig.7 Curves of the infrared absorption intensity of CH2O, NO, N2O and CO2
研究表明[24],RDX的初期分解过程是C—N键断裂[放热过程,式(8)]与N—NO2键断裂[吸热过程,式(9)]的竞争过程:
RDX→3CH2O+3N2O
(8)
RDX→3HCN+3HONO
(9)
GDY的加入,使得CH2O和N2O在较低的温度下即可生成,表明在竞争反应中,反应(8)占优,即GDY促进了C—N键的断裂,促进放热反应的发生。由于GDY的加入,提前发生C—N键的断裂,从而提前释放热量,热量也有助于热分解的发生,因此,GDY有助于RDX的热分解。
2.5 GDY与RDX安定性和相容性分析
按照GJB772A-97 502.1,采用DSC法进行相容性和安定性测试,测试结果见图8。
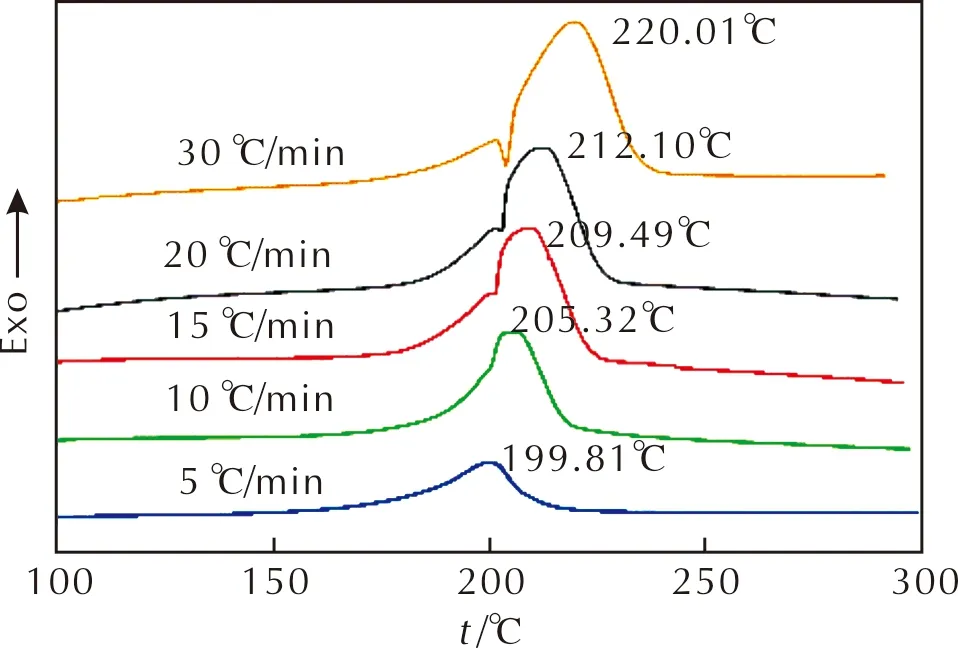
图8 GDY-RDX11的DSC曲线 Fig.8 DSC curves of GDY-RDX11
相容性和安定性评价依据有3个,加热速率趋于零时试样分解峰温Tp0按式(10)[25]计算,分解峰温改变量ΔTp按式(11)[25-26]计算,表观活化能的改变率按式(12)[25-26]计算。按照标准,此处活化能采用Ozawa法求得。
(10)
ΔTp=Tp1-Tp2
(11)
(12)
根据GJB安定性评价依据,Tp0值越高,其安定性越好。表3为Tp0和表观活化能计算结果。由表3可知,相比于RDXmo,GDY-RDX11的Tp0值降低,表明其安定性变差。依据相容性的判定依据,ΔTp大于5℃,则相容性差。

表3 Tp0和表观活化能计算结果Table 3 Calculation results of Tp0 and the activation energy
活化能的相对改变率ΔE/Ea为23.43%。表4为不同升温速率时,热分解峰温的差值。

表4 不同升温速率时热分解峰温的差值Table 4 The difference of decomposition temperature at different heating rates
由表4可知,不同升温速率下,ΔTp均远大于5℃,并且表观活化能的改变率为23.43%,大于20%,说明GDY与RDX不相容,等级为4级[25]。文献[26]表明,DSC法实验温度较高,与温度较低的实际环境相差较远,因此不相容时,不能仅凭DSC法判定混合体系相容性,需进一步采用其他方法来综合评估,如采用真空安定性试验、布氏压力计法和5s爆发点等实验综合评估相容性[27]。因此,RDX与GDY的相容性判定需做进一步分析。
2.6 其他炭材料与RDX复合物的热分解分析
文献中关于石墨烯、多壁碳纳米管、富勒烯等炭材料与RDX的复合样品,因测试仪器、测试条件、样品复合比例不太相同,不便比较。因此,本研究对这些炭材料与RDX复合物的热分解做了进一步探索。
图9(a)~(c)分别为G-RDX119、CNT-RDX119和C60-RDX119在不同升温速率下的DSC测试结果。
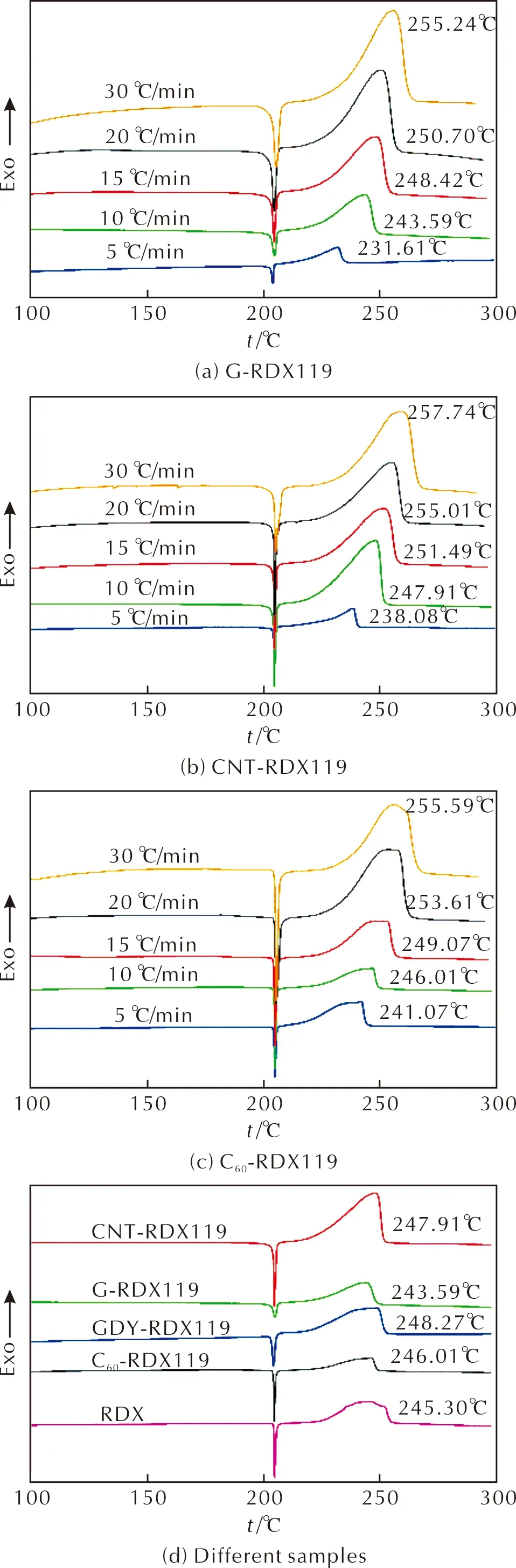
图9 G-RDX119、CNT-RDX119、C60-RDX119的DSC曲线以及当升温速率10℃/min时各样品的DSC曲线Fig.9 DSC curves of G-RDX119,CNT-RDX119,C60-RDX119 and DSC curves of different samples at the heating rate of 10℃/min
由图9(a)和(b)可以看到,相比图5(a)的RDXmo,石墨烯和碳纳米管均使RDX的放热峰峰形变尖,放热由两个峰变成一个峰,表明反应机理发生了变化。图9(c)的C60-RDX119与图5(b)GDY-RDX119的放热峰形比较相近,相比RDXmo,峰形也有变化。图9(d)是在升温速率为10℃/min时,4种炭材料的DSC曲线。由图9(d)可以看到,在升温速率为10℃/min时,相比RDXmo,只有石墨烯使RDX的放热峰温提前,其余均使放热峰温推后。
为进一步比较分析,分别采用Kissinger法、Ozawa法、Kissinger-迭代法和Ozawa-迭代法计算各样品的表观活化能,分别记为Ek、Eo、Ekd、Eod,结果见表5。
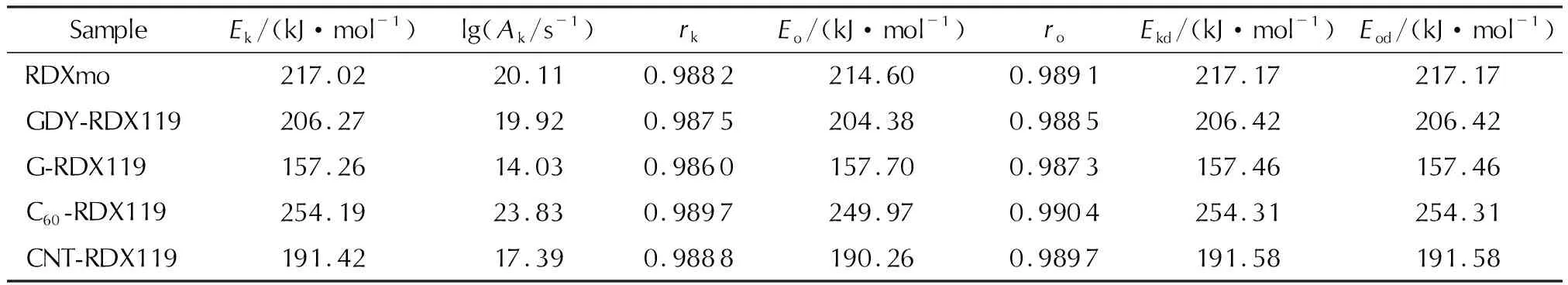
表5 纯RDX和不同炭材料与RDX复合物的热分解动力学参数Table 5 Kinetic parameters of the thermal decomposition of pure RDX and RDX composites with different carbon materials
由表5可以看到,不同方法计算得到的活化能比较接近,说明计算的数值可信。相比纯RDX,石墨烯、CNT、GDY均使RDX的热分解活化能降低,分别为(Kissinger法)59.76、25.6、10.75kJ/mol,而C60使RDX的活化能(Kissinger法)升高37.17kJ/mol。
3 结 论
(1)在N2气氛、100mL/min气体流量、10℃/min升温速率时,经研磨,质量分数5% GDY的加入使RDX的热分解峰温升高了2.97℃,表观活化能降低了10.75kJ/mol。
(2)TG/IR/MS联用技术分析表明,加入质量分数5% GDY后,主要气体产物种类没有发生变化,但是分解气体产物CH2O和N2O在较低温度处生成,GDY的加入促进了C—N键的断裂,从而促进RDX热分解反应的发生。
(3)DSC法相容性分析表明,GDY与RDX不相容,等级为4级。相容性需采用其他方法做进一步的分析。
(4)质量分数5% 炭材料(石墨烯、CNT、C60、GDY)加入RDX后的热分解结果表明,在升温速率为10℃/min时,只有石墨烯使RDX的放热峰温降低,其余均使放热峰温升高。石墨烯、CNT、GDY使RDX的热分解活化能分别降低59.76、25.6、10.75kJ/mol,而C60使RDX的活化能升高37.17kJ/mol。

