乌苯美司联合GP方案在晚期非小细胞肺癌患者治疗中的有效性及安全性研究
李杏欢 徐稳深
(惠州市中心人民医院博罗分院肿瘤血液内科,广东惠州516100)
非小细胞肺癌(NSCLC)60%左右的患者确诊时已处于中晚期,5年生存率仅为5%左右,预后差[1]。GP化疗方案作为晚期NSCLC治疗的经典方案,可有效缓解患者的临床症状,延长生存期,但对机体免疫功能损害较大,使部分患者无法耐受而放弃治疗,疗效常不尽人意[2]。乌苯美司可通过抑制CD13的活性来抑制肿瘤细胞的代谢、侵袭及增殖,增强T、B淋巴细胞功能来促进肿瘤细胞死亡[3]。本研究探讨乌苯美司联合GP方案在晚期NSCLC患者治疗中的有效性及安全性。
1 资料与方法
1.1 一般资料:选择2016年9月至2019年9月肿瘤科78例晚期NSCLC患者,均符合NSCLC的诊断标准[4],预计生存期3个月以上,排除既往恶性肿瘤史、伴有严重的器官功能障碍、严重感染、化疗史、相关药物过敏史者。根据治疗方法分为对照组(n=39)和研究组(n=39),对照组男23例,女16例,平均年龄(58.64±3.57)岁,TNM分期:Ⅲb期18例,Ⅳ期21例;病理类型:鳞癌19例,腺癌17例,鳞腺癌3例;研究组男24例,女15例,平均年龄(59.13±3.26)岁;TNM分期:Ⅲb期17例,Ⅳ期22例;病理类型:鳞癌18例,腺癌17例,鳞腺癌4例。两组一般资料无统计学差异(P>0.05)。
1.2 方法:对照组接受GP方案化疗治疗,第1d、第8d将1.0g/m2注射用盐酸吉西他滨溶于0.9%氯化钠溶液中静脉滴注,0.5h内完成;将75mg/m2注射用顺铂溶于0.9%氯化钠溶液500mL中静脉滴注分3天第1~3d,1h内完成,3周为1个周期,连续治疗4个周期;研究组患者在对照组的基础上口服乌苯美司胶囊,每次10mg,每日3次,持续服用4个月。
1.3 评价标准:疗效评价[5]:完全缓解(CR):已知病灶完全消失且维持4周以上,无新病灶出现;部分缓解(PR):已知病灶体积缩小50%以上且维持4周以上,无新病灶出现;稳定(SD):已知病灶缩小50%以内或增大25%以内;病情进展(PD):已知病灶增大25%以上或出现新病灶;客观缓解(ORR)为CR与PR之和。免疫指标:取空腹8 h以上外周静脉血5 mL,采用流式细胞仪利用免疫荧光标记法检测外周血CD4+、CD8+及CD4+/CD8+及NK细胞水平。毒副反应发生率对比。
1.4 统计学方法:运用SPSS20.0软件分析数据,计量资料采用t检验,计数资料采用卡方检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效:研究组的ORR较对照组稍高,但是差异无统计学意义(58.97% vs.41.03%,χ2值=2.513,P值=0.113),详见表1。
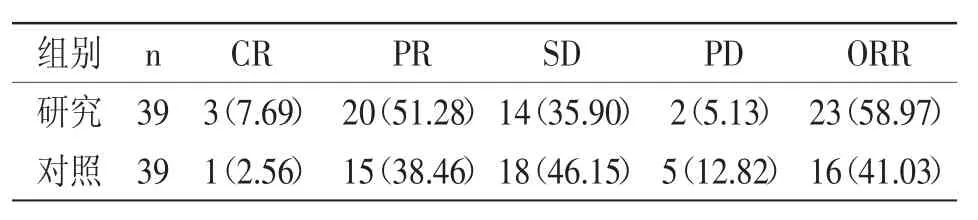
表1 临床疗效[n(%)]
2.2 细胞免疫指标变化:治疗后两组各细胞免疫指标均明显改善,且研究组优于对照组(P<0.05),详见表2。
表2 细胞免疫指标变化(±s)

表2 细胞免疫指标变化(±s)
注:与治疗前及对照组比较,*P<0.05,#P<0.05
?
2.3 毒副反应发生率:研究组血小板与白细胞减少的发生率显著低于对照组(P<0.05),两组恶心呕吐、腹泻、皮疹的发生率比较无统计学差异(P>0.05),详见表3。

表3 毒副反应发生率[n(%)]
3 讨论
GP化疗方案是晚期NSCLC治疗的标准一线化疗方案,但其疗效目前处于瓶颈期,加之化疗药物的毒副反应常会使患者的耐受性下降,从而影响化疗的顺利进行。调节性T细胞在机体免疫功能调节方面起着至关重要的作用,而免疫功能提升对抑制细菌及癌细胞功能具有积极意义[6]。乌苯美司可有效抑制肺癌细胞膜上CD13的活性及p38MAPK的磷酸化,进而抑制肿瘤细胞的分化、增殖、侵袭及转移[7]。同时还可促进集落刺激因子的合成,增强淋巴细胞及NK细胞功能,激活P53通路提高铂类药物对肿瘤细胞的敏感性,在GP化疗方案的基础上联合应用具有增效减毒的效果[8]。
本研究研究组ORR较对照组稍高;治疗后两组各细胞免疫指标均明显改善,且研究组显著优于对照组,提示乌苯美司可有效改善免疫功能。另外,研究组血小板与白细胞减少的发生率显著低于对照组,两组恶心呕吐、腹泻、皮疹的发生率比较无统计学差异。提示乌苯美司可有效降低化疗药物所致的血液毒性反应,提高机体对化疗药物的耐受性,对保证化疗治疗的顺利进行具有促进作用。
综上所述,乌苯美司联合GP方案可有效提高机体免疫功能,疗效安全显著。

