围手术期应用托伐普坦治疗肝硬化腹水的随机对照研究
张猛 刘娇 陈晹 李叶晟 黄杨卿
上海市公共卫生临床中心肝胆外科(上海201508)
肝硬化主要是由病毒、酒精、药物等长期刺激肝脏所造成的一种慢性、进行性、弥漫性肝病的终末阶段,是多种肝病终末期共同的病理变化[1]。很多肝硬化患者在疾病发展中晚期会出现不同程度的腹水表现,为肝硬化失代偿期常见并发症,是多种因素综合作用的结果[2]。肝硬化腹水患者常并发低钠血症,其原因与限钠饮食、利尿剂的应用和反复放腹水等因素有关,严重的可诱发脑水肿、肝性脑病,影响患者的预后[3]。肝硬化患者围手术期并发症如腹水的产生及可能出现的低钠血症对患者的预后有极大影响,可导致患者住院时长增加,费用上升,甚至术后可诱发危及生命的肝功能衰竭和重症感染[4]。
托伐普坦是一种新型非肽类选择性血管加压素V2受体拮抗药,适用于治疗各种疾病引起的高溶性和等溶性低钠血症[5],是欧洲肝病协会(EASL)治疗肝硬化低钠血症的推荐指导用药,具有强大的排水作用,其可促进自由水的排出,并且不伴有明显的电解质丢失,减轻水潴留[6-7]。虽然有很多研究报道指出托伐普坦对失代偿期肝硬化腹水患者具有较好疗效[8-9],但是在对围手术期肝硬化患者的腹水控制及术后恢复的研究仍较少,为此本研究观察了托伐普坦对围手术期肝硬化腹水患者的治疗效果及其安全性。
1 资料及方法
1.1 一般资料 本研究通过上海市公卫临床中心医学伦理委员会伦理审查(伦理审查批号:2018-S024-02 号),获得中国临床试验注册中心注册号:ChiCTR1800017639。研究对象为上海市公共卫生临床中心肝胆外科2018年10月至2020年5月住院需手术治疗的肝硬化患者,共110 例,肝炎肝硬化诊断均符合2015年中华医学会肝病学分会、中华医学会感染病学分会联合制定的《慢性乙型肝炎防治指南》的标准[10]。入院需手术患者经综合评估可施行手术治疗后,利用随机数字法将110 例患者随机分为观察组(托伐普坦+螺内酯治疗)和对照组(螺内酯治疗),见表1。两组年龄,性别,手术和Child-pugh分级差异无统计学意义(P>0.05),具有可比性。

表1 实验组与对照组患者基本情况Tab.1 Basic situation of the observation group and the control group 例
1.2 纳入排除标准 (1)入组标准:①患者年龄18 ~80 岁;②合并肝硬化需施行外科手术,且无明确手术禁忌的患者;③自愿参加并签署书面知情同意书患者。(2)排除标准:①符合托伐普坦说明书中禁忌的患者:托伐普坦临床应用过敏的患者;急需快速升高血清钠浓度的患者;高钠血症患者;对口渴不敏感或对口渴不能正常反应的患者;低容量性低钠血症的患者;无尿症的患者;②腹水较多,需通过穿刺引流放腹水的患者;③术前有休克、全身性感染的患者;④合并肝性脑病或肝肾综合征的患者;⑤2 周内有消化道出血史或医生判断可能会发生消化道出血的患者;⑥诊断为顽固性腹水患者;⑦妊娠试验阳性的患者;⑧滥用酒精或药物或正在参加其他临床试验的患者;⑨研究者认为不适合参加本试验的患者。(3)剔除标准:①不愿接受托伐普坦治疗患者;②随访记录缺失患者;③现有方案治疗出现不可控腹水出现的患者,应积极常规治疗(腹腔穿刺、TIPS、肝移植等)。
1.3 治疗方案 (1)观察组:入院日起,在常规综合治疗基础上加用螺内酯片40 mg,每日一次,30 d;托伐普坦片(国药准字H20110116,浙江大冢制药有限公司),第一日7.5 mg 口服,无不适后第2日起予15 mg 口服,每日一次,30 d,服药时饮水200 mL。(2)对照组:入院日起,在相同常规综合治疗基础上加用螺内酯片40 mg,每日一次,30 d,服药时饮水200 mL。(3)所有患者根据主要诊断施行外科手术,包括肝切除、脾脏切除及胆囊切除等。
1.4 疗效评价标准 (1)腹水程度判定:目前尚无统一有效的腹水程度判定金标准,相对于超声检查测量腹水多少,腹部CT 检查更为客观[11]。患者仰卧位3 ~5 min 后,腹部CT 检查,观察肝周低密度影,取低密度影面积最大的连续三张图像,测量低密度影肝脏面与对应腹壁间的最大径;如为包裹性低密度影,测量连续三张图像最大直径。计算平均值,如此平均值≤2 cm,为少量腹水,如此平均值>2 cm,为大量腹水。(2)腹水程度变化:记录术前、术后5日及术后1月腹部CT 检查为少量腹水和大量腹水患者例数,以百分比的形式统计大量腹水患者占比。(3)腹围差:测量患者入院日及出院日绕脐腹围,计算入院日与出院日腹围差值。(4)体质量差:测量患者入院日及出院日早餐前体质量,计算入院日与出院日的体质量差值。(5)LSM 差值:用弹性超声瞬时成像(fibro touch)测量肝脏硬度值(liver stiffness measurement,LSM),计算患者入院日及术后1月LSM 差值。
1.5 研究指标 主要研究指标:比较两组围手术期大量腹水患者占比差异;次要研究指标:比较两组患者围手术期腹围差、体质量差、住院时间、血电解质浓度是否存在统计学差异及药物相关不良反应。
1.6 统计学方法 采用SPSS 19.0 统计软件包进行分析。计量资料均以均数±标准差描述,采用独立样本t检验。计数资料用率(%)表示,采用χ2检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 腹水变化 术后5 d 及术后1 个月,观察组大量腹水患者占比明显低于对照组(术前1 d:39.62%vs.34.62%;术后5 d:24.53%vs.57.69%;术后1 个月:7.14%vs.22.22%,图1),且随用药时间延长,观察组大量腹水占比逐渐减少。

图1 两组患者术后5 d、术后1个月大量腹水患者占比比较Fig.1 Comparison of the proportion of patients with massive ascites on the 5th day and 1 month after operation between the two groups
2.2 LSM差值 入院日与术后1月LSM差值,观察组显著高于对照组[(0.75 ± 0.20)kPavs.(0.28 ±0.19)kPa,P<0.05,图2]。

图2 两组患者围手术期Fibro Touch 测量LSM 差值比较Fig.2 Comparison of LSM difference measured by Fibro Touch between two groups during perioperative period
2.3 腹围差 入院日腹围与出院日腹围差值,观察组显著高于对照组[(2.59±0.16)cmvs.(1.66±0.18)cm,P<0.05,图3]。
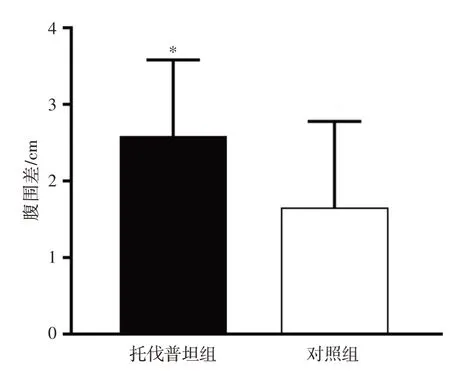
图3 两组患者围手术期腹围差值比较Fig.3 Comparison of the difference in abdominalcircumference between two groups during perioperative period
2.4 术后尿量 术后1 d 和7 d,观察组与对照组患者尿量比较,差异无统计学意义(P>0.05,图4A);而术后3 d[(2 875 ± 29.27)mLvs.(2 463 ±28.41)mL,P<0.01]和术后5 d[(2 775±21.11)mLvs.(2 524±24.80)mL,P<0.05,图4B]观察组患者尿量显著增多。
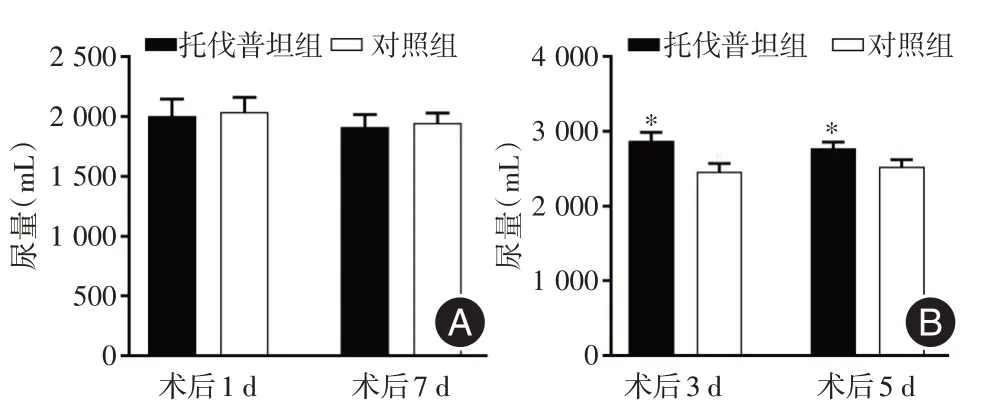
图4 两组患者术后尿量比较Fig.4 Comparison of postoperative urine output between the two groups
2.5 住院时长与体质量差 观察组患者住院时长显著少于对照组[(6.40±0.12)dvs.(7.33±0.12)d,P<0.05,图5A];入院日与出院日体质量差值,观察组显著高于对照组[(1.20 ± 0.08)kgvs.(0.92 ±0.07)kg,P<0.05,图5B]。
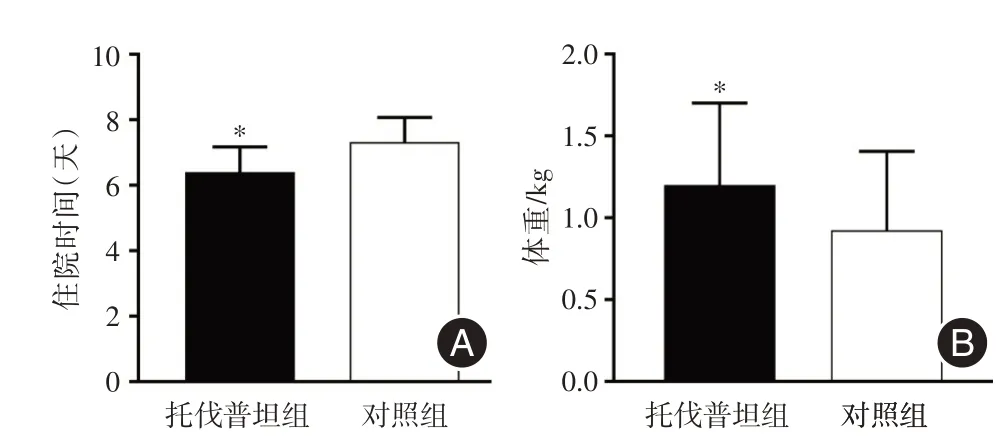
图5 两组患者住院时长及围手术期体质量差比较Fig.5 Comparison of length of hospital stay and perioperative weight difference between the two groups
2.6 血清Na+浓度变化 术前和术后1、7 d 及术后1 个月,观察组与对照组患者血清钠浓度均处于正常范围,两组比较差异无统计学意义(P>0.05,图6A);而术后3 d[(149.20 ± 1.69)mmol/Lvs.(141.60 ± 0.75)mmol/L,P<0.05]和术后5 d(143.60 ± 1.08)mmol/Lvs.(139.80 ± 0.82)mmol/L,P<0.05]观察组患者血清钠浓度高于对照组(图6B),且于术后3 d 观察组中2 名患者血清钠出现危急值(168 mmol/L、181 mmol/L),但未出现相关临床症状。
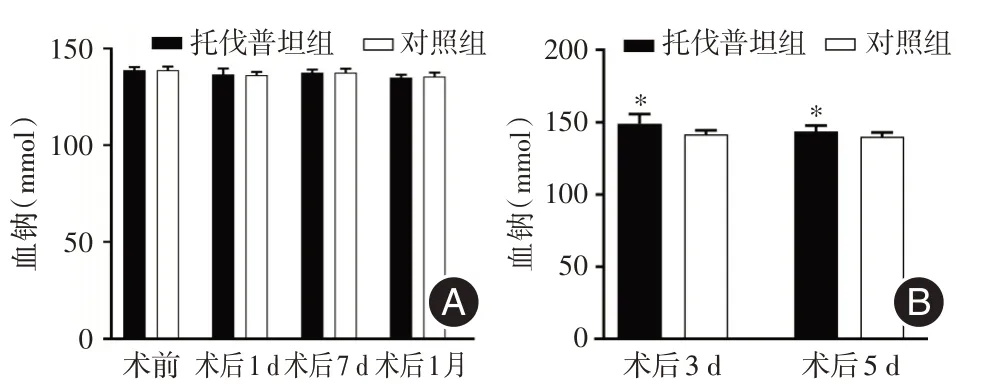
图6 两组患者围手术期血钠浓度比较Fig.6 Comparison of perioperative serum sodium concentration between two groups,3 day and 5 day after operation
2.7 血清K+浓度变化 术前和术后1、3、5、7 d 及术后1 个月,观察组与对照组患者血钾浓度均处于正常范围,两组比较差异无统计学意义(P>0.05,图7)。
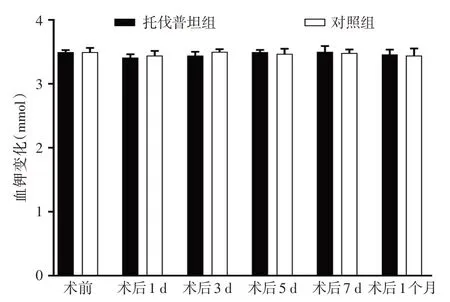
图7 两组患者围手术期血钾浓度比较Fig.7 Comparison of serum potassium concentration between two groups during perioperative period
2.8 药物相关不良反应 观察组患者均有不同程度口渴,均能耐受,未出现3 级以上药物相关不良反应,尤其是脱髓鞘等严重的不良反应。
3 讨论
目前研究认为,腹水的形成机制较为复杂,是由于门静脉高压及肝功能减退共同导致,肝硬化腹水的形成机制主要为:病理性的门静脉高压与低蛋白血症可导致高动力循环状态和(或)内脏动脉扩张、淤血,加上激素代谢障碍和肝淋巴液生成增加,血浆胶体渗透压降低,最终致使有效循环血量不足,肾灌注降低,从而激活肾素-血管紧张素-醛固酮系统(RAAS)和交感神经系统(SNS),引起肾小球滤过率降低,加剧水钠潴留[12]。中晚期肝硬化患者肝脏内血管扩张,动脉相对充盈不足,抗利尿激素反射性分泌增加,易引起稀释性低钠血症,进一步加重水排泄障碍[13]。抗利尿激素又称精氨酸加压素,目前已知存在3 种抗利尿激素受体V1a、V1b和V2受体,与水代谢密切相关的V2受体主要存在于肾集合管上,其激活后可诱导水通道蛋白开放,使集合管水通透性增加,促进水的重吸收[14]。托伐普坦是一种新型选择性精氨酸加压素V2受体拮抗剂,能够通过拮抗位于肾小管的抗利尿激素V2受体与抗利尿激素结合,抑制集合管对水的重吸收,从而产生利尿排水作用,且不伴有明显电解质丢失,可有效清除体内游离水分[15]。越来越多的研究表明,托伐普坦对失代偿期肝硬化患者难治性腹水有明显疗效[16]。肝硬化患者在手术后患病和死亡的风险增加[17],数据显示,对于肝硬化腹水患者,行腹腔镜胆囊切除术发病率和死亡率更高[18],因此,普通外科医生应该了解,在其他常规情况下,如胆囊切除术,对肝硬化腹水患者有重大风险。
本研究应用托伐普坦对围手术期患者肝硬化腹水的治疗,结果显示,应用观察组药物对围手术期肝硬化腹水患者治疗,患者腹水明显减轻、尿量增多、体重下降、腹围明显减小、住院时长缩短。本研究中,观察组患者尿量于术后3、5 d 显著增加,两组患者血清K+浓度均处于正常范围,对比无明显统计学差异,表明托伐普坦能增加尿量,且不影响肾功能,确保了良好的安全性。有研究表明,与传统利尿剂相比,应用托伐普坦可使血清Na+浓度明显升高[19]。本研究结果显示,在术后3、5 d,观察组患者血钠浓度升高,且术后3 d 观察组有2 名患者出现血清钠危急值(168 mmol/L、181 mmol/L),于相同时间段,尿量相应增多,说明应用托伐普坦药物,尿量增多与血钠升高正相关。研究表明慢性伴有症状的低钠血症患者的治疗须避免血钠升高过快,防止中枢神经系统脱髓鞘疾病的发生[20]。因此,应用托伐普坦药物治疗,应严密监测患者电解质变化,预防血钠快速升高导致的中枢神经系统脱髓鞘疾病的发生,本研究中两例血钠升高患者由于密切监测血钠浓度及合适的处理措施,故未发生相关并发症。观察组患者LSM 值比对照组明显减低,说明应用托伐普坦有助于肝硬化的治疗。本研究中,观察组多数患者出现服药后口干、口渴症状,但通过饮水可明显缓解,除2 例患者因血钠危机值停药,余患者研究期间未发生明显不良反应。可见,托伐普坦是治疗围手术期肝硬化腹水的有效方式,改善体液潴留,缓解患者围手术期并发症,值得推广。
综上所述,围手术期肝硬化患者应用托伐普坦可有效控制腹水,减少由于大量腹水导致的围手术期并发症发生,缩短住院时间,有助于肝硬化的治疗,纠正低钠血症,并且不发生低血钾等严重电解质紊乱的情况,具有安全性。

