单孔加一孔腹腔镜胃癌根治术的近期疗效观察
陈志永,贾东亚,王垚,姜庭荣
(马鞍山市人民医院普外四科,安徽 马鞍山 243000)
胃癌是全球第四大恶性肿瘤,也是肿瘤相关死亡的第三大原因[1]。手术是早期胃癌最有效的治疗手段。随着微创外科技术的快速发展,腹腔镜远端胃癌根治术日趋成熟,能够获得与开腹手术相当的根治效果,且创伤小、恢复快,已成为临床指南推荐的早期胃癌标准治疗方式[2]。随着传统五孔腹腔镜技术应用的增多,其存在的不足也日益凸显并引起关注,如Trocar孔多、手术切口大、切口疼痛明显、切口欠美观等。近年来,单孔腹腔镜技术(single incision laparoscopic surgery,SILS)逐渐兴起并成为热点[3-4],但操作难度大,临床应用受限[5]。单孔加一(single-port plus one-port,SILS+1)是由SILS进一步发展而来的新型改良腹腔镜手术,其通过形成倒三角平面,使手术难度降低,操作易于完成。本研究通过对比SILS+1腹腔镜技术与传统五孔腹腔镜手术围手术期基本情况、术后并发症及胃肠激素、炎症因子的差异,以探讨SILS+1腹腔镜手术的近期疗效,为临床提供参考。
1 资料与方法
1.1 一般资料
选取2018年1月至2020年12月马鞍山市人民医院96例行胃癌根治术的患者为研究对象,依据手术方式不同分为SILS+1组(n=45)传统组(n=51)。SILS+1组中,男性30例,女性15例;平均年龄(56.78±9.45)岁;平均体质指数(22.56±2.69)kg/m2;平均肿瘤直径(2.58±0.83)cm;侵犯淋巴血管4例;分化程度:低分化18例,低中分化19例,中分化8例;合并症:高血压5例,糖尿病3例,冠心病2例。传统组中,男性32例,女性19例;平均年龄(557.12±9.74)岁;平均体质指数(22.71±3.14)kg/m2;平均肿瘤直径(2.55±0.74)cm;侵犯淋巴血管5例;分化程度:低分化25例,低中分化17例,中分化9例;合并症:高血压9例,糖尿病4例,冠心病2例。两组患者一般资料比较,差异无统计学意义(P>0.05)。
纳入标准:(1)术后病理证实为I期胃癌;(2)无远处转移;(3)行远端胃切除术;(4)术前未行放化疗等治疗;(5)年龄20~80岁。排除标准:(1)既往有上腹部手术史者;(2)行肿瘤姑息性切除者;(3)合并其他肿瘤者;(4)伴严重基础疾病,无法耐受手术者;(5)临床资料不完整者。
1.2 方法
患者采取平卧分腿位,予全身麻醉。SILS+1组实施SILS+1腹腔镜手术:于患者脐周皱褶处,做一3~4 cm切口,然后置入穿刺套管,建立气腹(维持气腹压力为1.3~1.6 kpa),置入腹腔镜及手术器械,于左腋前线肋缘下约2 cm位置做1.5 cm切口,置入12 cm Trocar,为主操作孔,并放置好超声刀。先行远端胃根治性切除,然后在与Treitz韧带相距约30 cm位置的空肠打开系膜缘形成一小孔,放置60 mm直线切割器,一头推送至肛侧,另外一头插进残胃,进行残胃空肠侧侧吻合,缝合关闭开口。并于上述吻合口以下约25 cm的空肠实施布朗吻合术。在左上腹的Trocar孔位置留置引流管,关闭气腹,留取远端胃标本,依次缝合关腹,术毕。传统组实施五孔腹腔镜手术[6]:置入穿刺套管,建立气腹,行标准D2远端胃切除及淋巴结清扫。
1.3 观察指标
(1)围手术期基本情况:包括手术切口长度、手术时间、术中出血量、排气时间、胃管拔除时间、引流管拔除时间、首次进食半流食时间、术后住院时间、淋巴结清扫数目及术后并发症情况。(2)胃肠激素及炎症因子:术前1 d及术后3 d采用酶联免疫吸附法检测,试剂盒购于上海康朗生物科技有限公司,操作按说明书进行。胃肠激素包括胃泌素(gastrin,GAS)、胃动素(motilin ,MTL)、抑胃肽(gastric inhibitory peptide ,GIP);炎症因子包括C反应蛋白(c-reactive protein,CRP)、肿瘤坏死因子-α(tumor necrosis factor- α,TNF-α)、白细胞介素-6(interleukin-6,IL-6)。
1.4 统计学分析
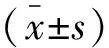
2 结果
2.1 两组患者围手术期基本情况比较
SILS+1组患者切口长度、术中出血量小于传统组(P<0.05),排气时间、首次进食半流食时间、术后住院时间较传统组提前(P<0.05);两组患者手术时间、胃管拔除时间、引流管拔除时间及淋巴结清扫数目比较,差异无统计学意义(P>0.05)。见表1。
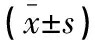
表1 两组患者围手术期基本情况比较
2.2 两组患者术后并发症比较
SILS+1组患者术后并发症发生率低于传统组,差异无统计学意义(P>0.05)。见表2。
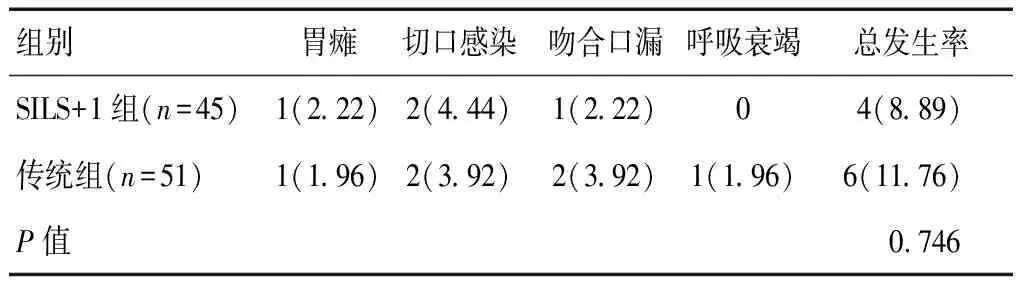
表2 两组患者术后并发症情况比较[n(%)]
2.3 两组患者血清胃肠激素水平比较
术前,两组患者血清GAS、MTL、GIP水平比较,差异无统计学意义(P>0.05);术后,两组患者血清GAS、MTL、GIP水平均降低(P<0.05),且传统组低于SILS+1组(P<0.05)。见表3。
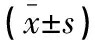
表3 两组患者血清胃肠激素水平比较
2.4 两组患者血清炎症因子水平比较
术前,两组患者血清CRP、TNF-α、IL-6水平比较,差异无统计学意义(P>0.05);术后,两组患者血清CRP、TNF-α、IL-6水平均升高(P<0.05),且传统组高于 SILS+1组(P<0.05)。见表4。
表4 两组患者血清炎症因子水平比较
3 讨论
腹腔镜技术作为早期胃癌的主要手术方式,可获得较好的近期疗效,远期疗效与开腹手术相当[7]。单孔腹腔镜技术通过单一小切口完成手术操作,具有腹壁破坏小、疼痛轻、切口美观、术后恢复快等优点[8],但由于缺乏操作三角,手术难度大,对术者要求高;而SILS+1腹腔镜技术在单孔基础上增加一个操作孔,使操作由小三角为大三角,大大降低了手术操作的难度[9]。
Omori等[10]首次报道了SILS+1腹腔镜技术在胃癌患者治疗中的应用,发现其疗效可靠,且微创美观;Liu等[11]研究也发现,SILS+1腹腔镜手术具有切口小、术后恢复快、更加微创的优势;江恩来等[12]报道还显示,SILS+1腹腔镜手术相比传统腹腔镜手术虽手术时间稍长,但近期疗效好,应激反应轻微,术后恢复快。本研究结果显示,相比传统组,SILS+1组患者切口长度较短,术中出血量较少,排气时间、首次进食半流食时间、术后住院时间均提前(P<0.05),而两组患者手术时间、淋巴结清扫数目及术后并发症发生率比较,差异无统计学意义(P>0.05),与魏丞等[13]的报道类似,表明SILS+1腹腔镜手术可获得更好的近期疗效,可能与手术切口小、躯体疼痛轻微等有关。
胃癌切除术会影响胃肠功能,检测胃肠激素的变化对于评估手术创伤及术后恢复有着重要意义。GAS、MTL、GIP均是机体重要的胃肠激素,有调控消化道运动、营养机体及参与代谢的多重作用[14-15]。本研究中,两组患者术后GAS、MTL、GIP水平均低于术前(P<0.05),且传统组低于SILS+1组(P<0.05),提示SILS+1腹腔镜技术可减轻对胃肠功能的影响,改善患者术后胃肠激素的表达。
手术创伤应激激活炎症反应,不仅会影响切口愈合,还会造成免疫抑制,进而延长术后恢复时间[16-17]。CRP、TNF-α、IL-6均是重要的炎症因子,能够反映机体的炎症应激反应。本研究结果显示,两组患者术后血清CRP、TNF-α、IL-6水平均升高(P<0.05),且传统组高于SILS+1组(P<0.05),与既往报道[18]一致,表明手术创伤会产生明显炎症反应,而SILS+1腹腔镜手术炎症应激反应较轻,有利于促进术后恢复,可能与手术切口更小、术中出血更少有关。
综上,SILS+1腹腔镜手术很好地融合了单孔与全腹腔镜手术的优势,在降低手术难度与追求美观之间找到一个合理的平衡点,兼具微创美观及可操作性,有望成为胃癌外科手术方式的新选择,但其远期疗效仍需进一步研究。

