高效液相色谱法测定肉制品中胭脂红的不确定度评定
周秀娟
(贵州省检测技术研究应用中心,贵州贵阳 550014)
胭脂红,又名食用赤色102号,为水溶性偶氮类人工合成着色剂。作为食品色素,胭脂红可用于果汁饮料、配制酒、碳酸饮料和糖果等食品的着色,而肉干、肉脯制品、水产品等食品中是不允许添加的,但胭脂红在食品中过量添加或违规添加的食品安全事件时有发生,严重威胁着消费者的身体健康与安全。本文参考国家标准《肉制品 胭脂红着色剂测定》(GB/T 9695.6—2008)[1]HPLC法,对肉制品中胭脂红测定结果的不确定度进行评定。
1 材料与方法
1.1 材料与试剂
样品为市场购买腌腊肉。胭脂红标准品(浓度为0.5 mg/mL,中国计量科学研究院)、水(二级水)、甲醇(色谱纯)、甲酸、石油醚、无水乙醇、钨酸钠、柠檬酸和乙酸铵。
1.2 仪器与设备
1260高效液相色谱仪(二极管阵列检测器)、色谱柱、精密天平、恒温水浴锅、聚酰胺小柱和超声波清洗机。
1.3 分析方法
整个检测过程均在(20±5)℃环境条件下进行。
1.3.1 前处理过程
采用万分之一天平称取5.0 g肉制品样品,置于50 mL离心管中,加30 mL石油醚,搅拌、静置,弃去石油醚,去除脂肪。加无水乙醇+氨水+水,溶液提取胭脂红,收集提取液于250 mL锥形瓶中,70 ℃水浴浓缩至约10 mL,加入1 mL硫酸溶液和1 mL钨酸钠溶液,混匀,继续70 ℃水浴5 min,取上清液全部过聚酰胺小柱,用约15 mL甲醇-甲酸水淋洗,最后用15 mL无水乙醇+氨水+水洗脱,收集洗脱液,氮吹至近干,用水定容至10 mL,经0.45 μm滤膜过滤,用高校液相色谱检测。
1.3.2 色谱条件
色谱柱:C18柱(150 mm×4.6 mm,5 μm);流动相:甲醇和0.02 mol/L乙酸铵溶液,梯度洗脱;流速1.0 mL/min;柱温35 ℃;检测波长508 nm;进样量20 μL。
1.3.3 标准溶液的配制过程
(1)50 μg/mL标准溶液的配制。用1 mL的分度吸量管流出式(A级)从0.5 mg/mL的标准储备液中移取1 mL于10 mL的单标线容量瓶(A级)中,用水定容至刻度。
(2)配制标准系列溶液,浓度分别为0.5 μg/mL、1.0 μg/mL、2.0 μg/mL、3.0 μg/mL、5.0 μg/mL 和 8.0 μg/mL。①8.0 μg/mL标准溶液配制。用1 mL分度吸量管从50 μg/mL的标准储备液中移取0.8 mL于5 mL容量瓶中,用水定容。②5.0 μg/mL标准溶液配制。用1 mL分度吸量管从50 μg/mL的标准储备液中移取1 mL于10 mL 容量瓶中,用水定容。③ 0.5 μg/mL、1.0 μg/mL、2.0 μg/mL、3.0 μg/mL 标 准 溶 液 配 制。 用 1 mL 分 度 吸量管从5 μg/mL标准溶液中分别移取0.1 mL、0.2 mL、0.4 mL、0.6 mL于4个1 mL容量瓶中,用水定容。
1.3.4 重复测定与加标回收率
按照1.3中前处理方法和色谱条件。取一阳性样品,在重复性条件测定6次,取平均值为最终检测结果;采用阴性样品添加浓度为3 μg/mL进行回收率试验,测定6次计算其回收率。
2 数学模型
试样中胭脂红含量的数学模型为:

式(1)中,x-试样中胭脂红的含量,单位mg/kg;c-从标准工作曲线计算得到的试样溶液中胭脂红的浓度,单位μg/mL;v-待测样液最终定容体积,单位mL;m-待测样品质量,单位g;-加标回收率校正因子。
3 不确定度来源分析
从测定过程和数学模型分析,胭脂红含量测定的不确定度来源有:①标准溶液引入的不确定度urel(c);②样品称样量引入的不确定度urel(m);③样品最终定容体积引入的不确定度urel(v);④样品前处理过程产生的不确定度urel(x);⑤测量回收率校正因子引入的不确定度urel(R)[2]。
4 不确定度的评定
4.1 标准溶液引入的不确定度
标准溶液引入的不确定度分为标准溶液定值、标准储备液的稀释、标准工作曲线的配制和标准曲线拟合4个部分。
(1)标准溶液定值引入的相对标准不确定度urel(c1)。由标准物质证书提供信息得知,标液浓度为0.5 mg/mL,其相对扩展不确定度为2%(k=2),即相对标准不确定度
(2)稀释得到50 μg/mL标准储备液引入的相对不确定度urel(c2)。该不确定度包括定容时容器的容量和环境温度变化两方面引入的不确定度。按照《常用玻璃量器检定规程》(JJF 196—2006)[3]规定的容量允许误差,定容时玻璃器具容量误差见表1,因温度变化产生的误差见表2。按三角分布,即
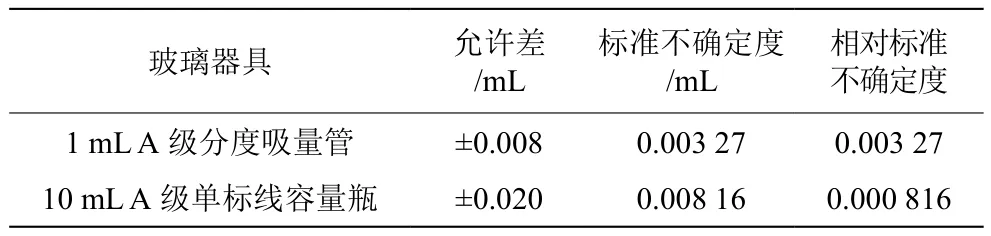
表1 容量误差
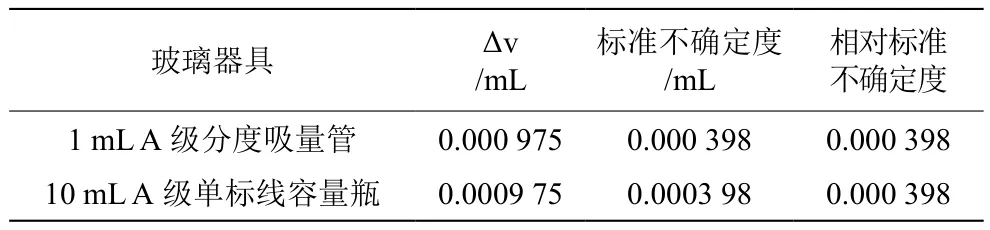
表2 温度变化误差
定容过程中,实验室环境温度波动为±5 ℃。20 ℃时,水的膨胀系数2.1×10-4℃,玻璃的膨胀系数为1.5×10-5℃,则:


式中:α水-水的膨胀系数,α玻璃-玻璃的膨胀系数,v20-20 ℃时谁的体积,T温度,Δv-水的体积差。
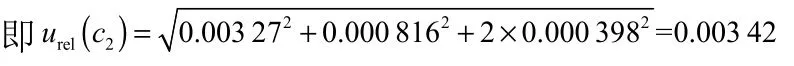
(3)标准工作曲线配制产生的相对标准不确定度urel(c3)。根据1.3.3配制过程中使用的一系列玻璃量具,其产生相对标准不确定度分量见表3和表4。

表3 容量误差
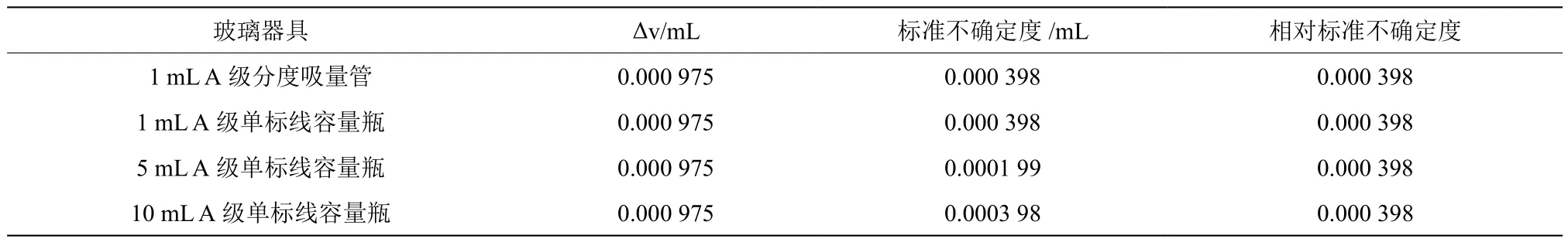
表4 温度变化误差
由容量误差引入的合成相对不确定度
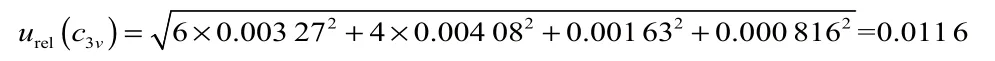
因环境温度变化引入的合成相对不确定度
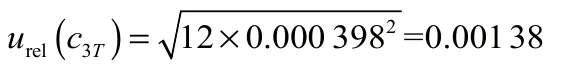
标准工作曲线配制产生的相对标准不确定度
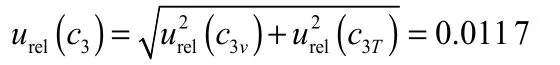
(4)标准曲线拟合产生不确定度[4]urel(c4)。用最小二乘法拟合标准溶液质量浓度-峰面积曲线,分别测定6种质量浓度的胭脂红标准液 0.5 μg/mL、1.0 μg/mL、2.0 μg/mL、3.0 μg/mL、5.0 μg/mL和8.0 μg/mL,每种质量浓度测定2次,得到相应的峰面积A测定结果见表5。
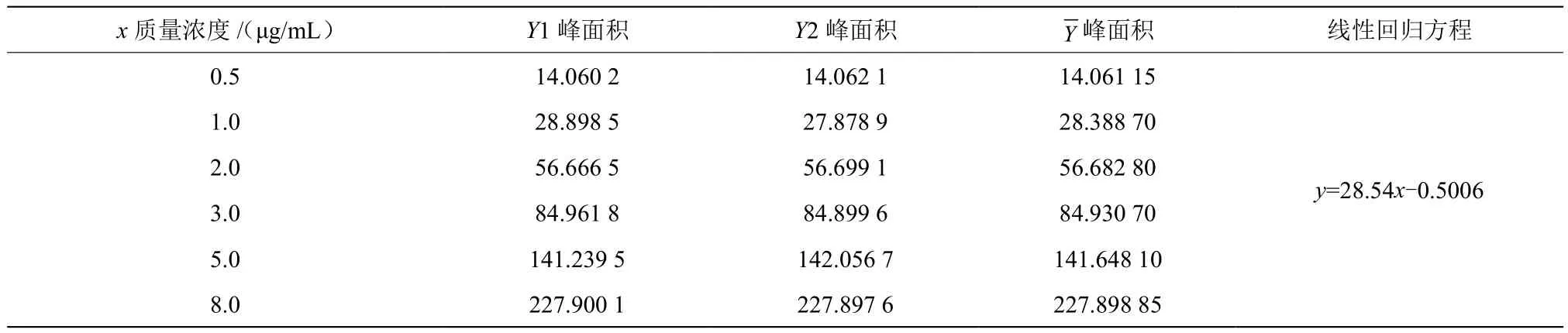
表5 最小二乘法拟合标准工作曲线结果
重复测定样品6次,将其峰面积代入线性回归方程计算测定浓度,再根据公式(1)计算待测物含量,其由标准工作曲线拟合所引入的标准不确定度为urel(c4)。
峰面积测量的标准偏差s为:
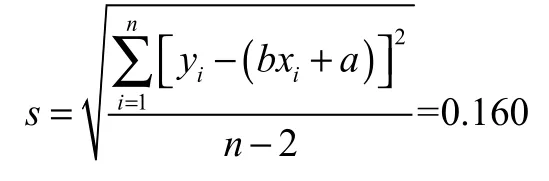

标准溶液引入的相对不确定度

4.2 样品的称量产生的不确定度urel(m)
根据JJG 1036—2008,其最大允许误差±1 mg,则标准不确定度称样质量为5.001 2 g,其相对标准不确定度
4.3 样品的最终定容体积产生的不确定度urel(v)
根据1.3.1中前处理方法,最终定容体积为10 mL,产生不确定度如下。
其相对标准不确定度为
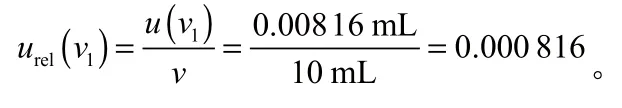
(2)环境温度变化引起溶剂体积变化,玻璃容量瓶体积的变化。
Δv=v1-v20=(a水-a玻璃)×v×(T1-T2),则相对标准不确定度
4.4 样品前处理过程产生的不确定度通过重复性检测评定urel(x)
该不确定度为A类不确定度,按照1.3的分析方法对同一样品重复测定6次,测定结果见表6。
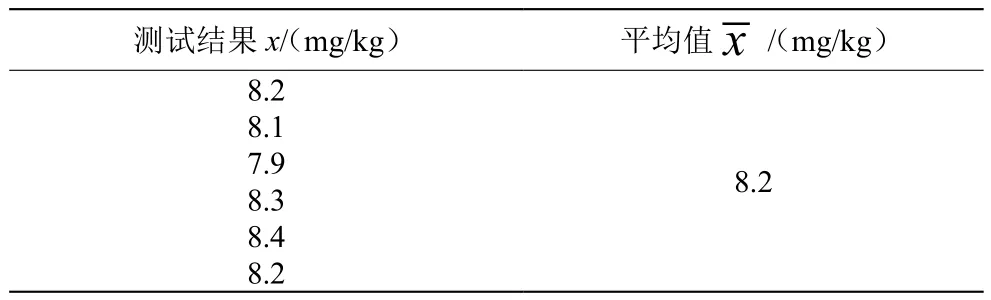
表6 重复性条件测试结果
4.5 加标回收率产生的相对标准不确定度urel(R)
按照1.3.1的前处理方法进行加标回收测定,回收率(R)测定结果见表7,该不确定度为A类不确定度。

回收率R/(%)平均回收率R/(%)1 0 6.0 1 0 5.0 9 8.8 1 0 3.0 9 9.5 1 0 4.0 1 0 3.0
为了确定回收率是否计入研制和含量的计算中,将回收率进行显著性t检验,说明与1.0无显著性差异,则计算中不需采用回收率校正因子对结果进行修正,回收率产生的相对标准不确定度不应纳入合成不确定度的计算[5]。
4.6 扩展不确定度评定和测定结果表示
5 结论
从对肉制品中胭脂红测量不确定度的分析可看出,每一步操作都会产生测量不确定度,其中标准溶液、样品重复性测量、加标回收引入的不确定度较大。标液的配制、稀释、标线的配制过程中,过程越复杂、使用器具越多,最后产生的不确定度越大。样品重复性测量产生不确定较大,可以通过关注固相萃取柱的回收率、提高样品的均匀性及人员的操作技能减小测量结果的不确定度。

