伴复杂染色体核型异常的多发性骨髓瘤肾损害一例
吕佳璇 李月红 庄震 李敏侠
患者,女,67岁,因“髋部疼痛1年,全身水肿、尿量减少10天”于2018年1月17日入院。患者1年前无明显诱因出现双侧髋部疼痛,间断口服洛索洛芬钠等止痛药物后未见好转,逐渐出现双侧肋下疼痛。10天前患者无明显诱因出现颜面部、双下肢水肿,且逐渐加重,尿量明显减少,每日约200 ml,伴乏力、恶心,生化检查结果示血肌酐1 118 μmol/L(41~81 μmol/L,括号内为正常参考值范围,以下相同)、血红蛋白51 g/L(115~150 g/L)。自发病以来,患者无口干、眼干、雷诺现象,无皮疹、咯血等,为求进一步治疗,遂来我院就诊。既往史、个人史、家族史无特殊。体格检查:T 37.2 ℃,P 76次/分,R 19次/分,Bp 176/96 mmHg。皮肤黏膜苍白,无瘀斑;双肺呼吸音粗,可闻及少量湿啰音;心界不大,各瓣膜区未闻及杂音;腹软,无压痛;双侧肋骨及髋关节压痛,双下肢有中度可凹性水肿。辅助检查:血常规:血红蛋白56 g/L,PLT计数205×109/L(125~350×109/L);尿常规:尿比重1.005,尿糖阴性,蛋白0.5 g/L;24小时尿蛋白212 mg(尿量200 ml);生化检查:总蛋白86 g/L(65~85 g/L),白蛋白29.9 g/L(35.0~52.0 g/L),尿素氮26.7 mmol/L(3.2~8.2 mmol/L),血肌酐872.1 mmol/L,血钙2.43 mmol/L(2.11~2.52 mmol/L),血磷2.44 mmol/L(0.85~1.51 mmol/L),二氧化碳22.3 mmol/L(20.0~31.0 mmol/L),乳酸脱氢酶227 U/L(120~250 U/L);全段甲状旁腺激素21.5 ng/ml(15.0~65.0 ng/ml);免疫球蛋白(Ig):IgG 45.89 g/L(7.00~17.00 g/L),IgG1 4 250 mg/dl(405~1 011 mg/dl);抗可溶性抗原(ENA)谱、抗中性粒细胞胞浆抗体、传染病指标结果均为阴性;血尿蛋白电泳结果:IgG-LAM型M蛋白血症,尿κ轻链10.60 mg/L(0~1.85 mg/L),尿λ轻链287.0 mg/L(0~5.0 mg/L);血β2微球蛋白30.1 mg/L(0~0.2 mg/L)。血细胞形态学检查结果:红细胞大小不等,呈轻度“缗钱”样排列,浆细胞偶见(图1)。骨髓形态学检查结果:增生活跃,粒系47%,红系28%,骨髓瘤细胞18.5%。核细胞:胞体大小不等,核圆,偏位,染色质聚集,胞浆量较多,初浆区消失。粒系各阶段比例及形态大致正常。余各阶段比例及形态正常。红细胞呈“缗钱”状排列,淋巴细胞比例形态正常。巨核细胞及血小板不少(图2)。初步诊断:多发性骨髓瘤(MM)。入院后予患者完善骨髓染色体核型分析检查,结果显示51~52,XX,t(1;19)(p10;q10),+der(1;19)(q10;p10),+2,+5,+7,-8,+9,add(12)(p13),+15,+mar[cp3]/46,XX[17]。分析20个中期分裂相,结果显示3个复合核型存在染色体数量及结构异常,其余为正常核型。IgH重排结果示:检测到IgVH、IgK基因重排克隆。荧光原位杂交(FISH)检查结果示:Iq21、CCND1基因位点均为扩增阳性,RB1、D13S319基因位点均为缺失阳性。肾脏超声检查结果示:右肾大小约13.4 cm×4.8 cm,皮质厚约0.9 cm,左肾大小约12.5 cm×6.9 cm,皮质厚约1.3 cm,实质回声增强。局部断层骨显像检查结果示:多发骨骼显像剂异常浓聚,肋骨和12胸椎病变符合骨折和MM。入院时患者因急性心力衰竭、急性肾功能衰竭行血液透析治疗,入院第7天给予血浆置换治疗连续3天,入院第9天给予化疗,方案为静脉注射硼替佐米2.0~2.3 mg、地塞米松20 mg每周1次治疗,4次为1个疗程,共治疗3个疗程。治疗1个月后患者尿量逐渐增加至1 200 ml/d,透析前血肌酐534 μmol/L,IgG 14.96 g/L,尿λ轻链 70.1 mg/L。治疗2个月后患者尿量增加至1 800 ml/d,髋部及肋部骨痛症状明显好转,透析前血肌酐308 μmol/l,IgG 17.31 g/L,尿λ轻链63.7 mg/L。复查骨髓形态学检查结果示浆细胞占2.5%。FISH检查结果:Iq21、CCND1、 RB1、D13S319基因位点均正常。治疗3个月后患者肾脏病理检查结果:光镜下可见17个肾小球,1个缺血性硬化,其余小球系膜细胞和基质轻微增生,毛细血管基底膜广泛空泡变性。肾小管上皮细胞空泡及颗粒变性,多灶状及片状萎缩,少数管腔内可见蛋白管型,肾间质多灶状及片状淋巴、单核细胞及浆细胞浸润伴纤维化。小动脉管壁增厚。免疫荧光下可见1个肾小球,IgA(-)、IgG(-)、IgM(-),C1q(-)、C3(-),FRA(-)。电镜下可见肾小球上皮细胞足突弥漫融合,未见电子致密物沉积;肾小管萎缩;肾间质胶原纤维增生伴淋巴单核细胞浸润。符合:亚急性肾小管间质性肾病(图4)。经过上述治疗后,患者尿量维持在1 500~2 000 ml/d,全身无骨痛症状,透析前血肌酐125 μmol/L,脱离透析。最终诊断:急性肾损伤,MM肾损害,管型肾病,亚急性肾小管间质性肾病;MM IgG LAM型,M蛋白血症,病理性骨折。患者长期治疗方案为间隔2周、2周、3周行VD治疗方案(静脉注射硼替佐米2.0~2.3 mg 、地塞米松20 mg),随诊至2020年9月30日血肌酐维持在125~150 μmol/L,血红蛋白维持在100~110 g/L。
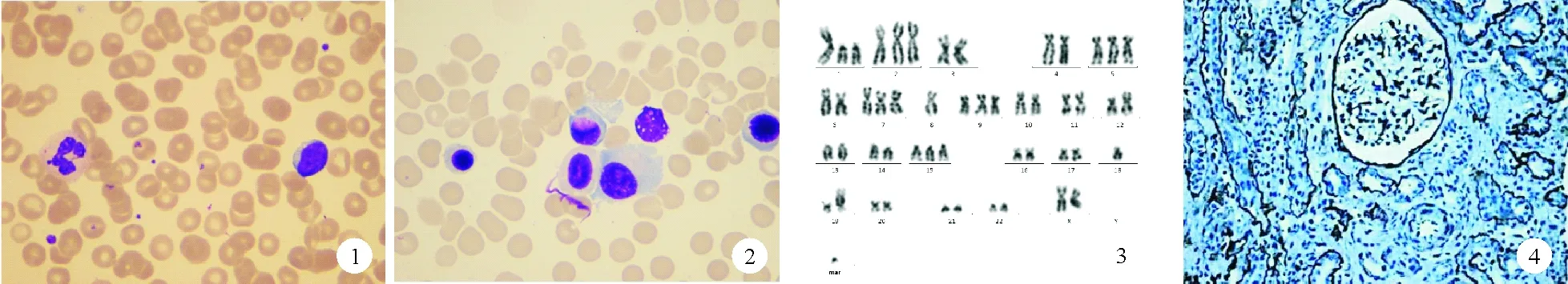
图1 患者血细胞形态学检查结果 图2 患者骨髓形态学检查结果 图3 骨髓染色体核型分析 图4 治疗3个月后患者肾脏病理检查结果[六胺银染色(PASM),×200]
讨 论
MM以浆细胞肿瘤性增殖、单克隆Ig增多为特征。男性发病率高于女性(男女比约1.4 ∶1),老年人多见[1-2]。肾脏是MM常见的受累器官,约20%的患者血肌酐>2 mg/dl,10%的患者需要肾脏替代治疗[3]。由于浆细胞的增殖活性较低,难以对MM进行常规细胞遗传学检查,仅在20%~30%的患者中发现异常核型。MM的危险分层及预后与细胞遗传学异常有关。本文通过对1例伴复杂染色体核型的MM肾损害患者给予积极药物及血液净化治疗后肾功能恢复过程进行介绍,并进行文献复习,以提高对此类MM肾损害患者的临床认识。
本例患者为老年女性,慢性病程急性加重,临床表现为贫血、急性肾损伤、病理性骨折,实验室检查结果可见高IgG1免疫球蛋白血症,骨髓检查结果提示单克隆浆细胞在骨髓中恶性增生,血尿蛋白电泳结果提示患者为IgG LAM型M蛋白血症,骨髓形态学检查结果可见18.5%骨髓瘤细胞,细胞遗传学结果分析患者染色体核型较复杂。治疗3个月后患者肾脏病理检查结果提示少数管腔内可见蛋白管型,考虑轻链管型肾病所致急性肾损伤诊断。治疗上针对原发病用药,给予VD方案(硼替佐米、地塞米松)治疗,避免肾毒性药物,积极给予血浆置换治疗及化疗后,患者全身骨痛情况明显较前好转,骨髓涂片浆细胞百分比下降至2.5%,肾功能好转,脱离透析。
MM可有多种肾脏病理表现,包括管型肾病和单克隆丙种球蛋白沉积病、管型肾病、淀粉样变性等[4-5]。肾功能衰竭可能是MM的首发表现[6],肾功能异常及其程度可影响患者生存率,有报道显示血肌酐<1.5 mg/dl患者1年生存率为80%,血肌酐>2.3 mg/dl患者1年生存率为50%,透析依赖型MM患者1年生存率约为30%,3年生存率约为10%[7]。MM产生大量单克隆游离轻链(FLC)引起轻链管型肾病[8]。一项研究纳入2 592例参与多中心MM试验患者,尿FLC>12 g/24小时患者肾损伤发生率高达54%,无尿轻链患者中肾损伤发生率不足2%[8]。
MM常见细胞遗传学异常根据预后分层,预后较好组包括三体、t(1;14) (q13;q32)、t(6;14)(p21;q32),中等预后组包括t(4;14)(p16;q32)、add(1q21),预后较差组包括t(14;16)(q32;q23)、t(14;20)(q32;q11)、del(17p)。该患者虽染色体核型变异复杂,且FISH检测显示有染色体1q+变异,乳酸脱氢酶(LDH)水平无明显升高,危险分层为中危,考虑经过合适的治疗(早期使用含硼替佐米方案)后,与标危骨髓瘤患者有类似结局。
2019年美国MM指南指出,MM患者行自体移植候选者首选治疗方案是以硼替佐米为主的化疗,其他化疗药物包括沙利度胺、地塞米松等[9-10]。有肾脏损害的患者血液净化方式包括血浆置换和高截留量血液透析[11],这两种方式可早期和快速清除FLC,有助于肾脏恢复,正在进行的两项大型研究(英国及德国开展的EuLITE 研究及法国的MYRE研究)有望提供有效的数据支持[12-13]。
综上,本例患者为老年女性,急性肾损伤、MM肾损害诊断明确,根据修订版国际分期系统考虑患者为R-ISS Ⅲ期,染色体核型异常复杂,相关报道尚为少见。其血β2微球蛋白水平明显升高,并出现急性肾损伤。根据FISH检测结果,考虑患者危险分层为中危MM,遂积极应用血浆Ig置换、血液透析、硼替佐米等治疗后,其肾功能较前明显恢复,MM相关指标好转,随诊2年患者肾功能、血浆Ig稳定。临床上如遇到贫血、肾功能异常、肾脏大的患者,需警惕血液系统疾病肾损害,完善免疫学检查及危险分层,根据临床指征,积极应用血液净化等治疗,可提高患者生存率和生活质量。

