含银离子羟基磷灰石表面涂层的钛板对6种牙周致病菌的体外抑菌作用
杨 磊 丹 丹 马 兰 贾 慧 王玉杰
(邯郸市口腔医院,邯郸 056001)
慢性牙周炎和慢性根尖周炎已经成为成人牙列缺失的主要病因。如今口腔种植技术逐渐成为解决牙体缺损和牙列缺失病例的首选治疗方案[1]。但是,由于慢性牙周炎和慢性根尖周炎患者自身存在对牙周致病菌的易感因素,以及口腔固有菌群失衡、根尖区术中致病菌清理困难、常规种植体表面处理不具有抗菌性能等原因,增加了常规种植或即刻种植病例的种植体周围炎的发生率[2,3]。因此,提升种植体抗菌能力逐渐成为口腔种植材料学的必要发展方向[4]。
银离子具有独特的理化性质和特殊的生物学效应,纳米银离子能够杀灭多种细菌,在一定的计量范围内无细胞毒性。目前已经有很多银离子医疗产品用于临床的预防、诊断、治疗,并取得了较好的疗效。在动物感染模型中发现,将银离子加入骨水泥,并用于兔全膝关节置换术,能够有效抑制金黄色葡萄球菌生物膜的形成,防止人工关节假体周围感染的发生[5]。 本研究的目的是比较普通羟基磷灰石表面钛板与含银离子羟基磷灰石表面钛板的体外抗菌能力,为今后口腔临床选择合适的种植体材料提供有价值的实验数据。
1 材料和方法
1.1 材料
1.1.1 主要设备 厌氧培养箱 (DYⅡ型,浙江义乌冷动机总厂),比浊仪(BIORED公司,美国),牛心脑浸液血琼脂平板(BHI-S培养基),牛心脑浸液琼脂平板(BHI-培养基),巯基乙醇酸盐转送液(TD液)。
1.1.2 实验菌株 由四川大学口腔生物医学工程教育部重点实验室提供以下6种菌株(A~F):
A.牙 龈 卟 啉 单 胞 菌(ATCC,33277)P.gingivalisATCC,33277;B.牙龈卟啉单胞菌381P.gingivalis381;C.牙髓卟啉单胞菌P. endodentalis(ATCC,34506);D.中间普雷沃菌P. intermedia(ATCC,25611);E.产 黑 色 素 普 雷 沃 菌P.meninogenica(ATCC,19040);F.具核梭杆菌E.nuclealum(ATCC,10953)。
1.1.3 实验材料 普通羟基磷灰石表面涂层的钛板与含银离子羟基磷灰石表面涂层的钛板由我院口腔科实验室制备,方法如下:电解液中Ag+浓度0.5 mmol/L。溶液温度40℃,pH值=4.0,脉冲电位-2 V,沉积时间2 h,热处理温度700 ℃。使用CHl660D电化学工作站,以钛片作为工作电极,铂盒板作为对电极.饱和甘汞电极作为参比电极进行电化学沉积。取100 mL电解液于烧杯中,将烧杯置于集热式恒温加热磁力搅拌器中,设定温度为40℃,缓慢搅拌。初始电位为3次开路电位测定的平均值,高电位0.30 V,低电位-2 V,阶跃次数72,脉冲宽度100/s。采样间隔1/s,静置时间0.5/s。完成电沉积后,将制得的样品放入马弗炉中,在空气中进行高温处理。升温速度为5℃/min,热处理温度设定为700 ℃,达到处理温度后保温2 h[6]。
1.2 体外抑菌研究
采用CLSI推荐的平板菌落计数法:将样品制备成1 cm×1 cm的正方形,正反两面紫外灯各照射30 min消毒,备用。取12个10 mL的 EP管(编号1~12),每管分别加入5 mL的 LB 液体培养基和100 μL活化后的6种细菌(浓度约为1×106CFU/mL),再分别加入不同的样品,放在37 ℃,200 r/min 的摇床中共培养 12 h。然后将混合液摇匀,取100 μL,稀释到一定的倍数后,再取 50 μL稀释混合液均匀涂于固体培养基上,在37 ℃培养24 h,记录每个平板中形成的菌落数量。每个实验平行操作3次,依据稀释倍数,计算出原始样品中所含细菌菌落总数。抗菌率的计算公式:抗菌率=(对照样品苗落数-被测样品菌落数)/对照样品菌落数×100%。
1.3 扫描电镜标本制备
将样品制备成1 cm×1 cm的正方形,正反两面紫外灯各照射30 min消毒,备用。取2个10 mL的 EP 管,分别编号1~2,每管依次加入 5 mL的 LB 液体培养基和100 μL活化后的P.gingivalis菌液(浓度约为 1×106CFU/mL),分别加入不同的样品,放在37 ℃,200 r/min 的摇床中共培养12 h。样品用3%戊二醛固定,PBS洗涤3次,用OsO4固定30 min,PBS洗涤3次,脱水:50%Alc,75%Alc,100%Alc(5 min/次),37℃干燥1 min,离子溅射仪喷金120 s,用扫描电子显微镜(S-3400N型,西门子公司,德国)观察材料表面。
1.4 材料表面细菌生物膜形成的评估
采用结晶紫(crystal violet,CV)染色的方法评估2种材料表面细菌生物膜形成[7]。实验方法同1.2,不同之处是样品与菌液的共培养时间是4 h。然后PBS洗涤材料2次,65 ℃干燥20 min,0.3%结晶紫(Sigma-Aldrich公司,美国),室温下孵育15 min,PBS洗涤3次,自然干燥后,采用96%EtOH洗脱CV,GloMax Multi分光光度计(Promega公司,美国)在600 nm吸光度下测量。
1.5 统计学分析
采用SPSS 21.0软件分析数据,计量资料采用t检验,以(±s)表示,计数资料以率(%)表示,采用卡方检验,P<0.05为差异具有统计学意义。
2 结果
2.1 2种材料表面的体外抑菌作用比较
2种材料对牙周致病菌株均具有一定的体外抑制作用。且含银离子羟基磷灰石表面的抑菌作用要强于普通羟基磷灰石表面(P<0.05),见表1。
表1 材料表面对6种牙周致病菌的体外抑菌率(±s, %)

表1 材料表面对6种牙周致病菌的体外抑菌率(±s, %)
?
2.2 扫描电镜观察
扫描电镜观察发现:未接触细菌的钛板表面光滑、无任何附着物或结晶体(图1A)。和细菌共培养过的材料表面存在数量不等的炎性附着物或结晶体,以及生长的细菌、凋亡中的细菌被大量的纤维膜包裹或覆盖于表面(图1B)。但含银离子羟基磷灰石表面的细菌和细菌生物膜明显减少(图1C)。

图1 钛板表面扫描电镜观察结果
2.3 材料表面对细菌生物膜细菌的清除作用
未接触细菌的材料表面无细菌生物膜形成(0%),含银离子羟基磷灰石表面的6种牙周致病菌的细菌生物膜菌量均明显低于普通羟基磷灰石表面(P<0.05),见表2。
表2 材料表面对细菌生物膜细菌的清除作用(±s, %)
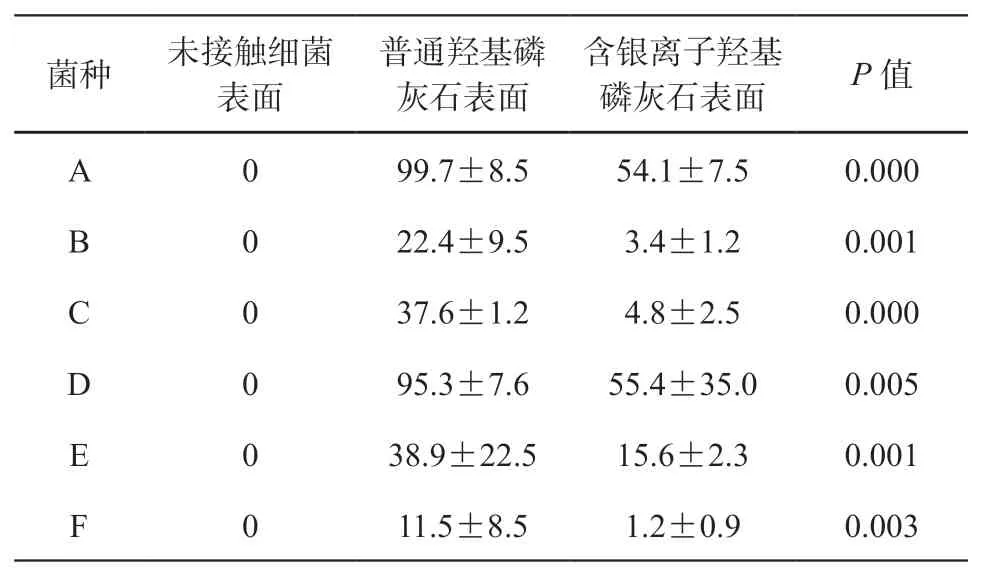
表2 材料表面对细菌生物膜细菌的清除作用(±s, %)
?
3 讨论
牙周病的病原菌已经逐渐明确,革兰氏阴性厌氧菌P. gingivalis、F. nucleatum等已经证明是牙周病的主要致病菌[8]。P. gingivalis的龈下定植与牙周病的发生和发展密切相关[9]。该菌为G-、无芽胞、产黑色素、专性厌氧的杆菌。它可产生内毒素、胶原酶、胰酶样蛋白酶、磷酸脂酶A以及氨、吲哚、有机酸、硫化氢等代谢产物,对牙周组织产生毒性及破坏作用。另外,P. gingivalis具有很强的诱导化脓性感染的能力,可产生多种炎症因子,能破坏宿主的防御系统,同时降解细胞基质蛋白而造成组织破坏。F. nucleatum是G-、无芽胞、不解糖或弱发酵碳水化合物的梭形厌氧菌,也是口腔常见的细菌之一,主要在龈缘和龈下菌斑定植[10]。该菌产生的脂肪酸、NH3、吲哚、H2S、内毒素可以抑制成纤维细胞增殖、诱导巨噬细胞产生IL-1,诱导外周血单核细胞和外周血多形核细胞的凋亡,从而逃避免疫杀伤细胞。另一方面,通过清除对免疫防御至关重要的免疫细胞而有助于其它病原菌的再生,进而导致牙周病的发生和发展。
种植体表面的羟基磷灰石涂层与哺乳动物牙齿、骨骼的无机质成分相同,结构相似,具有良好的生物活性和生物相容性。然而,HA易吸附蛋白质、氨基酸和其他有机质,这为细菌的生长提供了丰富的营养物质[11]。细菌在材料表面形成生物膜,继而生长繁殖。Ag+即使在10 ~ 70μg/mL 的低浓度范围也能对G-和G+菌表现出较强的抗菌活性[12]。从材料表面缓释出的Ag+通过静电力吸附在带负电的细菌细胞壁上,中断跨膜电子传递,还可与-SH 结合破坏酶蛋白的活性。接着Ag+从细菌尸体中游离出来,再与其他细菌结合达到循环杀菌的效果。因此,Ag+对细菌、真菌和病毒都具有良好的广谱抗菌能力[13,14]。研究表明,虽然Ag+对微生物的毒性强,但对人体细胞相对安全。Ag-HA无论是在富营养还是贫营养环境都表现出抗菌性能[15-17]。
本实验选择了6种具有代表性的牙周致病菌,通过采用CLSI推荐的平板菌落计数法检测普通羟基磷灰石表面钛板和含银离子羟基磷灰石表面钛板对这些致病菌的体外抑菌作用。结果发现,两种材料对牙周致病菌模式株均具有一定的体外抑制作用。但是,含银离子羟基磷灰石表面的抑菌作用要强于普通羟基磷灰石表面,表明含银离子羟基磷灰石表面钛板具有较强的体外抑菌作用。
此外,采用电镜扫描和结晶紫染色法发现,含银离子羟基磷灰石表面的细菌和细菌生物膜明显少于普通羟基磷灰石表面,并且6种牙周致病菌的细菌生物膜菌量均明显低于普通羟基磷灰石表面,提示含银离子羟基磷灰石表面可以抑制细菌生物膜的形成,减少细菌生物膜菌量,有利于种植体的长期存活率和种植成功率。进一步验证了含银离子羟基磷灰石具有良好抗菌性能,含银离子羟基磷灰石表面涂层的钛板抑制牙周致病菌的能力较强,尤其是对于P. endodentalis,P.intermedia以及E. nuclealum。其原因可能是由于是这3种细菌对于银离子的结合能力更强,银离子和细菌表面结合,进入细菌细胞后,作用于DNA,在双螺旋结构中形成嘌呤/银/嘧啶的化学键,取代相邻的嘌呤与嘧啶之间的氢键,形成一个更稳定的螺旋结构,阻止DNA解链,DNA分子不能有效复制,最终导致细胞死亡。
4 结论
表面含银离子羟基磷灰石涂层的钛板抑制牙周致病菌的能力较强,尤其是对于牙髓卟啉单胞菌、中间普雷沃菌、具核梭杆菌效果更明显,可以考虑作为口腔种植体材料,尤其可能对于慢性牙周炎、慢性根尖周炎、2型糖尿病等高风险人群具有重要意义。

