猪细小病毒病灭活疫苗佐剂筛选及配苗乳化工艺研究
李应鹤,初晓红,宋扬,徐刚,李贽,于镭
(哈药集团生物疫苗有限公司,哈尔滨150069)
猪细小病毒病是由猪细小病毒(PPV)引起的一种猪繁殖障碍病,主要表现为胚胎和胎儿的感染和死亡,特别是初产母猪产死胎、畸形胎和木乃伊胎,但母猪本身无明显的症状[1]。猪细小病毒病目前尚无有效治疗方法,主要采取预防措施,因此猪细小病毒病疫苗的生产工艺研究尤为重要[2]。本研究分别使用MontanideTMISA 206 VG佐剂(简称206佐剂)和白油佐剂进行猪细小病毒病灭活疫苗的配制,首先比较白油佐剂和206佐剂之间乳化工艺差异,再通过疫苗的物理性状检测、安全性检验和效力检验,分析两种佐剂对疫苗免疫效果的影响[3]。
1 材料
1.1 制苗用病毒液
浓缩后的猪细小病毒L株灭活病毒液(浓缩前病毒液红细胞凝集价为1∶512),由哈药集团生物疫苗有限公司制备和提供。
1.2 主要试剂
MontanideTMISA 206 VG佐剂(206佐剂),购自法国赛比克公司;2-溴乙胺氢溴酸盐(BEA),购自Sigma公司;Span-80和Tween-80,购自广州西陇化工有限公司;硬脂酸铝,购自天津市致远化学试剂有限公司。
1.3 红细胞凝集抑制抗原
猪细小病毒L株,批号为PPV-HI Ag-201401,红细胞凝集价为1∶512,规格为1.0 mL·瓶-1,均由哈药集团生物疫苗有限公司制备或提供。
1.4 血清
猪细小病毒阳性血清,批号为PPV-Pos-Serum-201401,HI效价为1∶512,规格为1.0 mL·支-1;猪细小病毒阴性血清,批号为PPV-Neg-Serum-201401,规格为1.0 mL·支-1,均由哈药集团生物疫苗有限公司制备或保存。
1.5 红细胞悬液
0.5%豚鼠红细胞悬液按现行《中国兽药典》进行制备。
1.6 试验动物
2~4日龄乳鼠,由哈药集团生物疫苗有限公司实验动物中心提供;1.5~2月龄的仔猪和5~6月龄的初产母猪(猪瘟中和抗体阴性、猪细小病毒HI抗体效价不超过1∶8),购自黑龙江省哈尔滨市郊某猪场,品种为长白。
2 方法
2.1 MontanideTM ISA 206 VG佐剂疫苗配制
2.1.1 油相制备
将206佐剂置于油相制备罐中,加热至30℃,备用。
2.1.2 水相制备
使用检验合格的猪细小病毒灭活液作为水相,同时采用ST-S无血清培养液作为对照组水相。
2.1.3 乳化
将油相与水相按体积比为1∶1混合,真空或正压加料并循环搅拌至油相与水相充分混合,乳化成双相油乳剂。疫苗制备情况见表1。

表1 206佐剂1 000头份疫苗配制 mL
2.1.4 分装
无菌定量分装,加盖密封,粘贴标签,置2~8℃保存,备用。
2.2 白油佐剂疫苗的配制
2.2.1 油相制备
取注射用白油94份,加入硬脂酸铝1.5份,边加热边搅拌,直至完全透明,再加入4.5份Span-80,充分混匀,116℃高压灭菌30 min后备用。
2.2.2 水相制备
取检验合格的猪细小病毒灭活液,混合抗原96份,加入4份灭菌Tween-80,待Tween-80完全溶解,制备成白油佐剂疫苗所需的水相;取配制好的ST-S无血清培养液96份,加入4份灭菌Tween-80,待Tween-80完全溶解制备成对照组水相。
2.2.3 乳化
水相和油相按体积比1∶1.5混合,先将油相注入预混罐中,2 500 r·min-1搅拌,缓慢加入水相,再注入乳化罐,以10 000 r·min-1乳化5~8 min,使混合物充分乳化。疫苗制备情况见表2。

表2 白油佐剂1 000头份疫苗配制所需成分制备mL
2.2.4 分装
无菌定量分装,加盖密封,粘贴标签,置2~8℃保存,备用。
2.3 疫苗检验
2.3.1 性状检验
按《中国兽药典》附录对206佐剂疫苗和白油佐剂疫苗的外观、剂型、稳定性和黏度进行检验。
2.3.2 无菌检验
按现行《中国兽药典》附录对206佐剂疫苗和白油佐剂疫苗进行无菌检验。
2.3.3 安全检验
用乳鼠检验:将2~4日龄乳鼠20只按表3随机分为4组,每组5只,每只皮下注射疫苗0.1 mL,观察7 d。
用猪检验:将断奶后1.5~2月龄猪8头按表3随机分为4组,每组2头,深部肌肉注射疫苗5 mL,观察21 d。

表3 不同佐剂疫苗与对照分组
2.3.4 效力检验及免疫期测定
将5~6月龄的初产母猪20头按表3分为4组,每组5头,第1组和第2组经颈部肌肉途径接种疫苗2.0 mL,第3组和第4组经颈部肌肉途径接种疫苗2.5 mL,另设对照猪5头,经颈部肌肉途径注射生理盐水2.0 mL。
各试验组初产母猪分别在免疫后第0、7、14、21、28、60、90、120、150、180、210天和240天对所有试验猪采血,分离血清,并测定猪细小病毒HI抗体效价。计算猪细小病毒HI抗体几何平均效价。
3 结果与分析
3.1 疫苗性状检验结果
对制备的4种疫苗进行性状比较,结果显示4种疫苗外观及稳定性一致,但采用206佐剂乳化工艺制备的疫苗与白油佐剂制备疫苗的黏度差异显著。结果见表4。

表4 疫苗性状检验结果
3.2 两种乳化工艺流程比较结果
206佐剂与白油佐剂两种乳化工艺流程比较,可以看出,猪细小病毒病灭活疫苗(L株,悬浮培养)在车间生产的情况下,配苗乳化采用206佐剂工艺相对简单。结果见表5。
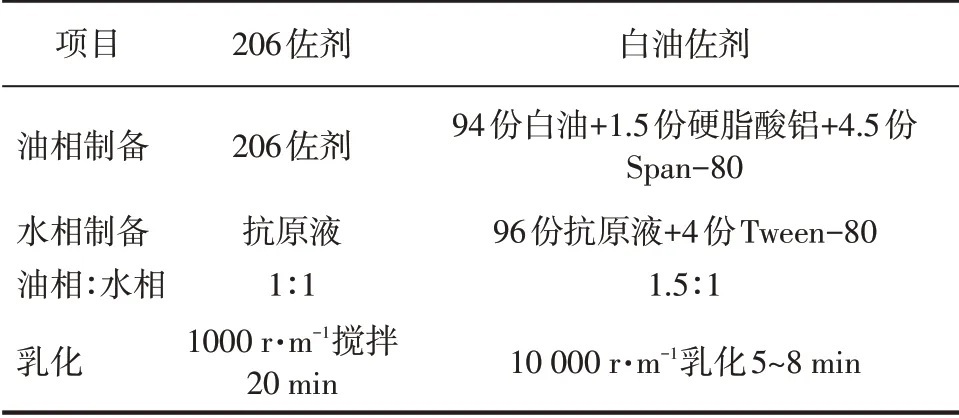
表5 乳化工艺流程比较结果
3.3 无菌检验结果
经接种T.G、G.A和G.P培养基检验,4种疫苗均无细菌、霉菌污染。
3.4 安全性试验结果
3.4.1 乳鼠安全性检验结果
以实验室制备的这4种疫苗(见表3),分别按0.1 mL·只-1颈部皮下注射3日龄同窝乳鼠5只,观察7 d。结果显示,分别用4种疫苗接种乳鼠后,在观察期内接种乳鼠全部健活,且无局部和全身不良反应。
3.4.2 猪安全性检验结果
以实验室制备的这4种疫苗(见表3),分别经深部肌肉注射疫苗5 mL·头-1,接种1.5~2月龄的猪2头,观察21 d。结果显示实验室制备这4种疫苗注射猪后,在观察期内接种猪全部健活,且无局部和全身不良反应。
3.5 效力检验及疫苗免疫期测定结果
以实验室制备的这4种疫苗(见表3),各经颈部肌肉免疫5月龄的初产母猪,每组5头。免疫后第7天分别测定猪细小病毒HI抗体效价,计算免疫HI抗体几何平均效价,进行疫苗效力评估,并进行疫苗免疫期测定。
免疫后第7天,第1组(见表3)免疫猪产生HI抗体显著高于第3组;免疫后第60天,第1组免疫猪HI抗体达到峰值。第1组免疫6个月后的HI效价仍大于规程要求的1∶64,可以满足猪生长期免疫保护的需要。
4 结论
使用MontanideTMISA 206 VG佐剂制备疫苗,乳化工艺相对简单;制备疫苗剂型为水包油包水型,黏度低,易注射,吸收良好;局部和全身均无不良反应,安全性良好;免疫后第7天猪细小病毒206佐剂疫苗免疫猪产生HI抗体显著高于白油佐剂疫苗,抗体效价高;免疫期为6个月,可以满足免疫保护期要求,因此确定MontanideTMISA 206 VG佐剂作为猪细小病毒病灭活疫苗的佐剂。

