负载型过渡金属氧化物催化剂催化分解臭氧性能研究
鹿靖麟,王 胜,赵 琨,王 婷,倪长军,汪明哲,王树东
(1.中国科学院 大连化学物理研究所,洁净能源国家实验室,辽宁 大连 116023;2.中国科学院大学,北京 100049)
平流层臭氧能吸收紫外线,保护生物免受辐射。然而,近地面臭氧会严重危害人类健康和动植物生长[1−9],从环境保护和人类健康的角度出发,高效臭氧消除技术的开发具有重要意义。目前,去除臭氧的方法主要有辐射分解法、热分解法、等离子体分解法、吸收吸附法以及催化分解法,其中,辐射分解法、热分解法、等离子体分解法[10,11]因高成本和低分解效率,限制其应用。而活性炭吸附法和化学吸收法,存在再生和废液处理等问题。
催化分解法可以实现低温下臭氧分解,方法简单而且分解效率高,是目前最有前景的臭氧分解去除技术,但是同时具有优良活性和稳定性的臭氧分解催化剂是研究的难点[12−17]。臭氧分解催化剂通常为活性炭、γ-Al2O3、分子筛负载贵金属(如钯、铂、金等)或过渡金属氧化物(如镍、锰、钴等)形成的负载型催化剂,或者是过渡金属氧化物催化剂。贵金属催化剂如Pd-Mn/SiO2-Al2O3催化剂[18]表现出优异的O3分解性能,已应用于车载臭氧净化器中。共浸渍的Pd、MnOx催化剂,由于Pd 和MnOx之间的协同作用,具有更高的臭氧分解活性。而贵金属高的成本限制了其广泛应用,所以过渡金属氧化物臭氧分解催化剂受到广泛关注。研究发现在过渡金属氧化物中,p 型半导体金属氧化物如MnO2、Co3O4、Fe2O3、NiO、CeO2和Ag2O等,比n 型半导体金属氧化物如CuO、V2O5、Cr2O3和MoO3等具有更高的臭氧分解活性[19],这可能是由于p 型半导体金属氧化物催化剂比n 型更容易接受电子[20]。在单一金属氧化物催化剂中,多数研究结果发现,MnO2具有最高的臭氧分解活性。但是,将过渡金属氧化物负载到Al2O3、SiO2[21]、SiO2-Al2O3[18]、还原石墨烯[22]、活性炭表面、TiO2[23]时,由于金属氧化物与载体作用力以及金属氧化物在载体上分散性能的差异,会显著影响其臭氧分解性能。有研究发现,Ni/Al2O3催化剂由于金属Ni 和NiO 的协同作用,具有更高的活性和耐水性能[21],也有研究认为Ni/Al2O3高的稳定性,是由于NiAl2O4[24]的形成。MnO2由于多变的价态和晶相[25],以及载体种类对Mn 配位环境的影响[21],都会影响其催化性能。载体的引入会改变过渡金属氧化物电子传输能力,从而影响催化剂的臭氧分解性能,导致与其不同的金属氧化物催化性能。而负载型催化剂由于高的比表面积和强度,是主要的商用臭氧分解催化剂的结构形式。
为了揭示负载型过渡金属氧化物催化剂催化分解臭氧的内在机理,选取单一金属氧化物具有较高活性的NiO、MnO2、Co3O4(p 型半导体)、Fe2O3以及CuO(n 型半导体),将其负载于γ-Al2O3,研究其臭氧分解活性和稳定性,在连续流固定床反应器中考察了不同催化剂的臭氧分解性能,结合催化剂理化性能表征以及臭氧分解催化剂反应前后微观结构的变化,阐明催化剂活性和稳定性与过渡金属之间的依存关系。
1 实验部分
1.1 实验材料和试剂
实验中催化剂载体选用直径为2.0−3.0 nm 的商用γ-Al2O3粉末;活性组分前驱体分别选用50%硝酸锰溶液(Mn(NO3)2,50%)、硝酸钴六水合物(Co(NO3)2·6H2O)、硝酸铁九水合物(Fe(NO3)2·9H2O)、硝酸铜三水合物(Cu(NO3)2·3H2O),均购自国药集团化学试剂有限公司;硝酸镍六水合物(Ni(NO3)2·6H2O),购自天津市大茂化学试剂厂。实验中所用药品均为分析纯。
1.2 催化剂的制备
将商用γ-Al2O3粉末压片成型、筛分,选用粒径为20−40 目的γ-Al2O3,置于773 K 马弗炉中焙烧2 h 后作为载体备用。首先测定载体吸水率,配置一定浓度的前驱体溶液,采用浸渍法将活性组分负载在载体上(负载量10%),然后于393 K 干燥2 h,773 K 下焙烧2 h,制得负载过渡金属氧化物的催化剂,被命名为M-Al(M=Ni、Mn、Co、Cu和Fe)。在研究催化剂失活原因时,新鲜催化剂被标记为M-Al(f);而反应20 h 以后收集的失活样品,被命名为M-Al(u)。
1.3 催化剂的表征方法
X 射线衍射在日本公司Rigaku RINTD/MAX-2500PC 型粉末X 射线衍射仪上进行。实验条件为Cu Kα 靶,管电压为40 kV,管电流为40 mA,扫描速率为5℃/min,20°−80°扫描。催化剂的比表面积以及孔结构测试是在Quantachrome 公司的NOVA 2200e 型全自动气体吸附分析仪上进行分析。测试前在200℃的真空条件下预处理3 h。H2程序升温还原(H2-TPR)分析和O2程序升温脱附(O2-TPD)分析,在美国Quantachrome 公司的ChemBET Pulsar 型化学吸附仪上进行测试。H2-TPR 测试每次取约200 mg 样品,置于U 型石英反应管中。首先,将样品在200℃下用He 吹扫2 h,除去样品表面杂质;冷却至室温后,将气路切换为10%的H2/Ar 混合气,待基线稳定后,以10℃/min升温至900℃,检测并记录信号值随温度的变化。O2-TPD 测试每次取约200 mg 样品,置于U 型石英反应管中。首先,将样品在200℃下用Ar 吹扫2 h,除去样品表面杂质;冷却至室温后,将气路切换为He,待基线稳定后,以5℃/min 升温至700℃,检测并记录信号值随温度的变化。X 射线光电子能谱(XPS)采用 Kratos Axis Ultra DLD,激发源采用Al Kα 射线(hv=1486.6 eV)。扫描电子显微镜(SEM)采用的是Zeiss g300,工作电压为15 kV。
1.4 实验装置和评价方法
催化剂催化分解臭氧活性的评价在微型固定床石英反应器中进行。系统由质量流量控制器、臭氧发生器(CFG,大连奥山环保科技有限公司)、低温循环泵(LTC-4/15,上海棱标仪器有限公司)、温控仪、反应炉、臭氧分析仪(49i,美国Thermo Scientific 公司)构成,石英反应器内径为6 mm。臭氧通过在臭氧发生器中放电电离纯氧和氩气的混合气体,这样可以避免空气源臭氧形成过程中产生的氮氧化物对反应的影响,然后通过空气将臭氧稀释到入口臭氧浓度,再进入反应器。采用臭氧分析仪测定进出口臭氧浓度。反应条件为:进口臭氧质量浓度29.5 mg/m3、WHSV=200000 mL/(gcat·h)、反应温度298 K、催化剂装填量为0.5 g。反应装置流程图如图1 所示。
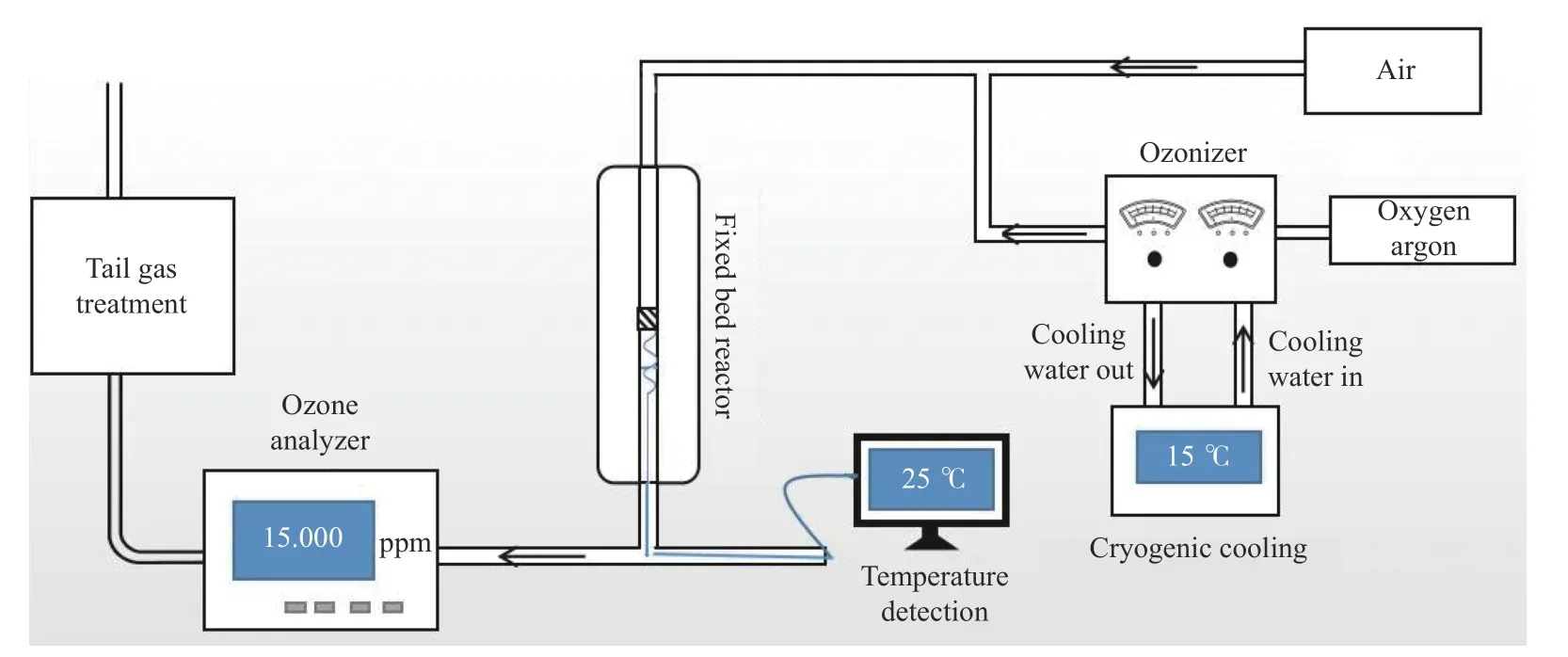
图1 催化臭氧分解工艺流程图Figure 1 A flow diagram of ozone catalytic decomposition
2 结果与讨论
2.1 臭氧催化剂催化性能
实验研究了25℃、WHSV=200000 mL/(gcat·h)条件下,γ-Al2O3负载不同过渡金属氧化物分解臭氧的催化性能,如图2 所示。由图2 可以看出,负载型催化剂的活性具有如下的顺序:Ni-Al>Mn-Al>Co-Al>Fe-Al>Cu-Al。和单一金属氧化的性能相比,基本满足p 型半导体金属氧化物的性能优于n 型,区别在于相关研究表明单一金属氧化物MnO2的催化活性优于NiO。而将其负载在γ-Al2O3表面,Ni-Al 催化剂具有更高的臭氧催化分解性能。
2.2 形貌与微观结构
2.2.1 XRD 表征
为了阐明催化剂微观结构与臭氧分解性能间的关联,首先通过XRD 研究了催化剂的晶体结构,图3 为五种催化剂的X 射线衍射谱图。由图3可以看出,所有样品在 2θ=45.7°、66.7°都有γ-Al2O3的特征峰,而在负载NiO 的催化剂(Ni-Al)中,在2θ=37.2°发现了镍铝尖晶石结构(JCPDS 10-0339)以及2θ=39.7°的NiO 的峰(JCPDS 22-1189),说明在催化剂Ni-Al 催化剂中,仅存在较少的NiO,同时还形成了NiAl2O4结构。此外,对比其他负载型金属氧化物催化剂可以看出,Ni-Al 催化剂XRD谱图结晶度最差,分散性较好;在负载锰的催化剂中,分别在2θ=28.7°、37.3°和52.7°观察到了MnO2的衍射峰(JCPDS 24-0735),而2θ=33°附近的小峰归属于Mn2O3(JCPDS 75-0921);在负载氧化钴的催化剂中,在2θ=31.3°、36.8°、44.7°、59.6°、73.9°处出现了CoAl2O4尖晶石的衍射峰(JCPDS 73-0238)。因此,基于XRD 表征结果可以推断Ni-Al 催化剂高的臭氧分解效率可能与其表面高的Ni 分散度以及NiAl2O4结构的形成有关。
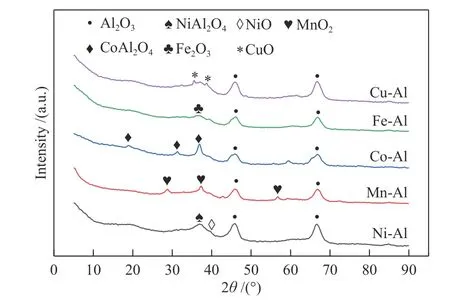
图3 不同催化剂的XRD 谱图Figure 3 XRD patterns of different catalysts
2.2.2 BET 测试
实验测定了空白载体γ-Al2O3及五种负载型臭氧分解催化剂Ni-Al、Mn-Al、Co-Al、Fe-Al、Cu-Al的BET 比表面积、孔容及孔径,见表1。由表1 可以看出,由于活性组分的负载,催化剂的比表面积和孔容出现了不同程度的减小,而孔径变化不明显,可能是活性组分主要填充了微孔结构。此外,进一步说明上述负载型催化剂的织构性质不是影响臭氧催化分解性能的关键。

表1 不同催化剂的理化结构参数Table 1 Texture properties of different catalysts
2.2.3 SEM 表征
为了进一步探究催化剂的表面形貌,对具有较好催化性能的Ni-Al、Mn-Al、Co-Al 催化剂进行了SEM 表征,如图4 所示。由图4 可以看出,催化剂表面无规则形貌。而从Ni-Al、Mn-Al、Co-Al 催化剂表面EDS 分析可以看出,Ni-Al 催化剂表面氧化镍颗粒分散较好,这与XRD 结果一致;而Mn-Al 催化剂表面有颗粒团聚发生;Co-Al 催化剂表面的Co3O4颗粒较少,这可能由于Co3O4进入到了γ-Al2O3载体内部。可以推断高的NiO 分散度是Ni-Al 催化剂优良活性的原因之一。

图4 三种催化剂的扫描电镜照片Figure 4 SEM and EDS images of three catalysts
2.2.4 TEM 和HETEM 表征
通过TEM 和HETEM 对样品的微观结构进行了进一步的分析表征。从图5(a)中可以发现,在Ni-Al 催化剂中,存在NiAl2O4的晶格衍射条纹,0.24 nm 对应NiAl2O4(311)面晶格间距[26];图5(b)中观察到MnO2(101)面[27](晶格间距为0.24 nm);图5(c)中观察到晶格间距为0.244 和0.2 nm 晶格条纹,分别对应于CoAl2O4(311)面和γ-Al2O3(200)面[28],并且通过对催化剂Co-Al 和催化剂Ni-Al 的不同区域进行元素分析(图5(d)、(e)),结果如表2、表3 所示,钴元素在不同位置的质量分数差别在一个数量级以上,形成的CoAl2O4可能发生了包埋和团聚,而Ni-Al 催化剂不同区域镍元素的质量分数和摩尔含量差别不大,所以Ni-Al 催化剂高的催化活性可能是由于其活性组分分散度高,并且形成了NiAl2O4结构促进了臭氧分解,从而具有最优异的臭氧分解活性。

图5 催化剂10% MOx/γ-Al2O3 的透射电镜照片Figure 5 TEM image of 10% MOx/γ-Al2O3

表2 钴氧化物负载型催化剂的元素分析Table 2 Elemental distributions over the Co-Al catalyst
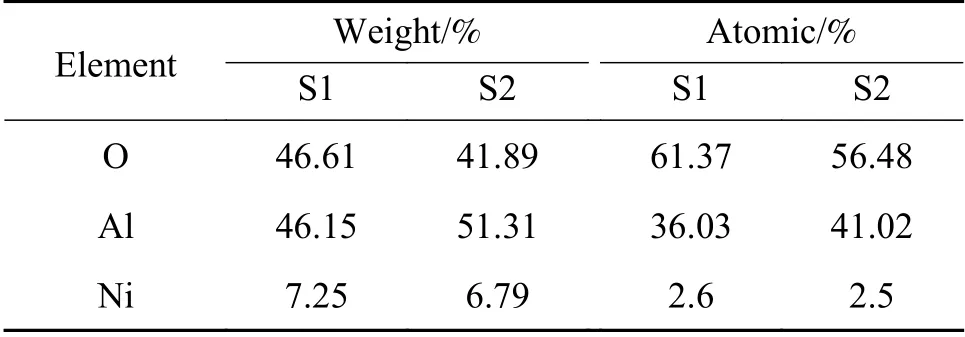
表3 镍氧化物负载型催化剂的元素分析Table 3 Elemental distributions over the Ni-Al catalyst
2.3 氧化还原性能
2.3.1 H2-TPR 和O2-TPD 分析
金属氧化物催化剂的氧化还原性能是影响其臭氧分解性能的重要因素。对新鲜催化剂进行了H2-TPR 测试(图6(a))。通常,当金属与载体之间相互作用较强时,其还原温度较高,在Ni-Al 催化剂中,600℃左右的还原峰归属于与γ-Al2O3载体相互作用较强的NiO,而750℃左右的还原峰归属于NiAl2O4的还原[26]。另外,从XRD、EDS 结果可知,NiO 在载体表面具有较高的分散,其与载体具有较强的相互作用[29,30];对于Mn-Al 催化剂,第一个还原峰是由MnO2还原为Mn2O3或者Mn3O4而形成的;第二个还原峰为MnO 还原峰[31];在样品Co-Al 中,出现的还原峰分别对应于Co3O4还原为CoO 再还原为金属钴[28];在样品Fe-Al 中,还原峰为Fe2O3还原为Fe3O4[32];在样品Cu-Al 中,CuO还原为Cu 的还原温度较低[33]。尽管,Ni-Al、Mn-Al 与Co-Al 催化剂在低温区没有H2-TPR 峰,可能是由于Ni、Mn 和Co 在催化剂表面具有高的分散度所致。

图6 不同催化剂的H2-TPR 和O2-TPD 谱图Figure 6 Redox properties of different catalysts
为了进一步说明催化剂氧化还原能力与催化分解臭氧性能之间的关联,研究了具有较高活性的新鲜和失活Mn-Al 及Ni-Al 催化剂的O2-TPD 性能(图6(b))。在低温(<200℃)的脱附峰为物理吸附氧物种的脱附峰,200−350℃的脱附峰一般是由于化学吸附氧和表面活性氧脱附而成,350℃以上的峰归属于晶格氧的释放[34]。由图6(b)可见,新鲜的Ni-Al 比反应后的Ni-Al 催化剂具有更多的吸附氧,因此,化学吸附氧和表面活性氧对催化臭氧分解具有促进作用。而由反应前后Mn-Al 催化剂的O2-TPD 结果可以发现,在新鲜的催化剂中,氧主要以晶格氧的形式存在,而反应后的催化剂在低温条件下存在较多的吸附氧,这与锰氧化物在催化分解臭氧的反应机理相吻合,即在锰氧化物催化剂上,臭氧分子及反应中生成的过氧化物是在氧空位上进行反应,而催化剂的失活是因为活性位氧空穴被占据[35],活性位点减少,分解效率降低。O2-TPD 结果表明,锰氧化物催化分解臭氧的活性位点为氧空位,而镍氧化物催化分解臭氧的活性位点为化学吸附氧,两种催化剂的反应机理不同,NiAl2O4结构的生成可能形成了更多的化学吸附氧[36]。
2.3.2 XPS 分析
图7 为反应前后,分别负载镍、锰、钴氧化物催化剂的XPS 谱图。由图7(a)可以看出,对Ni 2p3/2能谱可以分解为三个峰,其结合能分别为855.7、857.2、861.2 eV,分别归属于NiO 和NiAl2O4以及卫星峰[37,38],对比发现,反应后的催化剂中NiAl2O4的峰面积轻微减少;由图7(b) Mn 2p3/2谱图可以看出,在结合能分别为641.8、643.6 eV 处存在两个峰,分别归属于Mn2O3和MnO2[39,40],相对于新鲜催化剂,反应后的催化剂中MnO2对应的峰面积略有增加;由图7(c) Co 2p3/2可以发现,在结合能分别为779.8、781.5 与786.6 eV 处的三个峰分别归属于Co3O4、CoAl2O4以及卫星峰[41,42],与反应前新鲜催化剂相比,反应后的失活催化剂中CoAl2O4的含量明显减少。图8 对反应前后催化剂表面元素进行了定量分析,其中,Ni-Al 催化剂中反应后NiAl2O4的含量从41.7%下降为33.6%,可能是导致催化剂活性下降的原因。而在Mn-Al 催化剂中,反应后MnO2的含量略有增多,从50.74%上升至52%,这可能是由于锰氧化物在臭氧氧化下发生价态的转变。在Co-Al 催化剂中,反应后CoAl2O4明显减少,Co3O4明显增多。

图7 反应前后三种催化剂的XPS 谱图Figure 7 XPS spectra of fresh and used catalysts
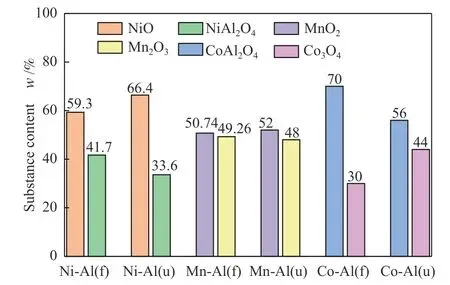
图8 新鲜和反应后催化剂的表面元素组成Figure 8 Surfaces composition on fresh and used catalysts
3 结 论
研究了γ-Al2O3负载不同过渡金属氧化物催化分解臭氧的性能,在入口臭氧质量浓度为29.5 mg/m3、298 K,WHSV=200000 mL/(gcat·h)下,Ni-Al 催化剂具有最高的臭氧分解活性,在20 h 内臭氧分解效率高于96%。
通过XRD 研究发现,在Ni-Al 催化剂中存在镍铝尖晶石相,同时其表面高分散度的镍物种也是其具有较高臭氧分解效率的原因。
H2-TPR 和O2-TPD 结果表明,不同过渡金属氧化物催化分解臭氧的反应机理不同,锰基催化剂臭氧分解的活性位为氧空穴;而Ni-Al 催化剂反应活性位是表面化学吸附氧。XPS 表征发现,反应后Ni-Al 催化剂中NiAl2O4的含量减少,进一步验证了NiAl2O4对于催化分解臭氧的作用,即生成的尖晶石结构会使金属氧化物形成较小的颗粒和较高的分散性,催化剂表面产生丰富的化学吸附氧。

