加速康复外科处理策略在破裂性腹主动脉瘤术后腹腔内高压中的应用研究
何 英 赵纪春 吴洲鹏 刘晓艳 刘 莉
四川大学华西护理学院/四川大学华西医院血管外科,四川 成都 610041
破裂性腹主动脉瘤(ruptured abdominal aortic aneurysm,RAAA)是血管外科常见的危急重症疾病,若不及时治疗,总体病死率为80%~90%[1]。手术是RAAA的主要治疗方式,包括开放性手术(open surgery,OS)和腔内修复术(endovascular aortic repair,EVAR)。由于术前行复苏治疗、术中使用主动脉球囊阻断及主-单髂支架等因素,RAAA术后常合并腹膜后血肿、出凝血功能障碍、弥漫性水肿,从而导致腹腔内压力(intraabdominal pressure,IAP)升高[2]。IAP持续性或病理性重复性升高≥12 mmHg(1 mmHg=0.133 kPa)定义为腹腔内高压(intra-abdominal hypertension,IAH)。若病情继续发展,可导致肠缺血坏死、肾缺血、肾功能不全等多器官功能衰竭,称为腹腔间隙综合征(abdominal compartment syndrome,ACS)[3]。研究显示,ACS是导致患者死亡的独立预测因素,其中,OS术后ACS的发生率为20%[4]。在国内,加速康复外科(enhanced recovery after surgery,ERAS)已在临床上得到广泛应用与推广[5-6],但是,其在血管外科领域涉及较晚。因此,本文应用ERAS理念协同多学科联合团队,提出以下处理策略,以预防RAAA术后IAH发生,减少并发症发生,降低RAAA围手术期病死率。
1 RAAA术后IAP的监测与预防
《重症患者腹内高压监测与管理专家共识》中[7],根据IAP将IAH分为4级:Ⅰ级,IAP为12~15 mmHg;Ⅱ级,IAP为16~20 mmHg;Ⅲ级,IAP为 21~25 mmHg;Ⅳ级,IAP>25 mmHg。以间歇性(每4~6 h监测1次IAP)测量为标准[8]。监测方法选择操作简单、不适感少、费用低廉的经膀胱测压方法:将Foley导尿管经尿道置入膀胱,排空膀胱后注入不超过25 ml的无菌生理盐水,以耻骨联合水平为零点平视液面。测量时需注意:(1)测量时传感器在腋中线水平归零;(2)于患者呼气末进行测量;(3)测量时双下肢放松,切勿屈曲体位,以使腹部肌肉完全放松;(4)若IAP为Ⅳ级,患者取平卧位后再次进行测量。一旦腹主动脉瘤患者出现瘤体破裂,若不及时救治,会出现失血性休克,而术中低体温、毛细血管渗漏、大量输液及输血等治疗均可加重心肺负荷,使包裹性血肿转为游离性血肿[9];术后出现腹胀、腹腔积液、积血、腹腔感染或腹腔脓肿等因素可使IAP升高,尤其是存在较大腹膜后血肿、血流动力学不稳定的患者,可继发弥漫性的器官水肿;传统手术后腹部切口可增加腹壁顺应性下降的风险,因此,术后应高度重视引起IAP升高的危险因素[10],即腹壁顺应性下降、腹腔内容物增加、液体复苏、年龄、出凝血功能障碍、床头抬高、机械通气、肥胖、烦躁或精神异常等。
2 RAAA术后各系统重症监护
2.1 心血管系统
IAP达到10 mmHg可促使横膈膜向上提升,导致胸膜腔内压升高,使下腔静脉及横膈膜以下的血液回流减少,降低心脏前负荷;横膈膜的提升和IAP的升高会降低心肌收缩力;IAP的持续上升可导致主动脉和全身动脉系统直接受到压迫,增加心脏后负荷;IAP对心脏功能的影响最终会造成全身低血压、右侧冠状动脉血流减少及缺血、右心室收缩力下降[11-12]。对于因瘤体破裂而发生失血性休克的腹主动脉瘤患者,液体复苏是改善其低血容量的重要手段,但是,大量液体复苏可能会增加细胞渗出、组织水肿,导致医源性IAH/ACS[13],因此,术前要维持相对稳定的低血压状态(收缩压70~90 mmHg),液体复苏时提高血浆和浓缩红细胞的输注比例。Phillips等[14]研究发现,行RAAA的OS时,提高血浆的输入量会降低围手术期病死率。从血流动力学角度看,EVAR术后,置入的覆膜支架可使动脉瘤壁避免直接的血流冲击,提高血流速率,改善血流动力学环境,但支架移位、内漏等术后并发症仍是血管外科医护团队需要解决的问题[15-17]。原通等[18]研究发现,EVAR术后再入院的主要原因依次为内漏、髂支闭塞、髂动脉远端瘤样扩张、瘤体破裂。
2.2 呼吸系统
IAP达到15 mmHg可通过横膈膜传导使胸腔内肺泡压力升高、无效腔增加、肺分流分数增加、功能残气量减少、胸壁顺应性降低等,进而发生低氧血症和高碳酸血症[19]。加之术前失血性休克、毛细血管渗漏等,IAP的升高进一步增加了肺血管抵抗,更易发生肺水肿。研究显示,使用呼气末正压通气(positive end expiratory pressure,PEEP)技术可扩张已塌陷的肺泡,促进肺泡功能恢复,但PEEP可同时过度扩张正常肺泡,导致机械性肺损伤,是IAP升高的独立危险因素[20],因此,呼吸机参数的设定应根据IAP水平进行调整,采取有效的机械通气,床旁心电监护动态观察血氧饱和度,判断低氧血症是否改善,保障呼吸机管道通畅。
2.3 中枢神经系统
IAH引起脑灌注压降低,使脑静脉血流流出受阻,导致颅内压升高,损害血-脑脊液屏障[21]。祁慧等[22]的研究证实,维持一定的液体复苏能增加心输出量,增加脑灌注。RAAA术后,应使用最佳的镇静、镇痛方式对患者进行监护,避免患者因情绪激动、烦躁导致IAP进一步升高。对于轻中度IAH患者,可使用神经肌肉阻滞剂控制IAP。
2.4 泌尿系统
少尿和肾功能不全是IAH进行性升高的早期临床表现[23]。RAAA术中开放阻断钳时,血液大量流入缺血组织,使原本血流丰富的肾动脉突然相对缺血,导致肾功能不全,尤其是合并慢性肾功能衰竭的患者,进而发生急性肾功能衰竭,而术后使用提高机体抗氧化能力的药物及运用远端缺血预处理方法可防治再灌注损伤的发生[24]。在急性肾损伤的表现中,肾功能和尿量受IAP的影响更大,而不是肾脏平均动脉压[25]:IAP >15 mmHg可引起少尿,IAP>30 mmHg会导致无尿。RAAA术后,应留置尿管,监测患者每小时的尿量。
2.5 消化系统
胃肠道是对IAP最敏感、反应最早的器官。IAH可减少肠系膜血流,明显降低肠道黏膜的血液循环,增加肠道通透性,导致内毒素血症,进而对线粒体造成不可逆转的损害和肠黏膜坏死[26]。当肠腔内压力升高达15 mmHg时,肠系膜血流受阻,肠黏膜屏障受损,肠道内细菌及内毒素异位,可导致全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)的发生[27]。Willemsen等[28]进行的全国性队列研究显示,腹主动脉瘤术后患者结肠缺血的总发生率为2.8%,RAAA术后患者结肠缺血的总发生率为15%;发生结肠缺血患者的病死率达50.6%;RAAA术后早期应禁食、禁饮,留置胃管行胃肠减压,必要时行肛管排气,以减轻胃肠道压力,加速肠道排气。
3 多学科团队协作
3.1 成立RAAA急诊绿色通道
联合急诊科建立腹主动脉瘤就诊绿色通道,一旦收治RAAA患者,立即启动快速流程(图1),建立静脉双通道,合理液体复苏,积极完善实验室检查、备血,协调放射科预留检查设备,由专人转运患者并完善影像学检查,同时协调急诊手术间备用,联系血管外科、麻醉科等科室的医师共同参与多学科诊疗团队(multi-disciplinary team,MDT)协作,将患者直接送入手术室行手术治疗,尽量缩短术前等待时间,争取抢救时机。
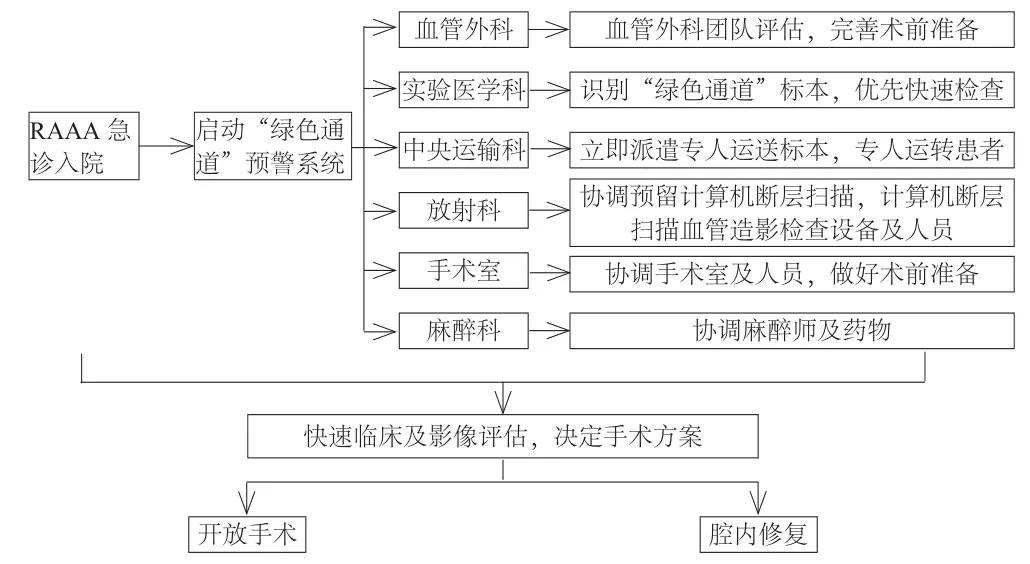
图1 RAAA绿色通道协作流程
3.2 RAAA治疗方式
快速评估患者的年龄、基础疾病、血流动力学情况,结合胸腹计算机体层血管成像评估腹主动脉瘤的解剖条件。若患者高龄或合并基础疾病,EVAR可考虑为首选方案;解剖条件差者根据个体情况考虑行OS,尽快行腹主动脉瘤切除+主-髂(股动脉)分叉型人工血管移植术[29]。
3.3 MDT团队诊治
术后,严密监测患者生命体征,记录输液量、每小时尿量,在无明显血容量减少而出现少尿或无尿时,请泌尿外科急会诊,使用利尿剂,定期监测尿素氮、肌酐等实验室指标以观察肾功能,必要时行血液透析。重视患者主诉,若患者出现腹胀、腹痛等不适,请消化内科、中西医结合科联合会诊,使用小茴香腹部热敷,避开手术切口,沿着顺时针方向轻轻推拿,每日2次;配合按摩穴位足三里,每日3次,每次20 min,可缓解呃逆、腹胀等不适。铁明慧等[30]的研究发现,参苓承气汤+灌肠可改善IAH脾虚气滞型患者的腹胀症状,降低肠黏膜通透性,改善肠屏障功能。
3.4 医护一体化模式
(1)医护一体床旁查房,提供责任制整体护理。(2)术后第1天行深静脉血栓栓塞症风险筛查,实施血栓防控三级预防:基础预防、物理预防、药物预防。(3)进行数字疼痛评估,给予超前镇痛。(4)进行营养风险筛查,纠正低蛋白血症,提高机体免疫力。(5)降低感染发生率,基于RAAA手术创伤大、病情危重、术中及术后监测尿量的特点,术中留置尿管,因此,术后3~5 d,生命体征平稳后将患者转回普通病房,即可拔除尿管。杨翰等[31]发现,在ERAS理念的指导下,人工全膝关节置换术后未留置尿管组患者的术后住院时间明显缩短,尿路感染发生率明显降低。(6)采用华西心晴指数问卷(Huaxi emotional-distress index,HEI)[32]、匹兹堡睡眠质量指数量表(Pittsburgh sleep quality index scale,PSQI)[33]评估患者的睡眠状态及情绪,于床旁行正性心理支持,缓解其焦虑、抑郁的情绪。必要时请心理卫生中心的医师会诊,对于睡眠障碍者短期给予助眠药物治疗。(7)伤口处理:术后3~5 d,由伤口治疗师换药,行红外线烤灯照射,每日2次,每次20 min。(8)功能锻炼:联合康复治疗师共同指导患者进行床上功能锻炼,如双下肢直腿抬高训练,踝泵运动,进行双上肢屈肘、伸直训练,双手支撑抬臀训练,每日2~3次,每次30 min。
4 小结与展望
RAAA的临床表现为突发腰背部剧烈疼痛,持续数小时或数天,伴有休克体征,是血管外科常见的高危疾病,院前病死率为59%~83%[34]。从治疗术式的选择方面,OS作为经典的手术方式,术后病死率达22%[35],而EVAR具有手术时间更短、术中失血量和输血量更少、住院时间更短的优势[36],由于发病急、病情重、手术创伤等因素,RAAA常规行重症监护,术后常见的并发症中,ACS的发病率为20%~25%[37]。研究显示,重症监护病房内ACS整体病死率和并发症发生率达67%[38],其中,EVAR后发生ACS的早期病死率为22.6%[39],若不及时干预,可导致缺血性结肠炎、多器官功能衰竭等,是影响患者预后甚至导致死亡的危险因素之一,严重威胁患者的生命。在ERAS管理模式下[40],RAAA的诊治需要血管外科协同急诊科、麻醉科、呼吸科、心脏大血管外科、泌尿外科、消化内科、神经内科、心理卫生中心等其他临床相关科室,不仅需要手术医师具有精湛的手术技巧,还需要高质量的护理团队,以患者为中心,术前减少诱发因素,避免过度积极的补液,实行规范的液体复苏[41],提高血浆与红细胞的输注比例,术后加强IAP的监测与管理,避免持续性IAH发生,降低RAAA后ACS的发生率,从而降低病死率,提高生存质量。

