结合临床个案探讨高龄严重骨质疏松患者的管理策略
吴露露,李楠 ,裴育 ,杨国庆 ,巴建明
(中国人民解放军总医院:1第一医学中心内分泌科,3第二医学中心内分泌科,北京100853;2广东省中医院内分泌科,广州 510006)
随着中国进入老龄化社会,骨质疏松的患病率大幅增加。骨质疏松性骨折危害巨大,是老年患者致残和致死的主要原因之一。如何管理高龄严重骨质疏松患者,避免再发骨折,减轻患者临床症状,提高生活质量,成为临床的一大挑战。本文拟通过对一例高龄严重骨质疏松症患者的治疗分析,探讨此类患者的治疗方案。
1 临床资料
患者,女性,94岁。2013年12月无明显诱因出现腰背部疼痛,胸腰段X片示“严重骨质疏松症伴胸椎压缩性骨折(T12)”,不规律服用碳酸钙D3、骨化三醇胶丸、骨疏康胶囊等。2014年5月27日因疼痛加重,复查胸腰段X片,示“胸8、10、12椎体压缩性骨折”,诊断为“严重骨质疏松症伴多发胸椎压缩性骨折”,开始规律服用碳酸钙D3片、骨化三醇胶丸。2015年10月因疼痛改善不明显,影响睡眠、活动,就诊于解放军总医院内分泌科门诊。否认糖尿病、风湿免疫性疾病等病史,无特殊用药史。否认烟酒嗜好。
入院查体身高147 cm,体质量32 kg,体质量指数:14.81 kg/m2,血压、心率无异常,甲状腺未扪及。胸廓无畸形,无挤压痛。脊柱无侧弯,叩击痛阳性,四肢关节无畸形。
实验室检查血钙2.51 mmol/L,血磷:1.15 mmol/L,甲状旁腺激素:11.53 pg/ml ,碱性磷酸酶:52.5 U/L,25-羟维生素D3:34.7 ng/ml,血清总I型胶原氨基端延长肽:22.53 ng/ml,血清β-胶原降解产物测定:0.122 ng/ml ,骨钙素:10.67 ng/ml。血常规、尿常规、血沉、肝功能、肾功能、血轻链、肿瘤标志物检查无明显异常。双能X线骨密度显示,椎体L1-4:0.429 g/cm3,T值:-5.6;左侧股骨颈:0.299 g/cm3,T值:-5.0;髋部:0.325 g/cm3,T值:-5.1。
放射线检查胸腰段正侧位片:胸8、10、12椎体压缩性骨折,胸腰段椎体骨质疏松;胸椎核磁共振检查:胸8、10、12椎体压缩改变,退行性变。详见图1。
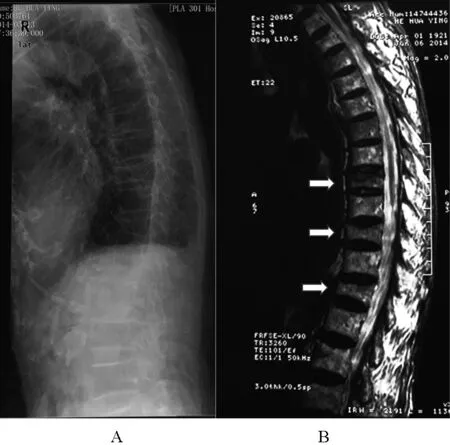
图1 患者治疗前影像Figure 1 Image before treatmentA: X-ray; B: magnetic resonance
临床诊断严重骨质疏松症,多发椎体压缩性骨折(T8、T10、T12)。
治疗与转归口服碳酸钙D3片0.6 g 1次/d、骨化三醇胶丸0.25 μg 1次/d。自2016年5月25日起,使用特立帕肽注射液,20 μg,1次/d皮下注射治疗,直至2017年10月11日停用(共约17个月)。患者于特立帕肽治疗期间,无新发骨折,腰背部疼痛明显减轻,股骨颈骨密度较基础增加23.1%,髋关节总和骨密度较基础增加36.9%,椎骨骨密度较基础增加12.4%,监测血钙、尿钙无升高。自2017年11月29日起调整为阿仑膦酸钠片70 mg, 1次/周,序贯治疗无再发骨折。治疗1年后复查股骨颈、髋关节总和骨密度,虽较特立帕肽治疗结束前下降,但分别较基础值增加3.7%和26.2%,而椎骨骨密度于特立帕肽治疗后进一步增高6.4%,较基础值增加19.8%。治疗前后骨代谢变化见图2,骨密度变化见图3。
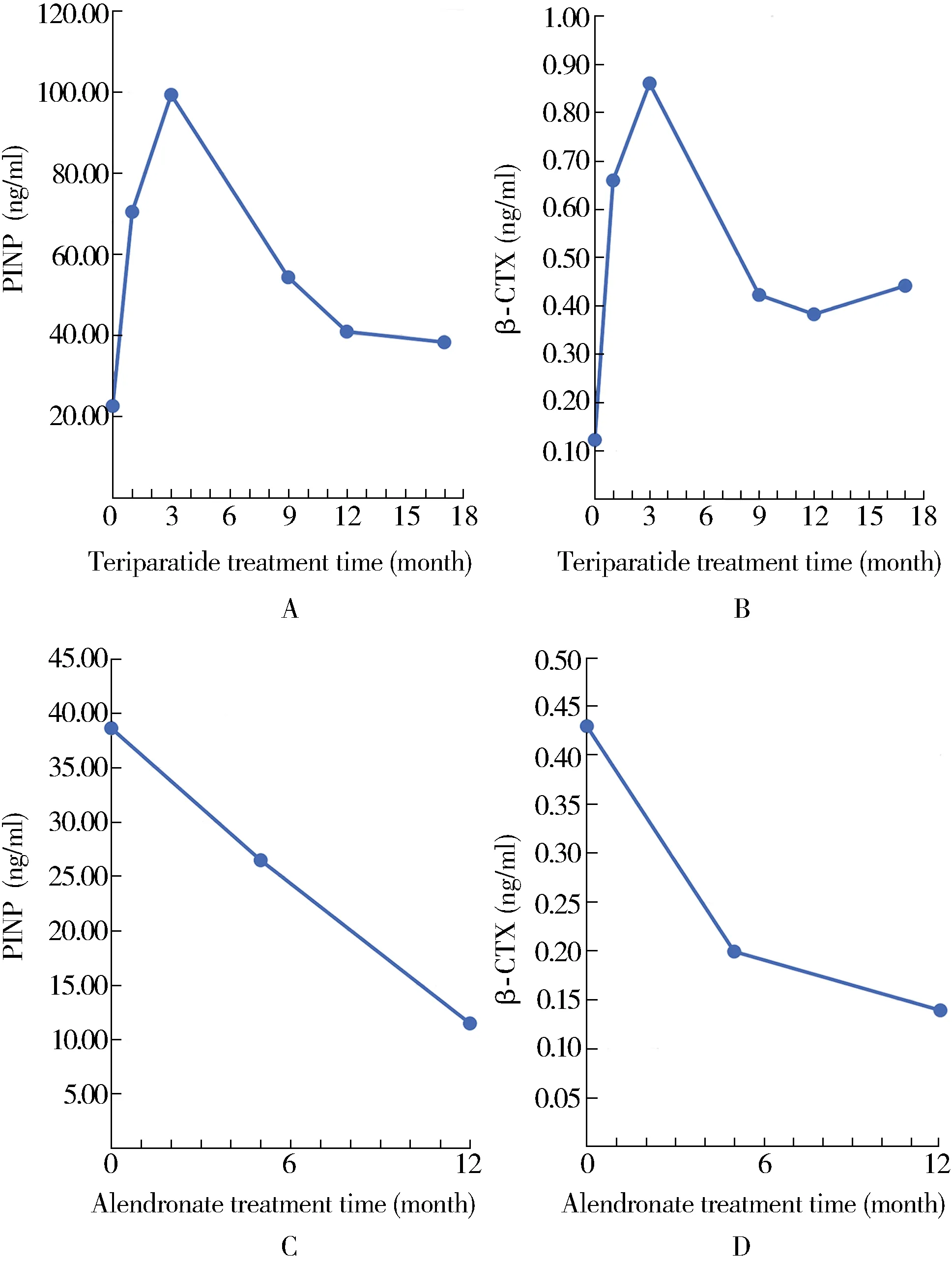
图2 治疗前后骨代谢指标的变化Figure 2 Changes in bone metabolism indexes before and after treatmentA: changes in PINP after teriparatide treatment;B: changes in β-CTX after teriparatide treatment;C: changes in PINP after alendronate treatment; D: changes in β-CTX after alendronate treatment P1NP: amino-terminal propeptide of type I procollagen; β-CTX: β-collagen degradation products.
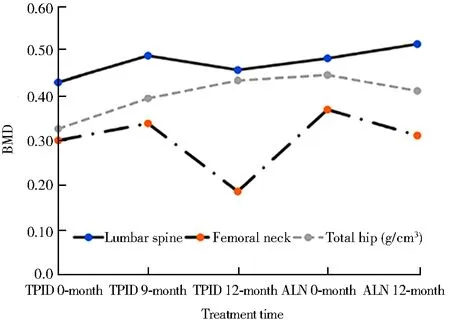
图3 治疗前后骨密度的变化Figure 3 Changes in bone mineral density before and after treatmentBMD: bone mineral density; TPTD: teriparatide; ALN: alendronate.
2 讨 论
骨质疏松症是一种与增龄相关的疾病。目前双磷酸盐制剂为各大指南推荐的一线抗骨质疏松药物。但对于以下特殊人群[1-3],如绝经后女性多次发生骨质疏松性椎体骨折或髋部骨折,65岁女性患有椎体骨折史且骨密度(bone mine-ral density,BMD) 2.5,尚未骨折,但BMD≤3.5且有骨折高危因素,既往抗骨质药物治疗无效或不耐受,众多指南更倾向于初始选择促骨形成药物——甲状旁腺激素(parathyroid hormone,PTH)及其类似物。
特立帕肽是第一个合成代谢类的药物,至今已超过40年。多个临床试验显示,其可显著改善患者背痛,增加骨密度,降低绝经后女性、老年男性、糖皮质激素相关的骨质疏松性椎体和非椎体骨折的风险。
在骨折预防试验中,1 637例既往有椎骨骨折的绝经后女性,随机分配至接受PTH(20或40 μg/d,皮下给药)或安慰剂治疗[4]。18个月后,相较于安慰剂组,20、40 μg治疗组患者腰椎BMD分别增加了9%、13%,股骨颈的BMD分别增加了3%、6%,减少1个或多个新发椎体骨折风险65%、69%,≥2次骨折风险77%、86%,降低至少1个中等或严重椎体骨折风险90%、78%,非椎体骨折风险35%、40%。而在使用类似分析的研究显示,阿仑膦酸钠(10 mg/d)降低新发椎体骨折风险48%,利塞膦酸钠(5 mg/d)降低41%,雷洛昔芬(60 mg/d)降低30%。
欧洲Forseto观察性研究[5](European Forsteo Observational Study,EFOS)纳入1 648例患者,其平均年龄为71.5岁,平均腰椎骨密度T值为-3.3 SD,既往平均骨折次数为2.9次。结果显示,应用特立帕肽18个月后,背痛显著改善,生活质量明显好转。
最常见的不良事件是高钙血症和高钙尿症。通常经过减少补钙和(或)暂停维生素D治疗,可使其得到缓解,必要时可调整PTH至隔日1次。在动物实验中,大剂量、长时间使用特立帕肽增加大鼠骨肉瘤的发生率,虽然在美国上市后7年的骨肉瘤监测研究中,未发现特立帕肽和人骨肉瘤存在因果关系,但美国FDA仍推荐其疗程不宜超过24个月。
PTH及其类似物抗骨质疏松性骨折疗效确切,但由于费用较高、需要每天皮下注射、存在长期应用的安全顾虑,因此,目前主要推荐应用于严重骨质疏松及常规抗骨质疏松治疗效果欠佳人群。
2016年一项回顾性研究分析了628例应用特立帕肽20 μg,1次/d,治疗2年的患者,根据年龄是否≥80岁,将其分为2组[6]。结果显示,年长组和相对年轻组在腰椎及股骨颈骨密度的增幅及耐受性方面,没有差异;提示特立帕肽的获益与年龄无关,不良反应不会随着年龄的增长而增加,为其应用于老年骨质疏松患者提供了有力的证据。
此外,随着近年对骨代谢研究的深入,对骨质疏松症核心病理生理机制的认识加深,Lippuner[7]提出新的治疗策略。建议在疾病的早期,应用促骨形成药物以最大程度地增加骨量、保持完整的骨微结构,后续应用骨吸收抑制剂来保持所获得的收益,以逆转骨质疏松症。
鉴于特立帕肽卓越的抗骨折疗效,且不受年龄及患者病情复杂程度的限制,以及起效快速,本病例中起始治疗选用该药。患者的临床反应与预期一致,用药1个月后症状好转,骨代谢指标提示骨形成显著增加,3个月后症状进一步减轻,18个月后症状显著改善,椎骨、股骨颈、髋部骨密度明显增加,未再新发骨折。停止PTH后,为维持其治疗所获得的BMD,建议应用抗骨吸收类药物,优选双膦酸盐。本病例序贯应用阿仑膦酸钠1年后,椎骨骨密度较特立帕肽治疗后进一步增高6.4%,较基础值增加19.8%。
本病例提示,对于重度骨质疏松的老年患者,早期应用特立帕肽,序贯阿仑膦酸钠治疗,可快速、有效地改善患者临床症状,增加椎体和髋部骨量,避免新发骨折。治疗期间患者耐受性良好,未见明显不良反应,血钙、尿钙无升高,安全性可。治疗过程中,骨密度曾有一过性下降,考虑为新骨形成、矿化不足可能性大。后续期待更大样本量研究,进一步验证此策略的可行性。

