阻塞性睡眠呼吸暂停低通气综合征严重程度与脑白质病变的相关性
杨 帆,刘日红,梁春艳,姚碧波
(湖南省胸科医院a.综合门诊; b.内二科,长沙 410006)
阻塞性睡眠呼吸暂停低通气综合征(obstructive sleep apnea hypopnea syndrome,OSAHS)是一种常见的睡眠呼吸紊乱疾病,其特点是睡眠过程中反复出现口鼻气流消失或明显减弱,并伴有日间嗜睡、疲乏无力等症状。我国的流行病学调查[1]显示,OSAHS患者发病率为2%~4%,男性高于女性,且随年龄增长,发病率呈逐渐增高趋势。OSAHS患者睡眠状态下反复出现呼吸暂停和低通气,使机体处于慢性间歇低氧的特殊内环境,进而对全身多个系统造成损害[2]。脑白质是中枢神经系统的重要组成部分,是神经纤维聚集的地方,脑白质中的中枢神经细胞的髓鞘损害,则会引起脑白质病变(white matter lesions,WML)。WML可由多种疾病导致,临床可见视觉、运动、感觉、小脑、自主神经及认知功能障碍等[3]。近年来的研究[4]显示OSAHS是导致WML的独立危险因素,但是其机制尚不明确。基于此,本研究探讨OSAHS严重程度与WML的相关性,以期为临床提供参考。
1 资料与方法
1.1 一般资料
以2019年1—12月湖南省胸科医院收治的150例OSAHS患者为研究对象。病例纳入标准:1)符合《阻塞性睡眠呼吸暂停低通气综合征诊治指南(基层版)》[5]中关于OSAHS的相关诊断标准;2)年龄≥18岁;3)行脑部MRI检查及多导睡眠呼吸监测(≥7 h),且资料完整;4)依从性较好。病例排除标准:1)由其他因素导致的WML;2)伴有其他中枢神经系统疾病、脑部肿瘤等;3)长期服用镇静催眠类药物、饮酒;4)精神异常;5)孕妇及哺乳期妇女。
按照呼吸暂停低通气指数(apnea hypopnea index,AHI)将150例OSAHS患者分为轻度组(AHI为5~15次·h-1)、中度组(AHI为16~30 次·h-1)和重度组(AHI>30次·h-1)。轻度组患者42例,其中男30例,女12例,年龄(49.52±10.11)岁;中度组患者50例,其中男35例,女15例,年龄(51.38±11.60)岁;重度组患者58例,其中男40例,女18例,年龄(53.77±12.81)岁。3组患者的性别、年龄比较差异均无统计学意义(P>0.05)。
1.2 研究方法
1.2.1 临床资料的收集
收集患者的性别、年龄、身高、体重、体重指数(body mass index,BMI)、基础疾病等。
1.2.2 蒙特利尔认知评估量表评分
蒙特利尔认知评估量表(Montreal cognitive assessment,MoCA)由执行与视觉空间功能、命名、记忆、注意力、语言表达能力、抽象思维和定向力12道题组成,共30个单项,答对得1分,答错得0分。总分为30分,≥26分为认知正常。
1.2.3 多导睡眠呼吸监测
于夜间安静条件下使用美国SW-SM2000CB便携式多导睡眠仪(德国万曼,型号:SOMNOlab)对患者进行多导睡眠呼吸监测,监测时间不少于7 h。监测当天嘱咐患者不要饮用含咖啡因的饮料、不喝酒、避免剧烈运动、保持平静心态,以免造成大脑兴奋,影响监测。记录最低血氧饱和度(lowest oxygen saturation,LsaO2)、血氧饱和度<90%时间(SaO2<90% time/total sleep time,TSTSaO2<90%)及不同睡眠体位下AHI。
1.2.4 WML的MRI诊断
采用常规序列及垂直于双侧海马的液体衰减反转恢复序列(fluid attenuated inversion recovery,FIAIR)进行MRI成像。WML定义为在FLAIR序列脑白质区呈高信号的点状或斑块状病变,边缘模糊,常两侧对称分布,常累及脑室旁、放射冠和半卵圆中心。采用Fazekas标准评估WML。在脑室周围,WML:脑室旁的线状或脑室脚的帽状病变,或已进入深部白质区;在深部白质区域,WML:单个病变或成组病变直径>3 mm。
1.3 统计学方法

2 结果
2.1 3组LsaO2、TSTSaO2<90%、BMI、MoCA评分和不同睡眠体位下AHI的比较
重度组LsaO2、MoCA评分均明显低于中度组与轻度组(P<0.05),中度组LsaO2、MoCA评分明显低于轻度组(P<0.05);重度组TSTSaO2<90%、BMI均明显高于中度组与轻度组(P<0.05),中度组TSTSaO2<90%、BMI均明显高于轻度组(P<0.05)。见表1。
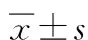
表1 3组LsaO2、TSTSaO2<90%、BMI和MoCA评分的比较
重度组的左侧卧位、右侧卧位及仰卧位AHI均明显高于中度组与轻度组(P<0.05),中度组的左侧卧位、右侧卧位及仰卧位AHI均明显高于轻度组(P<0.05);3组的仰卧位AHI均明显高于左侧卧位及右侧卧位AHI(P<0.05),3组的左侧卧位AHI与右侧卧位AHI比较差异均无统计学意义(P>0.05)。见表2。
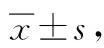
表2 3组不同睡眠体位下AHI的比较 次·h-1
2.2 3组WML发生率的比较
轻度组患者中发生WML 24例(57.14%)、中度组患者中发生WML 36例(72.00%)、重度组患者中发生WML 50例(86.21%),WML发生率随着OSAHS严重程度的增加而增高,3组之间比较差异有统计学意义(P<0.05)。
2.3 WML的独立危险因素分析
以年龄、性别(男为1,女为2)、OSAHS(是为1,否为0)、高血压(是为1,否为0)、糖尿病(是为1,否为0)、高血脂(是为1,否为0)为自变量,以WML(是为1,否为0)为因变量进行二分类logistic回归分析,结果显示:年龄(OR=7.748,95%CI:1.047~1.362,P=0.000)、OSAHS(OR=9.195,95%CI:3.753~28.566,P=0.000)为WML的独立危险因素。见表3。
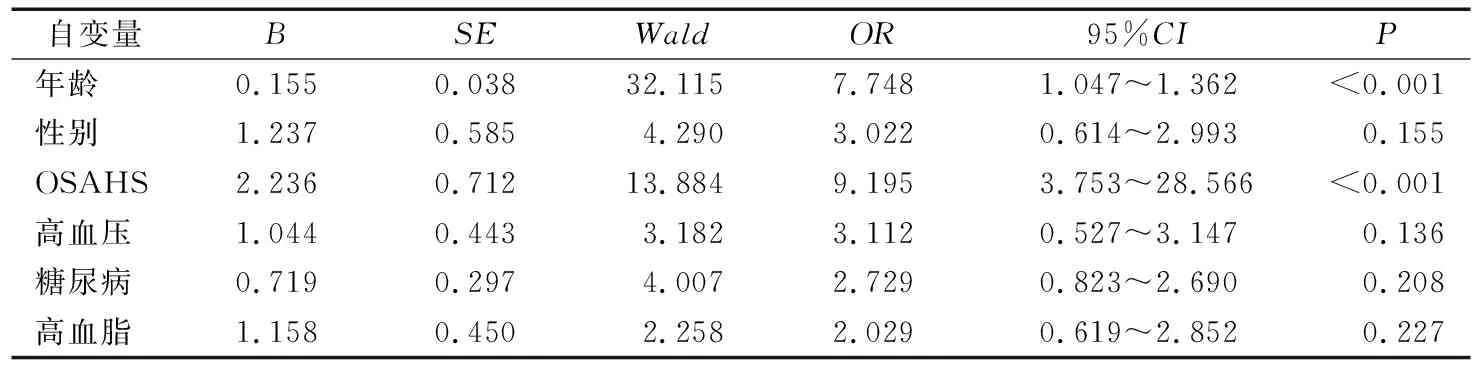
表3 WML独立危险因素的二分类logistic回归分析
2.4 OSAHS严重程度影响因素与WML的相关性分析
Spearman相关系数分析显示:TSTSaO2<90%(r=0.199,P=0.036)、仰卧位AHI(r=0.257,P=0.003)与WML呈明显正相关;MoCA评分(r=-0.248,P=0.010)与WML呈明显负相关;LsaO2、左侧卧位AHI、右侧卧位AHI与WML无明显相关性。见表4。

表4 OSAHS严重程度影响因素与WML的Spearman相关系数分析
3 讨论
OSAHS的直接发病机制是上气道的狭窄和阻塞,但其发病并非简单的气道阻塞,而是上气道塌陷伴呼吸中枢神经调节因素障碍。OSAHS的不良通气状态导致患者在夜间的睡眠分散,而在白天出现过度嗜睡,明显地降低了患者的生活质量与工作效率。这种不良通气状态还能够造成脑部间歇性的低氧血症,若低氧血症得不到改善则会导致大脑的脑白质损伤,造成认知功能障碍,严重影响患者的身心健康[6-7]。
脑白质是大脑内部神经纤维聚集的地方,由于其区域比细胞体聚集的大脑表层颜色浅,故名脑白质。软脑膜动脉微小分支血管是深部脑白质的血液供应路径,因为没有侧支循环的有效支持,血压变化比较容易影响这些微小分支血管[8]。由于OSAHS患者在睡眠过程中会反复出现低氧血症和血压波动,导致脑部的血流量减少及发生间歇性缺氧,从而导致脑部急慢性的缺血性改变,而这些改变导致这些深小动脉发生玻璃样变性以及硬化,使得轴突、髓鞘和细胞膜的完整性受到破坏,造成脑白质发生纤维化及脱髓鞘改变[9-10],即WML。
AHI与LsaO2能够反映OSAHS患者的睡眠呼吸障碍以及血氧降低程度,是评估OSAHS病情的2个重要临床指标。OSAHS最直接的生理反应是血氧下降,而肥胖在生理结构上能够导致咽部气道可塌陷性地加重。本研究结果显示,LsaO2随着OSAHS的加重而降低,TSTSaO2<90%、BMI、WML发生率均随着OSAHS的加重而增高。分析原因是,在低氧状态下OSAHS患者的心率、血压及通气指标等会增高,交感神经受到外周化学感受器的激活而兴奋,从而增强了通气反应与血流动力学[11]。这一系列反应会引起机体产生炎症反应。低血氧能够直接调节黏附分子的表达,对动脉粥样硬化发生与发展起到促进作用[12],而有研究[13]显示,颈部动脉的斑块形成以及粥样硬化,能够导致脑WML的体积变大;也有研究[14]显示,动脉粥样硬化等加重能够减少脑白质的灌注,造成脑白质发生缺血,破坏轴突细胞膜及髓鞘完整性,发生脱髓鞘改变。低氧状态的持续时间越长,会导致血管收缩、内分泌紊乱、神经调节功能失调等,从而导致WML发病率增加[15]。目前认为OSAHS患者睡眠体位发生改变造成患者的呼吸紊乱程度出现变化,是由于患者的上气道形态学发生了改变[16]。OSAHS患者在夜间睡眠过程中处于仰卧位时,咽腔前壁的组织及舌骨会向咽后壁发生移位,导致咽腔变得更加狭窄;而当患者睡眠过程中处于侧卧位时,仰卧位时的不利因素会得到减轻或消失,咽腔扩大,患者的气道阻塞程度得到减轻,通气情况得到改善[17]。这与本研究中不同睡眠体位下AHI随着OSAHS的加重而增高、不同严重程度OSAHS患者仰卧位AHI均明显高于左侧卧位及右侧卧位AHI的结果相符。WML与MoCA评分存在明显负相关性,脑白质病变与认知功能障碍密切相关,脑白质病变出现的认知损害主要表现在视觉空间与执行功能、延迟记忆、计算力和注意力等方面,尤其是执行功能,且脑白质病变病变程度越严重,其执行功能受损也越显著。本研究中,TSTSaO2<90%与WML存在明显相关性,LsaO2、BMI与WML的相关性不明显。造成这一原因可能与研究人群有关,还需要进一步研究。
综上所述,WML发生率随着OSAHS的加重而增加,WML与TSTSaO2<90%、仰卧位AHI存在明显正相关,与MoCA评分存在明显负相关。

