恩诺沙星乳在罗非鱼体内的药代动力学及组织分布
朱晓漫,刘永涛,杨秋红,胥 宁,刘绍春,董 靖,宋 怿,艾晓辉
(1.上海海洋大学水产与生命学院,上海 201306;2.中国水产科学研究院长江水产研究所,武汉 430223;3.中国水产科学研究院 农业农村部水产品质量安全控制重点实验室,武汉 430223;4.岳阳渔美康生物科技有限公司,湖南岳阳 414199)
恩诺沙星(enrofloxacin,ENR)是一种氟喹诺酮类动物专用抗菌药,具有广谱杀菌性,在养殖鱼类中被广泛应用于由嗜水气单胞菌(Aeromonashydrophila)[1]、大肠杆菌(Escherichiacoli)、维氏气单胞菌(Aeromonasveronii)[2]及粘球菌(Myxococcuspiscicola)[3]等引起的病症,其代谢产物为环丙沙星(ciprofloxacin,CIP)。国内外已有较多有关恩诺沙星在水生动物体内药代动力学方面的研究报道,Koc等[4]分析了口服和静脉给药10 mg/kg恩诺沙星在褐鳟体内的药代动力学,达峰时间(Tmax)为8 h,峰浓度(Cmax)为(2.30±0.08)μg/mL;Zhai等[5]研究了恩诺沙星在脊尾白虾体内的药代动力学;Kim等[6]研究了恩诺沙星在鲶体内的药代动力学。施建中[7]、徐维海等[8]研究了恩诺沙星在罗非鱼体内的残留消除规律,但恩诺沙星在罗非鱼(Oreochromsmossambcus)体内的药代动力学研究尚未见报道;恩诺沙星乳作为一种近年来开发的新剂型,国内外尚未展开其在水产动物体内的药代动力学研究。罗非鱼是联合国粮农组织推广养殖的品种之一,为我国重要的出口创汇水产品,无乳链球菌病是危害罗非鱼最严重的疾病之一,该菌在罗非鱼脑组织中分布量较多,因常规抗菌药物难以穿透血脑屏障,目前尚无好的防治药物[9]。本试验采用本实验室研制的恩诺沙星乳新剂型,研究了口灌给药方式下恩诺沙星乳在罗非鱼体内的药代动力学及其在各组织的分布规律,旨在为罗非鱼养殖过程中合理使用恩诺沙星乳提供理论指导。
1 材料与方法
1.1 实验材料
1.1.1 试验用鱼与养殖条件
健康罗非鱼96尾,由中国水产科学研究院长江水产研究所基地提供,平均体重为(100±20)g。试验前在玻璃水族箱(规格为1 m×0.6 m,水深0.5 m)中暂养一周。试验用水为充分曝气自来水,养殖和试验过程中水体持续充氧,保持水中溶氧大于 5.0 mg/L,pH为7.5~8.0,温度恒定在(30±1)℃。
1.1.2 仪器设备
实验中使用的主要仪器包括:Waters Acquity超高效液相色谱仪(Binary Solvent Manager、 Sample Manager、 FLR Detector、 配Empower色谱工作站,美国Waters公司);精密电子天平(AE-240, METTLE-TOLEDO公司);高速冷冻离心机; 氮吹仪(KD200,杭州奥盛仪器有限公司);浓配罐(100L,宜兴市江益环保有限公司);涡旋混合器(HQ-60-IV,北方同正);超声波清洗器(KQ2200DE,昆山市超声仪器有限公司)等。
1.1.3 药品与试剂
恩诺沙星标准品(纯度>99.0%,Dr.Ehrenstorfer GmbH),环丙沙星标准品(纯度>95.0%,Dr.Ehrenstorfer GmbH),恩诺沙星乳(无色至淡黄色液体,规格5 g:100 mL,恩诺沙星乳滴呈球形,平均粒径为(18.23±5.022) nm,山东鲁抗医药股份有限公司GMP车间中试生产,批号:1711001),乙腈、正己烷、水(色谱纯,美国CNW公司),甲酸(分析纯,国药集团化学试剂有限公司)无水硫酸镁(分析纯,国药集团化学试剂有限公司),肝素钠(源叶生物)。
1.2 实验方法
1.2.1 恩诺沙星乳药液的配制
首先将表面活性剂聚氧乙烯蓖麻油-40和助表面活性剂乙酸在浓配罐内搅拌混匀,然后加入油相肉豆蔻酸异丙酯和恩诺沙星原药,继续搅拌混匀,最后加入去离子水,继续搅拌直至体系变得澄澈透明,即形成恩诺沙星乳剂。制备出的恩诺沙星乳质量浓度为5%,用蒸馏水将恩诺沙星乳稀释10倍,所得药液的恩诺沙星含量为5 mg/mL。
1.2.2 口灌给药和样品采集
罗非鱼开始实验前停食24 h,随机抽取6尾作为空白对照,确定空白样品无恩诺沙星和环丙沙星残留后,以10 mg/kg 剂量对罗非鱼单次口灌恩诺沙星乳。分别在给药后的0.5、1、2、4、6、8、12、18、24、48、72、96、120、144、168 h采集血浆(抽取血液转移至1%肝素钠处理的离心管,轻轻转动离心管后4 000 r/min离心5 min,取上清),同时采集肌肉、肝脏、肾脏和脑组织,每个采样点设定6尾鱼为平行样,-20 ℃贮存待测。
1.2.3 样品前处理
在室温下,将冷冻样品自然解冻。准确量取血浆0.5 mL于10 mL离心管中,加入4 mL酸化乙腈(乙腈 ∶盐酸 ∶水=250 ∶1 ∶1),涡旋震荡30 s,加入0.5 g无水硫酸镁,涡旋震荡30 s,7 000 r/min离心5 min,取上清液于另一10 mL离心管中。剩余残渣再加入4 mL酸化乙腈,重复提取一遍,合并上清液。50 ℃氮气吹干,1 mL流动相(0.2%甲酸水∶乙腈=82∶18)复溶,加入1 mL 正己烷旋涡混合30 s去脂,7 000 r/min离心5 min,取1 mL下层溶液过0.22 μm有机滤膜,供超高效液相色谱仪分析测定[10]。
称取肌肉和肝脏样品1 g,以及全部的肾脏和脑组织样品于15 mL离心管中,加入6 mL酸化乙腈(乙腈∶盐酸∶水=250∶1∶1),涡旋震荡30 s,加入0.5 g无水硫酸镁,涡旋震荡30 s,7 000 r/min离心5 min,取上清液于10 mL离心管中。剩余残渣再加入6 mL酸化乙腈,重复提取一遍,合并上清液。50 ℃氮气吹干,2 mL流动相复溶,加入2 mL 正己烷旋涡混合30 s去脂,7 000 r/min离心5 min,取1 mL下层溶液过0.22 μm有机滤膜,供超高效液相色谱仪分析测定[10]。
1.3 色谱条件
色谱柱:ACQUITY UPLCTM BEH C18色谱柱(50 mm×2.1 mm,17 μm),柱温30 ℃;流动相:0.2%甲酸水(0.2%甲酸+99.8%水)∶乙腈=82∶18,流速0.3 mL/min;激发波长280 nm,发射波长450 nm;进样量:3 μL。
1.4 标准溶液的配制和标准曲线的制备
精确称取恩诺沙星、环丙沙星各10 mg,分别用乙腈溶解后定容至100 mL,配制成浓度为100 μg/mL的恩诺沙星和环丙沙星的标准品母液,4 ℃避光保存备用。用流动相将恩诺沙星和环丙沙星标准品母液依次稀释至10、50、100、500、1 000、2 000 μg/L,用超高效液相色谱检测。以标准品浓度作为横坐标(X轴)、峰面积为纵坐标(Y轴)绘制标准曲线,计算回归方程及相关系数。
1.5 方法回收率与检测限
取罗非鱼各组织的空白样品,分别加入10、50、100 μg/kg恩诺沙星和环丙沙星标准品,放置30 min,以“样品前处理”方法进行处理后进行超高效液相色谱检测,每个浓度3个平行,得到样品实测浓度,计算回收率和相对标准偏差(RSD)。以引起3倍基线噪音的药量的质量浓度作为最低检测限。
1.6 数据处理
标准曲线以及恩诺沙星、环丙沙星的药-时曲线用Microsoft Excel 2010进行计算和绘制;采用WinNonlin软件进行恩诺沙星和环丙沙星的药代动力学分析。
2 结果
2.1 标准曲线与方法回收率
在本实验方法条件下,恩诺沙星和环丙沙星在10~2000 μg/L的浓度范围内具有良好的线性关系,以 恩诺沙星和环丙沙星峰面积为纵坐标(Y轴),以化合物的质量浓度为横坐标(X轴),绘制得到的标准曲线方程分别为Y=2283.1X+5504.5和Y=1268.3X+5132.6,相关系数R2均大于0.999。在本实验条件下,恩诺沙星和环丙沙星最低检测限为2 μg/L,定量限为10 μg/L。如表1所示,恩诺沙星和环丙沙星在各组织中的平均回收率为75.21%~108.77%,RSD<10%,满足分析方法要求。

表1 恩诺沙星和环丙沙星在罗非鱼各组织中的回收率
2.2 恩诺沙星乳在罗非鱼血浆中的药代动力学特征
所得恩诺沙星乳在罗非鱼各组织中的药代动力学参数见表2。结果显示:血浆中恩诺沙星在2 h的药物峰浓度Cmax为4.38 mg/L、消除速率常数ke值为0.02 h-1、药时曲线下面积AUC为106.11(mg/L)·h;血浆中环丙沙星在8 h的Cmax为0.1 mg/L、ke值为0.01 h-1、药时曲线下面积AUC为5.35(mg/L)·h。

表2 罗非鱼单次口灌恩诺沙星乳后血浆中恩诺沙星和环丙沙星的药代动力学参数
2.3 恩诺沙星乳在罗非鱼脑、肌肉、肝脏和肾脏中的吸收与分布
如图1所示,单次口灌10 mg/kg恩诺沙星乳后,恩诺沙星在脑中的代谢规律与血浆基本一致,在给药结束后2 h含量到达峰值4.38 mg/L(血浆)、4.31 mg/kg(脑),随后在2~24 h内浓度迅速下降,24 h之后下降速率减缓,72 h后趋于平稳。肌肉中的恩诺沙星略高于血浆和脑,在给药结束后4 h含量到达峰值6.22 mg/kg。肝脏中,恩诺沙星在给药结束后1 h药物浓度到达峰值12.37 mg/kg,高于其他组织,之后在24 h内恩诺沙星浓度迅速下降但仍保持一个较高的浓度水平,达到3.0 mg/kg以上。肾脏中的恩诺沙星浓度达峰时间较其他组织晚,在6 h到达峰值7.82 mg/kg,6 h之后组织中药物浓度下降速率也比其他组织平缓,且之后各时间点的浓度均高于其他组织。
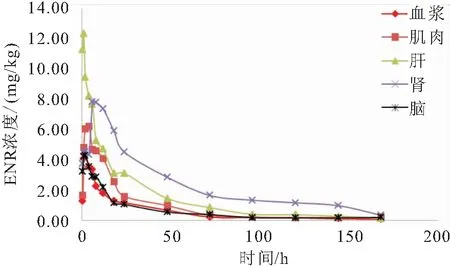
图1 单次口灌10 mg/kg恩诺沙星乳在罗非鱼各组织的药-时曲线
罗非鱼单次口灌10 mg/kg 恩诺沙星乳后,各组织中恩诺沙星的消除方程及参数见表3。各组织中恩诺沙星的消除半衰期T1/2为肾﹥脑﹥肌肉﹥肝、药物平均驻留时间MRT为肾﹥脑﹥肝﹥肌肉、药时曲线下面积AUC为肾﹥肝﹥肌肉﹥脑。

表3 罗非鱼单次口灌恩诺沙星乳后各组织的消除方程及参数
2.4 环丙沙星在罗非鱼体内的分布
通过检测环丙沙星和恩诺沙星在罗非鱼体内的含量,对数据进行统计和分析发现,血浆中环丙沙星占恩诺沙星的百分比约为4.68%、肌肉中约为3.97%、肝脏中约为6.03%、肾脏中约为3.22%。环丙沙星在血浆、肌肉、肝和肾中有检出,Tmax分别为8、6、4和6 h,Cmax分别为0.1 mg/L、0.39、0.15和0.23 mg/kg(见图2)。单剂量10 mg/kg口灌恩诺沙星后,其主要代谢物环丙沙星在罗非鱼各组织的分布为肝﹥肾﹥肌肉﹥血浆,与恩诺沙星在罗非鱼各组织中的分布情况一致。给药后168 h,血浆和肌肉中的环丙沙星下降到0.01 mg/kg以下,肝脏和肾脏中的环丙沙星下降到0.02 mg/kg以下。

图2 单次口灌10 mg/kg恩诺沙星乳后环丙沙星在罗非鱼体内的分布
罗非鱼单次口灌10 mg/kg 恩诺沙星乳后,其主要代谢产物环丙沙星的消除方程及参数见表4。各组织中环丙沙星的消除半衰期T1/2为肾﹥肝﹥肌肉、药物平均驻留时间MRT为肝﹥肾﹥肌肉、药时曲线下面积AUC为肾﹥肝﹥肌肉。

表4 单次口灌后罗非鱼各组织环丙沙星的消除方程及参数
3 讨论
3.1 恩诺沙星乳在罗非鱼体内的代谢规律
本实验条件下,恩诺沙星在罗非鱼血浆、肌肉、肝脏、肾脏和脑的Tmax分别为2、4、1、6和2 h,Cmax分别为4.38、6.22、12.37、7.82和4.31 mg/kg,AUC为106.11(mg/L)·h、159.02、250.42、392.71和103.14(mg/kg)·h。研究显示,单剂量口服或口灌10 mg/kg恩诺沙星,鲫血浆在0.5 h的Cmax为3.55 mg/L[11];大黄鱼血浆在7.67 h的Cmax为3.59 mg/L[12]。恩诺沙星乳在罗非鱼血浆中的药物峰浓度均高于鲫和大黄鱼,罗非鱼对恩诺沙星的吸收速度比大黄鱼快,比鲫慢。恩诺沙星在罗非鱼肝脏中最快达到药物峰浓度,且峰浓度最高,这可能是由于肝脏中含有多种药物代谢酶,是鱼类药物和毒物代谢的最主要器官。恩诺沙星在罗非鱼肾脏中消除最慢、T1/2和MRT最长、AUC最大,药物浓度在到达峰值之后就一直高于其他组织,恩诺沙星总吸收量最高,这是因为在恩诺沙星不断经过肾脏随着尿液排出的过程,其他组织中的一部分恩诺沙星会被运输到肾脏,从而导致恩诺沙星在肾脏中的蓄积。由此可见,肝脏和肾脏是罗非鱼代谢恩诺沙星的主要器官,对于恩诺沙星在罗非鱼体内的代谢和消除具有重要作用。恩诺沙星在脑组织中总吸收量较低,但T1/2和MRT都比较长,说明其在脑组织比在其他组织难代谢和消除,这可能是因为脑作为一个高度分化的器官,其中代谢药物的酶较少。
3.2 恩诺沙星的主要代谢产物环丙沙星在罗非鱼体内的代谢规律
恩诺沙星在鱼体内的主要代谢产物是环丙沙星,环丙沙星在罗非鱼血浆、肌肉、肝脏和肾脏的Tmax为8、6、4和6 h,Cmax为0.1 mg/L、0.39、0.15和0.23 mg/kg,AUC为5.35(mg/L)·h、6.5、14.99和15.83(mg/kg)·h。由数据可知,环丙沙星在血浆中的吸收和消除都比恩诺沙星慢,且浓度远低于恩诺沙星。在水产动物体内,大部分恩诺沙星都以原药形式代谢出体外[13]。本实验中环丙沙星在罗非鱼血浆、肌肉、肝和肾中含量占恩诺沙星的比例分别为4.68%、3.97%、6.03%、3.22%,说明恩诺沙星在罗非鱼体内很少代谢。肝脏中环丙沙星含量最高,一方面是因为罗非鱼给药后恩诺沙星肝脏中的浓度最高,另一方面也说明恩诺沙星主要在肝脏中脱乙基代谢成环丙沙星,这与大部分水产动物体内恩诺沙星的代谢规律相一致[14,15]。在脑组织中未检测到环丙沙星,说明脑组织基本不代谢恩诺沙星。环丙沙星在罗非鱼的肝、肾和肌肉组织中的T1/2和MRT都较大,表明环丙沙星在罗非鱼各组织的消除普遍较慢,滞留时间长。除此之外,各组织的环丙沙星在达峰时间之后都两次或多次出现含量降低、升高再降低的现象。这可能是由于恩诺沙星代谢环丙沙星后的肝肠循环产生的,鱼体中将恩诺沙星代谢成环丙沙星的主要器官是肝脏,恩诺沙星脱乙基后形成的环丙沙星由肝脏排出后进入肠道,组织对其产生了代谢后的再吸收。恩诺沙星和环丙沙星两种药物的双重代谢,造成了峰值时间后环丙沙星药物浓度的波动,在很多水产动物中,环丙沙星都呈现出这一规律[16-18]。
3.3 恩诺沙星乳的优越性
本研究所用的恩诺沙星乳新剂型,具有溶解度好、易吸收、抗菌活性强、与普通的恩诺沙星粉剂相比,其抑菌作用提升了1倍[19]。有研究表明,罗非鱼单次口灌40 mg/kg鱼体重恩诺沙星普通剂型,血浆中恩诺沙星在1 h的Cmax为3.47 mg/L[7]。本研究中,罗非鱼单次口灌10 mg/kg鱼体重恩诺沙星乳后,2 h的Cmax为4.38 mg/L,给药浓度是上述研究的四分之一,血药浓度峰值却高于3.47 mg/L,说明恩诺沙星乳新剂型促进了罗非鱼对药物的吸收,提高了生物利用度。封琦等[20]的研究也指出同一药物不同剂型在同一物种中的药代动力学特征也会有所不同。恩诺沙星乳纳米粒子粒径为纳米级,纳米粒子的重要特征是具有靶向作用,能够突破血脑屏障进入脑组织发挥作用[21]。由于血脑屏障的作用,所有大分子药物和98%的小分子药物都不能进入脑组织,很多神经性疾病不能被有效治疗[22]。据报道,β-内酰胺类抗菌药物中的第三、四代头孢类菌素药物的血脑屏障通透率仅为5%~15%[23];罗非鱼单次口灌10 mg/kg 恩诺沙星乳后,恩诺沙星在脑组织和血浆中的分布见图1,药物峰浓度分别为4.31 mg/kg 和4.38 mg/L,两者浓度差异不大,证实了恩诺沙星乳具有极高的血脑屏障透过性,完全突破了血脑屏障,可用于治疗鱼类中枢神经系统因细菌感染的疾病。
3.4 恩诺沙星乳的给药方案探讨
恩诺沙星对大多数水产动物致病病原菌的MIC均较小,如链球菌属(0.25~0.45 mg/L)[24]。根据邴晓菲等[25]以及曾苏[26]的研究,Cmax/MIC﹥8时,临床有效率可达90%。本实验中血浆中的恩诺沙星的Cmax=4.38 mg/L,脑组织中的Cmax=4.31 mg/L,其他组织的药物浓度均大于血浆和脑组织,可以满足绝大部分的水产动物疾病的治疗需要。以10 mg/kg单次给药恩诺沙星乳后,对MIC较高的链球菌(0.45 mg/L),血浆及各组织中有效药物浓度维持时间都在24 h以上。因此,对恩诺沙星敏感的病原菌所引起的疾病,可考虑单次给药10 mg/kg恩诺沙星乳,1日给药一次,连续给药3日。

