Al2O3掺杂对γ-C2S碳化性能的影响
明心昭,刘志超,王发洲,胡曙光,胡传林
(武汉理工大学,硅酸盐建筑材料国家重点实验室,武汉 430070)
0 引 言
硅酸二钙具有α、α′H、α′L、β和γ五种晶型[1],通常情况下,α-C2S、α′H-C2S、α′L-C2S、β-C2S在常温下都不能稳定存在,具有向γ-C2S转变的趋势,在β-C2S向γ-C2S晶型转变的过程中,由于Ca的配位数发生变化,引发约12%的体积膨胀,出现自粉化的现象[2]。β-C2S具有较高的水化活性,而γ-C2S几乎没有水化活性,因此在煅烧水泥熟料过程中采用急冷的方式来阻止β-C2S向γ-C2S的晶型转变。研究表明,γ-C2S在有水的情况下表现出较高的碳化活性[3-5],碳化反应速率是β-C2S的2倍[4],因此有学者利用γ-C2S高碳化活性的特点开展了许多研究工作。
现有研究大多利用化学纯试剂在实验室条件下制备得到γ-C2S,用于解析碳化反应动力学、碳化产物以及碳化体力学性能等[6]。为了进一步推广其应用,有学者利用石灰石、砂岩和铁矿等工业原料制备以γ-C2S为主要矿相的自粉化低钙水泥[7],并且不可避免地引入铝、铁、铬等杂质相,对C2S的晶型稳定性以及反应活性产生一定影响。目前,现有研究都集中于探究Al3+对β-C2S晶型稳定性的影响,相关研究[8-9]表明,Al3+可以稳定β-C2S晶型,防止熟料的粉化,但Feng等[10]以离子极化能力(C2/R,其中C表示离子电价,R表示离子半径)为判断依据,发现Al3+并不能阻止β-C2S向γ-C2S晶型转变。部分文献[11-13]也报道了Ba2+、V5+、Cr3+等离子对C2S晶型转变以及碳化活性的影响,但还未见Al2O3掺杂对γ-C2S碳化性能影响的报道。
本文通过研究不同Al2O3掺量对γ-C2S熟料的烧成与碳化性能(碳化放热、碳化体产物组成与力学性能等)的影响规律并分析作用机制,为γ-C2S的工业化制备提供技术支撑。
1 实 验
1.1 原材料
Ca(OH)2、SiO2和Al2O3均为分析纯试剂,由国药化学试剂集团有限公司提供。
1.2 样品的制备
设计4组不同Al2O3含量的γ-C2S水泥熟料,Ca(OH)2和SiO2摩尔比为2 ∶1,氧化铝掺量为Ca(OH)2和SiO2质量和的0%、2.32%、3.13%、3.94%,在1 400 ℃保温3 h煅烧得到,分别记为A0、A1、A2和A3。表1为A0~A3试样的原料配比。

表1 不同Al2O3掺量的γ-C2S原料化学组成Table 1 Chemical composition of raw materials for γ-C2S with different Al2O3 dosages
每组试样按照表1配制好后置于球磨罐中,然后称量物料质量80%的水倒入混料罐中并以250 r/min的转速混合3 h。将混好后的物料置于105 ℃的烘箱中烘干12 h,然后在高温炉中以5 ℃/min的速率升温到1 400 ℃保温3 h,烧结过后物料在炉内自然冷却,得到自粉化的γ-C2S熟料。通过乙二醇-乙醇法测得A0、A1、A2和A3的游离氧化钙低于0.145%(质量分数),表明生料易烧性良好。
1.3 试验方法
1.3.1 激光粒度仪测试
烧成熟料粉化后利用激光衍射粒度分析方法测试其粒径分布情况,选用英国马尔文公司生产的Mastersizer 2000激光粒度仪。应用理论为全量程完全的米氏理论,原理为当光线穿过物料时,反射光和透射光与物料粒径大小有关,根据入射光的偏离角度可以计算出粒径分布。累积分布曲线上50%处的对应粒径值为物料的D50,其可以表示熟料粒径大小。
1.3.2 碳化试样的制备及其碳化养护
按照0.15的水固比称取γ-C2S粉体和水溶液,将二者置于玛瑙研钵中搅拌均匀。称取12 g混合好的物料置于φ20 mm的模具中,成型压力为30 MPa,保压1 min,成型后的试样为尺寸φ20 mm×20 mm的圆柱体。将制备好的圆柱体试样放入不锈钢制的压力容器内进行碳化养护。碳化养护的条件参数为CO2浓度为100%,相对湿度RH≥95%,容器内相对压强为0.3 MPa,初始温度为室温,容器内通入CO2之前进行抽真空处理。
1.3.3 力学性能测试
利用美国MTS公司生产的CMT5105微机控制电子万能试验机对烧成熟料的碳化制品进行抗压强度测试,加载速率为1.2 mm/min。
1.3.4 矿物组成表征
通过对烧成熟料和碳化养护不同龄期的碳化制品进行X射线衍射测试,分析其矿物组成和非晶相的含量,仪器选择荷兰生产的Empyrean型X射线衍射仪(XRD)。熟料测试前需磨细,使其粒径都在74 μm以下(过200目方孔筛),扫描角度为5°~70°,步长为0.02°,仅做定性分析时的扫描速度为10(°)/min,做定量分析时的扫描速度为2(°)/min,同时在物料里面掺加质量分数为10%的α-Al2O3作为内标物。
1.3.5 碳化程度
碳化程度(degree of carbonation, DOC)的定义为硅酸钙矿物实际吸收CO2的质量与其理论上最大吸收CO2质量的比值。具体操作步骤为:将坩埚放入高温炉在1 000 ℃煅烧2 h至恒重称其质量,记为m0,再取10 g左右的样品置于坩埚中在300 ℃保温2 h后冷却至室温称其质量,记为m1,然后在1 000 ℃保温2 h后冷却至室温称其质量,记为m2,则300~1 000 ℃烧失量R和碳化程度α如公式(1)、(2)所示。
(1)
(2)
1.3.6 SEM测试
通过扫描电镜(SEM)对烧成γ-C2S和其碳化后的产物进行形貌观察,测试仪器采用美国FEI公司生产的QUANTA FEG450型环境场发射扫描电镜,在样品表面喷镀约5 nm厚的Pt导电层,测试电压一般为5 kV。
2 结果与讨论
2.1 Al2O3掺杂对γ-C2S熟料烧成性能的影响
图1为不同Al2O3掺量的γ-C2S烧成后粒径分布。Al2O3的加入降低了γ-C2S的粒径,D50由A0的15.09 μm分别降至6.05 μm(A1)、9.576 μm(A2)、8.913 μm(A3)。推测其原因是水泥中的铝充当水泥熟料中的溶剂矿物,降低液相形成温度,更加有益于离子迁移。在纯相γ-C2S的烧结过程中,由于无液相的生成,钙离子与硅离子迁移困难;随着Al2O3的加入,烧结过程中形成部分液相,促进了钙离子与硅离子迁移并结合生成硅酸二钙,因而使物料粉化效果更加显著。

图1 不同Al2O3含量的γ-C2S粒径分布Fig.1 Particle size distribution of γ-C2S with different Al2O3 dosages
图2为不同Al2O3掺量合成γ-C2S的XRD谱。A0的XRD谱上几乎全是γ-C2S的衍射峰,没有其他杂质相的衍射峰;同时从XRD谱中可以观察到29.7°即(130)晶面衍射峰强度随着Al2O3掺量的增加而逐渐加强,且对比γ-C2S的三大主峰(29.7°、32.52°和32.8°)来看,Al2O3的掺入并没有使其发生偏移。当引入Al2O3后在31.0°左右出现了钙铝黄长石(Ca2(Al(Al)SiO7),C2AS)的主衍射峰,而且随着Al2O3掺量的增加,C2AS的衍射峰强度逐渐增强,表明其含量逐渐增加。研究表明,在硅酸盐水泥熟料体系中C2AS的形成会导致水泥熟料粉化并且是Al2O3溶出的主要物相[14],因此在Al2O3掺杂γ-C2S的烧成过程中,C2AS可能会加剧β-C2S在500 ℃以下时向γ-C2S晶型转变过程中的自粉化,这也解释了引入Al2O3后γ-C2S熟料具有更小的粒径。
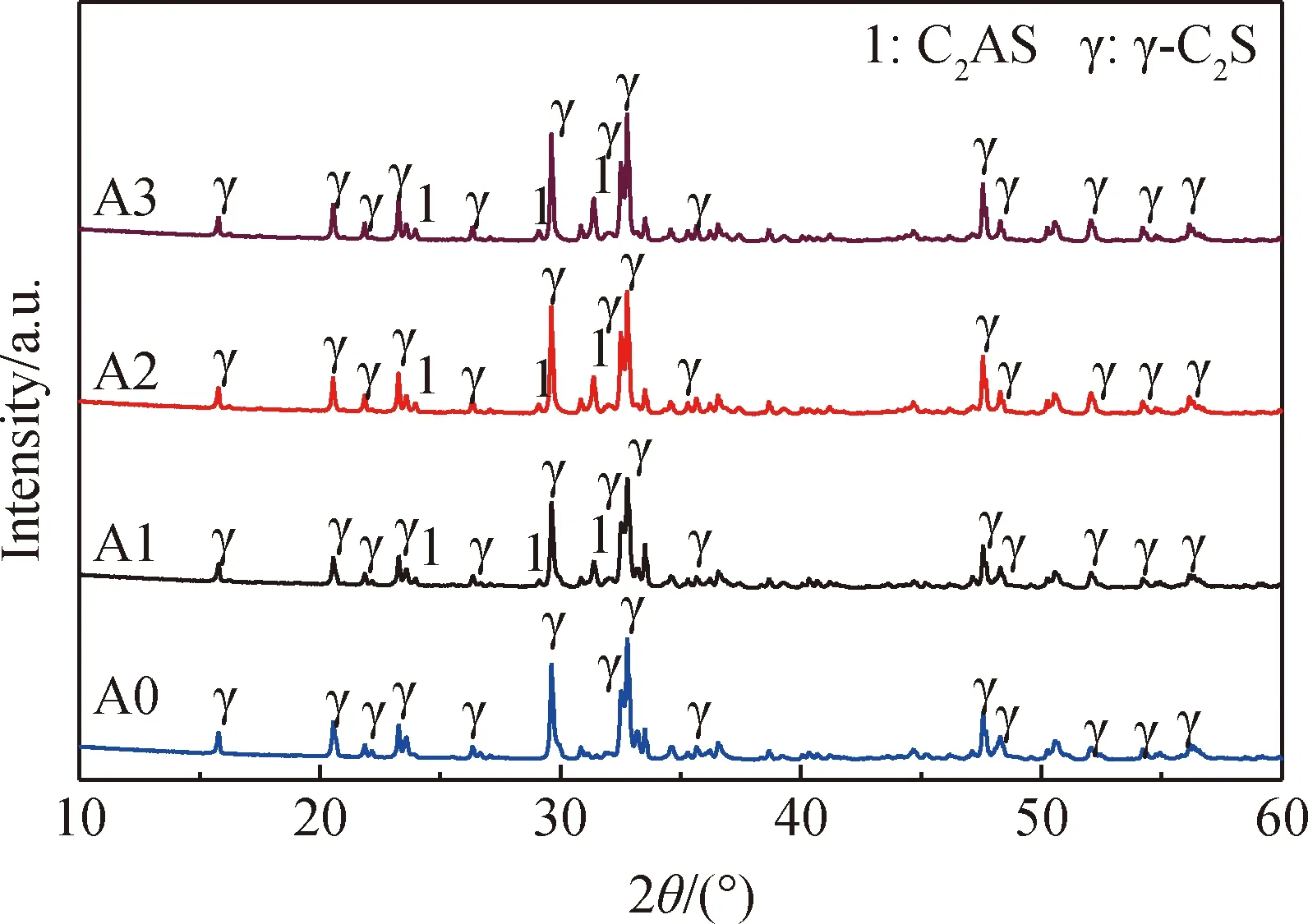
图2 不同Al2O3掺量合成γ-C2S的XRD谱Fig.2 XRD patterns of γ-C2S with different Al2O3 dosages
图3为不同Al2O3掺量合成γ-C2S自粉化后的微观形貌。Al2O3的掺入明显改变了γ-C2S颗粒的表面形貌。A0颗粒表面出现褶皱,是由于β-C2S向γ-C2S转变而带来自粉化所引起的效果;随着Al2O3掺量的增加,颗粒表面褶皱消失,变得光滑,颗粒也明显变小,且颗粒间紧密相邻。

图3 不同Al2O3掺量合成γ-C2S粉体颗粒的SEM照片Fig.3 SEM images of γ-C2S powder with different Al2O3 dosages
2.2 Al2O3掺杂对γ-C2S熟料碳化温升的影响
γ-C2S的碳化反应伴随着急剧放热[15],使得试样表面温度明显升高。因此,可以通过测量试样在碳化时温度的变化来表征Al2O3掺杂对γ-C2S碳化活性的影响。Al2O3掺杂的γ-C2S在碳化过程中的温度与累积温升分别如图4和图5所示。
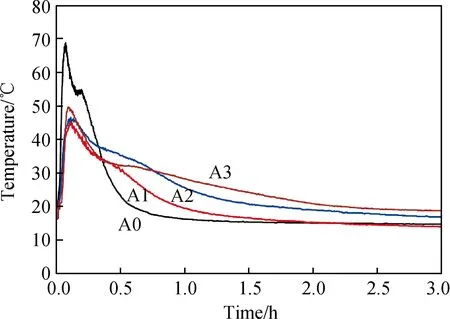
图4 Al2O3掺杂γ-C2S碳化升温曲线Fig.4 Carbonation temperature evolution of Al2O3 doped γ-C2S
A0试样碳化4.38 min后温度即达到最高68.9 ℃。碳化温度过高会导致试样内部水分蒸发过快,对后续碳化过程具有重要影响。Al2O3的掺入明显降低了γ-C2S的温升速率和最高温升,说明Al2O3掺杂延缓了早期γ-C2S表层的碳化反应速率。同时,Al2O3掺杂γ-C2S试样的降温过程更为缓慢和持久。从图5的碳化累积温升曲线也可以看出,随着Al2O3掺量的增加,γ-C2S的累积温升更大,达到稳定所需的时间更长,即Al2O3的掺入可以延长γ-C2S的碳化反应。原因可能是掺杂Al2O3后生成新的物相C2AS具有较低的碳化活性,使碳化过程中温升较A0试样的低,使反应更为温和,防止试样内部水分蒸发过快,从而有利于反应的持久进行。
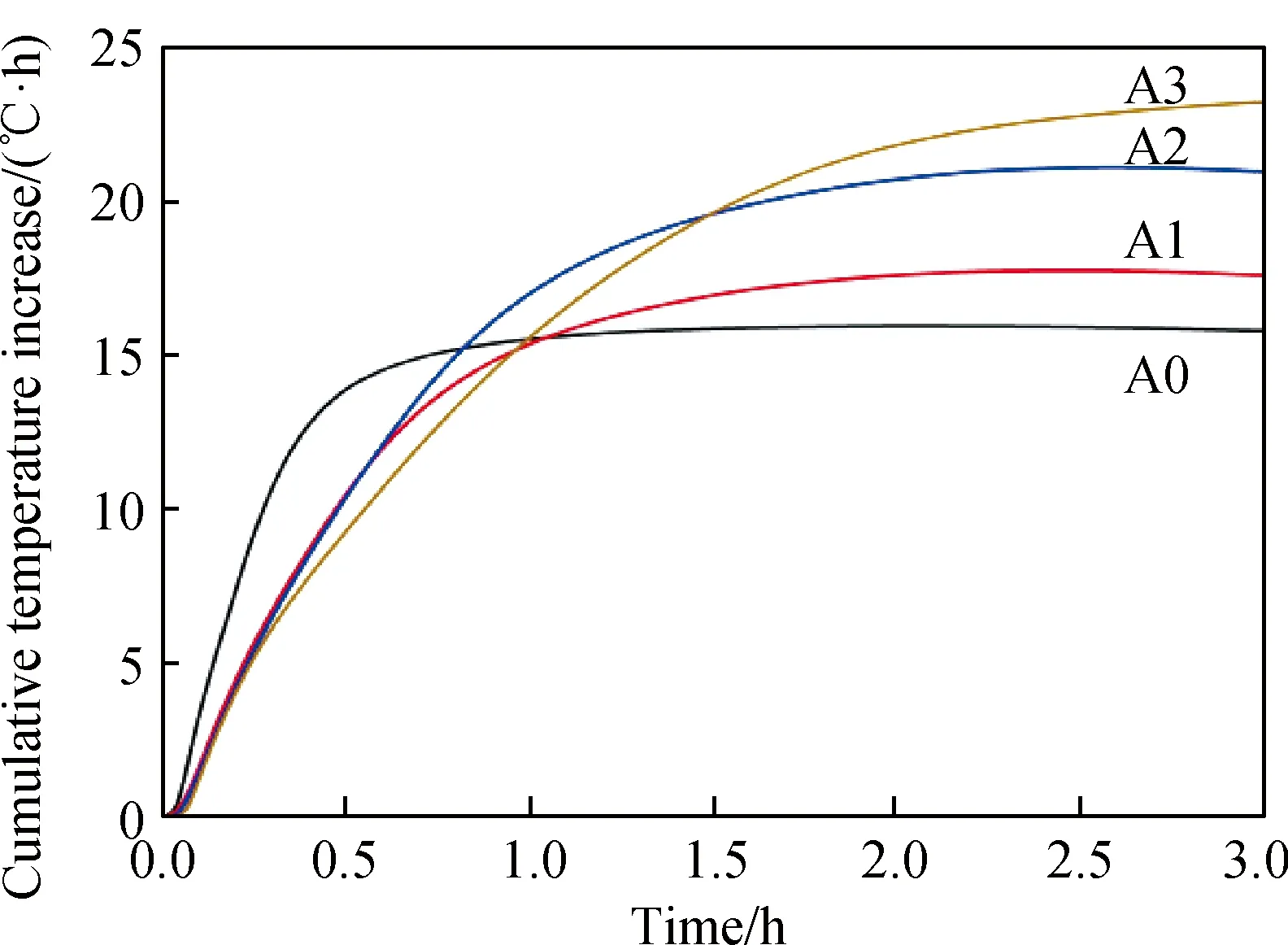
图5 Al2O3掺杂γ-C2S碳化升温积累曲线Fig.5 Cumulative temperature increase of Al2O3 dopedγ-C2S during carbonation
2.3 Al2O3掺杂对γ-C2S碳化体抗压强度和碳化程度的影响
不同Al2O3掺量的γ-C2S碳化体碳化不同时间的抗压强度如图6所示,Al2O3掺杂γ-C2S碳化体的碳化程度如图7所示。Al2O3的加入可以大幅度增加γ-C2S碳化体的抗压强度,其中A0~A3组碳化0.5 h时抗压强度分别达到了40 MPa、67 MPa、65 MPa和69 MPa,碳化5 h时不同Al2O3掺量的γ-C2S碳化体的抗压强度相比于碳化0.5 h时分别提高了69.55%、22.47%、31.86%和32.67%,而碳化24 h时的抗压强度分别为77 MPa、98 MPa、102 MPa和105 MPa。如前所述,Al2O3掺杂有利于碳化反应的持久进行,增加碳化体的整体碳化程度,从而有利于其抗压强度的提升。从图7可以看到,Al2O3能够明显提升γ-C2S的碳化程度,相比于A0组试样,γ-C2S的碳化程度分别增加了8.57%(A1)、10.14%(A2)和10.62%(A3)。
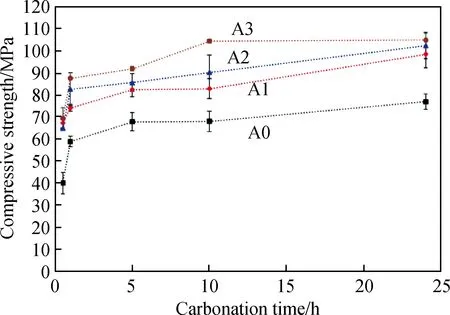
图6 Al2O3掺杂γ-C2S碳化体的抗压强度发展Fig.6 Compressive strength development of Al2O3 dopedγ-C2S carbonation body

图7 Al2O3掺杂γ-C2S碳化体的碳化程度Fig.7 DOC of Al2O3 doped γ-C2S carbonation body
相关文献表明除了碳化程度外,碳化产物碳酸钙的结晶程度也影响着碳化制品的抗压强度[16],采用XRD谱中碳酸钙衍射峰的半峰宽(full width at half maximum, FWHM)来衡量其结晶度。半峰宽是指衍射峰达到峰高一半时的峰宽,半峰宽越小,晶型越好。表2列举了高Al2O3掺量相比于空白组γ-C2S碳化24 h时碳酸钙的晶体结构参数。从表中可以发现,(104)和(113)两个主晶面的衍射峰的峰高在Al2O3掺杂后明显增加,而半峰宽却正好相反,这说明Al2O3掺杂后有利于碳酸钙结晶度的提高。
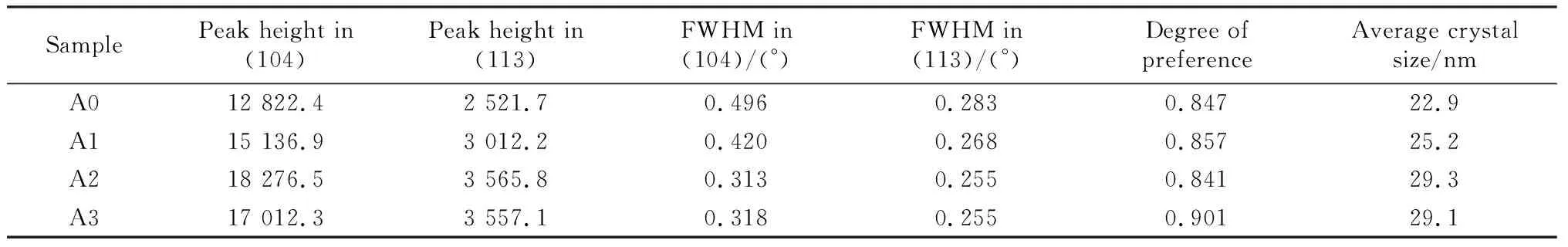
表2 Al2O3掺杂γ-C2S碳化24 h碳酸钙晶体结构参数Table 2 CaCO3 crystal structure parameters of Al2O3 doped γ-C2S carbonated for 24 h
碳酸钙(PDF卡片83-0578)晶体的择优取向度可用公式(3)计算:
(3)
式中:F为择优取向度;I113与I104分别为(113)、(104)晶面衍射峰强度值。
碳酸钙晶粒尺寸可以用Scherrer公式简要计算:
(4)
式中:D为晶粒垂直于晶面方向的平均厚度;K为常数;λ为X射线波长;B为衍射峰半峰宽;θ为衍射角。
碳酸钙晶体的择优取向度和晶粒平均尺寸见表2。从表中可以发现,掺杂Al2O3的γ-C2S碳化产物碳酸钙晶粒尺寸增加并且整体上提高了晶体的择优取向度,这说明Al2O3的掺入不仅可以提高碳酸钙(104)和(113)晶面的衍射峰强度,而且有利于提高其结晶度。
2.4 Al2O3掺杂对γ-C2S碳化体碳化产物的影响
图8为不同Al2O3掺量的γ-C2S碳化24 h后的XRD谱。从碳酸钙的衍射峰来看,不同Al2O3掺量的γ-C2S碳化后的碳酸钙晶型包括方解石(calcite)和文石(aragonite),以方解石型碳酸钙为主。对比γ-C2S碳化前后的XRD谱可以知道,钙铝黄长石(201)晶面衍射峰在碳化24 h后消失不见,生成了方解石晶型的碳酸钙,而(211)晶面主衍射峰强度变化不明显,说明钙铝黄长石的碳化活性较低。
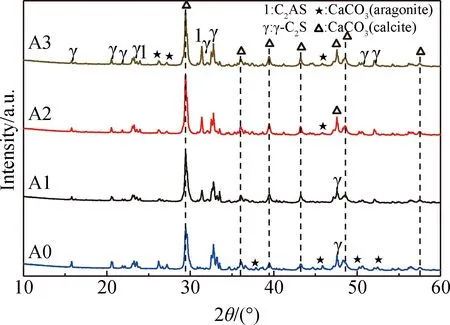
图8 不同Al2O3掺量的γ-C2S碳化24 h碳化产物Fig.8 Carbonated products of γ-C2S with differentAl2O3 dosages carbonated for 24 h
为了更好地确定碳化24 h不同试样中各个物相的相对含量,对样品进行了定量分析,结果如图9所示。掺杂少量Al2O3不仅会引入新相,而且会导致存在部分未转变的β-C2S,与文献[10]中Al2O3可以稳定β-C2S晶型的结果一致。Al2O3掺杂γ-C2S的无定形相的含量明显减少,且随着Al2O3掺量的增加而降低,A0~A3碳化24 h时无定形相的质量含量分别为41.11%、31.00%、28.22%和25.11%;在掺杂Al2O3后,方解石型的碳酸钙含量明显增加,这可以解释掺杂Al2O3后γ-C2S碳化体的抗压强度明显提高。值得注意的是文石相只出现在高Al2O3掺量的碳化产物中。可能是由于文石属于介稳态,而A0试样碳化放热更为剧烈,使文石在较高温度下可以稳定存在而不向方解石转变[17]。
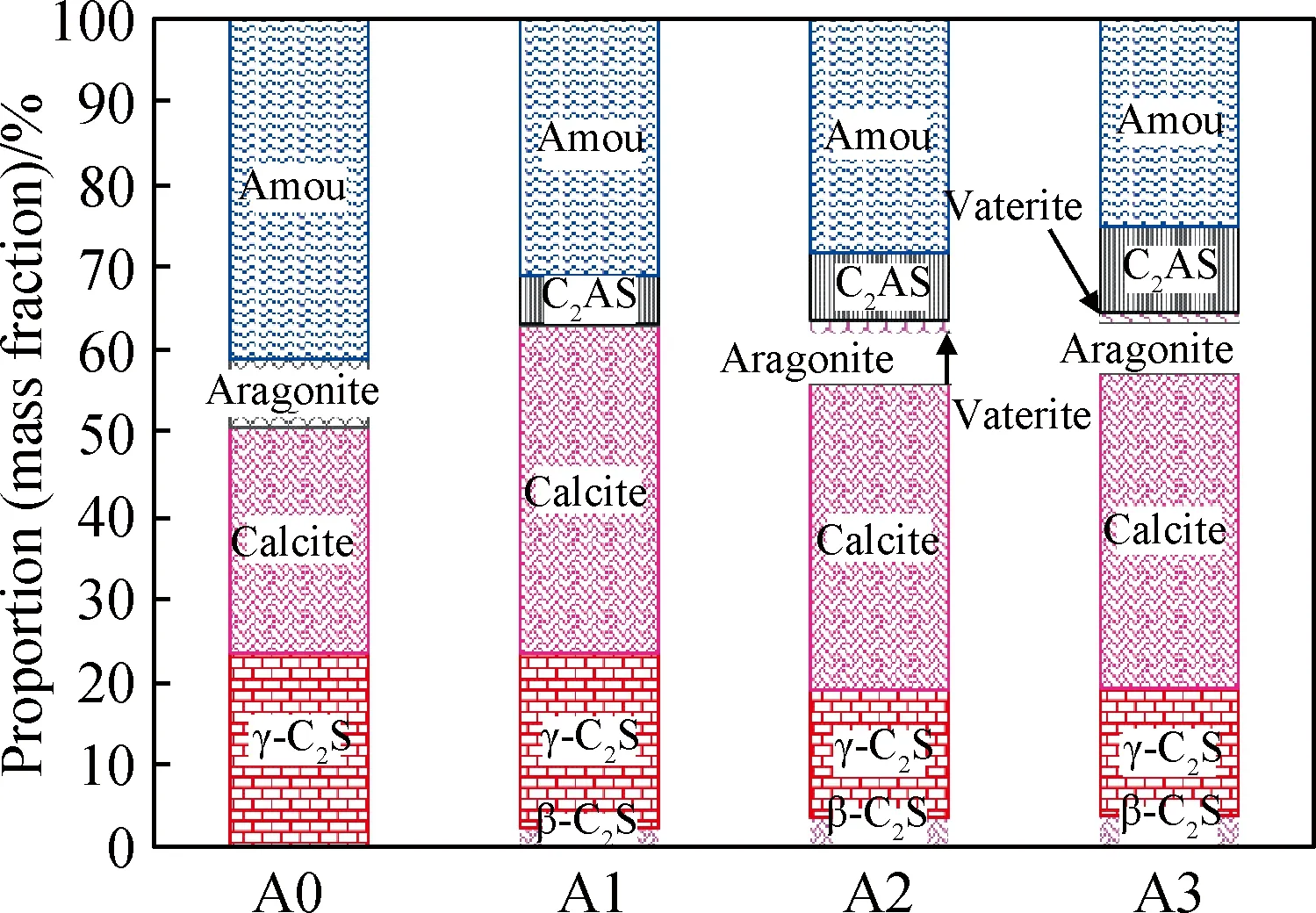
图9 不同Al2O3掺量的γ-C2S碳化24 h物相组成变化Fig.9 Phase composition changes of γ-C2S withdifferent Al2O3 dosages carbonated for 24 h
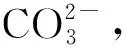

图10 Al2O3掺杂γ-C2S碳化24 h后的断面形貌Fig.10 Micrographs of fractured surfaces of Al2O3 doped γ-C2S carbonated for 24 h
3 结 论
(1)在最高煅烧温度1 400 ℃且保温3 h后,掺入Al2O3的γ-C2S的碳化强度和碳化程度均大幅度提高;Al2O3质量掺量为0%、2.32%、3.13%、3.94%时,γ-C2S碳化体碳化24 h的抗压强度分别为77 MPa、98 MPa、102 MPa和105 MPa;相比于未掺Al2O3,掺加Al2O3后碳化程度分别提高了8.57%、10.14%和10.62%。
(2)Al2O3的掺入降低了γ-C2S碳化放热的最高温度,延长了碳化放热时间,因而增加了累积放热量;随着Al2O3掺量的增加,方解石的含量增加而无定形相的含量减少,同时,促进了方解石型碳酸钙晶粒的生长,提高了方解石的结晶性,上述因素的综合影响有利于提高γ-C2S碳化体的抗压强度。

