高三尖杉酯碱联合阿扎胞苷与Venetoclax治疗难治/复发急性髓系白血病疗效观察
张文荟,陈香丽,陈玉清,刘忠文,孙 恺,臧玉柱
(河南省人民医院血液内科,郑州大学人民医院,河南 郑州 450002)
难治/复发急性髓系白血病(acute myeloid leukemia,AML)患者预后不良,再次完全缓解(complete remi-sson,CR)率一般不超过30%[1-2]。高三尖杉酯碱(homoharringtonine,HHT)是一种来自三尖杉的天然生物碱衍生物,基于HHT的三药联合治疗新诊断AML的总体生存(overall survival,OS)和3 a无事件生存(event-free survival,EFS)均优于国内常用的柔红霉素联合阿糖胞苷方案。Venetoclax是一种抗凋亡蛋白B细胞淋巴瘤因子-2的选择性小分子抑制剂,被美国食品药品监督管理局批准可与去甲基化药物联合用于治疗年龄较大或有合并症的新诊断AML患者[3]。阿扎胞苷(azacitidine,AZA)是被批准用于治疗AML的DNA去甲基化药物。国内外多项研究均已证实,阿扎胞苷联合Venetoclax治疗复发/难治AML的疗效显著[4-6]。HUANG等[7]的研究结果表明,HHT联合AZA具有协同抗白血病作用,此联合方案对预后不良AML有效。但目前未见到关于HHT联合AZA与Venetoclax (HAV方案)治疗AML的报道。基于此,本研究探讨HAV新型方案治疗难治/复发AML患者的疗效及安全性,现将结果报道如下。
1 资料与方法
1.1 一般资料选择2019年7月至2020年7月河南省人民医院血液内科收治的14例难治/复发AML患者为研究对象。难治AML的诊断参照2010年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN) 指南标准[8-9],复发AML的诊断参照《血液病诊断及疗效标准》[10]。所有患者签署知情同意书。14例患者中男11例,女3例;中位年龄55(18~75)岁,其中8例患者年龄>60岁;10例为原发性AML,4例为继发性AML(其中3例由骨髓增生异常综合征转化,1例由原发性骨髓纤维化转化);7例为难治AML(5例患者2个疗程诱导未达CR,2例患者3个疗程诱导未达CR),7例为复发AML(5例为第1次复发,2例为第2次复发,7例患者中1例在异基因造血干细胞移植后复发);14例患者的既往化学治疗疗程中位数为3(1~8)个;5例患者既往接受去甲基化药物治疗;10例患者伴有预后不良的染色体或基因,主要基因突变为TP53(4例)、FLT3(4例)、RUNX1(4例)、DNMT3A(3例)、ASXL1(2例)、SRSF2(2例)、IDH2(2例)及JAK2(2例);接受HAV方案治疗前,患者中位骨髓原始细胞占34.5%(0.0%~60.0%),中位外周血原始细胞占6.5%(0.0%~52.0%);美国东部肿瘤协作组评分中位评分为1(0~2)分;接受HAV化学治疗初始,9例患者伴有3级以上粒细胞减少,11例患者伴有3级以上血小板减少,5例患者伴有重度贫血;所有患者接受HAV治疗的中位疗程为2(1~5)个。根据 2010年NCCN 指南标准[8],并结合细胞遗传学和分子生物学将患者分为低危组(n=3)、中危组(n=5)、高危组(n=6)。
1.2 化学治疗方案HAV具体方案为:HHT(杭州民生药业集团有限公司,国药准字H33021658) 1.3 mg·m-2·d-1,第1~14天,静脉点滴;AZA(华润医药商业集团国际贸易有限公司,国药准字H20130067) 75 mg·m-2·d-1,第1~7天,皮下注射;Venetoclax(艾伯维医药贸易上海有限公司,国药准字520030048)第1天100 mg,第2天200 mg,第3天400 mg,第4天后每日400 mg,口服,持续给药14 d后停药14 d,28 d为1个周期。每例患者至少完成1个周期的HAV化学治疗。
1.3 观察指标(1)治疗效果:依据2003年CHESON等[11]报道的国际协作组关于AML诊断、治疗标准的修订报告,综合患者骨髓细胞形态学、骨髓微小残留病灶(minimal residual disease,MRD)、外周血中性粒细胞计数及血小板等指标进行疗效评估,观察总反应率(overall response rate,ORR),将治疗效果分为形态学CR、血细胞计数未完全恢复的完全缓解(complete remission with incomplete count recovery,CRi)、部分缓解(partial ression,PR)及治疗失败(no remission,NR)。每个治疗周期进行疗效评估1次,达CR、CRi或者PR者,可根据患者的体能状况及意愿,继续用该方案维持治疗。计算患者的缓解率,缓解率=(CR例数+CRi例数)/总例数×100%。(2)影响因素分析:分析对治疗效果和1 a OS率的影响因素。(3)不良反应:根据文献[12]中常见不良反应事件评价标准[12]对药物相关不良反应进行评估。
1.4 随访通过住院病历、门诊病历或电话进行随访,随访截止日期为2020年8月31日。
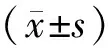
2 结果
2.1 治疗效果14例患者的ORR为78.6%(11/14),3例患者为NR(2个疗程后未达PR);7例患者获得CRi,2例获得CR,2例获得PR,未发生治疗相关死亡病例;获得CR的患者中位疗程为2(1~3)个。9例获得CR/CRi患者同时行MRD检测,其中6例患者MRD为阴性,3例患者MRD为阳性;9例获得CR/CRi的患者中6例患者在1个疗程后达CR/CRi,3例患者2个疗程后达CR/CRi。原发性AML和继发性AML患者的缓解率分别为90.0%(9/10)和0.0%(0/4),原发性AML患者缓解率高于继发性AML患者,差异有统计学意义(P<0.05):10例原发性AML中有9例获得CR/CRi,而4例继发性AML均未获得CR/CRi。
2.2 影响治疗效果和患者1 a OS率的危险因素单因素分析结果见表1。患者的性别、年龄、疾病状态、既往是否使用去甲基化药物治疗、既往化学治疗疗程对HAV方案治疗效果无影响(P>0.05);患者的AML类型及预后类型对HAV方案治疗效果有影响(P<0.05)。
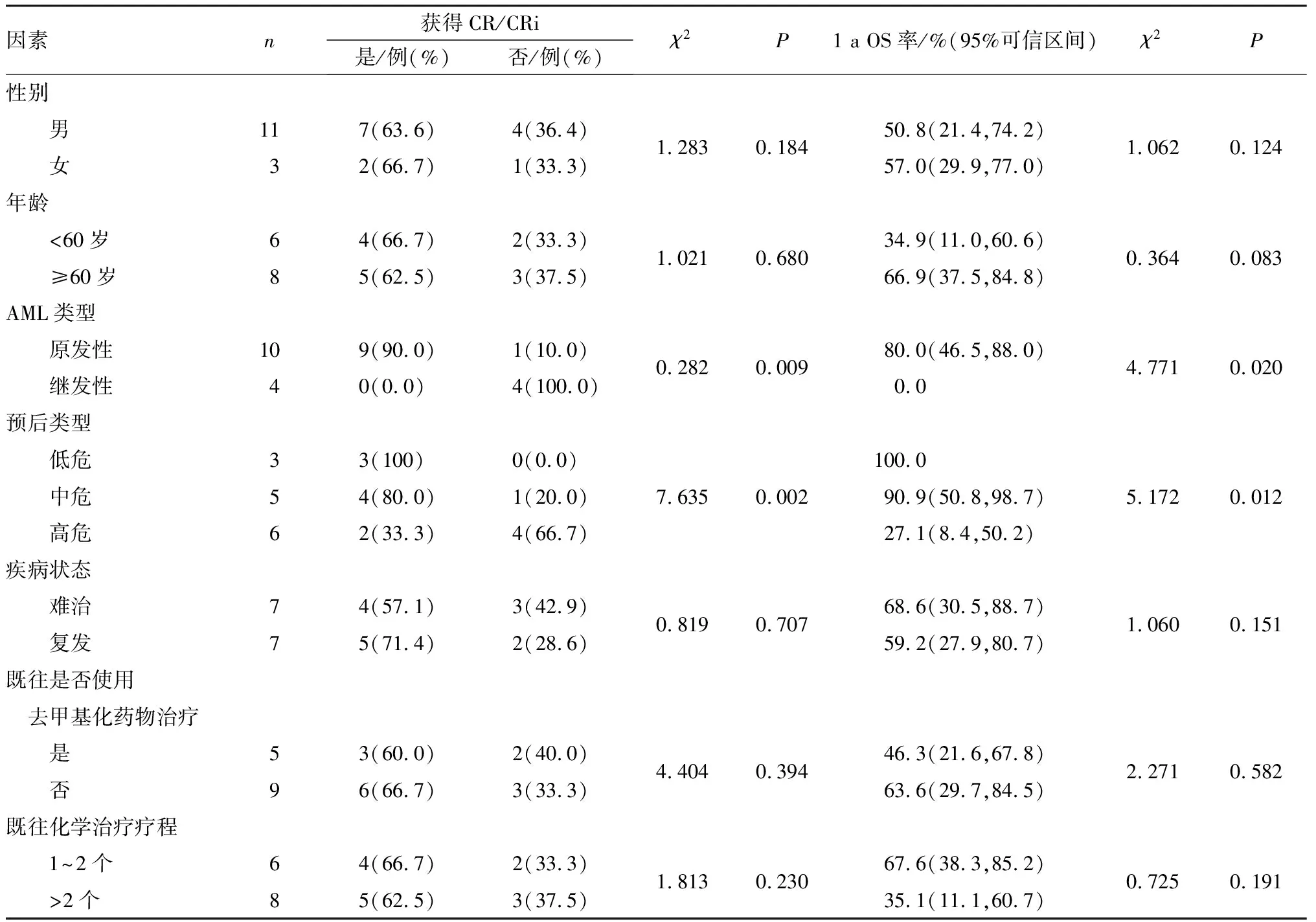
表1 影响HAV方案治疗效果和患者1 a OS率的危险因素单因素分析
患者的性别、年龄、疾病状态、既往是否使用去甲基化药物治疗、既往化学治疗疗程对1 a OS率无影响(P>0.05);患者的AML类型、预后类型对1 a OS率有影响(P<0.05)。
2.3 影响HAV方案治疗效果和患者1 a OS率的多因素分析结果结果见表2。多因素分析结果显示,预后类型是影响HAV方案治疗效果和患者1 a OS率的独立危险因素(P<0.05)。
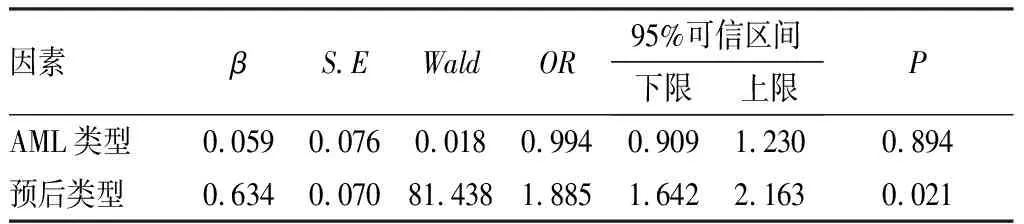
表2 影响患者HAV方案治疗效果和1 a OS率的危险因素多因素分析
2.4 不良反应患者在化学治疗期间均出现III~IV级白细胞减少或血小板减少,给予粒细胞积落刺激因子升白细胞、输注单采血小板后,白细胞和血小板计数升至正常水平。白细胞最低值为(0.09±1.08)×109L-1,粒细胞缺乏时间为(15.29±3.11) d,血红蛋白最低值(54.20±3.29) g·L-1,红细胞输注量为(10.13±2.27) U。血小板最低值为(9.35±1.92)×109L-1,单采血小板的输注量为(5.68±1.08) U。9例(64.3%)患者在中性粒细胞缺乏期间并发热,其中7例(50.0%)患者感染部位明确(肺部感染6例,肛周脓肿1例)。丙氨酸转氨酶异常1例(7.1%),血清肌酐升高1例(7.1%),治疗后均恢复正常。未发生与治疗相关的死亡。
2.5 随访患者中位随访时间为6.5 (1.0~12.5)个月,14例患者1 a OS率为57.1%。截止至随访日期,9例达CR/CRi的患者中有4例继续接受HAV方案进行化学治疗,5例终止治疗(3例接受异基因造血干细胞移植治疗,2例疾病复发)。
3 讨论
Venetoclax联合AZA方案治疗AML的疗效肯定且患者耐受性良好,无论是治疗新诊断AML[13-15],还是难治/复发AML[4-6],两药联合均显示一定的疗效。HHT联合AZA具有协同抗白血病作用,有临床研究结果显示,此两药联合对预后不良AML有效且患者耐受性良好[7]。本研究探讨了HAV新型组合方案在难治/复发AML患者中的疗效及安全性,结果显示,14例患者的ORR为71.4%(11/14),9例患者达到CR/CRi,2例患者达到PR。9例获得CR/CRi患者中有6例(66.7%)MRD达到阴性。6例患者1个疗程后达到CR/CRi,3例患者2个疗程后达到CR/CRi,提示此方案能使难治/复发AML患者获得快速缓解,对老年患者同样也安全有效。3例于CR后行异基因造血干细胞移植,说明此方案能为难治/复发AML患者争取移植机会。
值得注意的是,本研究中的14例AML患者具有高风险预后特征,主要表现为多数(10/14,71.4%)伴有预后不良的染色体或基因,尽管如此,本研究中患者的ORR为78.6%,高于接受常规挽救治疗患者的反应率[9,16]。ALDOSS等[5]研究发现,化学治疗联合Venetoclax治疗难治/复发AML患者的ORR为64%,且低危组患者的反应率更高(3例为低危组,11例为中危组,18例为高危组)。DINARDO等[13]使用Venetoclax联合去甲基化药物治疗43例难治/复发AML患者,结果发现,患者的ORR仅为21%;41例患者伴有预后不良或预后中等的染色体或基因,大多数患者之前至少接受过2次化学治疗。ALDOSS等[5]研究发现,在难治/复发AML患者中,原发性AML患者的CR率高于继发性AML患者,与本研究结果一致。ALDOSS等[5]研究发现,伴有预后良好染色体核型或基因的难治/复发AML患者有更好治疗效果。本研究中,低危组、中危组患者CR/CRi率高于高危组患者。研究显示,既往是否行异基因干细胞移植以及既往是否使用去甲基化药物进行治疗对疗效并无影响[5,7-8]。本研究结果显示,患者的年龄、性别、疾病类型、既往是否使用去甲基化药物治疗、既往化学治疗的疗程均对疗效无影响,与上述研究结果一致。本研究发现,获得最好疗效反应(骨髓MRD阴性)的中位疗程为2个疗程,获得首次CR大多发生在第1个疗程。鉴于此平均反应时间,如果患者在2个疗程后未达CR,可以停止该治疗方案,该研究结果为早期调整治疗方案提供了依据,也可能有助于降低因持续接受Venetoclax联合治疗出现的感染和出血风险。
HAV方案对患者的骨髓造血功能的抑制作用较严重,本研究中的患者均出现III级以上白细胞和血小板减少,9例(64.3%)患者在粒细胞缺乏期出现发热、血流感染。通过密切监测病情、积极调整抗感染治疗、及时输注血液制品、进入层流病房等手段,不良反应得到良好的控制,未发生与治疗相关的死亡。
综上所述,HAV新型方案对难治/复发AML患者有效且患者的耐受性良好,老年患者同样可耐受。原发性AML和低、中危组患者具有较高的CR率和OS。但本研究样本量较小,且属于单中心结果,需要扩大样本量进一步研究。

