儿童血流感染病原菌分布及耐药性分析
王 艳
(洛阳东方医院/河南科技大学第三附属医院检验科,河南 洛阳 471003)
血流感染是一种严重的全身感染性疾病,病原微生物在血液循环中呈一过性、间歇性或持续性存在,包括脓毒血症、脓毒症、菌血症,其可对机体所有脏器造成损害,严重者可导致休克、多脏器衰竭、弥散性血管内凝血甚至死亡。儿童尤其是婴幼儿黏膜和生物屏障未完全建立,对病原菌包括低毒力的条件致病菌易感[1];此外,滥用广谱抗菌药物、长期使用肾上腺皮质激素、器官移植和侵入性新诊疗技术的推广应用都是诱发儿童血流感染的主要原因,血流感染已成为儿童严重感染性疾病,其病死率高达12.0%~20.5%[2]。金黄色葡萄球菌是儿童感染最常见的一种病原菌,引起儿童多种感染性疾病,如皮肤脓疱疮、伤口感染、骨髓炎、细菌性心内膜炎和新生儿脓毒血症等;金黄色葡萄球菌尤其是耐甲氧西林金黄色葡萄球菌(methicillin-resistantStaphyloco-ccusaureus,MRSA)血流感染率明显升高,患者感染MRSA后治疗过程困难,预后较差,病死率高[3]。因此,及时、准确地检测儿童血流感染的病原菌并选择合适的抗菌药物是临床治疗的关键。本研究旨在探讨儿童血流感染的病原菌分布、耐药性,以期为临床治疗提供参考。
1 资料与方法
1.1 一般资料选择2017年1月至2019年12月洛阳东方医院(河南科技大学第三附属医院)儿科病房收治的70例血流感染患儿为研究对象。病例纳入标准:(1)年龄≤14岁;(2)血培养阳性;(3)符合《医院感染诊断标准(试行)》[4]血流感染诊断标准。病例排除标准:(1)血培养结果判定为污染;(2)近期使用过抗生素。本研究获得医院医学伦理委员会批准,患儿监护人均知情同意并签署知情同意书。
1.2 方法
1.2.1 血标本分离培养患儿在使用抗生素前从左右肘正中静脉或贵要静脉采集双套静脉血各1~3 mL 注入血培养瓶(购自山东鑫科生物公司),同1例患者不同部位所分离出的同1菌株只入选第1株。血培养瓶有细菌生长后,将阳性培养物接种于血平板,35 ℃恒温箱内过夜培养,挑取血平板上菌落。
1.2.2 病原菌鉴定及药物敏感性试验采用美国贝克曼公司MicroScan Walkaway 96 plus全自动细菌鉴定/药物敏感分析系统及配套的药敏卡片进行菌株鉴定和药物敏感性试验,严格按照《全国临床检验操作规程》进行操作[5],药物包括氨苄西林/舒巴坦、哌拉西林/他唑巴坦、头孢唑林、头孢呋辛、头孢曲松、头孢他啶、头孢吡肟、氨曲南、亚胺培南、美罗培南、阿米卡星、庆大霉素、环丙沙星、复方磺胺甲噁唑、左旋氧氟沙星、青霉素、苯唑西林、利福平、万古霉素、替考拉宁、红霉素、克林霉素、利奈唑胺、莫西沙星、氨苄西林、庆大霉素、米诺环素。药物敏感性结果依据美国临床和实验室标准化协会文件(CLSI M100,2018)进行判定。质控菌株为大肠埃希氏菌ATCC25922、铜绿假单胞菌ATCC27853和金黄色葡萄球菌ATCC25923,质控菌株来源于美国菌种保藏中心。
1.2.3 聚合酶链反应(polymerase chain reaction,PCR)法检测金黄色葡萄球菌耐药基因型采用MicroScan全自动细菌鉴定系统(购自美国贝克曼公司)鉴定出金黄色葡萄球菌;选取金黄色葡萄球菌纯培养菌落,金黄色葡萄球菌的溶葡萄球菌DNA裂解液和Taq Mix购自大连宝生物公司,依据DNA提取试剂盒(购自北京天根生化科技有限公司)说明书提取菌落基因组DNA。采用PCR法检测金黄色葡萄球菌耐药基因,PCR仪购自美国Bio-Rad公司。基因blaZ、mecA、ermA、ermB、ermC引物由武汉金开瑞生物工程有限公司合成(见表1)。20 μL反应体系:Taq Mix 10 μL,上、下游引物各1 μL,DNA模板2 μL,ddH2O 6 μL。反应条件:95 ℃预变性5 min;95 ℃变性40 s,64 ℃退火40 s,72 ℃延伸1 min,共35个循环;72 ℃延伸10 min,4 ℃保存。阳性参照基因:mecA(DNA提取自菌株ATCC43300)、blaZ(DNA提取自菌株ATCC43300)、ermA(DNA Tn554)、ermB(DNA Tn917)和ermB(DNA pE194)(菌株购自美国菌种保藏中心,DNA购自河南省细菌耐药监测中心),纯水作为阴性参照。将PCR扩增产物、阳性参照基因、阴性参照加入到含溴化乙锭的琼脂糖凝胶中,110 V电泳40 min,使用Tanon-3500凝胶成像系统(购自上海天能公司)拍照。根据目的基因片段长度,参照阳性对照判读菌株所含基因型。

表1 目的基因扩增引物
1.3 统计学处理应用WHONET 5.6软件分析菌株分布及药物敏感性数据。
2 结果
2.1 患儿病原菌分布情况结果见表2。患儿血培养的732份送检标本中,分离出70株非重复首次分离菌株,包括17种细菌和1株真菌(未计入构成比),其中革兰阴性菌构成比为31.88%,主要为大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌;革兰阳性菌构成比为68.12%,主要为金黄色葡萄球菌、凝固酶阴性葡萄球菌和肺炎链球菌,其中以金黄色葡萄球菌构成比最高(26.08%)。

表2 患儿血培养病原菌分布
2.2 主要革兰阴性菌对常用抗菌药物的耐药率结果见表3。大肠埃希菌对庆大霉素、环丙沙星、复方磺胺甲噁唑、左旋氧氟沙星有较高的耐药率,对哌拉西林/他唑巴坦、头孢他啶、亚胺培南、美罗培南、阿米卡星敏感。肺炎克雷伯菌对氨苄西林/舒巴坦和头孢唑林有较高的耐药率,对亚胺培南、美罗培南、阿米卡星敏感。铜绿假单胞菌对氨曲南有较高的耐药率,对阿米卡星和左旋氧氟沙星敏感。
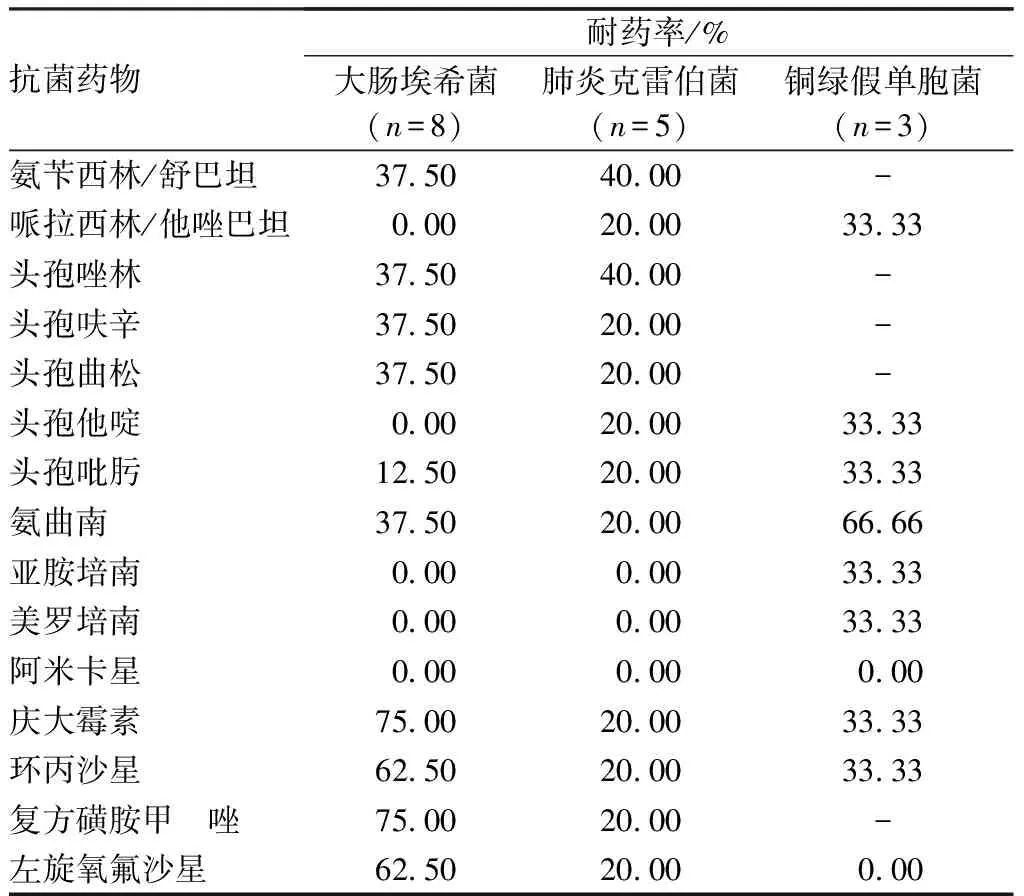
表3 主要革兰阴性菌对常用抗菌药物的耐药率
2.3 主要革兰阳性菌对常用抗菌药物的耐药率结果见表4。金黄色葡萄球菌对青霉素、红霉素、苯唑西林有较高的耐药率,对万古霉素和利奈唑胺敏感。凝固酶阴性葡萄球菌对青霉素、苯唑西林、红霉素有较高的耐药率,对万古霉素、替考拉宁、利奈唑胺敏感。肺炎链球菌对复方磺胺甲噁唑、红霉素、克林霉素有较高的耐药率,对利福平、万古霉素、利奈唑胺、莫西沙星、左旋氧氟沙星敏感。肠球菌对青霉素、红霉素、克林霉素、左氧氟沙星、氨苄西林耐药率较高,对万古霉素、利奈唑胺和替考拉宁敏感。
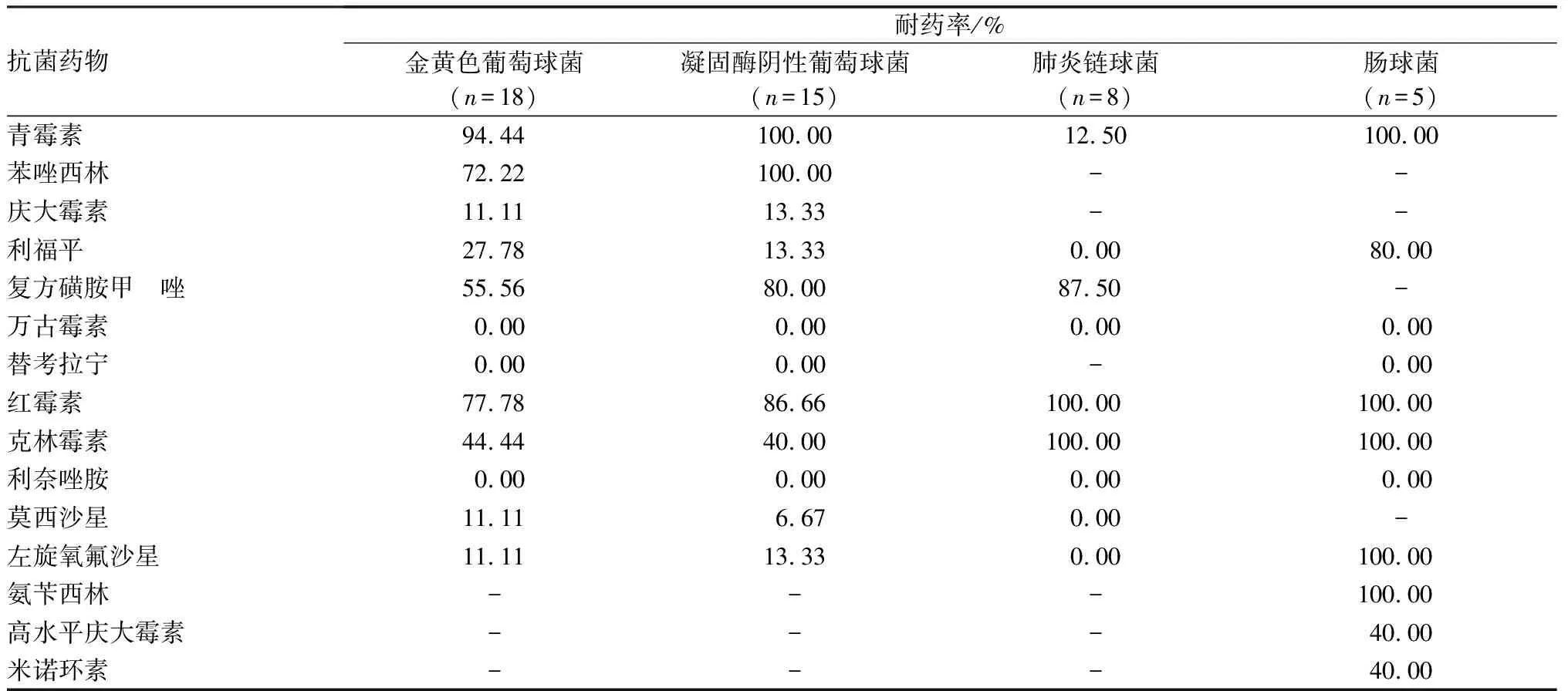
表4 主要革兰阳性菌对常用抗菌药物的耐药率
2.4 金黄色葡萄球菌耐药基因分析结果见表5。18株金黄色葡萄球菌中,包括13株MRSA和5株甲氧西林敏感金黄色葡萄球菌(methicillin-sensitiveStaphylococcusaureus,MSSA)。13株MRSA中mecA和ermA耐药基因检出率较高,其中有8株同时检出耐药基因mecA和erm基因(A或C)。5株MSSA中耐药基因 blaZ 和ermC 检出率较高。

表5 金黄色葡萄球菌耐药基因检测
3 讨论
血流感染是重症患者最严重的并发症之一,患者发生血流感染后,机体各种生理和生物化学功能异常,平均住院时间延长,预后和转归较差。基础疾病加重、全身炎症反应综合征、脓毒血症所致感染性休克等均是血流感染患者病死率较高的影响因素[6]。
TSUZUKI等[7]研究发现,导致血流感染的革兰阳性菌和革兰阴性菌中最常见的分别为金黄色葡萄球菌和大肠埃希菌。本研究纳入的69株细菌菌株中,革兰阳性菌构成比为68.12%,革兰阴性菌构成比为31.88%,其中构成比最高的是金黄色葡萄球菌(26.08%),其次为凝固酶阴性葡萄球菌(21.74%),再次是大肠埃希菌(11.59%)和肺炎链球菌(11.59%);该结果与全国细菌耐药监测网中国儿童及新生儿患者细菌耐药监测研究结果一致[8],提示金黄色葡萄球菌应为临床感染重点关注病原菌之一。
本研究检出的18株金黄色葡萄球菌中,对大环内酯类药物红霉素的耐药率高达77.78%;对喹诺酮类药物莫西沙星和左旋氧氟沙星耐药率较低,均为11.11%,但喹诺酮类药物因可能对14岁以下儿童骨骼发育有影响而被限制使用;对万古霉素的耐药率为0.00%,因此,治疗MRSA引起的儿童血流感染,万古霉素应成为临床首选用药。提示对于金黄色葡萄球菌引起的血流感染临床用药可选择的抗菌药物种类极其有限。
本研究药物敏感性试验结果发现,主要革兰阴性菌大肠埃希菌和肺炎克雷伯菌对碳青霉烯类抗菌药物美罗培南和亚胺培南的耐药率为0.00%;对第3代头孢类抗菌药物头孢曲松和头孢他啶、第4代头孢类抗菌药物头孢吡肟耐药性也相对较低;提示对于革兰阴性菌所致的血流感染可优先考虑使用第3、4代头孢类抗菌药物,如果抗感染治疗失败,可选择碳青霉烯类抗菌药物进行治疗。
本研究结果显示,3株铜绿假单胞菌中对碳青霉烯类抗菌药物美罗培南和亚胺培南、β-内酰胺酶抑制剂药物哌拉西林/他唑巴坦耐药率均为33.33%,对照患者的原始药物敏感性试验结果为同一株细菌,且此株细菌对单环类药物氨曲南也耐药。提示铜绿假单胞菌对3类结构不同的抗菌药物均耐药,呈现多重耐药性。因此,对于铜绿假单胞菌引起的血流感染临床用药面临困境,尤其对于儿童患者,需结合碳青霉烯类抗菌药物的最低抑菌浓度值,考虑联合用药方案,如氨基糖苷类联合碳青霉烯类;但氨基糖苷类抗菌药物阿米卡星因具有耳毒性,新生儿尽量避免使用,婴幼儿慎用,不得不考虑联合用药时要结合患儿的情况,最好进行血药浓度检测。
本研究分离出的18株金黄色葡萄球菌中包括13株MRSA和5株MSSA。徐卫华等[9]研究发现,临床上儿童发生金黄色葡萄球菌血流感染时应高度警惕 MRSA;相比于其他细菌感染,MRSA感染具有复杂的并发症和更高的病死率[3]。在过去几十年,大量文献报道了MRSA所引起的感染[7,10-12],具有多重耐药基因的MRSA在社区和医院出现的感染和流行成为全球主要健康问题,其可用药物之少引起广泛的关注。
MSSA在获得耐甲氧西林的mecA基因后成为MRSA,mecA基因编码表达异常的青霉素结合蛋白2a,可使大部分β-内酰胺类药物失去作用靶点,从而产生耐药性[13]。blaZ基因可诱导细菌产生青霉素酶,从而分解进入细菌体内的青霉素类药物[14]。MRSA菌株若同时含有mecA基因和erm基因则会表达甲基钝化酶,从而对大环内酯类抗菌药物呈现耐药[15]。本研究中有8株MRSA mecA和erm(ermA或ermC)基因检测均为阳性,说明该8株 MRSA产生了分解大环内酯类药物的甲基钝化酶,易呈现多重耐药性。
综上所述,儿童血流感染最常见病原菌为金黄色葡萄球菌尤其是MRSA,临床应重视病原菌的多药耐药性,合理应用抗菌药物。临床在经验用药时,需考虑流行菌株特征,提高血培养送检率,在获得鉴定和药物敏感性试验结果后及时调整,精准用药,并注意减少院内感染。但本研究数据覆盖面较小,研究对象所在医院为非妇幼专科医院,儿科收治患儿病种有限,且儿科血培养送检率相对其他科室低。因此,需要多中心的调查和研究,以了解本地区病原菌的分布和耐药性,指导临床针对儿童患者合理使用抗菌药物。

