碳热还原—浸出法回收废旧锂电池中的镍、钴、锰
代 云 邓朝勇 吴 浩
(1.稀美资源(广东)有限公司,广东 清远 513055;2.广东佳纳能源科技有限公司,广东 清远 513056)
随着国家环保形势的日益严峻和新能源汽车的日益普及,动力电池的使用量日益剧增。锂离子电池具有比能量高、循环寿命长、自放电率低和无记忆效应等优点,被广泛应用在便携式设备、电动汽车、储备电源等领域[1-3]。大量的锂离子电池需要及时处理,镍钴锰(NCM)三元材料是锂离子电池正极材料的重要组成部分,含有一定量的镍、钴和锰,具有一定的回收潜力,但目前综合回收体系尚未形成规模,回收率低,绝大多数未得到有效处理,不但浪费了大量的有价金属资源,而且还对环境造成了潜在危害[4,5]。
目前锂离子电池的综合回收方法主要包括火法冶金、湿法冶金以及火法与湿法相结合的方法。湿法冶金以能耗低、环境污染小、有价金属回收率高等优势,在复杂矿的绿色高效提取过程中应用较为普遍[6,7]。湿法冶金工艺技术中,浸出过程中的相关参数,如浸出温度、搅拌速率、液固比等在整个回收过程中起着关键作用,常见的浸出剂一般选择硫酸、盐酸等[8]。锂离子电池正极片是将前驱体烧结后形成的正极材料与粘结剂、乙炔黑混合后均匀涂抹在铝箔上形成的。由于乙炔黑和粘结剂不溶于酸,实际工业应用过程中需通过机械破碎将正极材料与铝箔进行分离后再对分离物进行浸出。LI等[9]在700 ℃焙烧除去粘结剂、乙炔黑和其它有机质,采用添加柠檬酸和双氧水方式浸出镍、钴、锰后再通过溶胶—凝胶法合成新的正极材料,所得材料具有优良的电化学性能,但该研究尚处于实验阶段,难以实现工业生产。MENG等[10]在650 ℃下对废旧锂电池正极材料焙烧后,在工作电压8 V、搅拌转速400 r/min的苹果酸体系中采用电化学还原浸出法浸出镍、钴、锰,三者的浸出率均在99%以上,但过程能耗高,不宜进行工业推广。
为了解决锂离子电池中正极材料和粘结剂、铝箔难以分离、常规湿法反应时间长、火法提取能耗高且污染环境的问题,并提高三元正极材料中镍、钴、锰的回收率,采用碳热还原—湿法浸出工艺对某NCM523型电池正极材料的有价元素进行回收。将废旧电池与工业焦粉混合均匀后焙烧,使原废旧锂电池正极材料发生分解,锂元素转换成可溶性碳酸盐,而镍、钴、锰不溶于水,采用常温水浸工艺提取出锂后的水浸渣用硫酸浸出回收电池中的镍、钴、锰,考察了碳热还原温度、碳热还原时间、浸出时间、浸出温度、搅拌速率、硫酸浓度等对Li、Ni、Co和Mn四种元素浸出的影响,得到最佳的浸出条件,为废旧锂离子电池三元正极材料的综合回收提供参考。
1 实验
1.1 原料与试剂
实验用废旧三元锂离子电池为某厂 NCM523软包锂离子动力电池,经过简单拆解后研磨,在干燥烘箱内以100 ℃烘干3 h。采用CPMS-2030型电感耦合等离子体发射光谱仪(ICP-OES)测得拆解后物料的主要成分见表1。实验用硫酸为工业级98%硫酸,水为工业纯水。
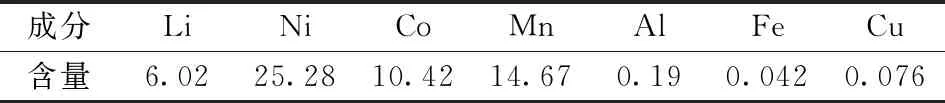
表1 拆解料的主要成分
1.2 实验方法
选择烘干后的破碎料120 g与工业焦粉(固定碳含量81.26 %)按照质量比3∶1进行混合,并置于马弗炉中焙烧。乙炔黑和粘结剂PVDF的分解温度分别306 ℃和316 ℃[11],但NiO、CoO、Co3O4和MnO2由于金属—氧键的结合能较高,需要足够的能量来破坏,因此,本文碳热还原温度选择为550、600、650、700 ℃,在最优的还原温度下研究碳热还原时间对锂浸出率的影响。反应过程中发生的电解质、PVDF分解和正极材料的还原的化学反应见式(1)~(4)。
LiPF6=LiF+PF5
(1)
(CH2-CF2-CH2-CF2)=(CH2-CF=
CH-CF2)+HF
(2)
Li(NixCoyMn1-x-y)O2+(1+2x+2y)/4C=
1/2Li2O+xNi+yCo+(1-x-y)MnO+
(1+2x+2y)/4CO2
(3)
Li2O+CO2=Li2CO3
(4)
将碳热还原后物料冷却并研磨、筛分,选择样品20 g作为实验料,碳热还原反应生成的镍、钴、锰均不溶于水,LiCO3溶解于水,利用常温水浸可以实现锂与镍、钴、锰的分离。由于LiCO3的溶解度随体系温度的增加而降低[12],在体系温度一定的情况下,水浸过程的液固比和浸出时间是影响锂浸出率的重要因素,液固比越小,可溶解物质的质量越小,浸出时间较短时,产物溶解不充分,也会影响水浸过程中锂的浸出率。因此,水浸过程也主要考虑这两种因素,通过锂元素的浸出率来确定最佳的碳热还原条件。
在最佳的碳热还原温度和水浸条件下,对废旧锂离子电池进行选择性提锂。将水浸后的渣放入烘箱,在100 ℃下烘干5 h得到酸浸提取镍、钴、锰的实验样品,通过单因素实验研究不同硫酸浓度、液固比、温度、反应时间、搅拌速率对镍、钴、锰浸出过程的影响,并计算浸出率。将单因素实验得到的最优组合进行综合性试验验证,确定该类型废旧锂离子电池最佳的回收工艺,对废旧锂离子电池中有价金属的综合回收利用提供参考。
2 结果与分析
2.1 Li元素最佳浸出条件的确定
固定碳热还原时间60 min、水浸温度25 ℃、液固比(mL/g,下同)10、搅拌速度100 r/min、水浸时间为90 min时,不同碳热还原温度下锂的浸出率如图1(a)所示。随着碳热还原温度的增加,锂的浸出率呈现出先增加后降低的趋势。这是因为,当温度较低时,电池材料被还原的程度较低,粘结剂和电解质解离不够完全,导致浸出困难;温度过高时,会造成Li2CO3的挥发而损失[13]。所以选择650 ℃为该研究条件下的适宜温度,此时具有较高的锂浸出率(84.52%)。
固定碳热还原温度650 ℃、水浸温度25 ℃、液固比10、搅拌速度100 r/min、时间90 min时,不同碳热还原时间下锂的浸出率如图1(b)所示。可以看出,随着碳热还原时间的延长,锂的浸出率呈现先增加后降低的趋势。随着碳热还原时间的延长,废旧电池正极材料的还原程度和结晶度增加,镍和钴都被还原成单质,此时锂的浸出较为容易。但随着时间的延长,会造成少量锂的挥发,所以较长的反应时间反而使得锂的浸出率降低,因此选择100 min为该研究条件下的适宜碳热还原时间,此条件下锂浸出率较高(88.21%)。
固定碳热还原温度650 ℃、碳热还原时间100 min,水浸温度25 ℃、搅拌速度100 r/min、时间90 min时,不同液固比下锂的浸出率如图1(c)所示。由图1(c)可知,随着反应体系液固比的增加,锂的浸出率呈现出先增加后降低的趋势。适宜液固比选择12,此条件下具有较高的锂浸出率(89.69%)。
固定碳热还原温度650 ℃、碳热还原时间100 min,水浸温度25 ℃、液固比12、搅拌速度100 r/min时,不同水浸时间下锂的浸出率如图1(d)所示。从图1(d)可以看出,随着水浸时间的延长,锂的浸出率呈现出先增加后趋于平缓的趋势。基于能耗和成本的考虑,适宜的水浸时间选择为120 min,此条件下具有较高的锂浸出率(91.68%)。
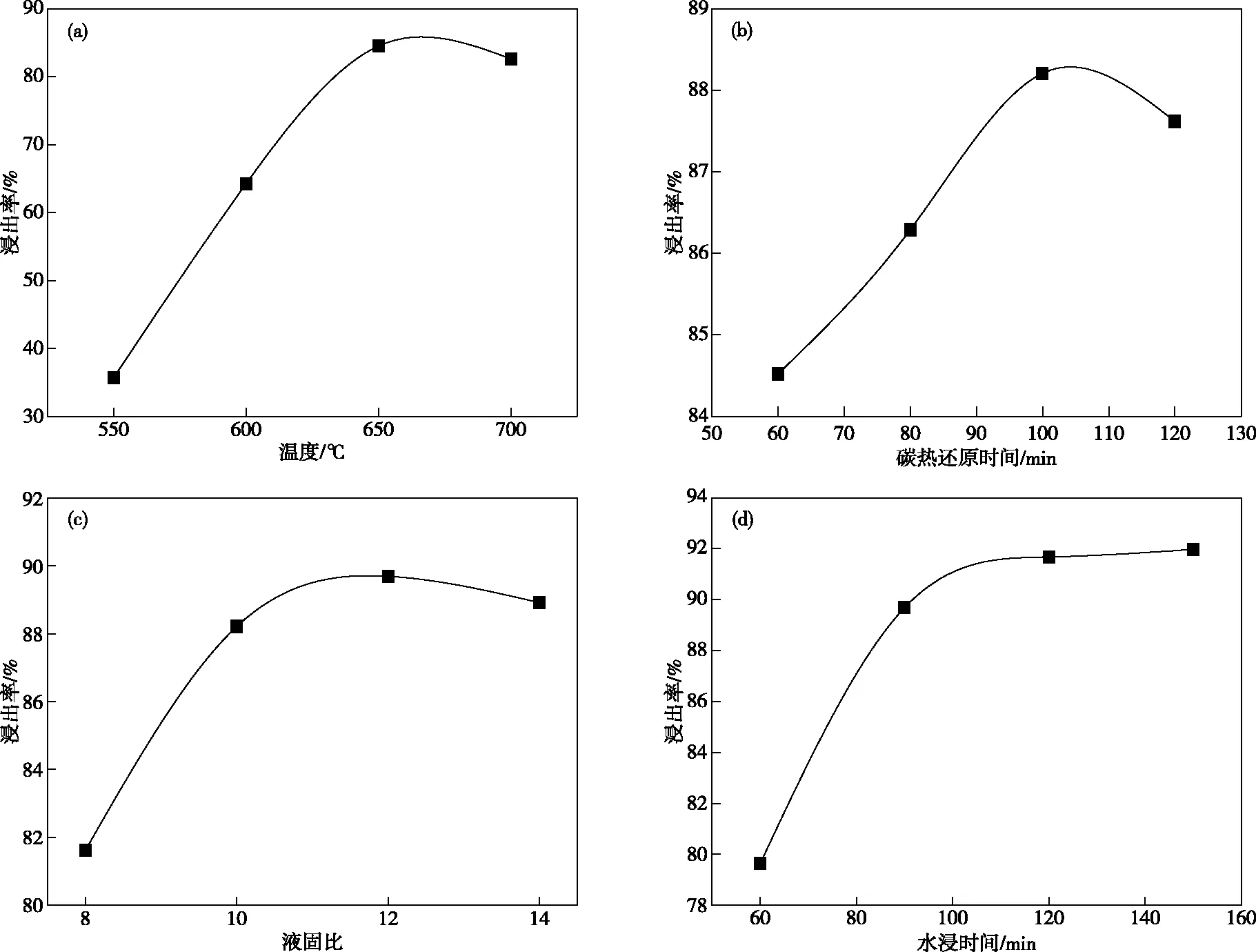
图1 不同碳热还原与水浸条件下锂的浸出结果
综上所述,较为适宜的碳热还原条件和水浸条件为:碳热还原温度650 ℃、碳热还原时间100 min;水浸温度25 ℃、水浸液固比为12、搅拌速度100 r/min、水浸时间120 min;该工艺条件下的锂浸出率较高(91.68%)。
2.2 镍、钴、锰元素最佳浸出条件的单因素实验
2.2.1 硫酸浓度对镍、钴、锰浸出率的影响
当浸出温度为60 ℃、搅拌转速为150 r/min、液固比为7、浸出时间为60 min时,硫酸浓度对水浸渣中镍、钴、锰浸出率的影响如图2所示。随着硫酸浓度的增加,各属元素的浸出率先增加后趋于平缓。这是因为,反应初期酸的浓度大,单位体积内提供的活性分子多,各组分的接触概率高,从而浸出率高。酸浓度继续增加时,由于受到体系限制,各元素的浸出率趋于平缓。综合考虑,最优硫酸浓度选择为2.0 mol/L,此条件下,Ni、Co、Mn的浸出率分别为77.64%、78.68%、80.99%。
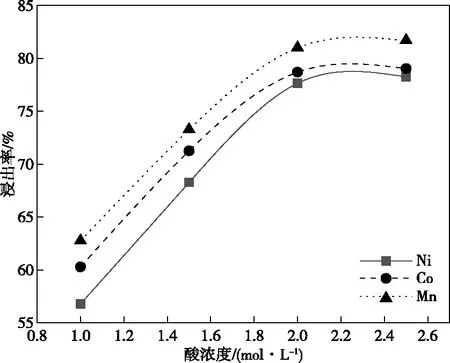
图2 硫酸浓度对水浸渣中镍、钴、锰的浸出率的影响
2.2.2 浸出温度对镍、钴、锰浸出率的影响
当硫酸浓度为2.0 mol/L、搅拌转速为150 r/min、液固比为7、浸出时间为60 min时,浸出温度对水浸渣中镍、钴、锰浸出率的影响如图3所示。各元素的浸出率随反应温度升高而增大,当温度大于 75 ℃后,浸出率基本变化不大。这是因为,随着温度的升高,活化分子数增加,分子之间的化学碰撞概率增加,反应速率增加,各元素的浸出率增加,但后期逐渐升温各元素的浸出率变化不大。综合考虑,认为75 ℃为该条件下的最优反应温度,此时Ni、Co、Mn的浸出率分别为81.56%、82.34%、86.81%。
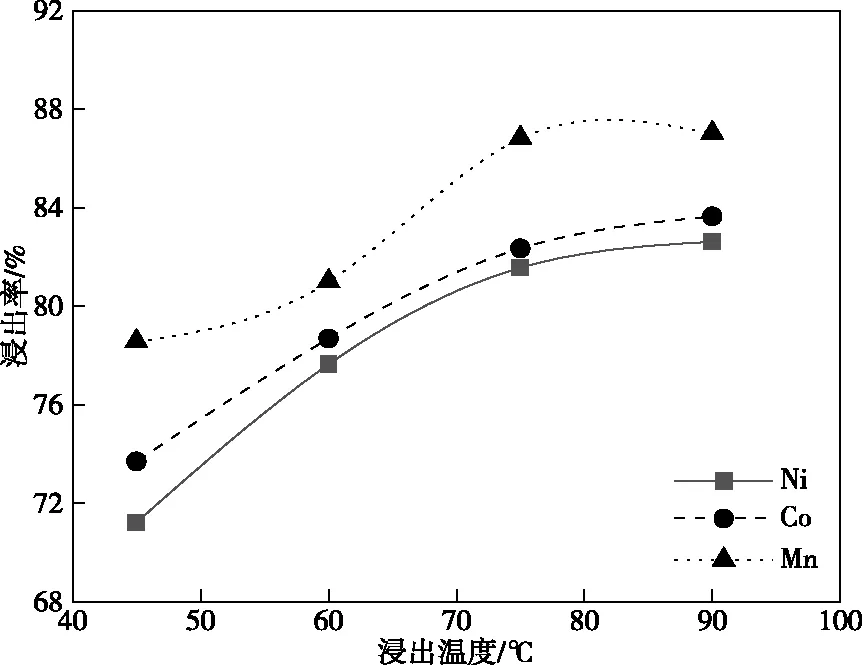
图3 浸出温度对水浸渣中镍、钴、锰的浸出率的影响
2.2.3 搅拌转速对镍、钴、锰浸出率的影响
当硫酸浓度为2.0 mol/L、浸出温度为75 ℃、液固比为7,浸出时间为60 min时,搅拌转速对水浸渣中镍、钴、锰的浸出率的影响如图4所示。随着搅拌强度的增加,镍、钴、锰三种元素的浸出率呈现先增加后平缓的趋势,在200 r/min时达到峰值。这是因为,加强搅拌强度可使反应体系中不同两相界面的相对运动增加、使得外扩散条件改善、加快了扩散反应速率。综合考虑,最优反应搅拌强度选择为200 r/min,在该条件下的Ni、Co、Mn的浸出率分别为85.92%、86.69%、89.08%。
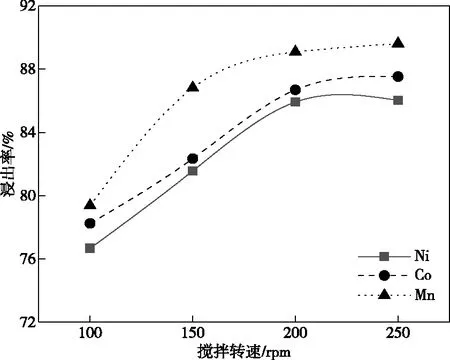
图4 搅拌转速对水浸渣中镍、钴、锰的浸出率的影响
2.2.4 液固比对镍、钴、锰浸出率的影响
当硫酸浓度为2.0 mol/L、搅拌转速为200 r/min、浸出温度为75 ℃、浸出时间为60 min时,液固比对水浸渣中镍、钴、锰浸出率的影响如图5所示。可以看出,各元素的浸出率呈现先增加后趋于平缓的趋势,这是因为,液固比较小时,矿浆浓度较大,部分矿物被包裹,浸出不完全,导致浸出率较低;随着液固比的增加,反应体系扩散条件得以改善,反应速率加快,使得镍、钴、锰的浸出效率逐渐增加。当液固比大于9时,镍、钴、锰的浸出率趋于平缓,基本保持不变,说明不再是扩散。综上所述,最优反应液固比9,此条件下的Ni、Co、Mn浸出率分别为90.51%、91.63%、93.06%。
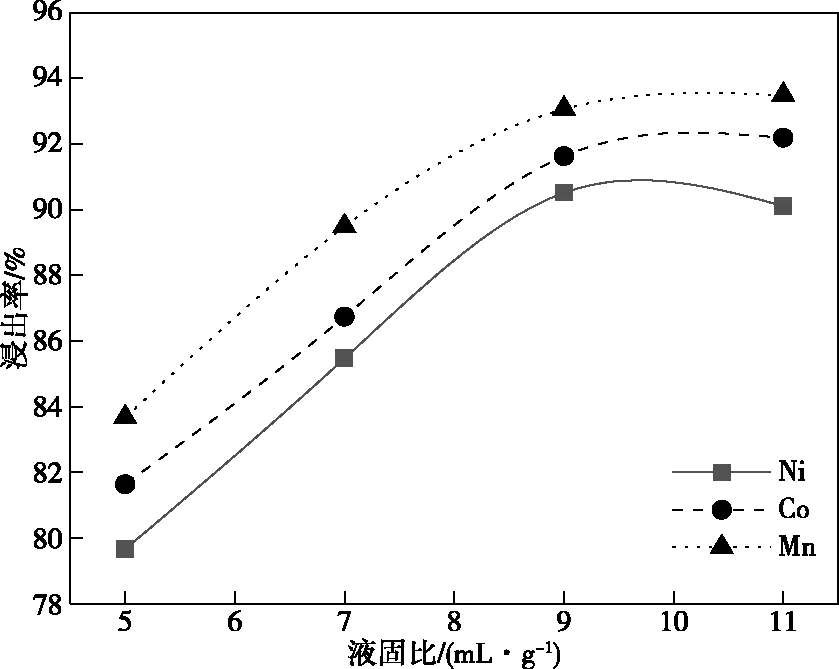
图5 液固比对水浸渣中镍、钴、锰的浸出率的影响
2.2.5 浸出时间对镍、钴、锰浸出率的影响
当硫酸浓度为2.0 mol/L、搅拌转速为200 r/min、液固比为9、浸出温度为75 ℃时,浸出时间对水浸渣中镍、钴、锰的浸出率的影响如图6所示。随着浸出时间的延长,各元素的浸出率变化趋于平缓,反应初期,随着时间的延长,水浸渣与酸反应更加完全,镍、钴、锰不断浸出。当反应时间再继续延长后,浸出率变化不大,这是因为,部分碳热还原过程中仍然有少量的高价镍、钴不易浸出。综合考虑,90 min为该条件下的最优反应时间,此条件下的Ni、Co、Mn浸出率分别为95.66%、96.02%、97.88%。
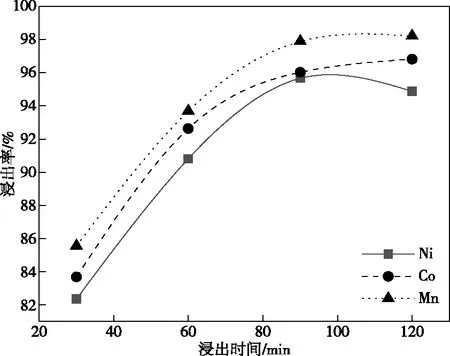
图6 浸出时间对水浸渣中镍、钴、锰的浸出率的影响
2.3 综合性试验
结合碳热还原、水浸和单因素试验结果可知,锂、镍、钴、锰的最佳浸出条件为:碳热还原温度650 ℃、碳热还原时间100 min、水浸温度25 ℃、水浸液固比12、搅拌速度100 r/min、水浸时间120 min,水浸后提取锂;将水浸渣烘干后的最佳硫酸浸出条件为:硫酸浓度2.0 mol/L、搅拌转速为200 r/min、液固比9、浸出温度75 ℃,浸出时间90 min。为了验证此条件下镍、钴、锰三种元素浸出的稳定性和优化条件的准确性,进行了4组综合试验,结果如表2所示。由表2可知,该组合优化条件下,锂、镍、钴、锰的浸出比较稳定,浸出率波动不大,锂的平均浸出率为91.61%,镍的平均浸出率为95.83%,钴的平均浸出率为96.22%,锰的平均浸出率为98.02%,实现了废旧电池中有价金属的循环再利用。
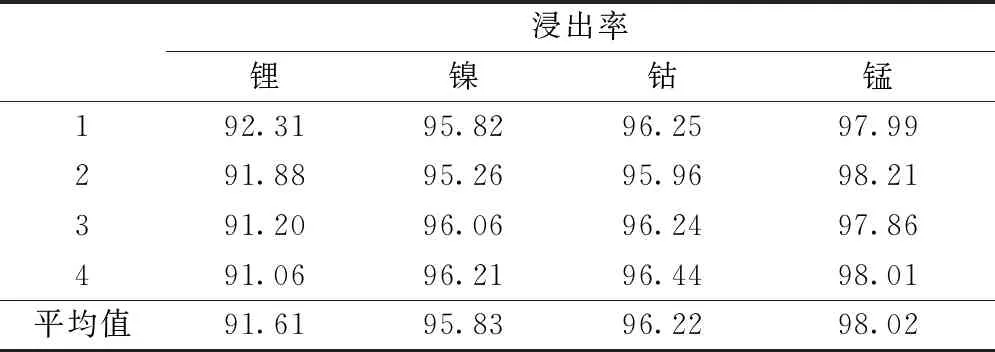
表2 综合性试验结果
3 结论
1)利用碳热还原、水浸提取锂后再进行湿法浸出是一种较为高效的三元废旧锂离子电池中有价金属的回收方法。
2)碳热还原—水浸最佳工艺条件为:还原温度650 ℃、还原时间100 min、水浸温度25 ℃、水浸液固比12、水浸搅拌速度100 r/min、水浸时间120 min,在该最佳条件下的锂浸出率可达91.61%。
3)硫酸浸出提取镍、钴、锰的最佳浸出条件为:硫酸浓度2.0 mol/L、搅拌转速200 r/min、液固比为9、浸出温度75 ℃、浸出时间90 min,在该最佳浸出条件下得到镍浸出率为95.83%,钴浸出率为96.22%,锰浸出率为98.02%

