程序性死亡受体1抑制剂治疗远处转移鼻咽癌疗效观察
李冰妍,陈林会,郑颖娟,梁天嵩,杨道科
(郑州大学第一附属医院放疗科,河南 郑州 450052)
鼻咽癌是来源于鼻咽黏膜上皮的恶性肿瘤[1],具有明显的区域和种族流行特点。在中国南方和东南亚,其发病率和死亡率均高于世界平均水平(1.2/10万、0.7/10万),分别占全球鼻咽癌发病和死亡的38.29%和40.14%[2-3]。由于鼻咽癌早期症状缺乏特异性,约70%的鼻咽癌患者首诊时即为局部晚期,治疗后远处转移率为15%~30%[4]。尽管放疗技术有了很大的改进,同时化疗也广泛用于局限性疾病,但大约20%~30%的病例会复发[5]。局部晚期或转移性复发的鼻咽癌预后很差。全身治疗选择非常有限,一线治疗方案均为以铂为基础的联合化疗,没有标准的二线治疗。因此,迫切需要新的肿瘤特异性治疗策略。
程序性死亡蛋白1(programmed cell death protein 1,PD-1)是Ⅰ型跨膜糖蛋白,由IgV域组成,与细胞毒性T淋巴细胞相关蛋白4、CD28和诱导型共刺激分子具有21%~33%的序列同一性[6]。由于PD-1缺乏CD28家族其他成员同型二聚化所需的膜近半胱氨酸残基,其通常单体形式出现于细胞表面[7]。PD-1有2个配体,PD-L1和PD-L2,这2个配体都是跨膜蛋白B7家族的成员,PD-L2的表达主要局限于抗原呈递细胞,而PD-L1表达于多种细胞,包括T细胞、B细胞、单核细胞、抗原呈递细胞和上皮细胞,在肿瘤细胞中也有明显表达[6,8]。目前PD-1抑制剂在结外NK/T细胞淋巴瘤、恶性黑色素瘤等临床试验中疗效和安全性均得到证实[9]。针对PD-L1/PD-1轴的抗体在多个临床试验中进行评估,并已被批准用于黑色素瘤、非小细胞肺癌、肾细胞癌、霍奇金淋巴瘤、膀胱癌、默克尔细胞癌和微卫星不稳定高或错配修复缺陷实体肿瘤等[10]。但目前针对晚期鼻咽癌的临床研究相对较少。研究[11]发现,PD-L1可以促进鼻咽癌细胞上皮间质转化,进而促进转移。此外,研究[12]还发现EB病毒阳性鼻咽癌的一个共同特征是肿瘤基质中淋巴细胞的密集浸润和肿瘤细胞中PD-L1的阳性表达,以上研究使其成为免疫治疗有吸引力的靶点。我们采用PD-1抑制剂治疗7例远处转移鼻咽癌患者,收集患者的临床资料以及用药结果并总结如下。
1 资料与方法
1.1 一般资料收集2019年06月到2020年11月郑州大学第一附属医院收治的远处转移鼻咽癌患者中7例应用PD-1抑制剂者,患者采用卡瑞利珠单抗或信迪利单抗治疗。所有患者诊断分期均根据美国AJCC第8版分期标准进行临床分期。
1.2 方法应用PD-1抑制剂的患者中有2例选择同期放化疗+辅助化疗作为初治治疗方案,2例选择诱导化疗2个周期后放疗+辅助化疗,3例选择放疗后辅助化疗。同期放化疗采用以铂类+氟尿嘧啶/尼妥珠单抗为主的方案,诱导化疗则选择多西他赛+顺铂+氟尿嘧啶或多西他赛+顺铂方案,辅助化疗选用多西他赛+顺铂+氟尿嘧啶、多西他赛+顺铂或奥沙利铂+雷替曲塞方案。在放化疗治疗结束后,患者出现远处转移,又采用局部微波射频手术以及全身化疗等方案继续治疗,治疗失败后选择应用PD-1抑制剂作为挽救治疗,5例选用卡瑞利珠单抗,2例选用信迪利单抗,治疗剂量为200 mg(21 d为1个周期),中位周期数为2(1~6)个。PD-1抑制剂治疗后,有1例(例2)进行了化疗(奥沙利铂+雷替曲塞+贝伐单抗)。见表1。
1.3 疗效判定按照WHO疗效评价标准RECIST 1.1进行疗效判定,近期疗效分为完全缓解、部分缓解、病情稳定、病情进展,客观缓解率(objective response rate,ORR)是指肿瘤体积缩小达到预先规定值并能维持最低时限要求的患者比例,以完全缓解+部分缓解计算。疾病控制率(disease control rate,DCR)指肿瘤缩小或稳定且保持一定时间的患者的比例,以完全缓解+部分缓解+病情稳定计算。疾病无进展生存时间(progression-free survival,PFS)定义为从患者确诊至疾病进展、死亡或随访终点的间隔时间。总生存时间定义为从患者确诊至患者死亡或随访终点的间隔时间。
1.4 随访随访截止时间为2020年11月,中位随访时间为23(14~47)个月,通过患者门诊复查或电话联系随访。
2 结果
2.1 临床病理特征7例患者中,男5例,女2例,中位年龄为53(32~64)岁。确诊时均为局部晚期(Ⅲ、Ⅳ期)鼻咽癌。见表1。
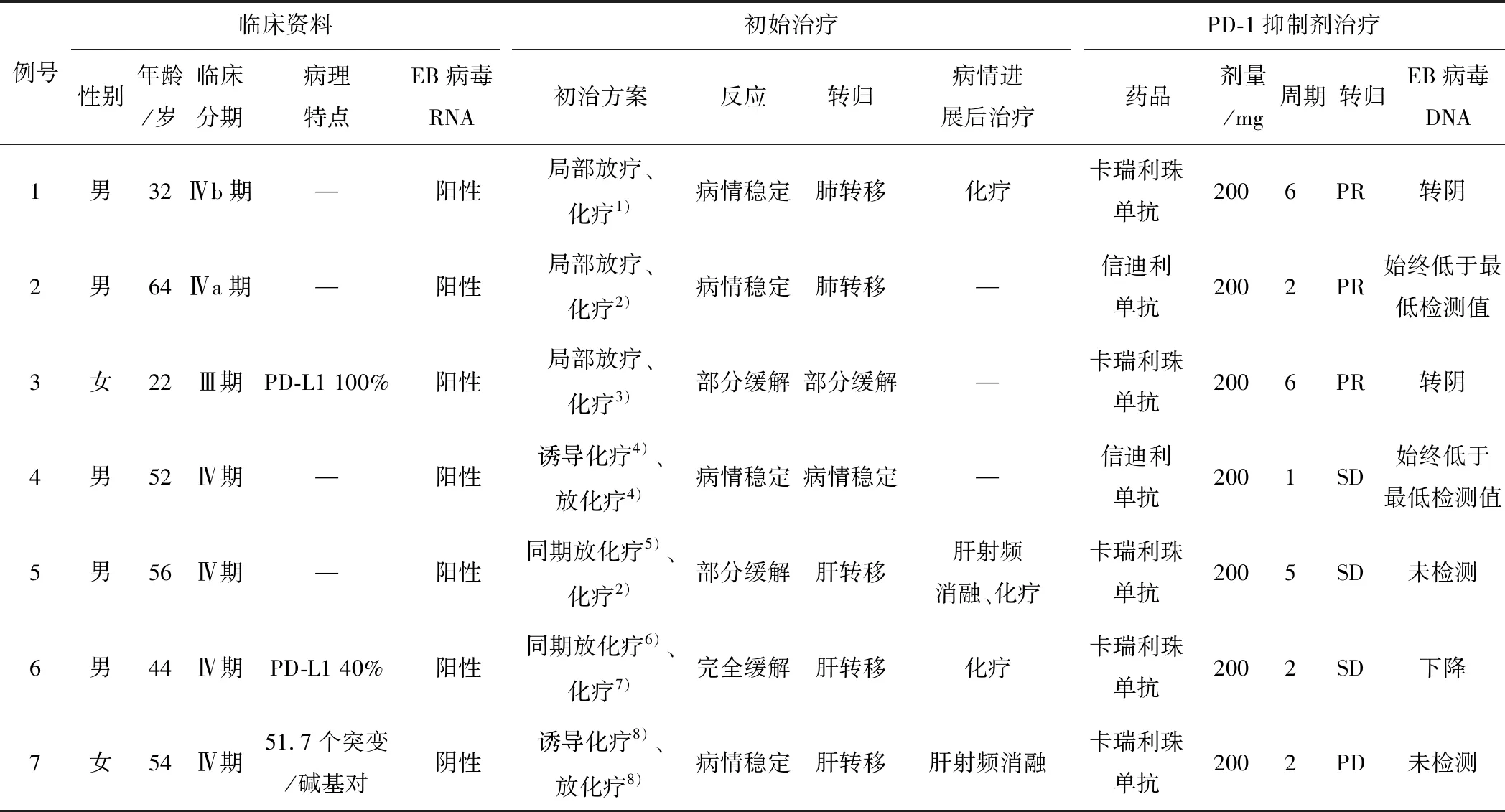
表1 7例应用PD-1抑制剂患者临床资料及治疗方式
2.2 EB病毒7例患者均在初诊时病理检测EB病毒编码RNA,其中有6例阳性,1例阴性。外周血EB病毒DNA检测结果及随治疗变化情况见表2。
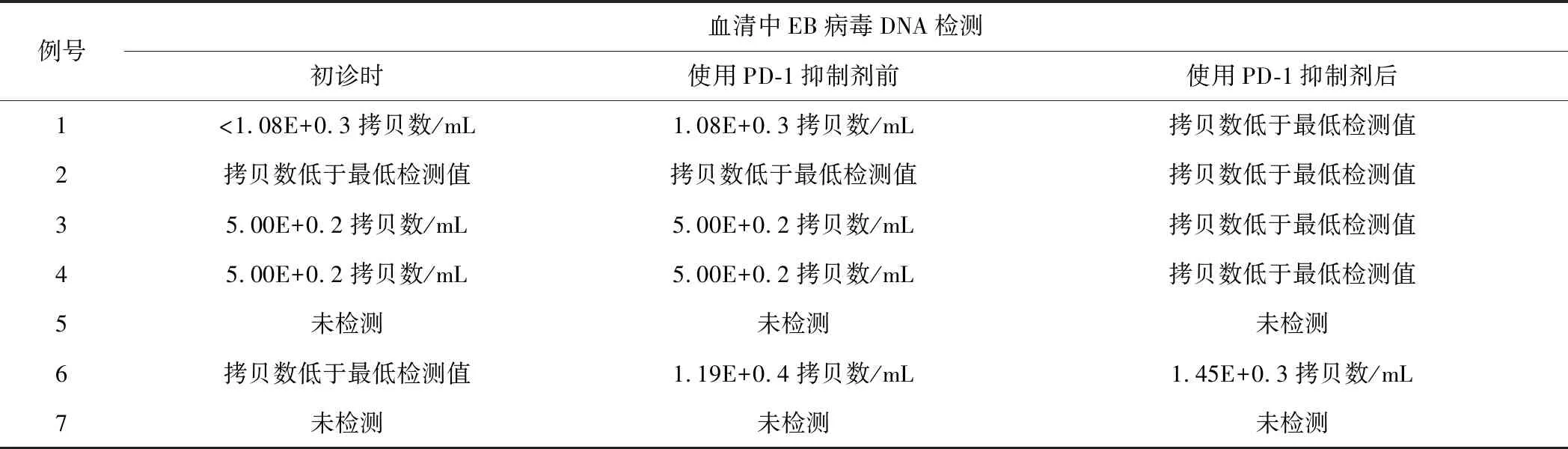
表2 7例局部晚期鼻咽癌患者EB病毒感染情况
2.3 疗效与转归初始治疗结束后,7例患者中4例获部分缓解,2例病情稳定,1例病情进展。之后有2例肺转移、3例肝转移。应用免疫抑制剂后7例患者中,3例达到部分缓解,3例病情稳定,1例病情进展。ORR为42.9%,DCR为85.7%。不良反应:1例出现皮疹。1例出现了Ⅳ度骨髓抑制。1例在应用1个周期后出现了免疫性肺炎后停药。
2.4 随访结果截止至随访结束,7例患者中1例死亡,6例存活。3例PR或SD患者仍处于相对稳定状态,3例患者支持治疗中,由于用药时间尚短,暂不能看出PD-1抑制剂对远处转移鼻咽癌PFS及总生存期的影响,需继续进一步随访。
3 讨论
鼻咽癌对放疗敏感,早期患者放疗后的5 a生存率达70%以上[13],但因其具有侵袭性强和易转移的特点[14],容易浸润周围组织间隙,并出现颈部淋巴结转移,4%~10%的初诊鼻咽癌可发生远处转移[15-16]。目前复发或转移性鼻咽癌的治疗方案有限,主要治疗手段包括再程放疗、挽救手术、化疗、靶向治疗等。通过手术和再程放疗来治疗局部复发鼻咽癌效果不佳,5 a生存率只有30%~40%[17]。而复发或远处转移患者多对全身化疗发生耐受。近年来,随着对免疫检查点抑制剂的不断深入研究,免疫治疗已成为多恶性肿瘤新的治疗方案。随着对EB病毒、鼻咽癌和免疫微环境的进一步研究,发现鼻咽癌组织中存在丰富的免疫细胞间质浸润和EB病毒抗原表达,这为鼻咽癌的免疫治疗提供了更多的理论依据[18]。
免疫逃逸是肿瘤发生的一个重要标志,鼻咽癌也不例外。鼻咽癌的病理特征为间质内大量非恶性免疫细胞浸润。这些细胞主要由CD3+T细胞组成,其次是CD8+T细胞、B细胞、调节性T细胞、自然杀伤细胞、中性粒细胞、树突状细胞和肥大细胞[19]。活跃的肿瘤细胞与丰富的免疫浸润共同存在,表明鼻咽癌微环境中存在潜在的免疫抑制。事实证明,鼻咽癌细胞中致密的免疫浸润并没有发挥抗肿瘤活性而是与鼻咽癌的生长和侵袭特性有关[20]。在鼻咽癌中,潜伏的EB病毒抗原潜伏膜蛋白-1上调PD-L1的表达,PD-L1在患者之间以及在肿瘤和免疫细胞之间有不同的表达[21-22]。研究[22-23]发现,PD-L1和(或)PD-1的高表达与患者较差的生存结果具有相关性。鼻咽癌是一种表达EB病毒抗原的免疫原性肿瘤。以前,人们认为与其他恶性肿瘤相比鼻咽癌的体细胞突变相对少见的[24],考虑其致癌性大部分来源于EB病毒的驱动。然而,最近对鼻咽癌活检组织进行的全外显子组和全基因组测序分析发现了比先前报道的更高的肿瘤突变负荷[25]。从理论上讲,这些编码突变会导致新抗原的表达,这与免疫检查点抑制的敏感性呈正相关。
免疫检查点主要通过调节免疫来维持机体正常免疫功能[7]。目前研究的免疫检查点主要有PD-1、PD-L1以及CTLA4等,其中,PD-1研究较多的分子,主要表达在活化T细胞以及其他免疫细胞的细胞膜上[26]。PD-1与其配体PD-L1结合后,胞质区ITSM结构域中酪氨酸发生磷酸化,从而抑制B、T细胞增殖,IFN-γ和IL-2等细胞因子的产生,以及免疫球蛋白的分泌,进而抑制自身免疫应答[6]。抗PD-1免疫疗法现已成为转移性或复发性头颈部鳞癌的标准治疗方法[27-28]。抗PD-1药物在其他病毒相关恶性肿瘤如人乳头瘤病毒感染的头颈部鳞癌、默克尔细胞癌、霍奇金淋巴瘤和肝细胞癌中也有疗效[5,28]。国内进行了2个Ⅰ期试验,均应用人源化抗PD-1抗体,卡瑞利珠单抗进行治疗[29-30]。第1个试验招募93例治疗难治性复发或转移性鼻咽癌患者。安全评价令人满意,有16%的患者发生了与≥3级治疗相关的不良事件。毛细血管瘤伴血管过度增殖反应在88%的患者中是常见的现象。ORR和中位PFS分别为34%和5.6个月。第2个试验研究了卡瑞利珠单抗单抗与吉西他滨-顺铂在一线姑息治疗中的联合应用。23例患者中有20例(87%)经历了与≥3级治疗相关的不良事件,最突出的不良反应为全身骨髓抑制、水肿和低钠血症。ORR高达91%,12个月PFS率为61%。此外,一项第3阶段的试验正在进行中,以评估卡瑞利珠单抗在同期放化疗(NCT03427827)后的作用。
在本研究中,我们应用的PD-1抑制剂为卡瑞利珠单抗及信迪利单抗,治疗的7例患者中,3例达到部分缓解,3例病情稳定,1例病情进展。反映良好的3例在第1个疗程即出现了疾病改善。ORR为42.9%。1例出现皮疹。1例出现了IV度骨髓抑制。1例在应用1个周期后出现了免疫性肺炎后停药。由于用药时间尚短,暂不能看出PD-1抑制剂对晚期复发鼻咽癌PFS及总生存期的影响,需继续随访。从本研究中发现,PD-1抑制剂对EB病毒编码RNA阳性反应尚可,且对EB病毒DNA拷贝数高的患者反应更好,且应用后对EB病毒DNA拷贝数有影响,可降低EB病毒DNA拷贝数。本研究中对患者PD-L1检测较少,暂无初始判断。今后需进一步完善病理中PD-L1检测,以及对PD-1抑制剂应用时机及联合化疗用药选择进一步探讨。
综上所述,我们应用PD-1抑制剂治疗7例远处转移鼻咽癌患者,6例有效,初步说明PD-1抑制剂对于晚期难治性及复发转移鼻咽癌患者是一个有效挽救方案。此外,部分患者应用药物后出现了皮疹及免疫性肺炎等副反应,因此,后续我们应该对鼻咽癌患者应用PD-1抑制剂的纳入标准,以及联合其他化疗药物应用等进行进一步研究和探讨。

