乳品微生物耐药性影响及防治途径研究进展
周浩,刘继超,赵军英,乔为仓,刘璐,郑健强,陈历俊
(1.北京三元食品股份有限公司,北京100163;2.大连工业大学生物工程学院,辽宁大连116034)
0 引 言
乳业是现代农业和食品工业重要组成部分,是健康中国、强壮民族不可或缺的产业。目前我国已跻身世界乳品生产和消费大国之列,据相关机构统计数据表明,中国乳牛最高存栏量曾达到1 700万头,2019年存栏维持在500余万头;2018年牛乳年产量达3 750万t,乳制品消费量接近4 000万t。低效的家庭饲养逐渐被高效的规模化养殖替代,截至2019年全国64%牧场形成规模化养殖,奶牛存栏量从几百头到上万头不等。几乎所有牧场都实现机械化,并且随着人工智能的发展,智能养殖、智慧农牧等概念也不断被提出。而随着养殖方式的改变,各种问题也接踵而来。高度集中的饲养方式导致传染病发生率提高,作为治疗首选的抗生素在畜牧养殖业中大量使用,使得环境中耐药微生物及耐药基因数量急剧增加并随食物链等途径不断扩散。微生物耐药即微生物进化过程中对抗菌药物耐受性的增强,不但会影响药物的疗效增加治疗成本,还可能对人体免疫机制及其它生理特性造成影响。随着我国乳品需求的增加,乳品安全问题成为关注焦点,而要提高乳品品质,原料奶生产环节不容忽视。本文主要针对牧场乳牛养殖中抗生素使用及其所导致的耐药性扩散问题,就生鲜乳中耐药微生物、耐药基因影响现状,以及牧场中主要存在问题和相关防治途径进行论述,旨在为牧场中抗生素使用和耐药微生物防治提供参考。
1 微生物耐药性产生及现状
1.1 微生物耐药性产生
1.1.1 乳品中微生物耐药性产生原因
生鲜乳极富营养,所以比其它食品更易受到微生物污染,加之生产环节复杂繁多,牛奶卫生质量极易受到各种因素影响[1-2]。牧场是生鲜乳生产中微生物污染的一个主要环节,见表1。有证据表明,生鲜乳中主要致病微生物之一的李斯特菌可在农场挤奶设备上聚集[3],并且其在生产设备上形成的生物膜(BBF)还是罐装牛奶中单核增生李斯特菌的潜在污染源[4]。由于生物膜膜内基因元件转移[5]、渗透屏障[6]、内部环境改变[7]和群体感应(QS)系统调节[8]等机制的影响,其在微生物耐药性产生过程中也起到很大作用[9]。其次由于生物安保不完善等问题导致子宫炎、乳房炎等疾病发病率提高,在治疗过程中大量使用甚至是滥用抗生素。而微量抗生素的使用就可能在微生物耐药性的发展和传播中发挥重要作用[10],1928年发现青霉素后几年内由于抗生素的使用金黄色葡萄球菌就进化出了专门降解抗生素的β-内酰胺酶[11]。部分牧场在对畜群日常管理中无法严格把控各类药物的用法用量,造成抗生素的过量投放,而有研究表明多种抗生素的联合使用可能会对其它敏感抗生素耐药性造成影响[12]。此外一些中小型牧场缺乏成型的抗性检验环节,难以有效应对耐药微生物的不断更替。

表1 牧场中可能导致微生物污染及其耐药性的主要因素
1.1.2 抗生素使用现状
我国畜牧养殖业中滥用抗生素的问题较为严重,2012年奶牛畜禽抗生素支出在20亿元以上,其导致养殖动物及相关环境中存在大量耐药基因以及耐药细菌,可能对生态环境、食品安全和人类健康造成威胁[13]。虽然目前欧美等国家已严格限制了畜牧养殖业中抗生素的使用[14],我国抗生素用量也呈逐年降低的趋势,见表2。但许多发展中国家抗生素使用量仍快速增长,2000年至2015年间全球抗生素用量增加了65%,且增长速度呈上升趋势[15]。
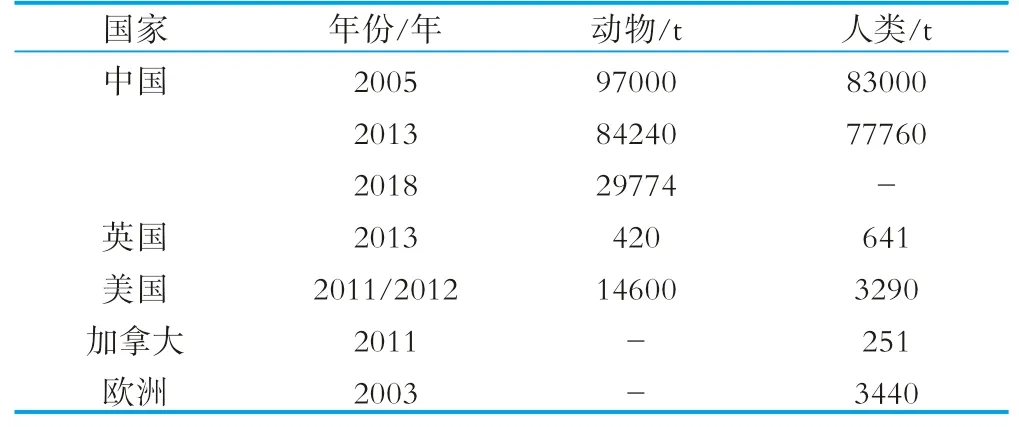
表2 部分国家抗生素使用总量分布情况[16-17]
1.2 微生物耐药现状
1.2.1 耐药微生物危害现状
目前,耐药微生物(ARB)导致全球每年超70万人死亡,其中美国每年发生280余万例耐药菌感染,导致3.5万例死亡[18];欧盟每年至少2500名患者死于耐药菌感染。并且“紧急威胁”耐药微生物数量已增加至5种,包括碳青霉烯类耐药肠杆菌、耐药性淋球菌、艰难梭状芽胞杆菌、碳青霉烯类耐药不动杆菌和耳念珠菌。其中碳青霉烯类耐药不动杆菌是世界卫生组织列出的1类病原体,两年间其耐药率在英国两所医院内增加了30%[19]。随着碳青霉烯类抗生素临床上的广泛使用和过度治疗,其耐药范围已扩展至亚洲、欧洲以及非洲等多个地区[20]。
生鲜乳生产加工过程中不可避免会受到外界环境影响,而由于畜牧业抗生素的大量使用,乳品成为耐药微生物重要传播媒介,其随食物链传播过程中可能对生物肠道菌群丰度及耐药性等造成影响[21-23],并通过影响菌群所介导的脂肪酸代谢等免疫反应调节因子而干扰抗体对流感疫苗反应[24],还可间接增加结肠癌发生率[25],对人体健康造成威胁。已有研究表明,牧场中超级细菌之一耐甲氧西林金黄色葡萄球菌(MRSA)菌株检出率较高,并且其耐药基因(ARGs)检出率显著高于甲氧西林敏感金黄色葡萄球菌(MSSA)菌株,见表3,多位点序列分型中还出现MRSA-IV型菌株[26-29]。由于乳品中金黄色葡萄球菌等有害微生物耐药性的增强,其三年间对澳大利亚、中国和瑞士等国家共造成200余例奶源性微生物感染事件的爆发[30]。即便是高温灭菌(UHT)乳,其残留的少量芽孢在特定环境下仍有可能继续繁殖。采用巴氏杀菌的低温奶和发酵乳,耐药微生物及耐药基因通过食物链进入人体的可能性更大[31]。

表3 金黄色葡萄球菌部分耐药基因及其作用机制[32-35]
1.2.2 传播现状
微生物耐药机制主要分为遗传学机制和生化机制两个方面,遗传学机制中获得性耐药基因是主要传播因素,其在牧场中转移现象可影响乳品中耐药微生物及耐药基因含量[36-37]。随着多黏菌素在畜牧养殖业中广泛使用,当下被普遍认为是对抗耐药细菌“最后防线”的多黏菌素mcr-1耐药基因或已通过食物链传播到中国健康人肠道菌群中[38]。美国CDC抗生素耐药问题高级顾问Michael Craig曾说过:“细菌非常聪明,学习能力超强”,在实验条件下,大肠杆菌对达到最低致死浓度1000倍的抗生素产生耐药性仅需10 d[39]。但在牧场中耐药基因也不是无限制传播,其受制于生态屏障并由种属进化关系所主导[40]。在对耐药基因转移机制的研究中通过活细胞显微镜发现,细胞中一个微小结构AcrAB-TolC多药物外排泵在耐药基因转移过程中起到关键作用[41],它在多数微生物中广泛存在通过短暂阻隔为携带有耐药基因质粒争取时间,介导了固有和获得性多药耐药[42]。已知外排泵系统主要包括耐药结节化细胞分化(RND)外排泵家族、主要易化因子超家族(MFS)、多重药物与毒性化合物外排家族(MATE)、小多重耐药外排泵家族(SMR)和ATP连接盒转运体家族(ABC)等[43]。即便是达到商业无菌的乳制品,由于基因在生物死后短时间内所维持的活性[44],仍有可能在多药物外排泵的帮助下影响肠道内细菌在基因水平上的药物抵抗机制。
2 乳品微生物耐药性检测及预防途径
2.1 微生物耐药性检测
目前对可培养微生物耐药表型传统检测方法如表4,主要包括肉汤稀释法、琼脂稀释法、E-test试纸法,K-B法、全自动仪器分析法等。随着分子生物学技术发展耐药基因检测常用PCR技术,较为便捷可靠,但对耐药基因可检测种类有局限性。而宏基因组学[45]凭借其可基于序列或功能筛选分析某种功能基因,并进一步深度测序的特性,是目前较有效的耐药微生物基因组分析手段。基于测序技术的应用,对于大量耐药基因的快速检测方法[46]也日趋成熟。

表4 微生物药物敏感性检测常规方法特点
2.2 生鲜乳中微生物耐药主要预防途径
生产加工是导致生鲜乳中耐药微生物污染的主要因素之一,应注重加强人员技术培训以及污染防控措施改进。若条件允许可针对整条生产链设置相应的监控环节,例如ATP荧光检测[51]、微生物测试片[52]以及全自动监测与采样系统[53]等生产链污染程度监控快检技术的应用。此外乳牛养殖中治疗各种疾病也会导致大量抗生素使用,乳房炎就是主要疾病之一。一方面要合理使用抗生素并加强监管[54];另一方面为避免将来无药可治,需不断寻求新的解决方法,深入研究细菌耐药机制尤为关键。如生物膜、主动外排系统、灭活酶产生、膜通透性改变、作用靶位改变[55]以及其它新发现的耐药机制如耐药癌细胞对脂质过氧化酶4(GPX 4)的依赖[56]等都需要更加深入的进行解析。
实际生产中应注重降低乳房炎患病率并寻找其它抗生素替代品及替代治疗方式减少抗生素使用,加强消毒管理并在饲料中添加富硒益生菌[57]降低患病率、对症下药控制抗生素使用、利用空气净化恒温恒湿等智能化养殖设备等都能有效缓解这一问题。此外,罂粟科植物提取物博落回(MCE)中含有的苄基异喹啉生物碱的有效成分,是一种促生长抗生素的潜在替代品[58]。在国外乳房炎治疗中,对于由大肠杆菌等引起的环境乳房炎还提倡自愈,但由于地域差异,这一方法并不适合国内乳房炎治疗。对于一些症状较轻的牛只还可采用疫苗、非淄类药物以及催产素促进致病菌外排。在非洲等地区还会采用人工多次放空乳房的方式进行治疗。国内治疗及预防乳房炎的方法主要包括疫苗、中草药[59]及抗生素等。其中中草药疗法见效慢,治疗不及时等问题还有待改进。目前国内只正式批准了抗生素作为治疗乳房炎的方法,因此,相关政策有待改进。
此外,还有噬菌体对病原微生物的裂解作用[60]、乳区注入生物氧(臭氧)灭活病原微生物[61]、影响细菌协同工作的胞外聚合物(EPS)生物膜抑制剂[62]、针对耐药菌感染多株细菌联合的微生态疗法[63]和针对耐药微生物群体感应(QS)系统的抑制剂中断疗法[64]等多种抗生素替代治疗方式,但实际疗效还有待进一步验证。整体来看,虽然目前对奶牛乳房炎等疾病的治疗方法种类较多,但实际生产中仍然对抗生素有很强依赖性,无法完全根治牧场中微生物耐药性加剧的问题。
3 总结与展望
生产生活中抗生素的大量使用导致微生物耐药性增强威胁人类健康。对于微生物耐药各国都在积极寻求解决方法,但尚无一个明确有效的方案。目前,畜牧养殖业中仍然对抗生素有较强依赖性。随着各国畜牧养殖业饲养规模的扩大,耐药微生物种类及其药物抵抗机制趋于复杂化,对人类威胁不断增加。因此,在实际生产中应着重于采取减少病原微生物感染的有效措施,建立完善的抗生素使用标准,加快微生物耐药机制研究及抗生素替代品开发,建立耐药微生物的全程控制技术。通过先进技术手段最大程度减缓微生物耐药性增强,减少其通过食物链传递对人类健康的危害,也为耐药微生物防治对策的制定提供理论支撑。

