含钙矿物表面转化行为及其在浮选中的应用
王若林 韩海生 孙 伟 孙文娟 卫 召 付君浩
(1.中南大学资源加工与生物工程学院,湖南 长沙 410083;2.中南大学战略含钙矿物资源清洁高效利用湖南省重点实验室,湖南 长沙 410083)
浮选是分离白钨矿与方解石、萤石、重晶石等伴生资源的有效手段[1-2]。钨矿及其伴生的萤石、方解石、重晶石均属于盐类矿物[3],在矿物浮选的矿浆系统中均会不可避免地发生溶解反应[4-5],溶出的离子在一定条件下可以与矿物表面发生反应,影响矿物表面物质组成和性质,从而改变钨矿物及伴生矿物的浮选行为。矿物浮选的矿浆体系涉及到气、液、固三相体系[6-7],必然与溶液化学息息相关。在单矿物浮选体系中,盐类矿物的溶解会释放出不同的离子[8],从而改变溶液组分[9-10]。而在两种或多种矿物共存的浮选体系中,由一种矿物溶解出的离子,会在另外一种或几种矿物的表面发生吸附作用,在充分反应的前提下完成表面转化[5,11]。因此,含钙矿物的表面转化通常分两步进行:一是不同溶解度的矿物溶出不同的离子进入溶液体系,二是离子作用于伴生矿物表面,使其具有其他矿物相同的性质。
含钙矿物及其伴生矿物之间的表面转化可以改变矿物表面电性[11-13]和定位离子[14]性质,影响浮选药剂对矿物的选择性吸附和浮选效果,是研究白钨矿、黑白钨混合矿浮选分离以及细粒黑钨矿浮选回收[15]的关键所在。盐类矿物的表面转化现象在浮选中普遍存在,如在磷酸盐矿物的浮选中,磷灰石表面转化生成方解石覆盖层的现象加大了矿物之间的分离难度,通常需要使用木质素铬铁盐加以抑制,才能实现磷灰石和方解石的浮选分离[5]。又如在萤石与方解石共存体系中,萤石在方解石矿物表面的转化会显著影响脂肪酸类捕收剂的选择性,通常需要使用酸化水玻璃对萤石的表面转化行为进行抑制[11]。由此可见,大多数研究都将矿物之间的表面转化定义为不利因素[16-17],并采取一系列手段削弱这一现象对浮选的影响。其实,矿物表面转化现象为提高伴生盐类矿物浮选选择性提供了全新的思路:通过定向表面转化反应将易被捕收剂捕收的脉石矿物表面转化生成难以被捕收的矿物或化合物,可以大幅度提高捕收剂的选择性,实现伴生盐类矿物的高效分离。例如,近年来在钨矿浮选中广泛应用的Pb-BHA配合物捕收剂[18-19]对白钨矿和方解石具有良好的捕收能力,但对萤石基本没有捕收能力[20]。在使用Pb-BHA配合物捕收剂浮选时,可以预先通过定向调控表面转化反应使易吸附Pb-BHA的方解石表面转化生成难以吸附Pb-BHA的萤石,从而进一步提高Pb-BHA的选择性捕收效果,实现钨与脉石矿物的高效分离。
本文以表面转化为基础,研究了白钨矿-萤石-方解石体系和白钨矿-萤石-重晶石体系中矿物表面转化行为及矿物浮选行为,并通过溶液化学计算、Zeta电位、X射线光电子能谱和原子力显微镜分析研究其表面转化和浮选作用机理,为半可溶性含钙矿物的高效回收利用提供了新的思路和方法。
1 试验材料及方法
1.1 试验样品
试验所用的白钨矿、萤石、方解石、重晶石均为纯度95%以上的单一纯矿物,购自中国长沙矿产宝石市场。纯矿物经过粗碎后,用陶瓷罐进行细磨,使粒度达到100%为-0.074 mm。取磨矿至-0.074 mm的部分样品,再磨至粒度小于2 μm,以备Zeta电位、XPS等测试使用。另取天然解理面较为平整的白钨矿、方解石和萤石单矿物固体,进行切割、冷嵌、磨平并充分抛光以备原子力显微镜观察使用。
1.2 试验药剂
试验及检测中所用的药剂均为分析纯。pH调整剂氢氧化钠、抑制剂氟化钠购买于广东省台山市化工厂;苯甲羟肟酸购买自长沙晶康新材料科技有限公司,硝酸铅购买于株洲化学试剂厂,两药剂按一定比例混合使用作为浮选捕收剂;起泡剂松油醇购买于天津市大茂化学试剂厂。
1.3 浮选试验
浮选试验所用仪器为XFG型挂槽式浮选机,主轴转速固定为1 680 r/min。单一纯矿物浮选试验操作如下:称取2 g纯矿物,加适量去离子水后搅拌1 min,按照pH调整剂→抑制剂→捕收剂→起泡剂的顺序依次加入药剂,每种药剂加入后调浆3 min,保持槽内液体总体积为40 mL。最后采用刮板手工刮取浮选泡沫,将精矿和尾矿分别烘干、称重,并计算回收率。
白钨矿-方解石混合矿由1 g白钨矿纯矿物与1 g方解石纯矿物混合而成,白钨矿-重晶石混合矿由1 g白钨矿纯矿物与1 g重晶石纯矿物混合而成。混合矿的试验方法与单一纯矿物的试验方法相同。最终精矿与尾矿产品分别称重后,用XRF分析各产品品位,并计算回收率。
1.4 Zeta电位测试
Zeta电位测试所使用的仪器为德国布鲁克ZetaPlus测试仪,测试温度为20℃。称取0.02 g粒度为-2 μm的测试样品,与40 mL浓度为10-2mol/L的KNO3背景电解质混合加入100 mL烧杯中制备矿物悬浮液。然后按浮选试验流程依次加入各药剂,搅拌时间与浮选试验相同。静置沉淀15 min后,取上清液进行Zeta电位测量。
1.5 X射线光电子能谱测试
XPS采用Thermo Fisher Scientific K-Alpha 1063 X系统进行测试,工作电压为12 000 V,仪器分辨率为0.50 eV。测试结果采用XPS peak进行分峰拟合。试验样品粒度为-2 μm,按照浮选试验流程依次加入药剂反应,并将加入药剂后的矿物悬浮液搅拌10 min,用去离子水洗涤3次、过滤置于50℃的真空烘箱中干燥后进行检测。
1.6 原子力显微镜测试
AFM采用Multimode V显微镜进行测试,测试中选择的测量模式为tapping mode,探头为RTESP-300-300型硅探头,共振扫描频率为1.5 Hz。将已经充分抛光的纯矿物样品薄片的待测表面用无水乙醇、去离子水多次冲洗,在原子力显微镜不同分辨率下观察并记录数据。将样品清洗后放入盛有一定浓度药剂溶液的烧杯中,搅拌10 min,然后用镊子取出,用去离子水清洗,经高纯氮气吹干后再次进行观察并记录数据。测试结果采用NanoScope Analysis软件进行分析。
2 试验结果与讨论
2.1 浮选试验结果及分析
2.1.1 单一纯矿物浮选试验
Pb-BHA配位离子捕收剂广泛应用于白钨矿及其伴生资源的浮选分离。图1是不同浮选pH下Pb-BHA配合物捕收剂对白钨矿、重晶石、方解石及萤石的可浮性研究(硝酸铅用量为3×10-4mol/L,BHA用量为1.5×10-4mol/L,松醇油用量为12.5 μL/L)。

由图1可知,Pb-BHA配合物捕收剂对萤石基本没有捕收能力,而对白钨矿、重晶石和方解石则具有很强的捕收能力。利用捕收剂的这一特性,浮选时加入微量的萤石或氟化钠使白钨矿、方解石和萤石表面生成CaF2或其他难溶氟化物,有望实现白钨矿与其他伴生矿物的浮选分离。
图2为萤石和氟化钠用量对Pb-BHA浮选白钨矿、重晶石和方解石效果的影响(pH=9.5,硝酸铅用量为3×10-4mol/L,BHA用量为1.5×10-4mol/L,松醇油用量为12.5 μL/L)。

由图2(a)可知:随着氟化钠用量的增大,白钨矿的回收率基本不变,氟化钠用量增加至300 mg/L时,方解石回收率从79.21%降至54.31%、重晶石回收率从73.56%下降至32.17%;当氟化钠用量大于200 mg/L时,方解石及重晶石的回收率趋于稳定。如图2(b)所示,萤石用量对3种矿物回收率的影响与添加氟化钠时相似。萤石用量小于100 mg/L时,随着萤石用量的增加,重晶石和方解石的回收率明显降低而白钨矿的回收率保持稳定。当萤石用量为100 mg/L时,重晶石和方解石浮选回收率分别下降至44.67%和47.88%;当萤石用量大于100 mg/L时,重晶石及方解石的回收率趋于稳定。
单一纯矿物浮选试验充分说明萤石对白钨矿、方解石和重晶石浮选的影响与氟化钠相似,而且对方解石和重晶石有更好的选择性抑制作用。这说明萤石与氟化钠可以通过在溶液中溶解产生氟离子F-与矿物表面发生作用,从而选择性地抑制脉石矿物。
2.1.2 人工混合矿浮选试验
单一纯矿物浮选试验结果说明了萤石对方解石、重晶石具有选择性抑制效果,可以作为含钙脉石矿物的天然抑制剂,提高白钨矿的浮选回收率。基于单一纯矿物浮选试验结果,进一步开展白钨矿与方解石及白钨矿与重晶石人工混合矿的浮选试验研究。
图3为白钨矿-方解石的浮选结果(pH=9.5,硝酸铅用量为3×10-4mol/L,BHA用量为1.5×10-4mol/L,松醇油用量为12.5 μL/L)。由图3(a)可知,随着氟化钠用量的增加,方解石和白钨矿浮选回收率都有所下降,其中方解石浮选回收率的下降幅度更大,白钨精矿WO3品位总体上逐渐升高,在氟化钠用量100 mg/L时达到最高,为36.76%。如图3(b)所示,萤石对白钨矿-方解石混合矿浮选的影响更加明显,在试验范围内随着萤石用量的增加,白钨矿回收率基本不变,而方解石的回收率从81.82%降至57.8%,白钨精矿中WO3品位逐渐升高,最终在萤石用量100 kg/t时达到最高,为38.75%。这说明在Pb-BHA配合物捕收剂体系下,萤石表面转化可以抑制方解石的浮选,从而实现白钨矿与方解石的浮选分离。

图4为氟化钠及萤石对白钨矿-重晶石混合矿浮选分离的影响(硝酸铅用量为3×10-4mol/L,BHA用量为1.5×10-4mol/L,萤石用量为125 mg/L、氟化钠用量为200 mg/L,松醇油用量为12.5 μL/L)。

由图4(a)可知,未添加萤石和氟化钠,当pH=7~8时,白钨矿浮选回收率与重晶石浮选回收率相差不多。当pH>8时,白钨矿回收率先逐渐升高,而重晶石浮选回收率逐渐降低,在pH=10时,白钨矿浮选回收率最高,达到76.45%,此时重晶石浮选回收率为54.23%,此时白钨矿精矿WO3品位也达到最高,为47.19%。当pH>10时,白钨浮选回收率和精矿品位都发生大幅度下降。在整个试验pH范围内,白钨矿的精矿品位一直较低,始终低于50%,精矿中重晶石杂质较多。这表明,在不使用抑制剂的情况下,单单使用Pb-BHA配位化合物不能实现混合矿中白钨矿和重晶石的分离,得到高品位白钨精矿产品。
从图4(b)可以看出,当pH<10.0时,白钨浮选回收率先降低后升高,在pH=10.0时回收率达到最高,为84.42%,而重晶石浮选回收率逐渐降低,在pH=10.0时回收率最低,为25.76%。在试验pH范围内,精矿中WO3品位整体逐渐升高,在pH=10.0时达到最高,WO3品位61.60%。如图4(c)所示,萤石对白钨矿和重晶石浮选的影响与氟化钠相似,pH=10.0时,白钨矿浮选回收率最高,达到76.14%,白钨精矿WO3品位达到60.89%,而重晶石回收率仅为36.72%。
2.2 溶液化学计算
白钨矿-萤石-方解石和白钨矿-萤石-重晶石共存体系中,相似的金属离子Ca2+或Ba2+表面活性点使得这类矿物的表面化学性质相近。同时,白钨矿、方解石、重晶石和萤石均属于半可溶性盐类矿物,具有一定的溶解性,并且存在相互转化的现象,这使各矿物的浮选行为变得更加复杂,矿物间的分离更加困难。例如,浮选溶液中的离子会发生水解反应,影响pH值的调节;白钨矿、萤石、方解石和重晶石溶解产生的WO42-、F-、CO32-、SO42-可以与矿物表面的金属活性位点发生化学反应,导致矿物之间发生表面转化[8]。
白钨矿及其伴生矿物的溶解反应如下所示:

利用溶液化学计算,可以得到萤石在白钨矿、方解石、重晶石表面转化的反应及平衡常数,如式(5)~(7)所示。

溶液化学计算表明,萤石在白钨矿、方解石和重晶石表面的转化存在明显的差异。其中,萤石在重晶石表面转化反应的溶度积最小,相同氟离子浓度下反应(式(7))最容易发生;萤石在方解石表面的转化向溶液中释放晶格中的弱酸根CO32-,其在弱碱性条件继续发生水解反应,从而使得反应(式(6))的正向反应持续进行;萤石在白钨矿表面转化的临界pH值为4.0,当pH>4.0时萤石-白钨矿矿浆中白钨矿溶解的WO42-在萤石表面发生化学反应生成 CaWO4[16],即反应(式(5))在弱碱性浮选条件下向着逆反应方向进行。因此,通过溶液化学计算,可以断定在浮选矿浆中萤石可以在方解石和重晶石表面转化生成氟化物,改变矿物表面组成,而在白钨矿表面基本不发生表面转化。
2.3 Zeta电位测试
表面电位影响浮选药剂的选择及作用,是决定浮选的因素之一。在两种或多种盐类矿物共存的体系中,其中一种或多种矿物的表面电性受另一种或多种矿物溶解组分的影响。当有表面转化发生,即原矿物表面被转化生成其他矿物时,该矿物表面电性就会趋向于转化反应后生成的矿物的表面电性,与转化前的原矿物表面电性有明显的差异。
图5为萤石对白钨矿、方解石和重晶石表面动电位的影响。可以看出,萤石对白钨矿的表面动电位基本没有影响,说明溶液中的萤石及溶解产生的F-基本没有在白钨矿表面吸附发生转化反应。未处理的方解石表面,其动电位随着pH的升高逐渐由正变负,等电点位于pH=8~9的区间内。当萤石加入后,方解石表面动电位曲线明显负移,在整个测试pH区间内表面动电位都为负值。未经过处理时,重晶石表面动电位随着pH值的升高逐渐由正变负,等电点pH<6.0。加入萤石后,重晶石表面动电位发生正移,等电点移至pH=8~9。这些结果表明,萤石溶出的F-可以在方解石和重晶石表面吸附并发生表面转化,改变矿物表面性质与组成反应[12]。

2.4 XPS测试
X射线光电子能谱可以反映白钨矿、方解石和重晶石在萤石处理前后特征峰的偏移情况。萤石处理后的白钨矿表面的X射线光电子能谱如图6所示。萤石处理后Ca2p3和Ca2p1峰对应的结合能从346.79 eV和350.34 eV微量偏移至346.84 eV和350.39 eV[21],O1s的W—O和Ca—O基团结合能峰值从530.24 eV和531.89 eV微量偏移至530.29 eV和531.79 eV。萤石处理前后的白钨矿Ca2p能谱和O1s能谱的结合能峰值偏移都很小,这充分说明了萤石对白钨矿表面的影响较小,经萤石处理后W—O和Ca—O基团的结合能仍保持稳定,进一步证实了萤石在白钨矿表面的转化非常弱[12]。

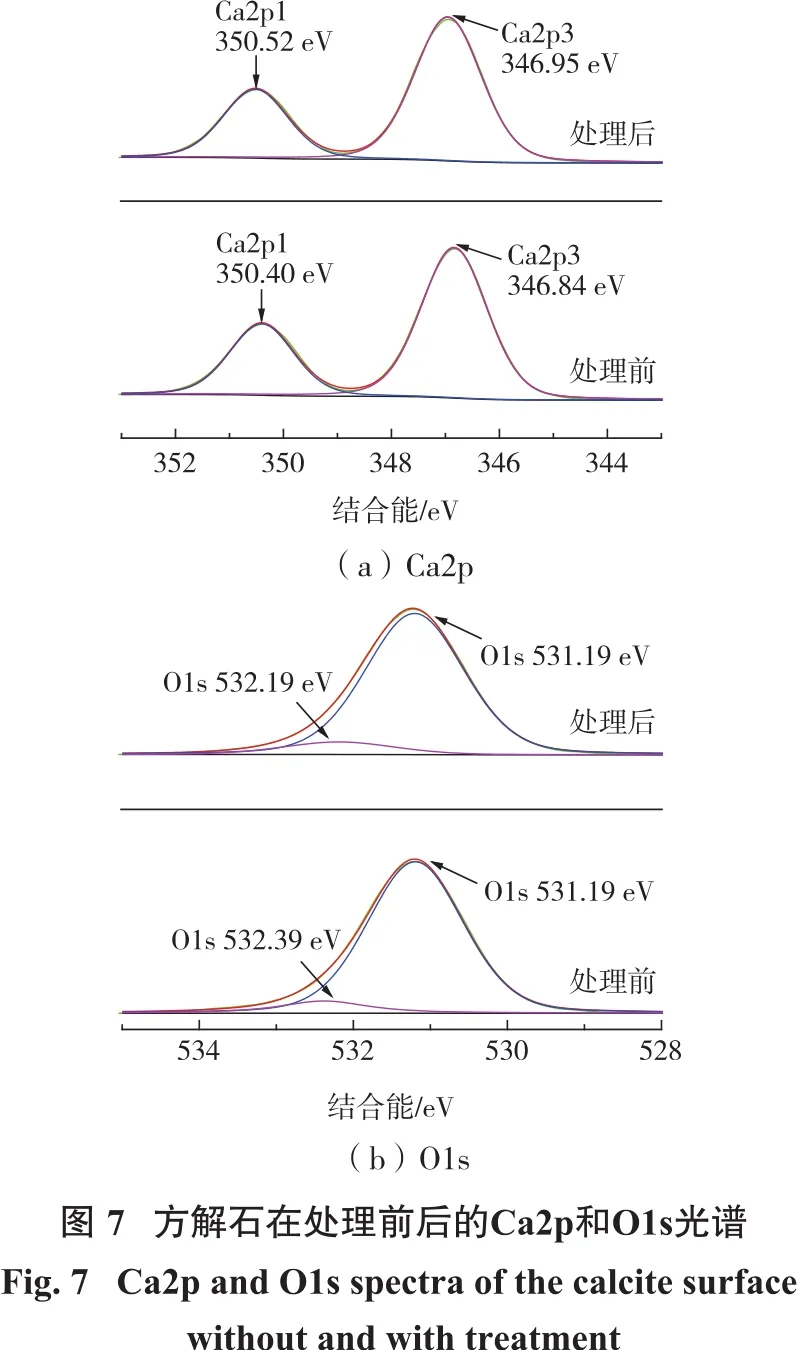
萤石和方解石表面转化过程中,萤石对方解石的钙活性位点的影响较大[12]。如图7所示,萤石处理后,方解石表面的Ca2p3和Ca2p1结合能从346.84 eV和350.40 eV大幅度偏移至346.95 eV和350.52 eV[22],偏移量分别为0.11 eV和0.12 eV;Ca—O基团的结合能从532.39 eV偏移至531.19 eV,发生了0.2 eV的偏移[8,12]。这说明Ca—O基团受到萤石的影响较大,在方解石与氟化钙之间发生了电子转移。由此可见,方解石表面的钙离子活性位点对萤石溶解产生的氟离子的吸附作用较强,容易在方解石表面转化生成CaF2薄膜。
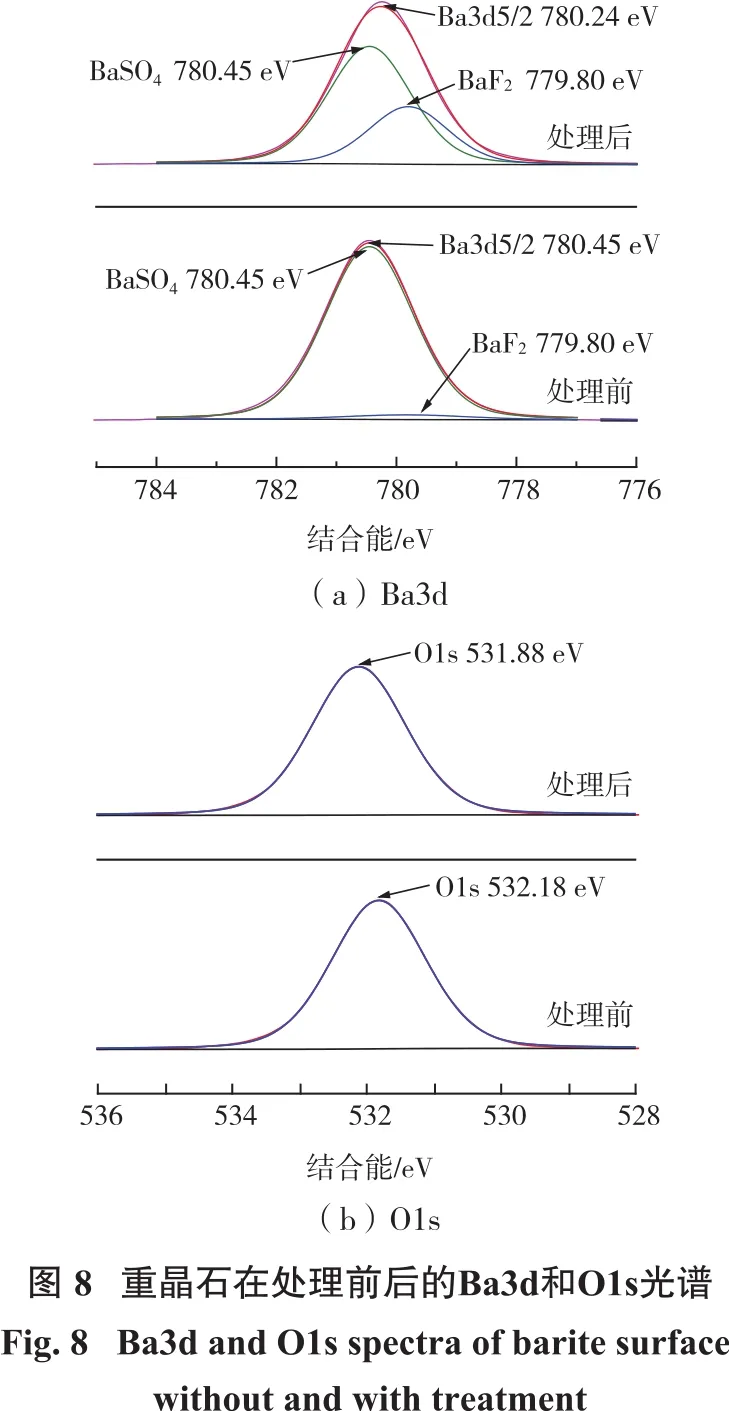
如图8所示,萤石在重晶石表面的转化反应可以明显改变重晶石中Ba3d和O1s的光谱。重晶石表面在经过萤石作用后,Ba3d总峰值从780.45 eV偏移至780.24 eV,BaF2对应的峰面积显著增强;O1s的峰值从532.18 eV减小至531.88 eV,偏移量为0.3 eV。这说明萤石在重晶石表面的转化与方解石类似,萤石溶解产生的氟离子可以通过重晶石表面的钡质点吸附在重晶石表面,转化生成稳定的BaF2膜,从而改变重晶石的特征峰。
2.5 AFM测试
矿物表面形貌可以显著影响矿物的浮选行为和浮选效果。利用原子力显微镜(AFM)能够直观地以二维和三维的角度观察矿物表面形貌和微观结构,进而帮助分析矿物表面的转化行为及其对矿物表面相貌的影响。如图9所示,萤石溶出的氟离子对白钨矿、方解石和重晶石进行表面转化时,3种矿物表面呈现出不同程度的形貌变化。在1.21 μm2的区域内,未处理的白钨矿表面粗糙度Ra=3.78 nm、Rq=4.76 nm[12]。经过氟离子处理之后,白钨矿表面粗糙度Ra和Rq分别变成4.30 nm和5.22 nm[12],表面粗糙度变化较小。

对方解石而言,氟离子处理前后表面形貌和粗糙度变化十分明显。未经过氟离子处理时,方解石表面较为平整,在3.79 μm2的区域内,粗糙度Ra=5.12 nm、Rq=7.63 nm[12]。经过氟离子表面转化处理后,方解石表面粗糙度Ra和Rq分别增加为30.6 nm和37.6 nm[12],分别增加了25.48 nm和29.97 nm,表面粗糙度明显增大。
类似地,氟离子也可以明显改变重晶石的表面形貌。未经过氟离子表面转化处理时,重晶石表面较为平整,在3.82 μm2的区域内,粗糙度Ra=3.69 nm、Rq=4.79 nm、Rmzx=34.6 nm。经过氟离子作用之后,重晶石Ra、Rq和Rmzx分别增大至4.72 nm、6.00 nm 和42.5 nm,表面粗糙度明显增大。
3 结 论
浮选试验结果证实了萤石对方解石和重晶石有明显的抑制作用,萤石的表面转化联合Pb-BHA配合物捕收剂作用可以实现白钨矿与方解石、白钨矿与重晶石的浮选分离;溶液化学及相关计算表明,相比于在白钨矿表面的转化,萤石更容易在方解石和重晶石表面发生转化反应并生成CaF2或BaF2;Zeta电位测试结果表明,萤石的表面转化反应对白钨矿表面电位影响极小,萤石的表面转化反应使方解石表面电位负移、重晶石表面电位正移;XPS及AFM测试结果表明,萤石表面溶出的氟离子F-对白钨矿影响极小,但可以明显改变方解石的Ca2p和O1s峰、重晶石的Ba3d峰和O1s峰,F-在方解石表面生成CaF2薄膜、在重晶石表面生成BaF2薄膜改变了矿物表面的粗糙度。表面转化可以显著影响钨及其脉石矿物的浮选行为,通过控制条件使矿物表面转化向着有利于钨矿浮选的方向进行,为白钨矿及伴生矿物的高效浮选分离提供了新的思路和方法。

