摭谈近年表格型实验判断题的考查要点及解答策略
宁夏 王开山
化学实验是高考考查的重点、热点和难点,是每年化学试卷必考的考点。纵观近年全国卷试题,表格型实验判断题成为实验考查的新题型。该类型试题因其结构简单、信息明确、考点丰富、知识覆盖面广以及兼顾基础知识和综合能力的考查而成为近年实验考查的新宠。
笔者结合近五年全国卷试题,梳理了表格型实验判断题的主要考点分布,并给出相应的解答策略,以供高三学生复习参考。
一、2016年至2020年全国卷(Ⅰ、Ⅱ、Ⅲ)表格型实验判断题主要考点分布统计
二、考点及解答策略分析
考点1 除杂方法判断
着重考查除杂试剂的选择和除杂顺序的合理性。
【解答策略】除杂的基本原则是“除杂不引杂”。根据保留物质和被除物质不同的物理性质或化学性质,常用的除杂方法有物理方法(溶解、过滤、萃取、分液、蒸馏)和化学方法(生成沉淀、气体或其他易分离的物质)等。所以,掌握重要物质的物理性质和化学性质是解答该考点试题的关键。同时需要注意,为了得到纯净、干燥的物质,最后一步一般是通过浓硫酸或其他干燥试剂除去水。
考点2 实验现象判断
着重考查对重要实验现象的掌握程度,包括实验过程中的颜色、状态、气味等的变化。
【解答策略】实验现象与具体的化学反应有关。准确解答实验现象判断类试题的关键是扎实掌握常见元素的单质及其化合物的重要性质和典型化学实验原理及其实验现象。
考点3 制备操作判断
着重考查实验设计与探究能力,包括对实验操作和实验仪器的选择以及对操作顺序、方法及试剂选择合理性的判断。
【解答策略】要依据实验目的来判断制备操作的准确性和合理性。明确相关物质的性质和实验原理,注意从制备操作的可行性、严密性、经济性、安全性等方面作出判断。
考点4 实验结论(物质性质、酸性强弱、Ksp大小等)判断
着重考查得出的实验结论的逻辑性、正确性和合理性。
【解答策略】实验结论是对实验现象和实验结果进行概括、分析、推导得出的普遍事实或规律。准确分析、理解和掌握具体的实验过程以及原理是判断实验结论正确与否的关键。要注重平时实验基础知识的积累。要注意的是,有些结论与具体的实验无关,它是客观存在的事实。
三、高考真题赏析
【例1】(2020·全国卷Ⅰ·9)下列气体去除杂质的方法中,不能实现目的的是
( )
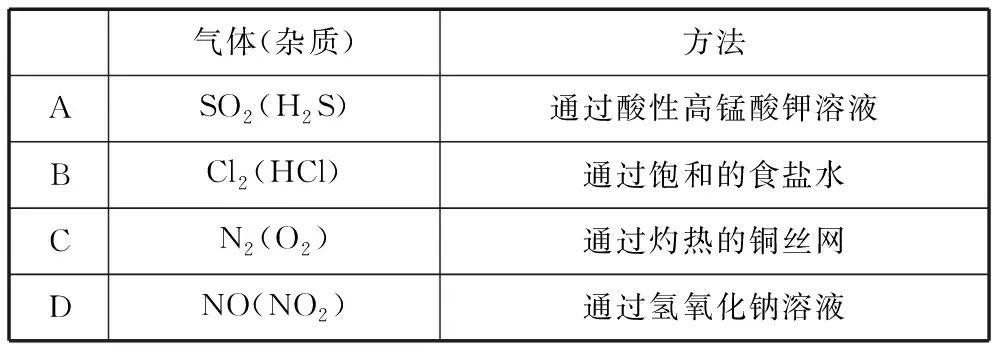
气体(杂质)方法ASO2(H2S)通过酸性高锰酸钾溶液BCl2(HCl)通过饱和的食盐水CN2(O2)通过灼热的铜丝网DNO(NO2)通过氢氧化钠溶液
【答案】A
【考点分析】该题四个选项考查混合物的除杂。A、C、D涉及化学反应,B既有物理性质(溶解性)的思考,也渗透化学平衡思想。

【例2】(2019·全国卷Ⅱ·10)下列实验现象与实验操作不相匹配的是
( )
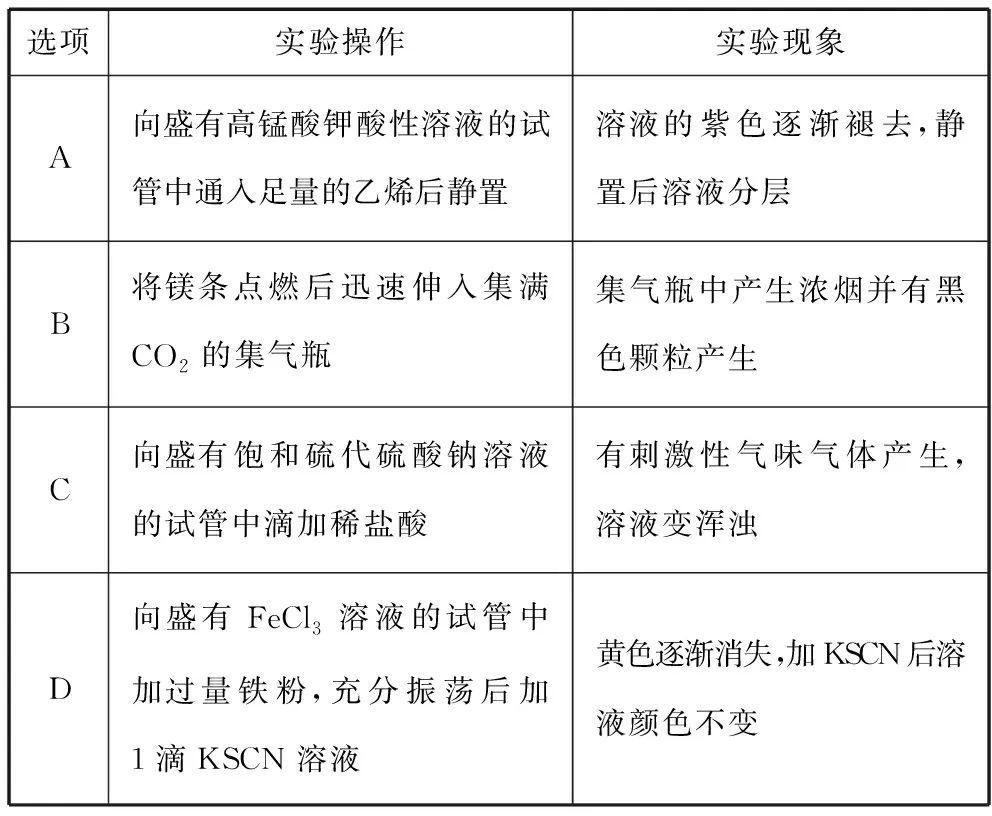
选项实验操作实验现象A向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置溶液的紫色逐渐褪去,静置后溶液分层B将镁条点燃后迅速伸入集满CO2的集气瓶集气瓶中产生浓烟并有黑色颗粒产生C向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸有刺激性气味气体产生,溶液变浑浊D向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN 溶液黄色逐渐消失,加KSCN后溶液颜色不变
【答案】A
【考点分析】该题四个选项考查重要反应的实验现象判断,涉及重要物质的典型化学性质。

【例3】(2018·全国卷Ⅱ·13)下列实验过程可以达到实验目的的是
( )

编号实验目的实验过程A配制0.400 0 mol·L-1的NaOH溶液称取4.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250 mL容量瓶中定容B探究维生素C的还原性向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化C制取并纯化氢气向稀盐酸中加入锌粒,将生成的气体依次通过NaOH溶液、浓硫酸和KMnO4溶液D探究浓度对反应速率的影响向2支盛有5 mL不同浓度NaH-SO3溶液的试管中同时加入2 mL 5%H2O2溶液,观察实验现象
【答案】B
【考点分析】该题考查实验方案设计与评价,综合性较强。涉及一定物质的量浓度溶液的配制、性质实验探究、气体的制备与净化、外界条件对反应速率的影响等。
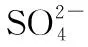
【例4】(2017·全国卷Ⅱ·10)下列由实验得出的结论正确的是
( )

实验结论A将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明生成的1,2二溴乙烷无色、可溶于四氯化碳B乙醇和水都可与金属钠反应产生可燃性气体乙醇分子中的氢与水分子中的氢具有相同的活性C用乙酸浸泡水壶中的水垢,可将其清除乙酸的酸性小于碳酸的酸性D甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红生成的氯甲烷具有酸性
【答案】A
【考点分析】该题考查实验结论的正误判断。主要是根据具体的化学反应来判断相应实验结论的正误,难度不大。
【解析】乙烯与溴发生加成反应,生成1,2-二溴乙烷,1,2-二溴乙烷在四氯化碳中具有很好的溶解性,最终得到无色透明溶液,A选项实验结论正确;钠与水反应比与钠与乙醇反应剧烈,说明水中的氢比乙醇中的氢活泼,B选项实验结论错误;水垢的主要成分为碳酸盐,根据强酸制弱酸原理和乙酸能除去水垢可得出:乙酸的酸性强于碳酸的酸性,C选项实验结论错误;甲烷与氯气在光照条件下发生反应生成氯甲烷和氯化氢,氯甲烷不具有酸性,但氯化氢具有酸性能使湿润的石蕊试纸变红,D选项实验结论错误。
【另解】本题也可直接判断结论的正误。B、C、D三个选项的结论始终是错误的,与具体的实验无关。
【例5】(2017·全国卷Ⅲ·9)下列实验操作规范且能达到目的的是
( )
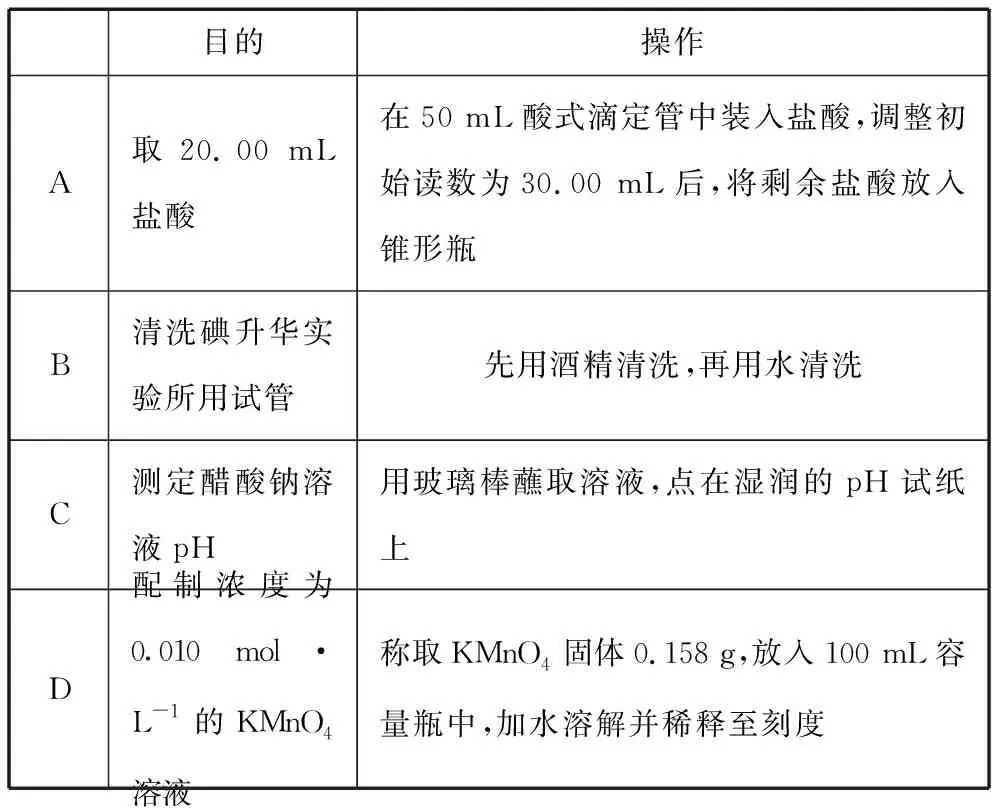
目的操作A取20.00 mL盐酸在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶B清洗碘升华实验所用试管先用酒精清洗,再用水清洗C测定醋酸钠溶液pH用玻璃棒蘸取溶液,点在湿润的pH试纸上D配制浓度为0.010 mol·L-1的KMnO4溶液称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度
【答案】B
【考点分析】该题考查实验基本操作评价。涉及滴定管的结构、碘的物理性质、pH试纸的使用和盐类水解及一定物质的量浓度溶液的配制等。
【解析】滴定管的最大刻度并没有在最下方,最大刻度到尖嘴部分还装有盐酸,所以滴定管中剩余盐酸的体积大于20.00 mL,A选项操作不能达到实验目的;根据“相似相溶原理”,碘易溶于酒精,可用酒精清洗碘,又由于酒精与水互溶,再用水清洗即可洗净,B选项操作能达到实验目的;先将pH试纸湿润,相当于稀释了待测溶液,会造成醋酸钠溶液pH偏低,C选项操作不能达到实验目的;容量瓶是定容容器,不能在容量瓶中溶解KMnO4固体,D选项操作不能达到实验目的。
【例6】(2016·全国卷Ⅲ·9)下列有关实验的操作正确的是
( )

实验操作A配制稀硫酸先将浓硫酸加入烧杯中,后倒入蒸馏水B排水法收集KMnO4分解产生的O2先熄灭酒精灯,后移出导管C浓盐酸与MnO2反应制备纯净Cl2气体产物先通过浓硫酸,后通过饱和食盐水DCCl4萃取碘水中的I2先从分液漏斗下口放出有机层,后从上口倒出水层
【答案】D
【考点分析】本题考查实验基本操作和实验安全。涉及浓硫酸的稀释、氧气的制备、物质除杂和分离以及萃取实验等。
【解析】浓硫酸稀释会放热,故浓硫酸的稀释过程是将浓硫酸倒入水中并不断用玻璃棒搅拌,A选项错误;密闭容器的温度降低,容器内气体的压强也会降低,实验后应先移出导管后熄灭酒精灯,防止发生倒吸,B选项错误;实验室制得的Cl2中混有HCl和H2O,而HCl气体极易溶于水,应先用饱和食盐水除去少量的HCl气体,然后再通过浓硫酸除去H2O,C选项错误;CCl4的密度比水大,位于分液漏斗的下层,应该先从下口倒出有机层,再从上口倒出水层,D选项正确。
表格型实验判断题依然是今后实验考查的重要题型,只要考生在平时复习过程中夯实实验基础知识,重视实验基本操作、基本原理和实验方案评价,定会高效解答该类型试题。

