达雷妥尤单抗治疗复发难治性系统性轻链型淀粉样变性的疗效和安全性观察
任贵生 郭锦洲 赵 亮 徐维玮 陈文萃 刘志红 黄湘华
系统性轻链(AL)型淀粉样变性是由于单克隆浆细胞产生的游离轻链异常折叠形成淀粉样物质沉积在组织或器官中,导致功能障碍的一种疾病[1],可累及肾脏、心脏、肝脏等多个重要器官,病情凶险,预后差。其发病率估计为10~14例/百万人口·年,但由于漏诊或误诊,实际发病率可能更高[2]。随着硼替佐米等蛋白酶体抑制剂、来那度胺等免疫调节剂和自体外周血造血干细胞移植(ASCT)的广泛应用,患者的预后获得了很大改善,但仍有部分患者治疗无效或复发,亟需新的治疗手段。达雷妥尤单抗(DARA)可以与单克隆浆细胞表面的CD38相结合,通过抗体依赖性细胞介导的细胞毒作用(ADCC)、抗体依赖性细胞吞噬作用(ADCP)、补体依赖的细胞毒作用(CDC)诱导细胞凋亡,此外还能够调节免疫微环境并快速消除免疫抑制细胞[3-4],已于2019年被中国国家药品监督管理局批准用于治疗复发难治性多发性骨髓瘤(MM)患者。目前,国外已有少数研究提示了DARA对于复发难治性AL型淀粉样变性是安全有效的[5-8],但其在中国患者中的治疗效果尚缺少研究进行证实。基于此,本研究回顾性分析了19例接受DARA治疗的中国复发难治性AL型淀粉样变性患者,以探讨其临床疗效及安全性。
对象和方法
研究对象2020年7月至2020年12月在国家肾脏疾病临床医学研究中心确诊并接受DARA单药治疗的复发难治性AL型淀粉样变性患者共19例。
治疗方案每次DARA给药剂量为16 mg/kg。第1个月每周给药1次,第2个月每2周给药1次,后续每月给药1次。给药过程中根据患者有无输液反应及反应的程度调整速度,如出现常见不良反应术语评定标准(CTCAE 5.0版)3级及以上不良反应则停药。DARA给药前予甲泼尼龙80~120 mg静滴,同时予异丙嗪肌注、氯雷他定和对乙酰氨基酚口服防止过敏,给药过程中同步予地塞米松20 mg静滴预防输液反应。根据情况酌情予护胃、利尿等对症治疗。
观察指标观察DARA治疗前后临床及实验室指标的变化:24h尿蛋白定量、血常规、血生化、血单特异性游离轻链、血清免疫固定电泳、N端前脑钠肽(NT-proBNP)、肌钙蛋白T(TnT)。根据有关指标评价血液学及器官反应,并记录治疗过程中的不良反应。
相关标准及定义复发是指经治疗取得缓解且维持3个月后出现血液学和(或)器官进展,而难治则是指经初始方案治疗3个月后血液学及器官均无反应[9]。患者按照Mayo 2012分级系统及严重心脏受累患者的欧洲分期,分为Ⅰ、Ⅱ、Ⅲa、Ⅲb、Ⅲc和Ⅳ级[10-11]。在血液学反应的评估上,对于基线血游离轻链差值(受累轻链与未受累轻链的差值,dFLC)>50 mg/L的患者,如治疗后血游离轻链完全正常、血液及尿液免疫固定电泳均阴性,则定义为完全缓解(CR);如血dFLC<40 mg/L,则定义为非常好的部分缓解(VGPR);如血dFLC下降超过50%,则定义为部分缓解(PR);如达不到PR,则定义为血液学无反应(NR)[9]。对于基线血dFLC在20~50 mg/L的患者,如治疗后血dFLC<10 mg/L,定义为低游离轻链差值下的部分缓解(low-dFLC PR),反之则认为NR[12]。肾脏反应的标准为:尿蛋白定量下降50%(至少下降≥0.5 g/d)且血清肌酐上升不超过基线的25%,而心脏反应的标准为:对于基线NT-proBNP>650 ng/L以上者下降幅度大于基线的30%,且降低300 ng/L以上;或基线心功能为NYHA分级3或4级的患者,心功能分级降低至少2个级别;或心脏射血分数增加≥20%[9]。
统计学方法采用《SPSS 22.0》软件进行统计。计数资料采用百分数表示,正态分布的计量资料采用均数±标准差表示,非正态分布的计量资料采用中位数(范围)表示。
结 果
基线资料纳入19例患者中男性7例(36.8%),中位年龄为56(47,77)岁,中位病程为36(21,79)个月(表1),。Mayo分级:Ⅰ级13例(68.4%),Ⅱ级2例(10.5%),Ⅲa级4例(21.1%)。所有患者均有肾脏受累,11例(57.9%)有心脏受累,均无肝脏受累证据。患者尿蛋白定量5.2±4.5 g/24h,血清肌酐97.24±61.88 μmol/L,6例(31.5%)患者估算的肾小球滤过率(eGFR)<60 ml/(min·1.73m2)。12例(63.2%)患者血dFLC> 50 mg/L,7例(36.8%)患者的血dFLC在20~50 mg/L。
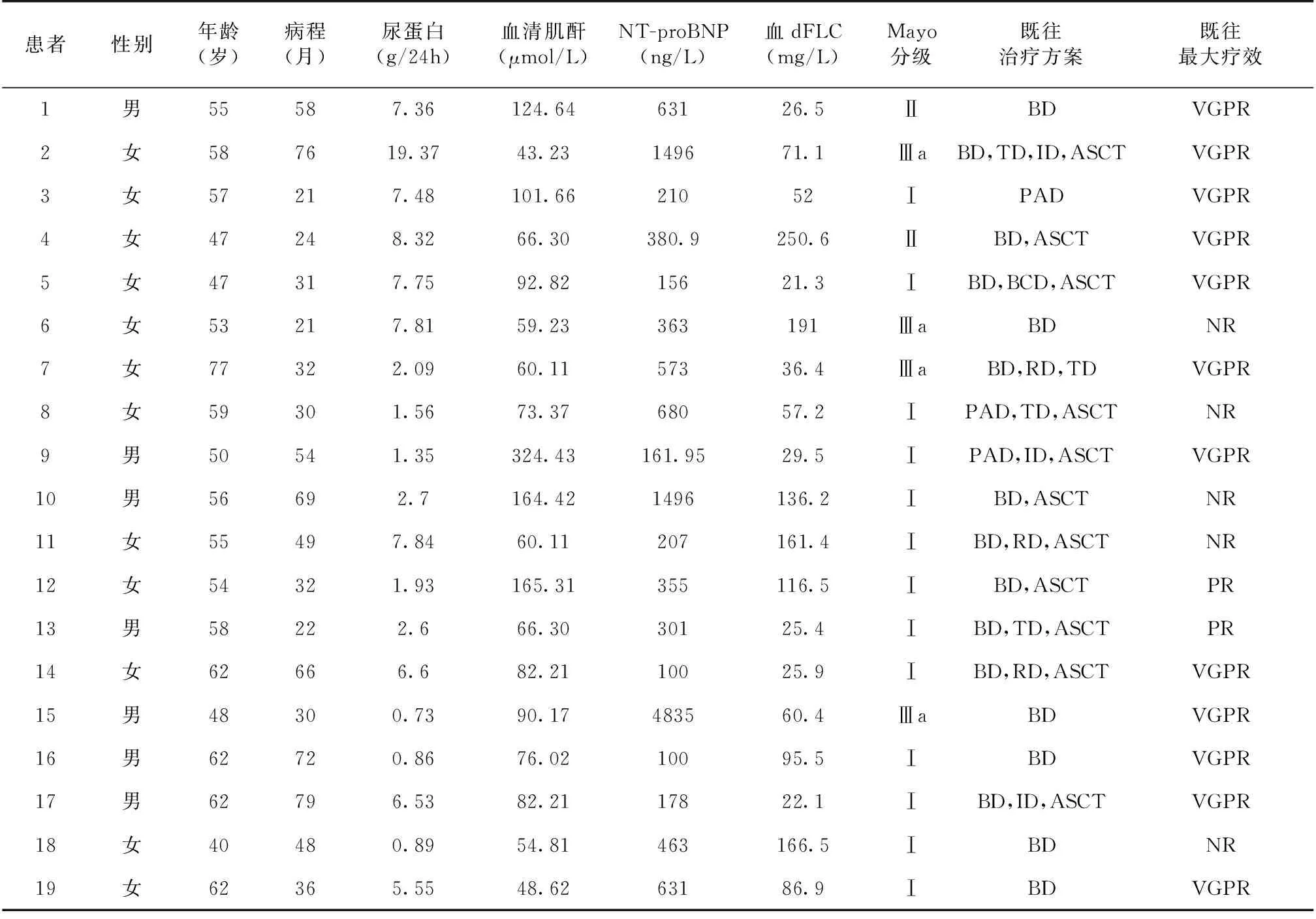
表1 19例患者的基线资料
患者既往接受了中位2(1,4)线治疗,均曾经接受硼替佐米治疗,6例(31.6%)曾接受免疫调节剂治疗,11例(57.9%)患者曾行ASCT。12例(63.2%)患者既往最佳疗效为VGPR,2例(10.5%)为PR,5例(26.3%)为NR。
疗效评估患者中位接受4(3,12)次DARA治疗。11例(57.9%)患者在接受第1次治疗后血dFLC即下降至<10 mg/L(图1)。19例患者中有16例(84.2%)实现血液学缓解,3例(15.8%)对治疗无反应。对于12例基线血dFLC>50 mg/L的患者,4例(33.3%)实现血液学CR,6例(50%)达到VGPR。患者6治疗前血dFLC为191 mg/L,经4次治疗后上升至232.1 mg/L,而患者10治疗前血dFLC为136.2 mg/L,经11次治疗后仅下降19.5%,疗效评估为NR。在7例基线血dFLC 20~50 mg/L的患者中,有6例(85.7%)疗效达到low-dFLC PR。患者7在7次治疗后血dFLC无明显变化,疗效为NR(图2)。
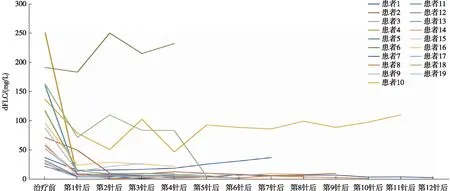
图1 患者治疗过程中血游离轻链差值(dFLC)的变化
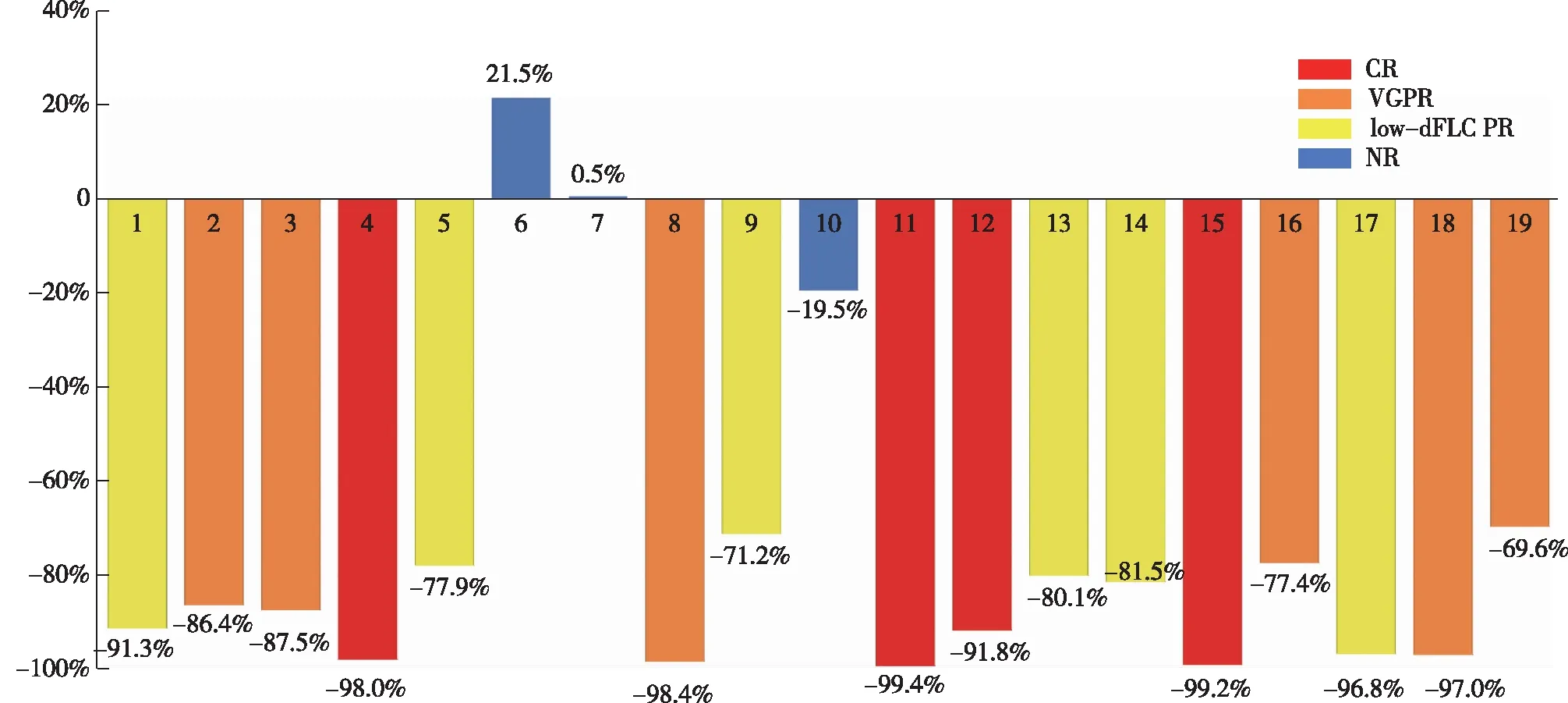
图2 患者末次治疗后血dFLC的变化幅度dFLC:游离轻链差值;CR:完全缓解;VGPR:非常好的部分缓解;low-dFLC PR:低游离轻链差值下的部分缓解;NR:无反应
中位随访4(1,7)个月,19例患者均存活,有3例(15.8%)获得肾脏缓解。患者1在治疗7个月后尿蛋白定量从7.36g/24h下降至2.54g/24h,患者2在随访4个月后尿蛋白定量从19.37g/24h下降至2.87g/24h,患者5在治疗6个月后尿蛋白定量从7.75g/24h降至1.5g/24h。其余患者尿蛋白定量及血白蛋白水平无明显变化,但血清肌酐均保持稳定。在11例心脏受累的患者中,患者2的NT-proBNP从1 496 ng/L下降至383 ng/L,获得心脏缓解,其余10例患者心肌标志物稳定。
不良反应大多数不良反应与输注相关,且程度轻微。7例(36.8%)患者在第1次治疗过程中出现咳嗽,发生在开始治疗后1.5(1.5,3.5)h,分级均为1级。1例(5.3%)患者在治疗开始后2h出现1级的寒战,体温正常。10例(52.6%)患者在首次治疗开始1.75(1.75,3.5)h后出现咽喉不适,分级为1级。上述输注相关不良反应在暂停输注后均迅速自发缓解,没有患者需要终止治疗。在第2次及以后的治疗中,没有患者发生输注相关不良反应。
非输注相关相关不良反应包括中性粒细胞减少(2例,10.5%)、感染(1例,5.3%)、发热(4例,21.1%)。患者5在第4次治疗后中性粒细胞降至1.6×109/L,后自行恢复,患者11在治疗3次后中性粒细胞下降至1.23×109/L,给予粒细胞刺激因子200 μg皮下注射后迅速恢复,未影响后续治疗。3例患者在首次用药的第2天出现低热,感染指标正常,血培养阴性,给予小剂量甲泼尼龙口服后体温降至正常。患者6在第4次治疗后出现发热,体温最高38℃,胸部CT示双肺炎症,CRP上升至128.5 mg/L,真菌G试验阳性,予头孢噻肟钠舒巴坦联合伏立康唑治疗后感染得到有效控制(表2)。
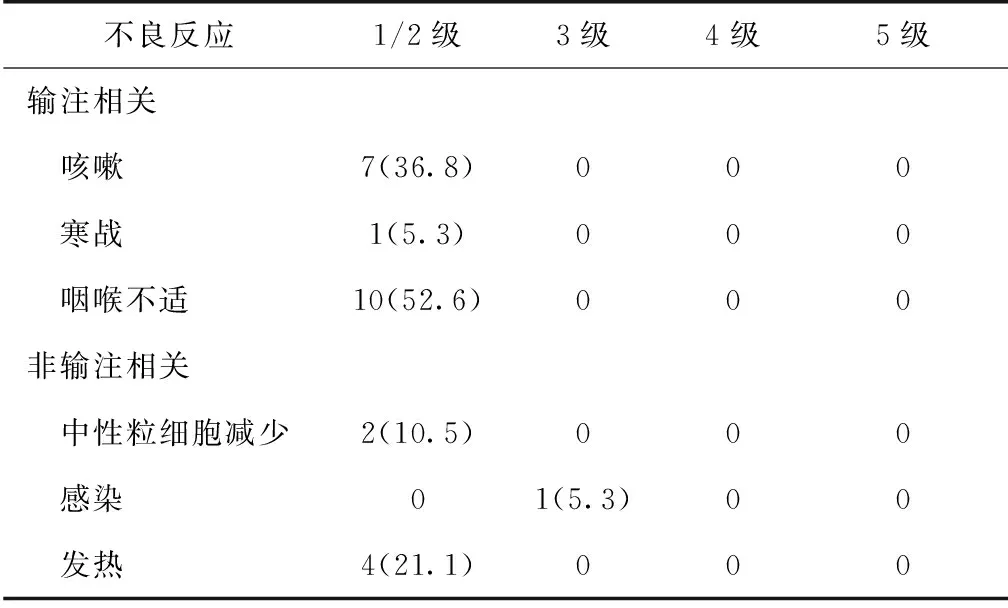
表2 达雷妥尤单抗治疗的不良反应[n(%)]
讨 论
随着对AL型淀粉样变性认识的不断深入以及硼替佐米、ASCT等的广泛应用,患者的生存时间明显延长,生活质量也获得了很大提高,但仍有40%的患者在诊断后2年内死亡[13],这主要是由于部分患者不能耐受高强度的治疗[6],或在治疗过程中反复复发或对多种药物无反应所致。对于复发或难治的患者,他们的血液学持续不缓解,器官功能进行性恶化,需要革命性的治疗手段才有可能进行挽救。在2016年,Mayo医学中心开始进行DARA治疗复发难治性AL型淀粉样变性的探索,2例患者均获得血液学CR[14],从此开启了疾病治疗的新篇章。
在AL型淀粉样变性的治疗中,快速、深度、持续的血液学缓解至关重要,这是患者实现器官缓解、改善预后的决定性因素。获得VGPR及以上血液学缓解的患者更易获得器官缓解[6-7],而血液学CR或血dFLC<10 mg/L则预示着最佳的预后[15]。在我们的研究中,19例患者中有11例(57.9%)在接受第1次治疗后血dFLC即下降至<10 mg/L,说明DARA可以实现快速的血液学缓解。在中位接受4(3,12)次DARA治疗后,12例基线血dFLC>50 mg/L的患者中有4例(33.3%)实现血液学CR,6例(50%)达到VGPR,而7例基线血dFLC 20~50 mg/L的患者中有6例(85.7%)疗效达到low-dFLC PR(血dFLC<10 mg/L)。19例患者总体的血液学缓解率达到84.2%,且均为VGPR及以上。在Abeykoon等[5]的研究中,DARA单药治疗复发难治性AL型淀粉样变性的血液学缓解率为78%,VGPR及以上为64%,而在Sanchorawala等[6]的研究中,对应的数据分别为90%和86%。Roussel等[7]的研究所报道的缓解率低于上述2项研究,40例患者的血液学缓解率为55%,VGPR及以上为47.5%,Kimmich等[8]则发现,DARA单药所带来的血液学缓解率为64%,VGPR及以上为48%,而联合硼替佐米则分别为66%和55%。我们的数据与上述研究对比可发现,DARA在中国人群中的疗效不亚于欧美人群。
需要注意的是,即使达到理想的血液学缓解,患者的器官功能恢复仍然出现较晚。在Kimmich等[8]的研究中,中位随访6个月,患者的肾脏缓解率为24%,心脏缓解率为22%。而Sanchorawala等[6]的研究显示,患者肾脏获得首次反应的中位时间为18周,获得最佳反应的中位时间为54周,心脏则分别为20周和44周,患者的肾脏缓解率可达67%,心脏缓解率可达50%。Chung等[16]的研究发现,52%的患者可获得肾脏缓解,中位反应时间为6月,而55%的患者可获得心脏缓解,中位反应时间为3.2月。在我们的研究中,19例肾脏受累的患者有3例(15.8%)获得缓解,而11例心脏受累的患者中有1例实现缓解,这与我们的随访时间尚短有关。DARA的维持性治疗有助于器官深度缓解,而只要血液学仍处于缓解状态,即使在治疗6~12月后仍未出现器官反应也不建议增加药物或者调整治疗方案[17-18]。相信随着治疗的继续和随访时间的延长,本研究中的患者会越来越多地实现肾脏和心脏缓解。
DARA的不良反应较少,且大多数为输液相关。在我们的研究中,咳嗽、咽喉不适的发生率分别为36.8%和52.6%,大多数发生在输注开始2h左右,程度轻微,可自发缓解,与文献中报道一致[19]。此外,4例患者出现非感染性的低热,2例出现轻度的中性粒细胞减少,均可迅速恢复,未影响治疗。患者6为中老年女性,在治疗过程中发生肺部细菌合并真菌感染,可能与患者持续存在的胸腔积液有关,这也提示我们在治疗过程中需要加强对患者一般状态的评估和治疗强度的把握。
本研究为DARA治疗复发难治性AL型淀粉样变性的初步观察,仅纳入4例(21.1%)Mayo分级为Ⅲa级的患者,因此对于器官受累严重的患者,DARA的疗效和安全性还需要进一步验证。在后续的研究中,我们将更多地纳入Mayo分级Ⅲ-Ⅳ级的患者,以全面评估DARA在复发难治性AL型淀粉样变性中的应用价值。此外,随访时间较短,对于器官缓解和患者的长期疗效仍有待进一步观察。
小结:对于复发难治性AL型淀粉样变性患者,DARA可实现快速、深度、持续的血液学缓解,为患者的器官功能和预后的改善奠定基础,且药物的不良反应轻微、可控。

