痛风病中药效用机制研究平台构建及应用
林志健 黄政凯 王雨 杨婷 张冰

摘要 目的:建立中药防治痛风病的药效评价平台,为评价中药防治痛风病的药效特点与作用机制提供技术支撑。方法:集成“成分-疾病”靶标网络分析、病证结合动物模型、器官模型、细胞模型、分子生物学5个层次,从多层次系统构建中药防治痛风病的药效评价平台。结果:本课题组成功构建了基于尿酸生成与排泄、尿酸盐沉积以及沉积致炎的“整合论治”痛风病药效评价平台。该平台已进行了中药菊苣等多个中药品种的药效评价研究。结论:该平台集成了病证结合、整体动物、组织器官以及细胞分子生物学的研究技术,能够对中药多成分、多靶点、多层次的整合论治特点进行系统评价,已展现出较好的痛风病防治药物综合评价优势,可为临床防治痛风中药的研发提供参考和指导。
关键词 痛风病;中药;整合论治;药效研究平台;应用
Platform Construction and Application of a Research Platform on the Mechanism of Chinese Medicine for Gout
LIN Zhijian,HUANG Zhengkai,WANG Yu,YANG Ting,ZHANG Bing
(School of Chinese Materia Medica,Beijing University of Chinese Medicine,Beijing 102488,China)
Abstract Objective:To establish a platform for evaluating the efficacy of Chinese medicine(TCM)in the prevention and treatment of gout disease.Methods:Our team integrated 5 modules for the gout disease study,the “component-disease” target network analysis,the animal models of combination of disease and syndrome,the organ models,the cell model and the molecular biological analysis module.A platform for evaluating the efficacy of Chinese medicine in preventing and treating gout was established from a multi-level system.Results:Our team had successfully constructed the drug efficacy evaluation platform based on gout disease induced by uric acid production or excretion,urate deposition and urate induced-inflammation.The platform has been used to evaluate the drug efficacy of Cichorium intybus L.and other Chinese herbal medicines.Conclusion:The platform integrates the research technologies of disease and syndrome,whole animals,tissues and organs,and cell and molecular biology.It can systematically evaluate the characteristics of multi-component,multi-target,and multi-level integrated treatment of traditional Chinese medicine,and has shown good advantages in comprehensive evaluation of drugs for the prevention and treatment of gout,which can provide reference and guidance for the development of Chinese medicines for the prevention and treatment of gout.
Keywords Gout disease; Chinese medicines; Integrated treatment; Pharmacological research platform; Application
中圖分类号:R242文献标识码:Adoi:10.3969/j.issn.1673-7202.2021.01.007
痛风病是指与高尿酸血症、尿酸盐沉积密切相关的进展性代谢疾病,其疾病进程包括高尿酸血症阶段、尿酸盐沉积阶段、急性炎症阶段。据《2019中国痛风诊疗指南》,中国高尿酸血症的总体患病率达13.3%,痛风性关节炎发病率达1.1%[1],临床治疗需求迫切。2019年美国风湿病学会学术年会《2020痛风临床实践指南(草案)》突破以往痛风急性炎症不可进行降尿酸治疗的认识局限,率先明确指出痛风性关节炎的治疗在抗炎的要同时进行降尿酸干预[2]。然而,目前临床应用的抗痛风病药物多为化药,作用靶点明确,分别以降低血尿酸、抗炎镇痛为治疗目的,虽阶段性疗效显著,但缺乏降尿酸、抗炎的整体干预,并均存在不同程度的安全风险[3],难以满足痛风病临床治疗需求。因此,契合疾病特点,可整体干预痛风病,且安全性好的药物研发将是未来痛风病防治的重要方向。
我们在整体观指导下,探讨中医药在痛风病的临床治疗中的特点,发现祛湿化浊除痹的治疗法可取得较好的临床疗效[4]。研究发现其干预环节不仅涉及高血尿酸的降低[5]、急性炎症的缓解[6],亦包括贯穿痛风病进展始终的尿酸盐沉积的改善[7],具多环节、多靶点的整合论治优势。但中医药治疗往往具有经验性、实践性的特点,目前对痛风病类复杂疾病的优势效用尚缺乏一致性的评价体系。本课题组已从尿酸水平升高、尿酸盐沉积及沉积致炎三阶段,集成“成分-疾病”靶标网络分析、病证结合动物模型、器官模型、细胞模型、分子生物学5个层次,建立了痛风病中药效用机制研究平臺。因此,本文以痛风病中药效用机制研究平台为核心,围绕平台建设思路、模块构架及应用等方面介绍中药防治痛风病药效评价平台的建设情况,以期为临床药物研究提供参考,满足痛风病临床治疗的迫切需求。
1 平台建设思路
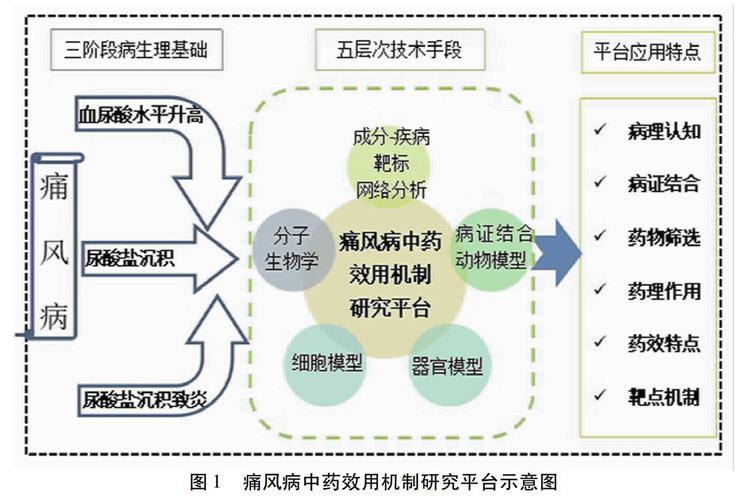
我们认为痛风病中药效用机制研究平台建设应以痛风病的病理过程及中医药对痛风病的治疗原则为基础。经过多年的探索,本课题组成功构建了“三阶段,五层次”符合中药特点的痛风病中药效用机制研究平台。该平台切入痛风病发生的整体过程,围绕血尿酸水平升高阶段、尿酸盐沉积阶段以及尿酸盐沉积致炎3个阶段,集成“成分-疾病靶标网络分析、病证结合动物模型、器官模型、细胞模型及分子生物学”5个层次。该研究平台能够体现中西医对痛风病的病理认知,中医病证结合的治疗思路,以及药物作用靶点与通路的综合药效评价。同时可为中药单方、复方、有效部位、有效成分等多形式的药物筛选与药理药效及作用机制提供技术支持;可针对药物防治痛风病的不同阶段、不同层面进行药效评价与机制分析,揭示药物作用的特点与靶点机制,切实服务于痛风病防治的药物筛选与评价。
2 研究平台架构及关键技术
中药防治痛风病药效评价平台集多项药理与生物学研究技术为一体,具体包括“成分-疾病”靶标网络分析、病证结合动物模型、器官模型、细胞模型、分子生物学,符合痛风病的动态发展与全程干预的药效评价需求。研究平台的架构与功能特点见表1。
2.1 成分-疾病靶标网络计算模块构建
课题组围绕痛风病不同病理阶段的靶点群,构建了痛风病的潜在靶点库;同时系统梳理古今文献构建抗痛风病多个中药的成分数据库。利用网络药理学、分子对接、成分-靶点相互作用分析、功能注释、通路富集等生物信息学技术,搭建了成分-疾病靶标网络计算模块。如课题组通过同源建模技术构建肠道浓度型核苷转运蛋白2(Concentrative Nucleoside Transporter2,CNT2)、分子对接技术构建尿酸生成代谢黄嘌呤氧化酶(Xanthine Oxidase,XOD)、腺苷脱氨酶(Adenosine Deaminase,ADA)、鸟嘌呤脱氨酶(Guanine Deaminase,GDA)、尿酸排泄转运体葡萄糖转运蛋白9(Glucose Transporter 9,GLUT9)、有机阴离子转运体1(Organic Anion Transporter 1,OAT1)、有机阴离子转运体3(Organic Anion Transporter 3,OAT3)及肾脏尿酸盐转运蛋白1(Urate-anion Exchanger 1,URAT1)等靶点与菊苣、茯苓等多个中药及复方的成分-靶点网络,为开展痛风病药效评价研究提供有益参考。
2.2 病证结合动物药理模型构建
课题组利用禽类鹌鹑与人类一样缺乏尿酸酶,尿酸作为嘌呤代谢的终产物的特点,模拟痛风病重要病因,采用添加酵母浸膏粉配制的高嘌呤食饵进行饮食诱导,建立鹌鹑高尿酸血症及痛风模型[8-9]。该模型突破和规避了啮齿类动物具有尿酸酶的技术瓶颈与模型缺陷,成功模拟出痛风病发生发展过程中血尿酸水平升高、尿酸盐沉积以及沉积致炎的病理特点。该模型具有“病证结合”的特点,在中药防治痛风病的药效评价中具有突出优势,为降低血尿酸、抗痛风药物的实验研究及开发提供了稳定可靠的动物模型,已用于多种药物降尿酸及抗痛风的药理评价,受到同行的认可,已被国内大型药理工具书《中药药理实验方法学》《中药药效研究思路与方法》《药理实验方法学》《痛风病学》收载。
同时,根据中医对痛风病的认知,观察“四诊”的证候表现,通过计算机软件辅助的数字化定量分析方法采集模型动物的“四诊”信息,成功建立动物模型“四诊”客观化数字化诊断技术[10]。该技术能较好地从环境、饮食等综合因素模拟临床病因、辨析模型动物证型,可体现痛风病的病机发展规律。
2.3 离体器官药理模型构建
课题组切入痛风病发生发展过程中的靶器官,关注尿酸排泄的2个重要靶器官肠道及肾脏,已成功构建大鼠离体肾灌流及肠灌流模型,可排除体内神经-体液因素的干扰,直观反映药物在靶器官的药理效应,观察靶器官对尿酸排泄转运的干预效果,并广泛应用于尿酸排泄及其机制的研究。如大鼠离体肾灌流器官模型,通过检测灌流液尿酸水平与离体肾脏输尿管尿液的尿酸水平,计算肾脏尿酸排泄率,实现体内实验与体外实验的桥梁衔接,直观分析中药小分子化合物对尿酸肾脏排泄途径的干预作用,包括肾小球滤过、肾小管重吸收、肾小管分泌及重吸收环节,可用于促进肾脏尿酸排泄的药物的发现和评价[11]。肠道是尿酸的肾外排泄途径,通过离体肠灌流模型可排除肠道菌群对尿酸分解的干扰,在十二指肠及空肠中部形成肠道灌流回路,持续收集流出灌流液,测定尿酸含量,进而评价尿酸在肠道的排泄过程。离体肾灌流与肠灌流模型综合模拟了尿酸的排泄过程,在促尿酸排泄药物的评价中起到重要的技术支持。
2.4 细胞药理模型构建
课题组围绕尿酸生成、尿酸排泄、沉积致炎病理环节,构建肝L02细胞模型、肠IEC-6、肠CaCo-2模型、肾HKC及HK2模型、尿酸盐致巨噬细胞炎症模型体系,可实现对肝脏尿酸生成代谢、肠道嘌呤吸收、肠道尿酸排泄、肾脏尿酸排泄以及尿酸盐沉积致炎的药理观察与作用靶点机制分析。多种细胞药理模型综合运用,在中药干预肠道嘌呤吸收、体内尿酸代谢、肠道与肾脏尿酸排泄的靶点及机制研究中具有突出优势。
2.5 分子生物学分析构建
课题组在整体动物模型、器官模型及细胞模型的基础上,以尿酸生成代谢、尿酸排泄及尿酸盐沉积致炎靶点群为切入点,结合“成分-疾病靶点”网络计算结果,利用分子生物学技术手段分析中药成分对痛风病的疾病靶点的综合调控与干预,从蛋白及基因调控层面阐释中药的作用机制。
该效用机制研究平台可涵盖痛风病发生发展过程中血尿酸水平升高、尿酸盐沉积、沉积致炎的病理特点,同时具有反映中医证候特征的客观指标,满足研究防治痛风病的药物筛选与药效评价技术需求。另外,该平台各层次的应用潜力还体现在与其他药理基础研究的联合分析,如与基因组学、肠道组学、蛋白组学、转录组学、代谢组学等现代药理研究技术的联合应用。
3 研究平台应用
3.1 中药及中药复方降尿酸功效与机制研究
3.1.1 基于“病证结合”动物模型菊苣及菊苣复方降尿酸效果及机制研究
整体动物模型研究提示,菊苣可从多途径降低血尿酸水平。菊苣提取物5~15 g/kg剂量下可显著降低高尿酸血症大鼠或鹌鹑模型的血尿酸水平[12-14]。高尿酸血症大鼠模型实验显示,其一菊苣提取物能上调空肠和回肠中ATP结合盒蛋白G蛋白亚家族成员2(ATP-binding Cassette of Half-transporter Protein,ABCG2)的mRNA及蛋白表达,使肠道肌酐排泄量及肠道尿酸排泄量明显升高,促进肠道尿酸排泄;其二菊苣提取物能降低可肾脏中尿酸转运体URAT1和GLUT9蛋白表达,抑制肾脏尿酸重吸收,从而促进肌酐和尿酸的清除,显著降低血清尿酸和肌酐水平。高尿酸血症鹌鹑模型实验显示,其一菊苣提取物可显著抑制肝脏尿酸代谢酶XOD及ADA,减少尿酸的生成;其二菊苣提取物可上调鹌鹑肾脏转运相关受体OAT1-LIKE、OAT3-LIKE的mRNA表达,促进鹌鹑肾脏尿酸分泌。
本课题组以菊苣复方干预“脾虚湿盛”症候的高尿酸血症鹌鹑模型,鹌鹑“四诊”表征候改善,表现为粪尿形状改善,湿中及水分减少,气味减轻,羽毛光泽、明亮,舌体呈现淡红色。另外,菊苣颗粒治疗鹌鹑高尿酸血症并腹型肥胖(接近临床“脾虚痰湿”证)的药效研究发现,菊苣颗粒可有效降低鹌鹑血尿酸,并呈现出剂量依赖性,大剂量菊苣颗粒的降尿酸效果优于小剂量。而其机制特点主要体现在菊苣颗粒可抑制血清XOD活性,减少尿酸的生成,可从尿酸生成代谢环节防治高尿酸血症[15]。
3.1.2 基于离体器官模型中药降尿酸活性成分筛选及机制分析
本课题组建立的大鼠离体肾灌流及肠灌流模型在中药降尿酸研究中提示,菊苣有效成分山莴苣苦素、菊苣萜苷K、菊苣萜苷E、秦皮甲素以及菊苣多糖与其代谢物质可调控肠道尿酸转运体ABCG2,调控肾脏尿酸转运体GLUT9、URAT1、OAT1、OAT3等。在离体肾脏灌流及肠灌流模型中,直观观察尿酸经肠道与肾脏途径的排泄,检测到肾脏输尿管流出液与肠道灌流流出液中尿酸含量增高。
3.1.3 基于細胞模型中药降尿酸活性成分确认及降尿酸机制分析
本课题组建立小肠隐窝上皮细胞(IEC-6)模型,观察菊苣成分菊苣酸和山莴苣苦素对肠道嘌呤核苷转运蛋白(CNT2)的影响[16]。IEC-6细胞可内源性表达CNT2,具有生长快速、传代稳定等特点,具有肠上皮细胞的功能,能较好地模拟正常生理条件下肠道嘌呤核苷的转运过程。加入0.1 mmol/L菊苣酸后,腺苷底物转运量显著减少(P<0.01),推测抑制肠道CNT2靶蛋白的活性从而减少肠道嘌呤吸收可能是菊苣降尿酸作用的机制之一。
3.2 中药及中药复方抑制尿酸盐沉积的药效特点及机制分析
本课题组建立的高钙高蛋白饮食诱导的尿酸盐内脏沉积鹌鹑已用于参苓白术散、菊苣及芹槐的干预研究[17-18]。参苓白术散干预后,鹌鹑状态逐渐好转,毛色出现光泽,鹌鹑走动次数增加,舌质逐渐恢复为鲜红色;肾脏部位的尿酸盐结晶随给药时间逐渐减少,在实验期间已基本消失。菊苣提取物可显著缓解肾脏的尿酸盐沉积状况,同时表现出显著的降尿酸效果、能够显著降低血清炎性反应因子水平,推测菊苣提取物抑制尿酸盐沉积的疗效可能与促进尿酸排泄相关。芹槐提取物可改善鹌鹑模型病理组织损伤,减少肾脏组织的尿酸盐沉积,但高剂量芹槐提取物药效不如低剂量芹槐提取物,与此同时,实验结果显示芹槐低剂量组降尿酸效果也优于芹槐高剂量组,提示芹槐提取物治疗尿酸盐沉积存在药效剂量窗口。
3.3 中药及中药复方缓解尿酸盐沉积致炎的药效特点、有效成分及机制研究
3.3.1 基于动物模型中药治疗痛风性关节炎药效特点及机制研究
本课题组通过建立耳廓肿胀、痛风性关节炎等多种炎症模型,采用醋酸扭体法、热板反应等疼痛实验,进行痛风性关节炎的相关药理研究,研究药物的抗炎镇痛作用。本课题组的实验研究表明,菊苣提取物可抑制关节腔注射尿酸盐结晶诱导的急性痛风炎症。通过观察菊苣为主的二秦菊苓汤对小鼠耳廓肿胀、醋酸扭体反应、热板反应及痛风性关节炎大鼠关节肿胀度、组织匀浆IL-1水平的影响[19],证实二秦菊苓汤可抑制二甲苯诱导的小鼠耳廓肿胀、醋酸诱导的小鼠扭体反应,提高小鼠痛阈值,还能干预关节局部炎症小体NLRP3及IL-1、IL-6与TNF-α介导的炎症通路,改善痛风性关节炎大鼠的踝关节肿胀从而达到干预痛风的目的。
3.3.2 基于细胞模型中药缓解炎性反应的有效成分及机制研究
本课题组从硫代乙醇肉汤处理的大鼠腹腔中分离出的巨噬细胞,可用于验证痛风性关节炎与NF-κB、NLRP3信号通路的病理联系[20]。经过菊苣提取物和菊苣代表性成分菊苣酸干预后发现,均可降低尿酸盐结晶诱发巨噬细胞分泌的IL-1β水平,证实了菊苣提取物和菊苣酸的体外抗炎作用。同时经过Western Blot技术分析NF-κB、NLRP3信号通路相关蛋白靶点活性,提示菊苣提取物及菊苣酸可抑制p-p65和NLRP3蛋白表达,通过NF-κB、NLRP3信号通路双重抑制IL-1β的释放。
本课题组另从尿酸诱导的氧化应激与“肠-肾”组织炎症损伤关联角度进行探索分析,选用肠道上皮细胞Caco2、肾脏上皮细胞HKC塑造高尿酸血症细胞模型[21],观察Caco2、HKC细胞中MDA、IL-6水平。研究结果发现高尿酸状态下的Caco2、HKC细胞中MDA、IL-6水平均显著升高,说明高尿酸诱发的炎症损伤存在着氧化应激的参与。菊苣提取物干预后,可显著降低Caco2、HKC细胞中MDA、IL-6水平,提示菊苣提取物可抑制高尿酸状态下氧化应激状况,改善“肠-肾”组织炎症损伤。
4 结语与展望
本课题组构建的痛风病中药效用机制研究平台可作为痛风病中药药效评价及筛选的基础平台。该平台主要包括“成分-疾病”靶标网络分析、病证结合动物模型、器官模型、细胞模型、分子生物学5个层次,可覆盖中药成分验证研究、整体动物的尿酸代谢、尿酸盐沉积、致炎情况药理研究、靶器官对尿酸排泄转运的干预研究、细胞及分子药理观察与作用靶点机制分析等研究过程,贯通痛风病发病全流程,从干预尿酸生成、排泄,尿酸盐沉积及尿酸盐致炎多方面系统评价中药防治痛风病药效作用及特点,阐明中药防治机制,可为临床防治痛风中药的研发提供参考和指导。
目前,该平台已对菊苣等中药防治痛风病的药效开展评价研究及机制探索,研究结果提示菊苣可从减少尿酸的生成、促进尿酸的排泄以降尿酸,缓解尿酸盐沉积,抑制尿酸盐致炎三方面综合防治痛风病的发生、发展。该平台为痛风病的中药开发研究提供合适实验方法和科学依据等,通过对中药的药效进行评价研究,阐明防治痛风病中药的药理机制,可为客观诠释中药防治痛风药效提供科学依据,为抗痛风病中药的继承和创新研究提供新思路和新方法,切实服务于临床痛风病的治疗和药物研发。
随着痛风病中药效用机制研究平台建立,活性成分及其药理作用将得到充分挖掘,中医药防治痛风病研究工作的不断深入,将进一步推动痛风病病理、药理研究发展,为临床提供可满足痛风病患者需求的优质中药,为抗痛风病中药的开发和利用提供更加广阔的前景。
参考文献
[1]中华医学会内分泌学分会.中国高尿酸血症与痛风诊疗指南(2019)[J].中华内分泌代谢杂志,2020,36(1):1-13.
[2]Fitzgerald JD,Dalbeth N,Mikuls T,et al.2020 American College of Rheumatology Guideline for the Management of Gout[J].Arthritis & Rheumatology,2020,72(6):744-760.
[3]杨澍,高秀清,高杉.抗痛风药不良反应文献分析[J].中国药房,2016,27(5):624-627.
[4]孙宇洁,付书璠,李慧,等.近30年中医药治疗痛风临床用药规律数据挖掘研究[J].中药药理与临床,2020,36(4):208-213.
[5]申启荣,王江录,余宙,等.具有降尿酸作用的药食两用中药的筛选[J].南昌大学学报:理科版,2015,39(2):175-178.
[6]解颖.中药复方治疗急性痛风性关节炎的临床研究[J].科技资讯,2019,17(3):252-253.
[7]杨加琼.复方柴胡散治疗鸡尿酸盐沉积效果初探[J].中国农学通报,2006,122(11):50-53.
[8]刘小青,张冰,刘春梅,等.鹌鹑高尿酸血症模型建立初探[J].中国病理生理杂志,2001,17(10):111-113.
[9]王海鸽,张冰,林志健,等.高蛋白高钙日粮对鹌鹑尿酸代谢及痛风发生的影响[J].中国家禽,2018,40(19):22-27.
[10]林志健,张冰,刘小青,等.基于数字化定量的高尿酸血症鹌鹑模型“四诊”证候研究[J].北京中医药大学学报,2013,36(5):317-321,361.
[11]朱深银,周远大,刘庆山,等.离体大鼠肾脏灌流技术在发现和评价促尿酸排泄药物中的初步应用[J].中国药理学通报,2006,22(12):1452-1456.
[12]Wang Y,Lin ZJ,Zhang B,et al.Cichorium intybus L.promotes intestinal uric acid excretion by modulating ABCG2 in experimental hyperuricemia[J].Nutrition & Metabolism,2017,14:38.
[13]Wang Y,Lin ZJ,Zhang B,et al.Chicory(Cichorium intybus L.)inhibits renal reabsorption by regulating expression of urate transporters in fructose-induced hyperuricemia[J].中医科学杂志(英文),2019,6(1):84-94.
[14]李丽玉.基于肾脏排泄途径的菊苣降尿酸作用机制研究[D].北京:北京中医药大学,2015.
[15]林志健.高尿酸并腹型肥胖鹌鹑模型证候特征及菊苣颗粒的作用机制研究[D].北京:北京中医药大学,2012.
[16]周月.基于分子对接技术探讨菊苣抑制嘌呤吸收作用机制[D].北京:北京中医药大学,2017.
[17]王海鸽.鹌鹑痛风模型的建立及示例药应用研究[D].北京:北京中医药大学,2019.
[18]褚梦真.鹌鹑尿酸性肾病动物模型的建立与应用初探[D].北京:北京中医药大学,2020.
[19]聂安政.二秦菊苓汤处方、工艺优化及干预痛风作用研究[D].北京:北京中医药大学,2017.
[20]Wang Y,Lin ZJ,Zhang B,et al.Cichorium intybus L.Extract Suppresses Experimental Gout by Inhibiting the NF-κB and NLRP3 Signaling Pathways[J].International Journal of Molecular ences,2019,20(19):4921.
[21]王雨,林志健,張冰.中药菊苣改善氧化应激性炎症介导的“肠-肾”尿酸排泄研究[J].中华中医药杂志,2020,35(5):2552-2557.
(2020-12-10收稿 责任编辑:徐颖)
基金项目:国家自然科学基金项目(U20A20406,81673618);国家科技重大专项“重大新药创制”项目(2017ZX09301024)
作者简介:林志健(1983.05—),男,博士,副教授,执业药师,硕士研究生导师,研究方向:中药防治代谢性疾病研究,E-mail:linzhijian83@126.com
通信作者:张冰(1959.08—),女,博士,教授,主任医师,博士研究生导师,研究方向:中药防治代谢性疾病研究,E-mail:zhangbing6@263.net

