钼化工废水中氨氮测定影响因素及消除方法
蒙 欢
(金堆城钼业股份有限公司质量计量监测中心,陕西 渭南 714000)
0 引 言

根据标准HJ535-2009《水质 氨氮的测定 纳氏试剂分光光度法》所述,水样中的悬浮物、余氯、钙镁等金属离子以及有机物[1]等都会影响氨氮的测定,再加上其他误差的影响,造成测定结果有很大误差,而钼化工废水中氨氮含量的多少是指导生产单位废水处理设施稳定运行和排放的依据,因此氨氮含量的准确测定尤为重要。本文从以下几个方面分析了影响氨氮测定的因素以及消除方法,以保证检测数据准确报出,进而指导生产。
1 试剂和设备
1.1 试验主要试剂
除非另有说明,本试验所用水均为无氨环境下用超纯水设备制备。
无氨水、氯化铵(优级纯)、酒石酸钾钠(ρ=500 g/L)、硫代硫酸钠溶液(ρ=3.5 g/L)、硼酸溶液(ρ=20 g/L)、硫酸锌、氢氧化钠等。
纳氏试剂:称取16.0 g氢氧化钠,溶于50 mL水中,冷却至室温。称取7.0 g碘化钾加入到前面50 mL氢氧化钠溶液中,用水稀释至100 mL。贮于聚乙烯瓶内,用聚乙烯盖子盖紧,于暗处存放,有效期一年。
1 000 ug/mL氨氮标准贮备溶液:称取3.819 0 g 氯化铵(100~105 ℃干燥2 h),溶于水中,移入1 000 mL容量瓶中,稀释至标线。
10 ug/mL氨氮标准工作溶液:吸取氨氮标准贮备溶液5.00 mL于500 mL容量瓶中,稀释至刻度。临用前配制。
1.2 主要试验仪器
723N可见分光光度计,20 mm比色皿;pH计;智能一体化蒸馏仪;超纯水制备系统等。
2 试 验
2.1 试验原理
水中氨或铵离子与纳氏试剂(碘化汞和碘化钾的碱性溶液)发生强烈化学反应,生成淡红棕色络合物,根据朗伯-比尔定律,该络合物在波长420 nm处[1]的吸光值与氨氮含量成正比。
2.2 标准曲线的绘制
在8个50 mL比色管中,分别加入0、0.50、1.00、2.00、4.00、6.00、8.00、10.00 mL氨氮标准工作曲线溶液,其所对应的氨氮含量分别为0、5.0、10.0、20.0、40.0、60.0、80.0、100.0 μg,加水至标线,加入1.0 mL酒石酸钾钠溶液,摇匀,再加入纳氏试剂1.0 mL,摇匀。放置10 min后,在波长420 nm下,用20 mm比色皿,以水为参比,测量其吸光度。以空白校正后的吸光度为纵坐标,以其对应的氨氮含量(μg)为横坐标,绘制校准曲线,见图1。工作曲线为:A=0.006 8C+0.001 4,相关系数0.999 9。
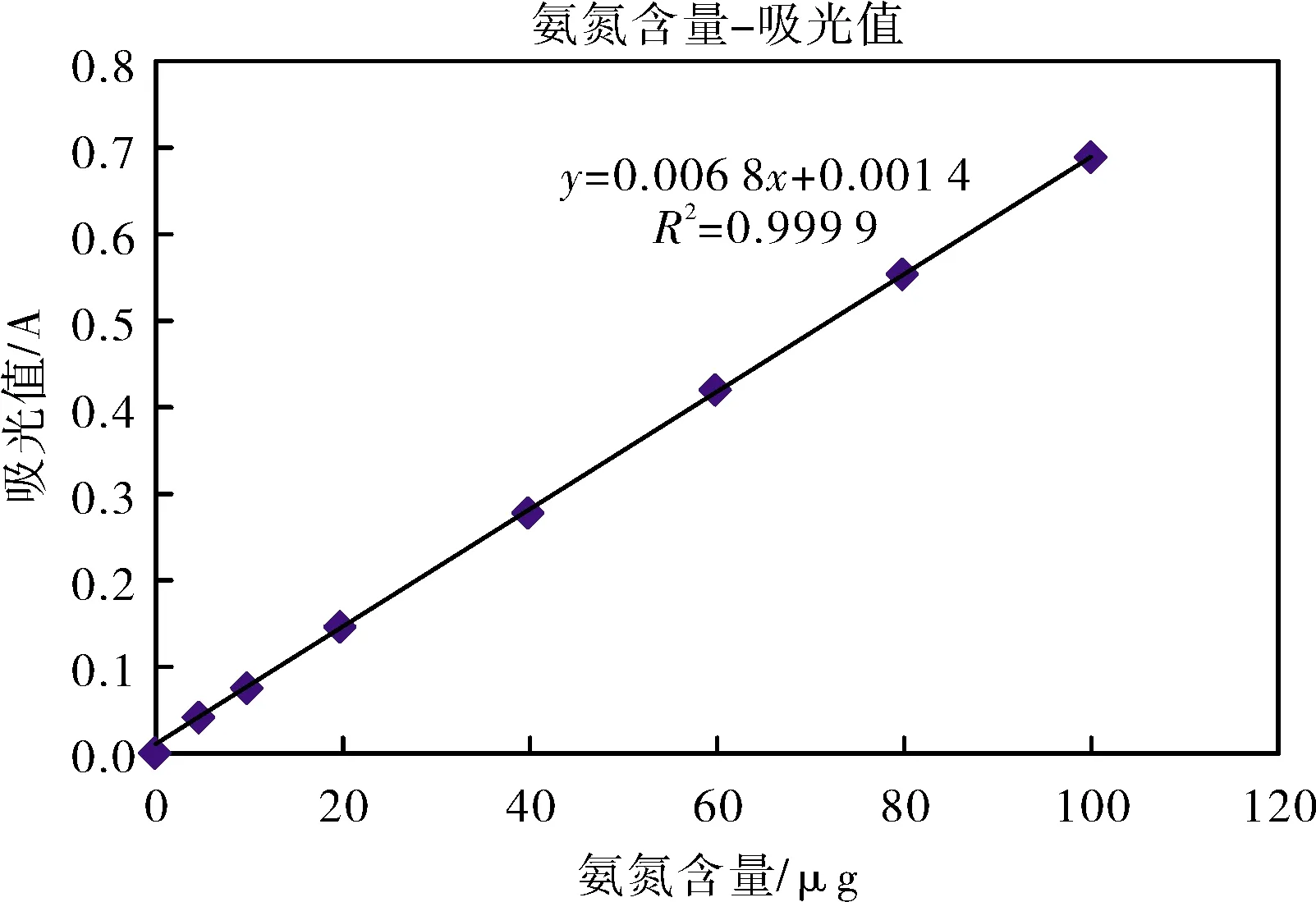
图1 氨氮工作曲线
2.3 样品测定
(1)清洁水样:直接取50 mL,按与标准曲线相同的步骤测量其吸光度。
(2)有悬浮物或色度干扰的水样:取经预处理的水样50 mL,按与标准曲线相同的步骤测量其吸光度(预处理的水样显色之前应该控制溶液体系pH为中性[1])
(3)预处理方法。
除余氯:加入适量硫代硫酸钠溶液去除,用淀粉-碘化钾试纸检验是否除尽。
絮凝沉淀:100 mL样品中加入1 mL硫酸锌溶液和0.1~0.2 mL氢氧化钠,调节pH约为10.5[1],混匀,放置使之沉淀,用吸量管吸取适当体积上清液进行分析。
蒸馏法:取50 mL硼酸溶液于接收瓶内,并将冷凝管出口插入硼酸溶液液面之下。取250 mL样品于蒸馏烧瓶内,用pH计测定其pH值,确保其在6.0~7.4之间[1],必要时用氢氧化钠或盐酸调节,加入2.5 g轻质氧化镁及2~3粒玻璃珠,加热蒸馏。弃去初始的30 mL馏出液,收集馏出液至200 mL时停止蒸馏,加水定容至250 mL。
3 干扰因素试验与结果讨论
3.1 水样本身干扰物质
本次试验所用水为某化工生产企业园区废水,按照HJ535-2009《水质 氨氮的测定 纳氏试剂分光光度法》[1]中水样采集方法,采集本文试验废水为:集中废水池(紫红色样品),编号为1号;集中处理池(颜色不定,微黄、棕色或橙黄浑浊样品),编号为2号;外排口废水(无色澄清样品),编号为3号。
3.1.1 水样有色、浑浊的影响
有色度和浑浊干扰的水样,一般测定结果会偏高。分别取两个不同的1号、2号样品,记为1号-1、1号-2、2号-1、2号-2进行预处理,分析结果见表1。
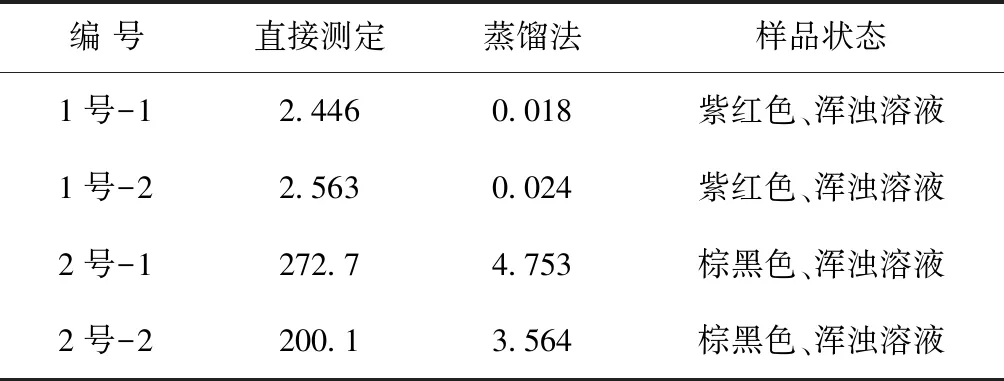
表1 不同预处理方法氨氮测定结果 mg/L
消除方法:有颜色或浑浊的水样需进行蒸馏处理,消除色度干扰。当氨氮浓度超过曲线最大浓度时,显色会出现浑浊现象,此时需要对样品进行稀释处理,稀释后溶液显色时的颜色在最低标准曲线浓度和最高标准曲线浓度对应的颜色之间,即可消除影响。
3.1.2 余氯的影响
样品中的余氯会与Hg离子发生反应[1],当余氯含量较高时,这个反应优先发生,导致纳氏试剂与氨氮的反应减弱或无法进行,进而影响氨氮结果的测定。
在浓度为0.502±0.023 mg/L的样品中加入不同浓度的氯离子标准样品测定氨氮结果,结果见表2。
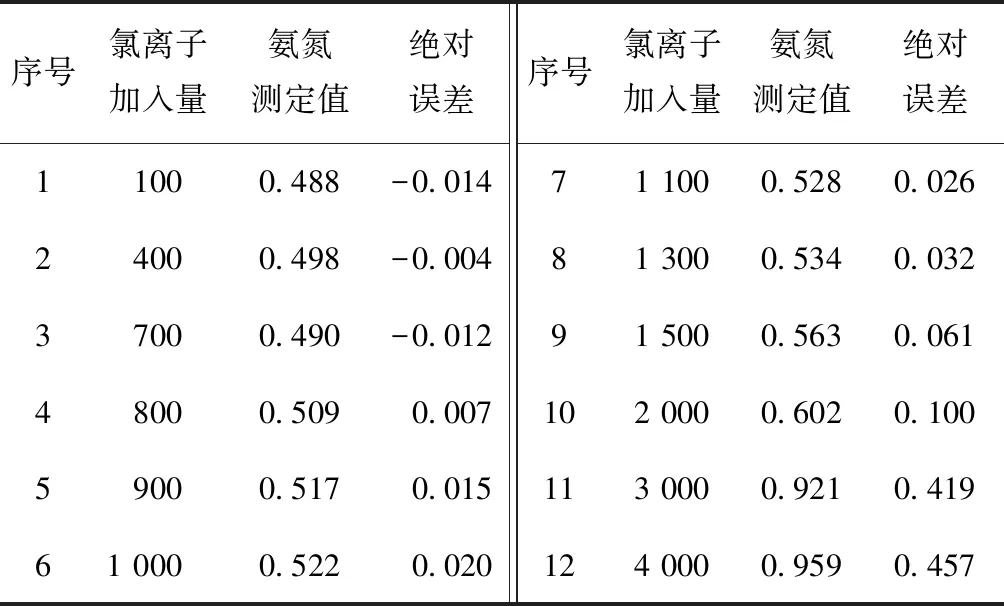
表2 氯离子对氨氮测定结果的影响 mg/L
由表2可以看出:氯离子浓度低于1 100 mg/L时,对氨氮结果影响不大,都在误差范围内(±0.023);当氯离子浓度超过1 100 mg/L时,测定结果偏高,并且氯离子浓度越高,影响越大。
对表2中超过误差范围(±0.023)的样品进行絮凝沉淀和预蒸馏处理,结果见表3。

表3 不同浓度氯离子水样氨氮测定结果 mg/L
由表3可以看出:氯离子浓度介于1 100~4 000 mg/L之间时,采用絮凝沉淀法进行预处理,效果不明显,而采用预蒸馏处理可以达到很好的效果。
3.1.3 金属离子的影响
水样中的钙、镁等金属离子在碱性条件下容易水解产生沉淀,影响氨氮的测定,一般加入酒石酸钾钠进行掩蔽即可达到效果[1];但是当含量较高时,易与纳氏试剂中OH-反应生成沉淀或者产生浑浊,此时需要进行预蒸馏处理,消除影响。
3.1.4 水样存放时间
由于工业废水中存在大量的干扰因子,存放时间不同会对结果产生影响,因此进行不同保存时间对氨氮浓度的测定试验。根据HJ535-2009对样品进行预处理[1],然后进行吸光值测定,结果见表4。
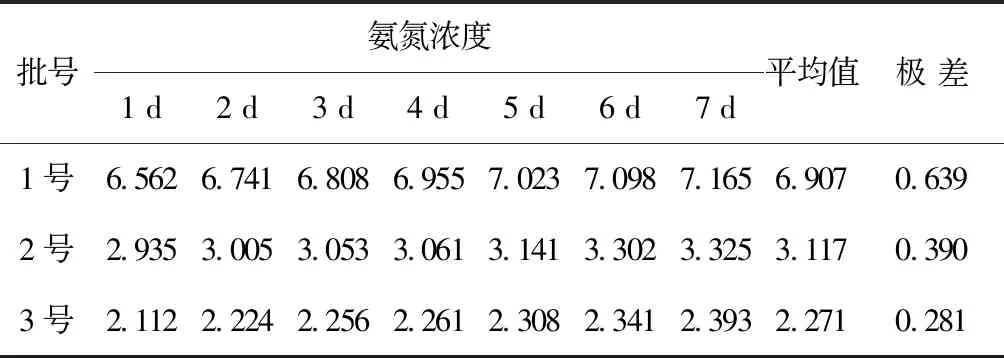
表4 水样保存时间对氨氮结果的影响 mg/L
由表4可以看出:随着时间的延长,工业废水中氨氮含量总体呈增加趋势,2号样品因加入处理药剂,不同时间反应程度不同,导致样品的颜色不同,氨氮含量也有所不同。因此采集的样品应该尽快分析,若不能及时分析,应加入H2SO4(在硫酸中可以将氨气转化为稳定且不挥发的硫酸铵,防止氨的流失)调节pH≤2(此时各种形态的氨氮转化为不挥发性的铵盐),2~5 ℃(可减缓物理挥发和化学反应速率)下可保存7 d[1]。
3.2 显色条件的影响
3.2.1 反应体系pH值
pH值对氨氮测定有显著影响。取预蒸馏处理的样品加入不同量纳氏试剂调节体系pH值,再测定氨氮结果,具体试验数据见表5。
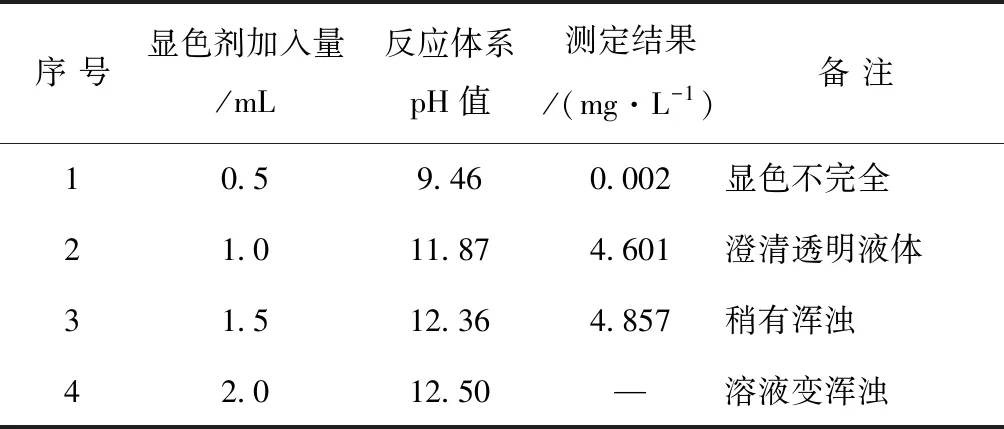
表5 反应体系pH值对氨氮结果的影响
3.2.2 显色温度及显色时间
温度影响纳氏试剂与氨氮反应的速率,进而影响氨氮的测定结果。测定氨氮含量为20 μg的标准溶液,以纯水为参比,测量其吸光值。试验中温度梯度为5、10、15、20、25、30、35 ℃;时间梯度为5、10、15、20、25、30、35、40 min。试验结果见图2、图3。
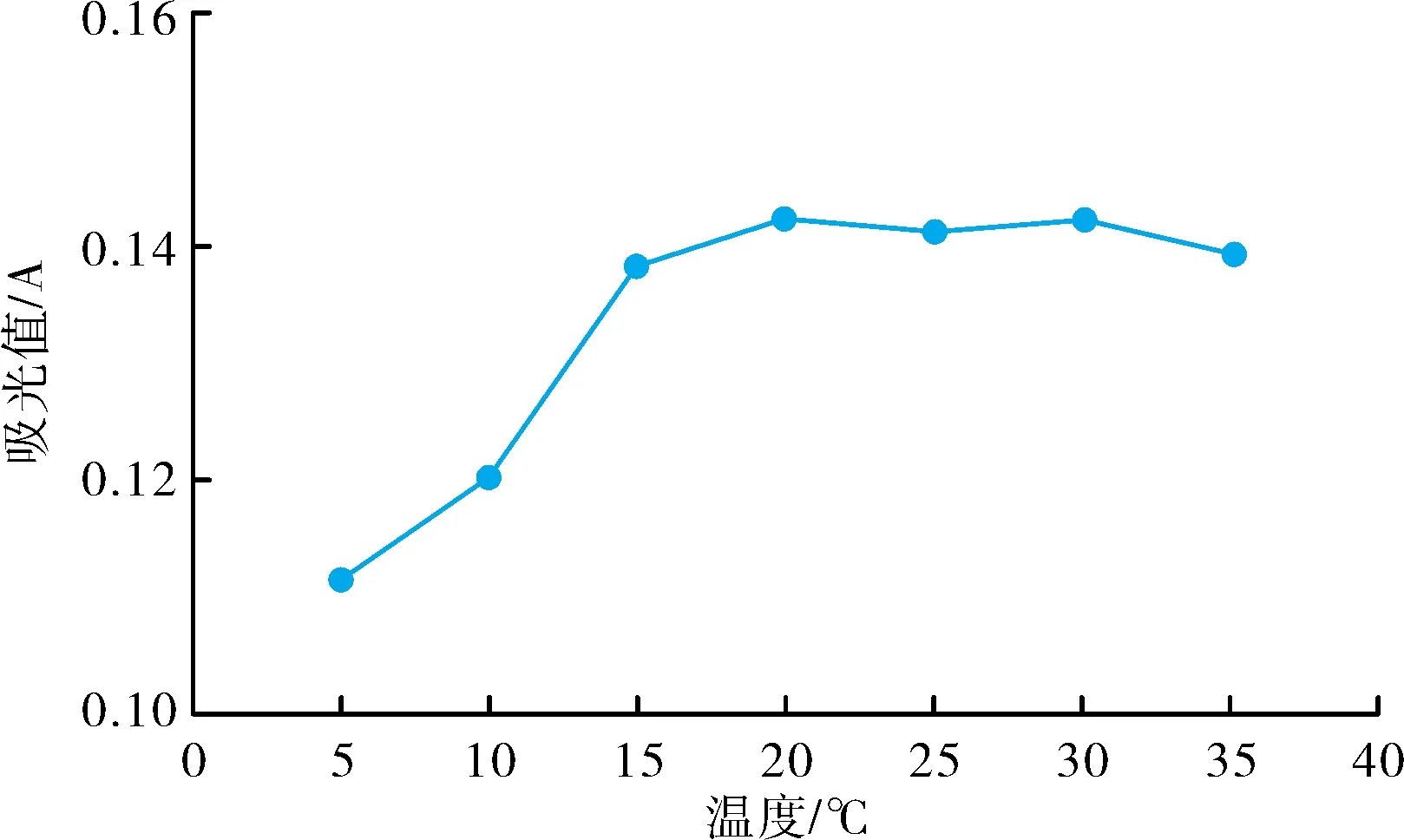
图2 吸光度与显色温度的关系
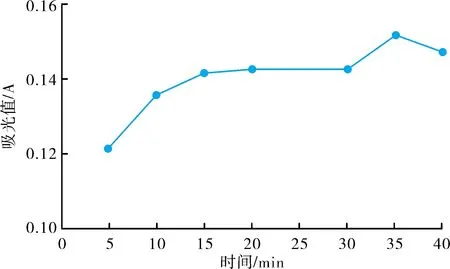
图3 吸光度与显色时间的关系
由图2、图3可知:温度在15~30 ℃时,可以保证分析结果的可靠性;温度在5~15 ℃时,显色不完全,吸光值变化大,导致结果偏低;>30 ℃时,溶液体系会褪色,吸光值下降。显色时间在15~30 min之间,吸光度基本无变化,颜色较稳定,显色时间<15 min,显色不完全,测定结果偏低,显色时间>30 min,吸光值不稳定,结果不可靠。
4 结 论
本文通过分析影响钼化工废水中氨氮含量测定的因素及其消除方法,确定了适宜的实验条件,确保了氨氮检测结果的准确性及可靠性。其中有色浑浊水样会导致氨氮结果偏高,氯离子浓度1 100~4 000 mg/L时,测定结果偏高,水样中钙镁离子含量太高会产生沉淀,都会影响氨氮测定,均需要进行预处理;水样中氨氮含量随保存时间推移总体呈增加趋势,因此采集后应立即分析。除此之外,在测定过程中应严格控制反应体系pH在11.8~12.3范围内,显色温度在15~30 ℃,显色时间在15~30 min。

