经导管主动脉瓣置换术在高龄主动脉瓣狭窄患者中的应用
徐东辉,罗新锦,张晶,丘俊涛,李飞,王旭
(中国医学科学院阜外心血管病医院心外科结构二病区,北京 100037)
主动脉瓣狭窄( aortic valve stenosis,AS)是最常见的心脏瓣膜病之一,具有症状的AS可以明显缩减患者的预期寿命。在老年人口中,主动脉瓣狭窄有着较高的比例,在75~76岁人群中中重度主动脉瓣狭窄患者占2.5%[1],而80岁以上的人群中该比例上升至8.1%[2]。高龄主动脉瓣狭窄患者往往合并较多其他疾病,很多患者无法耐受常规的外科手术,只能采取药物保守治疗。而对于主动脉狭窄的患者,药物治疗往往不能起到有效的缓解。经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)创伤较小,目前已应用于高龄主动脉瓣狭窄患者的治疗。本研究旨在探讨TAVR在高龄主动脉瓣狭窄患者中的应用,报道如下。
1 对象与方法
1.1 研究对象
回顾性分析2019年1月 至2020年12月于中国医学科学院阜外心血管病医院行TAVR手术的主动脉瓣狭窄患者142例。其中男性90例,女性52例;年龄(72.45±8.95)岁。随访时间3个月至1年。
纳入标准: (1)中危以上主动脉瓣狭窄(美国胸外科医师协会手术风险评分> 4分);(2)年龄≥65岁。排除标准:(1)存在抗凝禁忌证患者;(2)脑血管事件急性期;(3) 合并需同期再血管化的冠心病。
1.2 方法
1.2.1 术前准备 术前患者均行经胸超声心动图检查和冠状动脉螺旋CT(multi-slice computed tomography,MSCT)检查。超声心动图在短轴切面测量主动脉瓣环直径。CT资料经荷兰PIE医学影像公司的3 MENSIO软件进行分析重建和主动脉瓣环平面、流出道平面、窦管交界平面、升主动脉平面进行测量,评估主动脉无窦、右窦、左窦的大小及冠状动脉开口高度。根据评估结果和术中造影情况,选取合适大小的术中瓣膜。
1.2.2 手术方法 手术均在外科杂交手术室内进行,患者行监护麻醉。经颈内静脉植入心内膜临时起搏导线至右心室。根据患者术前CT测量主动脉瓣环内径,确定植入支架瓣膜的尺寸。手术开始的同时支架瓣膜进行组装。根据术前下肢动脉CT评估,选择主入路切开直视穿刺股动脉,置入10 F下肢动脉鞘管。对侧副入路置入6 F角度猪尾导管至无冠窦窦底,并行主动脉根部造影验证投照角度。使三个主动脉窦窦底平面与视频平面完全垂直,并且按照无冠窦、右冠窦、左冠窦顺序从左至右一字排开。经主入路将猪尾导管置入左心室,并交换Landerquist支撑导丝。交换20 F或18 F大鞘,准备进行瓣膜释放操作。将瓣膜输送器沿主入路送至主动脉根部,释放时将临时起搏器调至120~180次/min,根据不同根部结构特点,采取不同释放策略,将支架瓣膜尽量与瓣环完全贴合。释放完成后撤出输送系统,并交换猪尾导管至左室内。经副入路行主动脉根部造影,验证支架瓣膜位置及功能。术中应用启明公司的Venus-A瓣膜,根据患者情况选用瓣膜型号分别为23、26、29、32号。
1.3 统计学处理

2 结 果
1.1 2组患者一般资料比较
共纳入患者142例,其中年龄≥80岁患者22例(15.5%)为高龄老年组,65岁≤年龄<80岁患者120例(84.5%)为老年组。2组性别、身高、体质量、高血压发生率、糖尿病发生率、脑血管病发生率、外周动脉粥样硬化发生率、心肌梗死病史、慢性肺病、急诊手术例数、心功能分级、肺高压发生率、左室舒张末径、主动脉瓣的峰值压差及平均压差比较,差异均无统计学意义(均P>0.05)。2组左室射血分数比较,差异有统计学意义(P<0.05;表1)。
1.2 2组患者围手术期临床结果比较
2组中转外科手术发生率、术中使用体外循环辅助率、术中左室破裂发生率、术后使用体外膜肺氧合辅助循环率、术后外周血管并发症、术后起搏器植入率、术后致残性脑卒中、围术期死亡发生率比较,差异均无统计学意义(均P>0.05;表2)。
非股动脉入路患者共6例(4.2%)。老年组:左侧锁骨下动脉入路1例(0.7%),升主动脉入路1例(0.7%),经颈动脉入路3例(2.5%);高龄老年组:经颈动脉入路1例(4.5%),差异均无统计学意义(均P>0.05)。
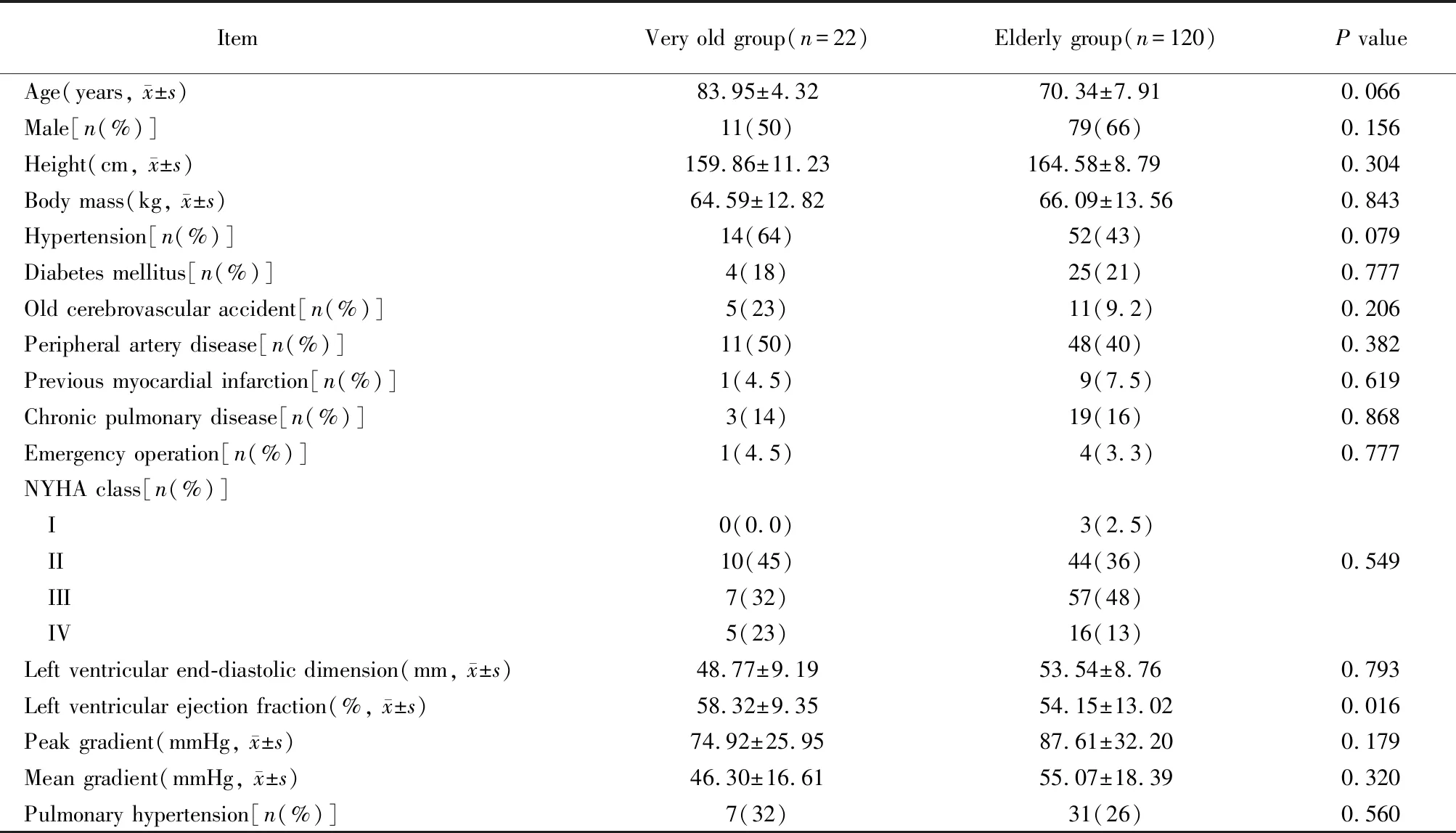
表1 2组患者一般资料比较
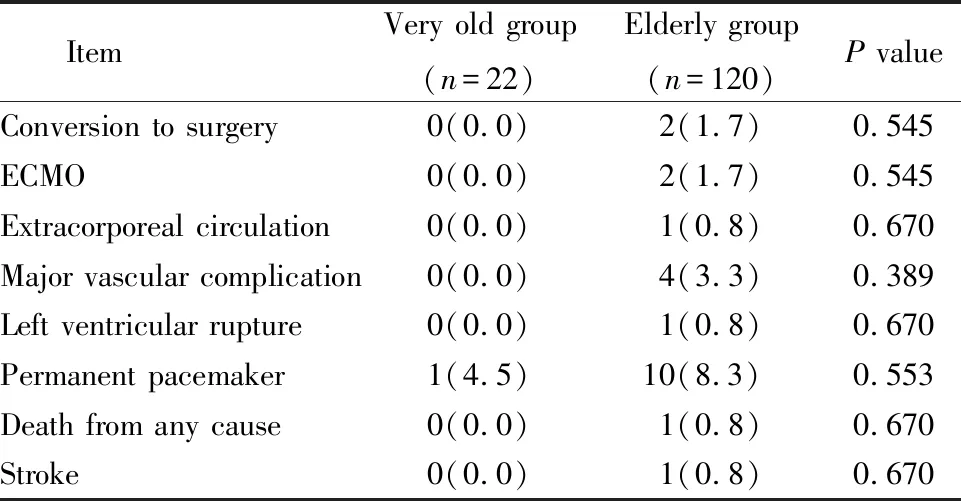
表2 2组患者围手术期临床结果比较
3 讨 论
对于症状严重的主动脉瓣狭窄患者,如果只进行保守治疗,预后较差,术后1年的死亡率可以达到30%甚至更高[3]。在TAVR之前,常规的外科手术是治疗主动脉瓣狭窄的首选方法。当然随着年龄的增长,手术的死亡风险会显著增加[4]。同时老年人往往合并较多的基础疾病,增加了手术风险,使得80岁以上的患者很多无法接受外科的治疗。在Bouma等[5]的研究中,高龄患者(≥80岁)中进行外科换瓣的实际发生率的只有 23.8%。TAVR作为微创技术,自2002年首次应用于临床以来[6],改变了传统上主动脉瓣狭窄患者的治疗方法,对于很多高危及无法耐受手术的患者,取得了较好的临床效果[7,8]。根据本研究的结果分析可以发现,对于主动脉瓣狭窄的患者,高龄老年患者与老年患者,两者围手术期的各项并发症的发生率均无明显的统计学差异。可见TAVR手术对于高龄患者,是一种有效的治疗方法。
本研究中,高龄老年组无死亡病例,老年组死亡1例(0.75%),远低于国际其他中心报道。分析原因,本研究数据为2019年及2020年较新数据,患者的术前评估,管理及术中策略的制定、术中的操作,已有较多成熟的经验。从侧面验证,目前经导管主动脉瓣置换术,已成为较为成熟的技术。致残性脑卒中和外周血管的并发症也是让人担心的问题。有研究表明,年龄的增加会增加卒中和外周血管并发症的发生率[9]。本研究认为,这可能与血管的钙化和脆性增加有关。本研究认为脑卒中的发生与瓣环及瓣膜的钙化有关,过度的球囊扩张会造成钙化的脱落,造成致残性的脑卒中和冠状动脉堵塞。在球囊扩张时,首先应注意球囊的选择,避免过大的球囊,其次应注意扩张时,要逐步增加用力,防止瓣膜暴力撕脱。同时对于高龄的患者,也应尽量避免后扩张,高龄患者瓣膜薄弱,后扩张会增加主动脉夹层的发生率。
本研究经颈动脉入路完成4例,经左侧锁骨下动脉完成1例,经升主动脉完成1例,其余138例均经股动脉完成。经股动脉路径创伤最小,最为经典,但高龄患者常有下肢动脉的狭窄。术前的评估尤为重要,如果钙化严重,建议切开直视下操作,术后股动脉缝合应注意内膜的完整性。如下肢入路无法完成操作,可以尝试颈动脉或锁骨下入路。经心尖及升主动脉入路术后生活质量略差于经外周血管入路,但仍好于接受常规手术的患者[10]。微创入路的TAVR对于80岁以上的患者,无论是身体机能的恢复,还是心理健康的恢复,都有比较积极的作用[11]。
抗凝是主动脉瓣术后抗凝的重要问题,在既往的临床试验中,很多中心及专家推荐使用双抗进行抗凝治疗[12]。而在随后的临床中发现,使用双抗抗凝的患者可能存在亚临床血栓,影响瓣叶的开合[13]。我们的经验是对于没有抗凝禁忌证的患者,推荐使用华法林抗凝半年,对于有抗凝禁忌证或者合并严重冠心病的患者,推荐使用双抗治疗。对于高龄的患者,应评估患者出凝血情况,谨慎选择抗凝方案。
综上,高龄主动脉瓣狭窄患者手术风险较高,如不进行手术治疗,也有很高的死亡率。经导管主动脉瓣置换术,手术创伤较小,有较好的临床效果,对于高龄主动脉狭窄患者,是一种有效的治疗方法。本研究为单中心的回顾性分析,随访时间较短,有待更多的研究及数据指导高龄主动脉瓣狭窄患者的治疗。
中华老年多器官疾病杂志2021年6期
