纤维化性间质性肺疾病预后因素的前瞻性队列研究
赵铁梅,刘凯迪,段智梅,华琳,张明月,圣朝军,吴洁
(1解放军总医院第一医学中心呼吸与危重症医学科,北京 100853;2首都医科大学生物医学工程学院生物医学信息学系数学与生物信息学教研室,北京 100069)
纤维化性间质性肺疾病(fibrosing interstitial lung diseases,FILD)是肺部高分辨CT(high resolution CT,HRCT)表现为纤维化的一大类间质性肺疾病的总称。FILD中特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)最典型,是一种随着肺功能逐渐恶化发生的致死性疾病,诊断后其中位生存期约3~5年。其他可以引起肺纤维化的间质性肺疾病包括结缔组织病相关间质性肺病(interstitial lung disease associated with connective tissue diseases,CTD-ILD)、慢性过敏性肺炎、非特异性间质性肺炎等。2018年Wells等[1]首次在纤维化性间质性肺疾病中提出了进行性纤维化型的概念。同期研究指出,在非IPF的间质性肺疾病中,18%~32%的患者可以发展为进行性纤维化型,预后同样不佳[2]。因此,我们对FILD患者进行前瞻性研究,总结患者的临床特点,分析发展为进行性纤维化型的风险因素,给临床医师提供指导,改善患者预后。
1 对象与方法
1.1 研究对象
选择2019年5月至12月在解放军总医院呼吸内科诊断为FILD的患者进行临床观察。入组诊断标准:肺部HRCT表现为肺纤维化[3],网状影伴牵拉性支气管扩张,伴或不伴有蜂窝影。疾病诊断标准:IPF的诊断参照特发性肺纤维化诊断标准——Fleischner学会白皮书[4]。结缔组织病参照各自的国际通用标准进行诊断[5-8]。本研究通过解放军总医院医学伦理委员会审批(伦理批号:S2019-091-01号),研究经患者及家属知情同意,并签署知情同意书。
1.2 方法
1.2.1 临床资料 收集患者的年龄、性别、环境职业暴露、吸烟、基础疾病、治疗用药等资料,行肺CT、肺功能、血气分析等检查或检验;听诊有无爆裂音,查看有无杵状指;给予患者6 min步行试验(6-minute walk test,6 MWT)、加利福尼亚大学圣地亚哥分校呼吸困难问卷(shortness of breath questionnaire,SOBQ)进行呼吸困难评分[9],并随访1年。
1.2.2 肺部影像评分 肺部HRCT表现参照文献标准按照蜂窝影、网格影分别进行评分[10]。
1.2.3 病情的判断 随访1年时,参照George提出的标准[11],满足下列1条判断为进行性纤维化型:(1)用力肺活量(forced vital capacity,FVC) 相对下降≥10%;(2)FVC相对下降≥5%,肺一氧化碳弥散量(diffusion capacity of carbon monoxide,DLCO)下降≥15%;(3)FVC相对下降≥5%, HRCT显示纤维化增加;(4)FVC相对下降≥5%,症状加重;(5)症状加重,HRCT显示肺纤维化增加。未达到进行性纤维化型标准的判断为病情稳定。
1.3 统计学处理
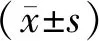
2 结 果
2.1 临床资料
58例患者中,29例吸烟,吸烟患者的吸烟年支为(688.96±620.54)。60.34%(35/58)患者诊断为IPF,24.14%(14/58)诊断为CTD-ILD,15.52%(9/58)不能诊断为IPF和CTD-ILD的患者归为其他原因所致的肺纤维化(表1)。
2.2 预后随访结果
随访至1年,43.10%(25/58)患者病情评估为稳定;22.41%(13/58)患者在后期随访时因不愿再次行肺功能、肺CT检查,无法进行病情评估;20.69%(12/58)患者发展为进行性纤维化型,其中IPF患者占28.57%(10/35),CTD-ILD患者占14.29% (2/14)(P=0.466)。13.79%(8/58)患者死亡,其中IPF患者占17.14%(6/35),CTD-ILD患者占14.29%(2/14)(P=1.000);死亡原因:6例为纤维化急性加重,1例因肺癌行放疗出现放射性肺炎,1例为脑梗死。

表1 纤维化性间质性肺疾病患者的临床特征
2.3 基于竞争风险模型的分析
2.3.1 发展为进行性纤维化型的单因素分析 发展为进行性纤维化型的风险因素是诊断为IPF,HRCT网格影评分高和HRCT蜂窝影评分高(表2)。
2.3.2 死亡风险因素的单因素分析 单因素分析结果显示死亡的风险因素是6 min步行距离(6-minute walk distance,6MWD)短和SOBQ评分高(表3)。其中6 min步行试验按步行距离分组(<300 m、300 m≤MWD<375 m、375 m≤6MWD<450 m、≥450 m),进行Gray检验,<300 m的患者死亡率明显增高(P=0.016)。
2.3.3 多因素分析 将单因素分析结果显著的因素采用Fine-Gray竞争风险回归模型进行多因素分析。结果显示,HRCT网格影评分高是发展为进行性纤维化型的风险因素(RC=0.687,HR=1.99,95%CI1.03~3.85,P=0.04);未发现死亡的风险因素。

表2 FILD发展为进行性纤维化型的风险因素

表3 FILD患者死亡的风险因素
3 讨 论
FILD是一组具有不同病因、治疗方法及一系列疾病表现的异质性疾病。FILD中IPF预后不佳已得到共识。2019年Wijsenbeek等[2]发表的研究显示,18%~32%非IPF的间质性肺疾病患者可以发展为进行性纤维化型,被诊断后患者生存时间仅为30~45个月,预后同样不佳。本研究结果显示,随访1年,已有13.79%(8/58)的患者死亡,其中CTD-ILD患者死亡率与IPF患者相仿,75.00%(6/8)的死亡原因为纤维化急性加重;除外死亡患者,仍有20.69%(12/58)的患者可发展为进行性纤维化型,与国外报道相似,值得临床医师重视。其中,诊断为IPF的患者发展为进行性纤维化型的风险更高,提示我们对IPF患者要给予更多关注。
既往针对间质性肺疾病预后风险的研究大多针对死亡风险。从HRCT影像类型来看,普通型间质性肺炎型(usual interstitial pneumonia,UIP)的死亡率高于其他类型。Yunt等[12]分析了类风湿关节炎相关间质性肺疾病HRCT不同影像表现与预后的关系,结果显示,确定UIP型(以胸膜下肺基底部分布为主,异常的网格影,蜂窝样改变伴或不伴牵拉性支气管扩张)与可能UIP型(胸膜下肺基底部分布为主,异常的网格影)的死亡率无显著差异,把UIP型与可能UIP型合并为一组后与非特异性肺炎型(基底部分布为主,磨玻璃影范围大于网格影)相比,生存率明显下降(P=0.03)。我们也针对肺纤维化的常见影像,蜂窝影和网格影进行研究,单因素分析结果显示,HRCT网格影和蜂窝影评分高是发展为进行性纤维化型的风险因素,多因素分析结果显示HRCT网格影评分高是发展为进行性纤维化型的风险因素,提示我们对FILD患者要仔细查看和动态随访HRCT网格影和蜂窝影的范围和变化,对范围广、随访后出现进展的患者要给予积极治疗,以改善预后。从患者的症状和运动耐量来看,常应用6 MWD、呼吸困难评分来进行评估。加拿大学者Chan等[13]回顾了2011年至2017年诊断为CTD-ILD的患者,结果显示,较低的基线6 MWD是死亡的预测因子,基线6 MWD每下降100 m的风险比为1.4(95%CI1.1~1.7)。本研究结果亦显示,6 MWD<300 m、SOBQ评分高的患者死亡风险增加,提示我们在临床工作中要详细询问患者的气短症状,如有条件应进行6 MWD评估。从合并症来看,FILD患者容易出现一种或多种临床合并症。Raghu等[14]将1990年到2015年的文献进行分析,入选了126项研究,结果显示,IPF患者常见的合并症为肺动脉高压、肺癌、慢性阻塞性肺疾病、睡眠呼吸暂停、缺血性心脏病、胃食管反流,这些合并症可增加IPF的死亡风险。本研究结果也提示,74.14%的FILD合并一种或多种临床合并症,最常见分别为肺气肿和(或)肺大泡、胃食管反流、高血压病、糖尿病、冠心病,虽然统计分析结果未提示这些疾病是发展为进行性纤维化型或死亡的风险因素,但不除外与样本量偏小、随访时间偏短有关,这些是本研究的不足之处。从抗纤维化治疗来看,吡非尼酮治疗进行性FILD可延缓FVC的下降[15],我们的研究中因为部分入组患者使用吡非尼酮不正规(中断或减量应用),未做相关病情进展和死亡的风险分析。
综上,本研究结果显示,FILD患者预后不佳。诊断为IPF、HRCT网格影和蜂窝影评分高的患者发展为进行性纤维化型的风险更高;6 MWD<300 m、SOBQ评分高的患者死亡风险更高,值得临床医师关注。下一步我们将扩大样本量、延长随访时间并动态观察指标的变化进行进一步探索。

