亚急性瘤胃酸中毒对泌乳奶牛血浆生化指标及代谢组的影响研究
亓王盼,牟英玉,张涛,张继友,毛胜勇*
(1.国家动物消化道营养国际联合研究中心,江苏省消化道营养与动物健康重点实验室,南京农业大学消化道微生物研究室,江苏南京210095;2.动物科学类国家级实验教学示范中心,南京农业大学,江苏 南京210095)
亚急性瘤胃酸中毒(subacute ruminal acidosis,SARA)是由于反刍动物长期采食过量的易发酵碳水化合物,导致瘤胃内挥发性脂肪酸(volatile fatty acid,VFA)大量累积,使瘤胃p H值较长时间内维持在5.2~5.8之间的一种营养代谢疾病[1-2]。SARA严重影响奶牛瘤胃健康、泌乳性能及机体健康,其已成为危害现代奶牛健康生产的主要问题之一[3]。反刍动物患SARA后,瘤胃的消化代谢受到影响,尤其是VFA浓度及组成发生改变,由于VFA是反刍动物能量物质的主要来源,因此,VFA的组成及数量的变化可能影响到进入机体的营养物质数量[4-5],进而影响到机体营养代谢。一些研究也发现,SARA可影响奶牛机体氨基酸和碳水化合物代谢[6-7]。然而,以往的这些研究主要集中在对某种或某类代谢物的研究,很少有研究探讨SARA对奶牛整体代谢的影响。
近年来,代谢组学的发展为研究机体代谢提供了新思路,代谢组学可以检测出关键代谢通路上的多种代谢物,有助于加深对代谢紊乱背后机制的了解。代谢组学技术目前已用于监测奶牛瘤胃代谢组的变化[8-10]。血液是机体重要的媒介体液,其中包含了很多由机体代谢产生并联系不同器官组织的代谢产物[11]。Zhang等[12]通过对奶牛血液代谢组学的检测来筛选与奶牛酮病有关的生物标志物;最近,Sun等[13]通过对血液及其他体液的代谢组的共同检测,筛选出与奶产量和奶品质相关的代谢物并作为生物标记物。迄今,关于SARA对奶牛血液代谢产物的影响的研究仍主要集中在对血液中葡萄糖、游离脂肪酸、β-羟丁酸、胆固醇等常规参数的测定[7,14],而对其血液整体代谢产物的研究相对较少,因此,本试验通过对奶牛血浆生化指标及血浆代谢组的测定,研究了SARA对奶牛血浆代谢产物的影响,拟为寻找与SARA相关的代谢标记物以及为SARA的诊断和治疗提供新依据。
1 材料与方法
1.1 试验设计
本试验于2019年2月在江苏省泰州市姜堰牧场进行。选取8头装有永久性瘤胃瘘管、健康和体况相似的2~3胎泌乳中期奶牛,随机分为两组,每组4头奶牛。试验采用全混合日粮。一组饲喂精粗比为4∶6的对照组日粮(control group,CON),一组饲喂精粗比为6∶4的处理组日粮(subacute ruminal acidosis group,SARA),试验周期为21 d。全混合日粮配方及营养水平见表1,每天8:00和19:00各饲喂1次。在试验期间采用单栏拴系饲养,剩余采食量控制在采食量的10%左右。奶牛自由采食与饮水。
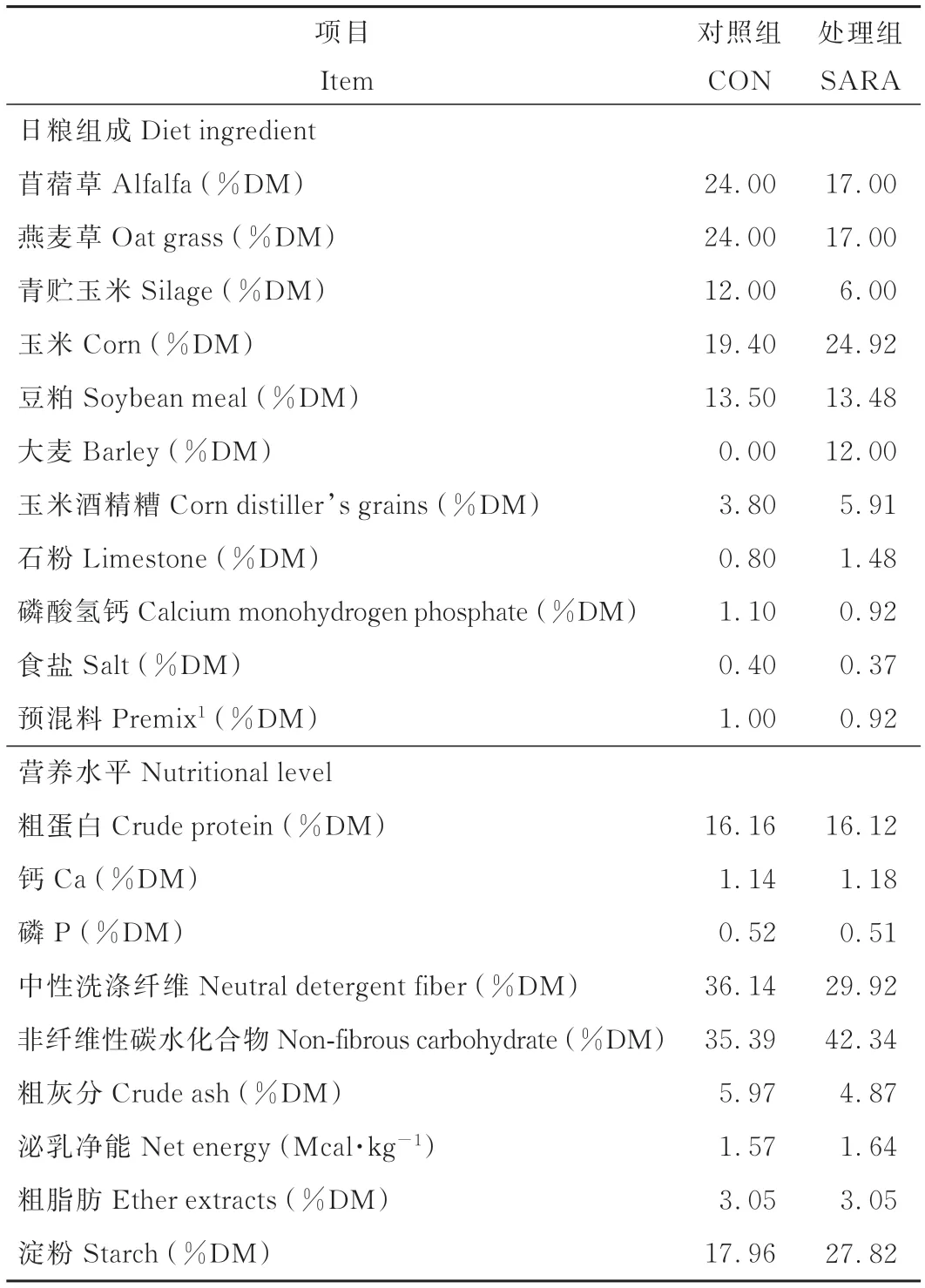
表1 日粮配方及营养水平Table 1 Ingredient and nutrient composition of diet
1.2 样品采集
于试验期每周的最后2 d检测采食量,于试验期每周最后1 d晨饲后0、2、4、6、8及12 h从瘤胃腹囊部采集瘤胃内容物,将所取得的瘤胃内容物经4层纱布过滤。所得瘤胃液立即用便携式p H计(HI 99161;HANNA Instruments,美国)测定其pH值。于试验期每周最后1 d晨饲后6 h,用肝素钠真空采血管从颈静脉采集10 mL血液,室温下2500 r·min-1离心10 min分离出血浆,一部分存放于液氮中,用于后续代谢组学检测,一部分存放于-20℃,用于后续生化指标的测定。
1.3 血浆生化指标测定
使用β-羟丁酸(β-hydroxybutyric acid,BHBA)、葡萄糖(glucose,Glu)、总胆固醇(cholesterol,TC)、甘油三酯(triglyceride,TG)和游离脂肪酸(nonestesterified fatty acid,NEFA)测定试剂盒(建成生物,南京)对试验期每周最后1 d采集的共24个血浆样品中的β-羟丁酸、葡萄糖、胆固醇、甘油三酯和游离脂肪酸含量进行测定。具体方法参照试剂盒说明书。
1.4 代谢组学分析
样品预处理:将24个血浆样本置于室温解冻,用移液枪吸取100μL样本于1.5 mL EP管中;加入300μL甲醇,并加入10μL内标(2.8 mg·mL-1,2-氯苯丙氨酸);涡旋混匀30 s,-20℃静置1 h;置于4℃离心机中,12000 r·min-1离心15 min;吸取200 μL上清液,转入进样小瓶中待检测。采用LCMS(Thermo,Ultimate 3000LC,Q Exactive)仪器分 析 平 台,C18色谱柱[Hyper gold C18(100.0 mm×2.1 mm,1.9μm)];色谱分离条件为柱温40℃;流速0.3 mL·min-1;流动相组成A:水+5%乙腈+0.1%甲酸,B:乙腈+0.1%甲酸;进样量为10μL,自动进样器温度4℃;流动相梯度洗脱程序参考表2;之后按照正模式:加热器温度300℃;鞘气流速:45 arb;辅助气流速:15 arb;尾气流速:1 arb;电喷雾电压:3.0 KV;毛细管温度:350℃;S-Lens RF Level,30%;负模式:加热器温度300℃;鞘气流速:45 arb;辅助气流速:15 arb;尾气流速:1 arb;电喷雾电压:3.2 KV;毛细管温度:350℃;S-Lens RF Level,60%的质谱检测参数进行检测。
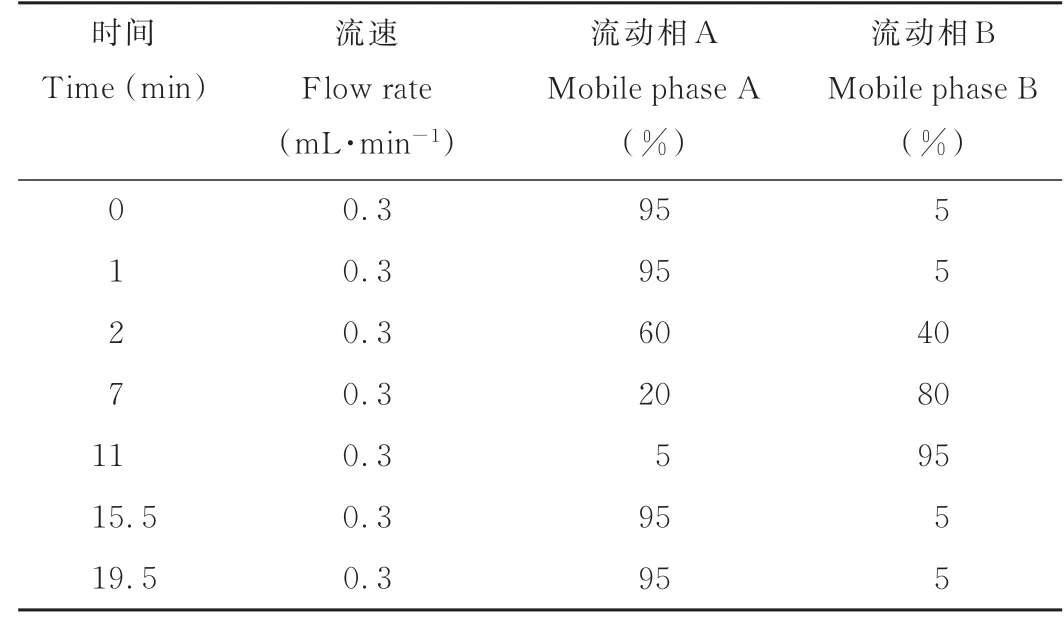
表2 流动相洗脱程序Table 2 Mobile phase elution procedures
1.5 数据分析
采用SPSS 22.0中的混合模型(mix model)对瘤胃p H进行统计,其中日粮和饲喂天数作为固定效应因子,牛作为随机效应因子,每天的采样时间点作为重复测量因子。采用SPSS 22.0中的一般线性模型(general linear model,GLM)对血浆生化指标进行统计。P<0.05表示差异显著,0.05<P<0.1表示具有差异显著的趋势。使用Compound Discoverer软件(Thermo公司)对LC/MS检测数据进行提取和预处理,并在Excel 2010中对数据进行归一化及后期编辑,最后整理成二维数据矩阵形式,包含保留时间(retention time;RT)、分子量(molecular weight,Comp MW)、观察量(样本名称)、可提取物质个数(ID)和峰强度等信息。运用SIMCA-P软件(Version 13,Umetrics AB,Sweden)对最终得到的数据进行多维统计分析。通过主成分分析(principal component analysis;PCA)和偏最小二乘法判别分析(partial least squares discriminant analysis;PLS-DA)获得实验参数和样本信息之间的相互关系,同时获得描述变量对模型的贡献度的数值(variable importance in the projection,VIP)。用非参数检验计算两组P值,然后用′p.adjust′[R(v3.6.1)]对P值进行false discovery rate(FDR)校正。以VIP>1,FDR<0.05为条件来筛选差异代谢物。通过MetaboAnalys(thttp://www.metaboanalyst.ca)进行差异代谢物的通路分析,并计算两组差异代谢物之间的倍数变化关系(fold change,FC)。
2 结果与分析
2.1 瘤胃pH变化
与CON组相比,SARA组的pH显著降低(6.13 vs 5.65,P=0.002),在1 d内小于5.8的时间大于3 h,因此本试验成功诱导SARA模型。两组之间的干物质采食量没有显著差异(23.79 vs 22.40,P=0.524)(图1)。

图1 晨饲后12 h内瘤胃p H随时间的变化Fig.1 Changes in the ruminal p H within 12 h after morning feeding(means±SEM,n=4)
2.2 血浆生化指标
与CON组相比,SARA组的β-羟丁酸浓度显著下降,甘油三酯的浓度显著上升,葡萄糖的浓度有显著增加的趋势(表3)。

表3 亚急性瘤胃酸中毒对血浆生化指标的影响Table 3 Effects of SARA on plasma biochemical indexes
2.3 血浆代谢组学分析
根据Excel数据表中的Mass值,基于网络数据库Metlin进行全谱鉴定。本试验共鉴定出207种代谢物,这些代谢物主要包括氨基酸类、核苷类、糖类、有机酸类、脂肪酸类、脂质类等。
2.3.1主成分分析和最小二乘法分析CON和SARA组比较的PCA得分结果表明,CON和SARA组能明显分开(图2A,B),说明两组样本之间的血浆代谢物存在明显差异。PLS-DA模型中两组形成两个明显的组别,分布在第一主成分两侧(图2C,D),正负模式条件下的R2Y和Q2分别为0.984,0.770和0.974,0.769,R2Y代表在Y轴方向模型的累积解释率,Q2代表模型的累积预测率;置换检验分析可以看出,回归线在Y轴上的截距均小于0(图2E,F),说明该模型对两组的区分有较好的预测和解释。
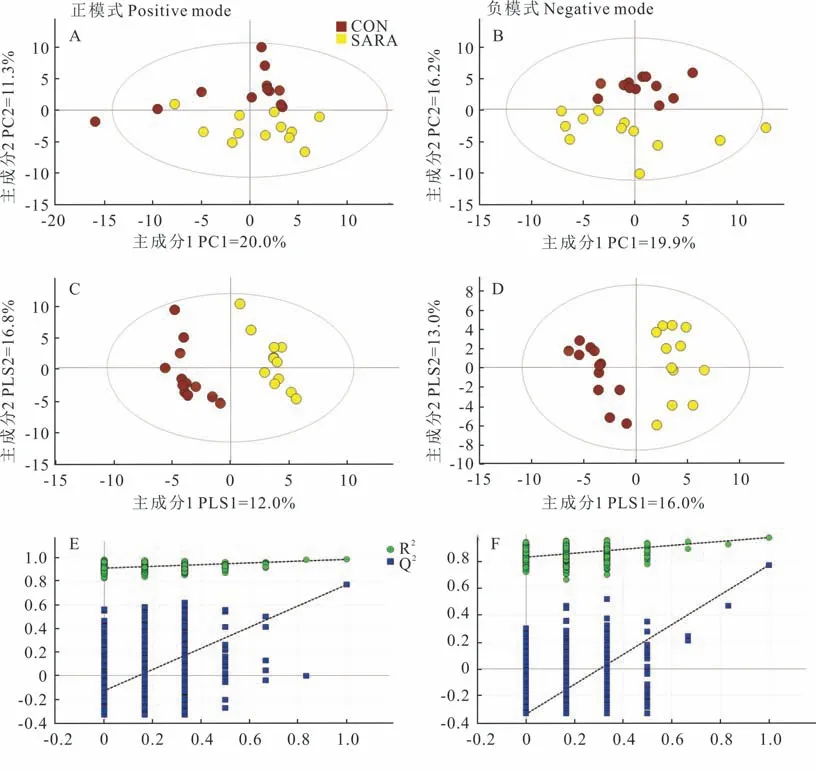
图2 CON和SARA组正负模式下的主成分分析得分(A,B),偏最小二乘法分析得分(C,D)和置换检验(E,F)Fig.2 PCA model score scatter(A,B),PLS-DA model(C,D)and permutation test(E,F)
2.3.2 血浆差异代谢物筛选 以VIP>1,FDR<0.05为筛选标准,最终筛选出26种差异代谢物,主要为脂质及脂肪酸、氨基酸、有机酸和苯甲酸类物质(表4)。与CON组相比,SARA组7-酮脱氧胆酸、脱氧胆酸、胆酸、12-酮脱氧胆酸、12(13)Ep-9-KODE和12,13-DHOME显著上调,十一烷二酸、十六烷二酸、9-HODE、血氧烷B3和前列腺素E2显著下调;除L-天冬酰胺外,所有的氨基酸类物质均显著下调;所有的有机酸和苯甲酸类物质均显著下调。进一步使用MetaboAnalyst4.0网站对差异代谢物进行代谢通路分析,发现与SARA相关的差异代谢物主要富集在氨酰t-RNA生物合成和缬氨酸,亮氨酸和异亮氨酸的生物合成这两条代谢通路上(图3)。对差异代谢物进行聚类分析,直观的显示出了这些差异代谢物在两个组的每个样品中的具体情况。可以看出(图4),CON组的4头牛显著聚为一类,SARA组的4头牛显著聚为一类,同时胆酸类物质显著聚为一类,SARA组均显著上调。
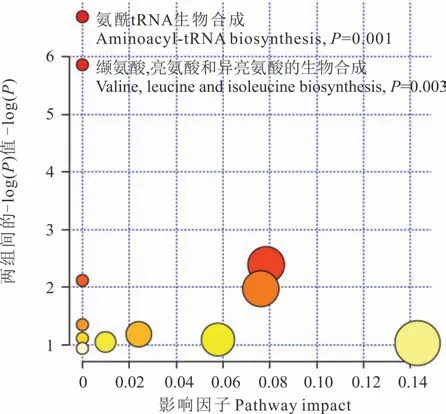
图3 两组差异代谢通路图Fig.3 Metabolome pathway of the significantly different metabolites identified in the two groups

图4 CON组和SARA组的血浆差异代谢物分层聚类分析热图Fig.4 Heatmap of hierarchical clustering analysis of differential plasma metabolites in CON and SARA group

表4 血浆差异代谢物Table 4 Plasma differential metabolites
3 讨论
代谢组学是对特定条件下的特定生物样品中的所有代谢物所进行的定性定量分析,目前该技术已广泛应用于疾病发生、药物残留和食品检测等领域。本试验采用LC-MS平台,检测了患SARA后,奶牛血浆代谢物的变化情况,拟进一步探究SARA与奶牛机体新陈代谢之间的深层联系,并寻找与SARA相关的生物标志物。
3.1 脂代谢
本研究发现,相比于CON组,SARA组奶牛血浆中的BHBA含量显著下降,而甘油三酯的含量显著上升,同时引起了一些脂肪酸浓度发生变化。有研究指出,血中的BHBA、游离脂肪酸和甘油三酯是反刍动物乳腺合成乳脂的重要前体物[15-16],这些物质浓度的变化可能会对乳脂合成造成影响。同时,BHBA是酮体的主要成分之一,是肝脏中由脂肪代谢过程合成的小分子。先前有研究表明,当奶牛饲喂含大麦谷物的日粮时,血浆中BHBA的浓度会随着大麦比例的增加而降低[14];Guo等[7]和孙燕勇等[17]也发现患SARA的奶牛血浆中BHBA浓度降低,李小杉等[18]和孙玲伟等[19]在临床上证实,发生亚临床酮病时,奶牛血液中BHBA含量为1.2 mmol·L-1。本试验中,血浆BHBA含量都在正常范围内,可以初步判断SARA发生时试验动物无酮病隐患。甘油三酯主要是在肝脏、脂肪组织和小肠中合成,其中以肝脏的合成能力最强。有研究指出,血浆中甘油三酯浓度的增加与脂肪肝有关,引发机体炎症反应[20]。综上,这些物质浓度的变化可能表明SARA引起奶牛肝脏功能受损,使机体脂代谢发生紊乱。
胆汁酸主要是由肝脏中的胆固醇合成,胆酸是一种初级胆汁酸,主要在肝脏中合成,脱氧胆酸是一种次级胆汁酸,主要由胆酸在肠道中合成[22]。本研究发现,SARA组奶牛血浆中的多种胆汁酸类物质(7-酮脱氧胆酸,脱氧胆酸,胆酸和12-酮脱氧胆酸)聚为一类并且含量均显著上升。有研究表明,高浓度的胆汁酸对机体有毒性作用,胆汁酸浓度过高时会对培养的牛胰管上皮细胞造成组织损伤[21]。另外,胆汁酸在脂质代谢中起重要的调节作用,胆汁酸的合成速率与高脂血症患者血浆甘油三酯水平的升高有关[23]。因此,SARA组胆汁酸含量的增加可能与甘油三酯含量的增加有关。肝肠循环是调节胆汁酸代谢的重要途径,胆汁酸在肝脏合成后经胆盐输出泵进入胆囊,进食后分泌入肠道,最后在回肠中被重吸收,然后通过门静脉血液回到肝脏,重新分泌到胆汁中[22],该过程是一个动态平衡过程。由此,本研究中,发生SARA的奶牛血浆中胆汁酸含量的升高,可能预示着其胆汁酸的肝肠循环受阻,大量胆汁酸淤积在血浆中无法回到肝脏。本试验同时发现,SARA组奶牛血浆中的前列腺素E2和类前列腺素的浓度下调。前列腺素(prostaglandin,PG)是生物体内的一种局部激素,它具有多种生理活性作用,能与特异性受体结合后介导细胞增殖、分化、凋亡等一系列细胞活动以及调节雌性生殖功能和分娩、血小板聚集、心血管系统平衡[24]。其主要是由不饱和脂肪酸组成的,因此,前列腺素在SARA组浓度的下调可能也与脂肪酸代谢有关。
3.2 氨基酸代谢
本实验发现,与CON组相比,SARA组的L-天冬酰胺显著上升,其余发生变化的氨基酸(精氨酸、色氨酸和苏氨酸)均显著下降。在上述氨基酸中,精氨酸主要参与TCA循环和尿素循环[25];色氨酸和苏氨酸均为生糖氨基酸,生糖氨基酸水平的降低,表明它们可能作为底物进入三羧酸循环提供能量或参与糖异生过程产生葡萄糖[26]。差异代谢物中虽没有检测到甘氨酸的变化,但在SARA组奶牛血浆中发现多种酰基甘氨酸(异丁酰甘氨酸、异戊酰甘氨酸、马尿酸和4-羟基马尿酸)的浓度降低。在这些发生显著变化的酰基甘氨酸中,马尿酸是苯甲酰甘氨酸,是苯甲酸与甘氨酸的缀合物,其主要在肝脏中合成,通过此反应,机体可清除苯甲酸的毒性。因此,SARA组马尿酸浓度的降低,可能会造成苯甲酸等代谢废物在体内的积累,增加机体的患病风险[13,27]。
3.3 糖代谢
在本试验中发现SARA组血浆中葡萄糖浓度有显著升高的趋势,这可能与SARA条件下奶牛瘤胃内丙酸浓度增加有关[28],由于进入肝脏的丙酸数量增加,因而经糖异生作用生成的葡萄糖的量也有所上升,该结果也与前人的研究结果一致[7,14,29]。6-磷酸-2-脱氢-D-葡萄糖酸酯是磷酸戊糖途径的中间产物,其在SARA组奶牛血浆中的含量减少,在一定程度上暗示了糖代谢的磷酸戊糖途径受阻,葡萄糖氧化分解减少。最后,针对以上讨论,将差异代谢物可能参与的代谢途径进行总结(图5)。
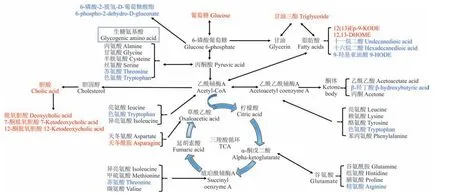
图5 奶牛血浆差异代谢物可能参与的代谢途径Fig.5 Proposed metabolic map of main plasma differential metabolites
4 结论
综上所述,本试验采用LC/MS代谢组学技术,研究了饲喂高谷物日粮后奶牛血浆代谢物的变化情况。结果表明,与CON组奶牛相比,SARA组奶牛血浆中甘油三酯、胆汁酸类物质、12(13)Ep-9-KODE、12,13-DHOME和L-天冬酰胺等物质含量升高,而BHBA、十一烷二酸、十六烷二酸、PGE2、L-精氨酸、L-色氨酸、L-苏氨酸、6-磷酸-2-脱氢-D-葡萄糖酸酯和马尿酸等物质含量降低,表明SARA组奶牛脂代谢、氨基酸代谢和糖代谢都受到了不同程度的影响,这些物质也可作为判断SARA的潜在生物标志物。

