微流控芯片POCT室内质量控制方案的探索
葛丹红,唐立萍,欧元祝,虞啸炫,刘文彬,林斐然,龚敬凯,朱宇清
(上海市临床检验中心,上海 200126)
随着即时检测(point-of-care testing,POCT)在临床科室的广泛应用,其检验结果的质量控制成为一个迫切需要解决的问题。发达国家POCT发展较早,已建立起完善而规范的管理体系。美国从2016年起,对于非豁免的检测项目实行个性化的质量控制计划,实验室可通过对分析前、分析中、分析后的全面风险评估来决定室内质量控制(internal quality control,IQC)的频率和水平[1]。澳大利亚临床生物化学家协会规定对POCT设备必须每月检测1次质控品,对新批号的试剂也必须检测质控品[2]。在瑞士,IQC频次根据分析系统的操作繁易程度确定,一般复杂的检测系统每天至少2次IQC,相对简单的检测系统最少每2周进行1次IQC[3]。目前,我国尚未形成规范而完善的POCT质量管理体系,POCT的质控程序仍然参照常规检验的要求,必须每天检测2个水平的IQC质控品。POCT有其自身的特点,无论是标本采集、加样方式,还是检测方法,均不同于常规检测,其质控方式亦不应完全照搬传统模式。
微流控芯片POCT设备通过精确的微量流体控制实现快速反应,被广泛应用于临床生化、免疫、核酸检测等多个体外诊断领域[4-6]和众多临床科室[7]。本研究旨在探讨等效质控在微流控芯片POCT质量控制中的可行性和有效性,为建立适合POCT的IQC方案提供新思路。
1 材料和方法
1.1 样本来源
收集2018年1—3月上海市第六人民医院无溶血、脂血、黄疸的临床剩余血清样本,检测钾(potassium,K)、钠(sodium,Na)、氯(chlorine,Cl)、葡萄糖(glucose,Glu)。
1.1 仪器和试剂
i-STAT 300-G手持式血液分析仪(美国雅培公司)及配套电子模拟器、i-STAT 3水平定值质控品(批号为301100、311094、321100)、急诊11项(CHEM8+)测试卡片(干化学法,批号为H18061)。生化质控品(批号为222ULCM、826 UECM)购自英国朗道公司。
1.3 方法
1.3.1 混合血清样本制备 根据浓度将血清样本进行分类,制备成3个不同水平(L1、L2、L3)的混合血清,覆盖医学决定水平。将混合血清充分混匀后分装于冻存管,-80 ℃保存备用。每日检测分装的血清样本,以验证仪器的检测性能;尤其是在第2阶段,用于评价未检测液体质控品的工作日仪器检测结果的稳定性。
1.3.2 实验准备 由经培训合格的人员进行操作。实验开始前查看环境温度(16~30 ℃)和气压(40~113 kPa),确认仪器状态,确保电池电量充足、电压符合要求(>8 V),确保仪器当前使用软件在有效期内、标准曲线和定标数据已更新、仪器运行状态良好,确认检测卡片正确存放并处于有效期内,按仪器说明书要求将检测卡片于室温条件下平衡5 min。
1.3.3 西格玛(sigma,σ)水平分析 参照美国临床实验室改进修正法规(the Clinical Laboratory Improvement Amendments of 1988 ,CLIA'88)和美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)EP15-A2文件推荐的方法,使用2个水平的生化质控品进行室内不精密度评价,计算每个项目2个水平质控品室内不精密度[变异系数(coefficient of variation,CV)],按照公式CV=[(CV12+CV22)/2]1/2合成每个项目的CV。检测i-STAT 3水平定值质控品,质控品靶值溯源至美国国家标准与技术研究院认证的标准物质。计算每个水平混合血清样本检测结果与靶值之间的偏移(bisa,Bias),按照公式Bias=[(Bias12+Bias22+Bias32)/3]1/2,将3个水平混合血清样本的Bias合成为每个项目的Bias。按照公式σ=(TEa-Bias)/CV计算每个项目的σ水平。
1.3.4 质控频率评估 (1)第1阶段(连续4周,20个工作日)。每天开机后先使用仪器配套的电子模拟器进行电子质控,电子质控未通过不能进行样本检测;电子质控通过,再检测2个水平液体质控品,然后检测2个水平的混合血清样本。(2)第2阶段(连续9周,45个工作日)。每天开机后先进行电子质控,每周检测液体质控品1次,每天检测混合血清样本1次。将液体质控数据输入上海市临床检验中心质控软件,绘制Levey-Jennings质控图,采用Westgard Sigma规则判断质控数据是否在控。
1.3.5 混合血清样本结果分析 使用Excel 2010软件分析全过程、第1阶段、第2阶段4个项目3水平混合血清样本检测结果的、s、CV。计算不同阶段每个项目的分析总误差(total analytical error,TAE)[8]。以第1阶段检测结果的x为靶值,计算第2阶段检测结果与第1阶段检测结果之间的绝对偏差(absolute deviation,AD)和相对偏差(relative deviation,RD)。
2 结果
2.1 4个项目的σ水平
K、Na、Cl、Glu 4个项目的σ水平及推荐质控规则见表1。
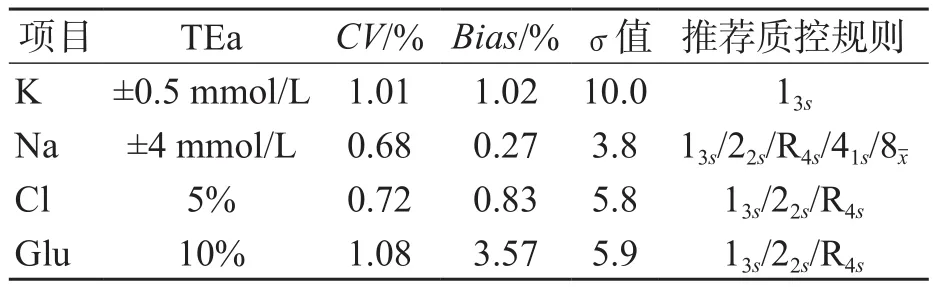
表1 4个项目σ水平及推荐质控规则
2.2 电子质控结果
整个研究过程所有电子质控结果均为通过。
2.3 液体质控结果
每天分2批次检测2个水平的生化质控品,连续检测10 d。根据累计的20次质控结果计算各项目IQC靶值和s。采用Westgard Sigma规则对2个阶段的IQC数据进行判断。根据各项目σ水平选用不同的质控规则,K项目使用13s规则,Na项目使用规则,Cl和Glu项目使用13s/22s/R4s规则,整个研究过程2个阶段所有质控结果均在控。4个项目液体质控结果见图1~图4。
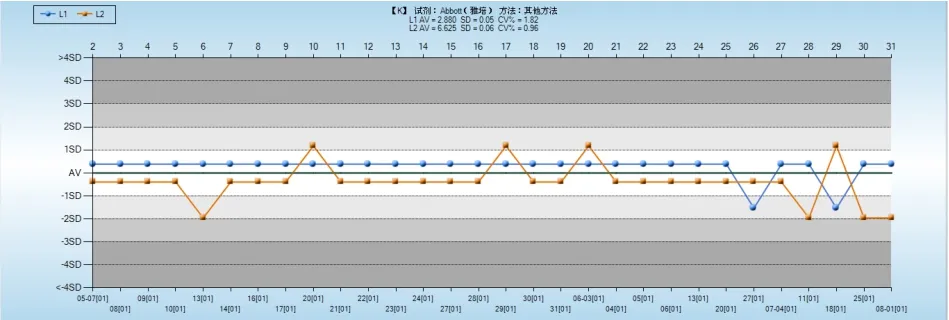
图1 K液体质控结果

图2 Na液体质控结果
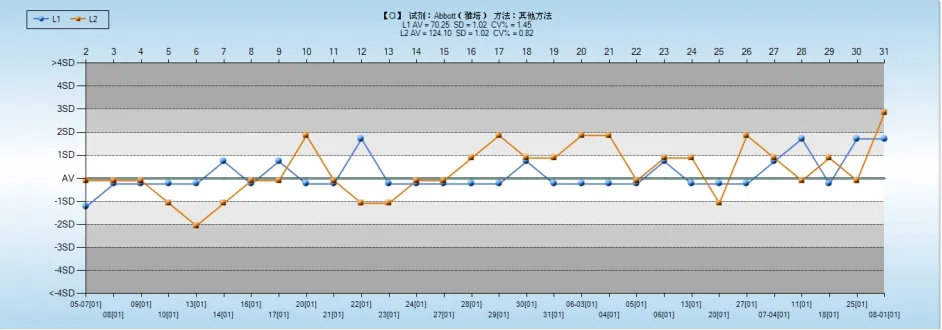
图3 Cl液体质控结果
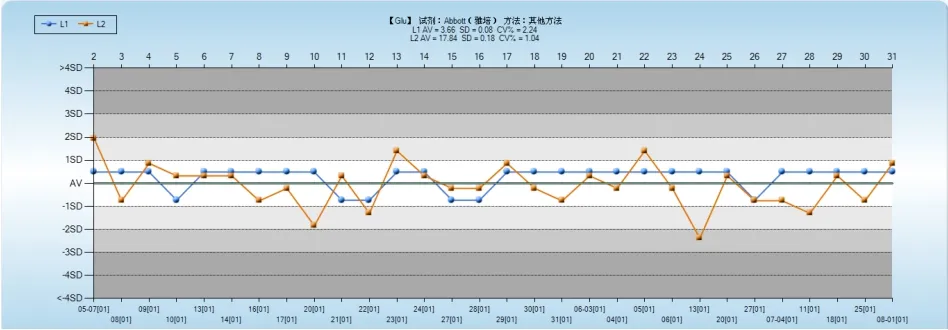
图4 Glu液体质控结果
2.4 混合血清样本检测结果统计值
整个研究过程、第1阶段、第1阶段4个生化检测项目3水平混合血清样本检测结果的CV均<1/3TEa,且TAE<TEa。所有项目第2阶段与第1阶段检测结果的AD或RD均<1/3TEa。见表2。
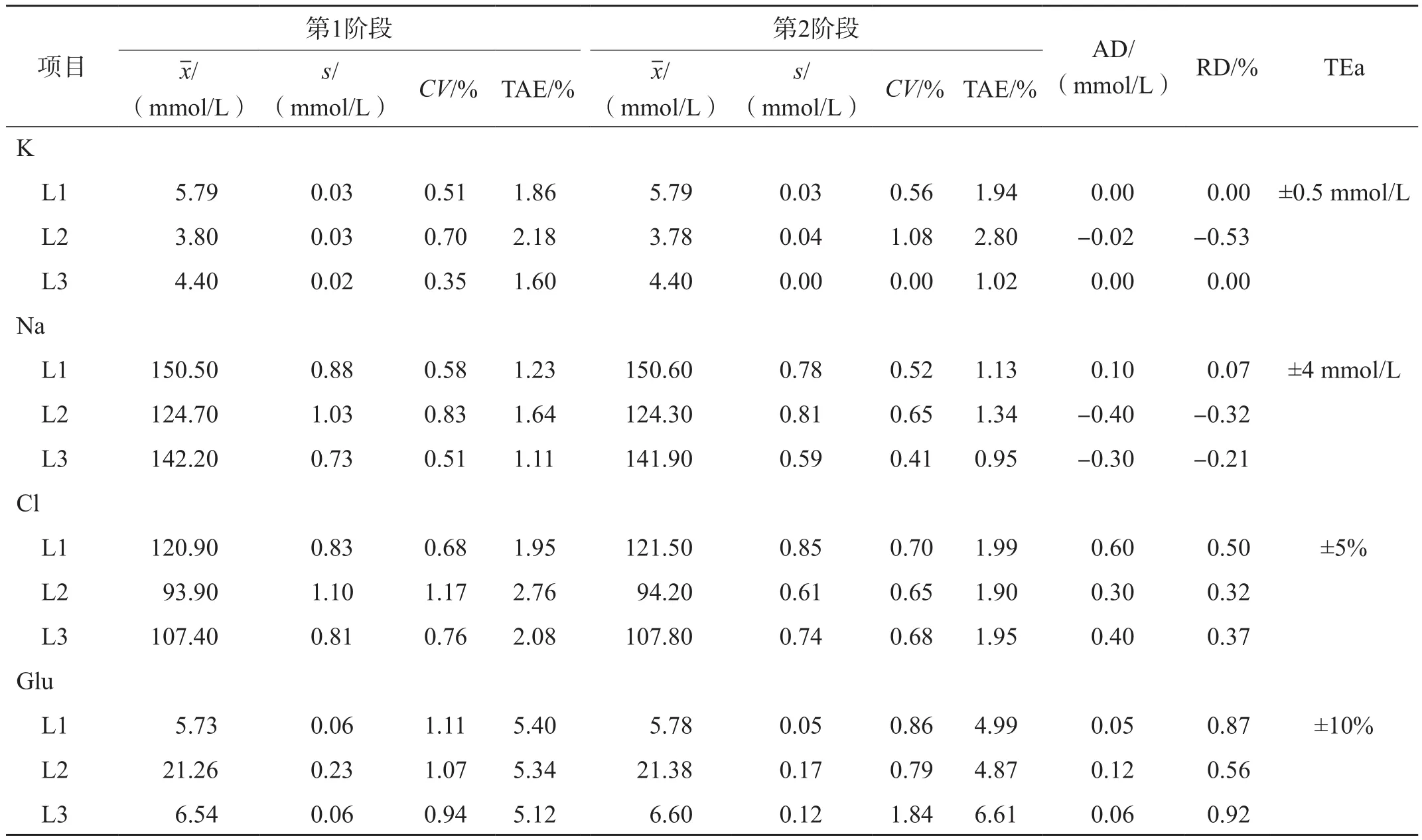
表2 混合血清样本4个项目检测结果统计值
3 讨论
质量控制不仅是质量管理的一部分,更是其关键。质量控制包括选择合适的质控品、质控规则和质控品检测频率等。ISO 15189要求对检测项目、所用的方法或检测程序设计恰当的质控程序,以达到检验结果的预期质量,但并未对质控品的检测频率提出具体要求[9]。目前,大多数临床实验室采用“默认质控”模式,即每24 h检测2水平质控品。然而,POCT设备的操作者大多没有实验室背景,未经过专业培训,对于复杂的统计质量控制方法难以接受,且由于所需成本较高,这种传统的质控模式在实际工作中很难推广。上海市临床检验中心近几年在对上海地区POCT的质量督察中发现,仍有相当一部分的POCT未开展IQC。为此,我们尝试探索一种在保证检测质量的前提下行之有效,且易于被POCT操作者接受的IQC模式。
微流控芯片POCT的每张测试卡片是一个独立的检测单元,即使储存于相同环境的卡片之间也可能存在差异。当使用卡片检测液体质控品时,只是对当前使用的这张卡片的质量进行了验证,而检测患者样本使用另一张测试卡时检测性能可能又不一样了。虽然检测液体质控品可以对分析中的全过程进行质量控制,但实际上仅对当前使用的卡片进行了验证,对同一批号测试卡片过多的检测液体质控作用有限,且会增加时间和检测成本。仪器检测结果的再现性主要还是取决于测试卡片生产过程的质量控制。相较于测试卡片,微流控芯片POCT仪器主要发挥了“电子读数仪”的功能[10]。微流控芯片体积非常小,检测信号的仪器要具有更高的灵敏度和信噪比、更快的响应速度,才能满足临床检验低检测限、高灵敏度、良好的重复性和较宽的线性范围等要求。其配套的电子模拟器,即通常所说的“电子质控”,对仪器读取信号的性能进行监测也是其质量控制的重要内容。因此,对于微流控芯片POCT的IQC,科学、合理地使用电子质控和液体质控是关键。本研究尝试采用等效质控程序,每天进行电子质控,以保证每天对仪器性能进行监测,将相同批号测试卡片液体质控的频率降低,在对卡片质量进行有效监测的同时,有效降低了时间和经济成本。
美国于2013年提出了“个性化质量控制计划”的概念,将检测系统内置设备的技术改良纳入了质量管理体系,根据实验室自身特有因素,如患者情况、检测设备、试剂、环境、检测人员等,通过风险评估来识别检测过程中潜在的失败和误差来源,并量身定制个性化的、有效的质控操作规范[1]。本研究中,每次检测前,微流控芯片POCT仪可自动单点定标,且每次检测流程内有近200项自动化监控;研究过程中使用相同批号的试剂,严格控制检测环境,实验由操作熟练的检验人员完成,尽可能降低这些因素对检测结果的影响。李润青等[11]应用六西格玛管理法对17个生化检测项目的性能进行了评估,证明了这一方法是较理想的质量管理方法。本研究用六西格玛管理法对4个生化检测项目的性能进行评价,发现K项目性能达到世界级表现(σ≥6);Cl、Glu 2个项目性能达到优秀表现(6>σ≥5);Na项目性能达到临界表现(4>σ≥3),所有项目的分析性能均在医学可接受水平。
本研究在每天检测电子质控的前提下,第1阶段连续20个工作日每天检测2个水平液体质控品和混合血清样本,在此基础上还增加了第2阶段实验,即连续9周每周检测2个水平液体质控品1次,混合血清样本仍然每天检测,以观察在降低液体质控频率的情况下仪器的检测性能。研究过程中每天的电子质控均通过。使用Westgard Sigma质控规则判断液体质控结果,既保证了较高的误差检出率,又保持了尽可能低的假失控概率[12],结果显示所有项目均未发生失控。整个研究过程每天检测3个水平混合血清样本,结果显示所有项目3个水平混合血清样本检测结果的CV均<1/3TEa,且TAE均<TEa,提示仪器在不同阶段均保持了良好的分析性能。在第2阶段,本研究将液体质控频率减少到每周1次,但是仍每天检测血清样本1次,通过对第2阶段血清样本结果的分析,以及第2阶段检测结果和第1阶段检测结果的比较,发现在未做液体质控的检测日,仪器检测结果的不精密度和偏差均在临床可接受范围内。
我们认为应当谨慎地的对待降低质控频率的做法。CLSI于2011年发布了通过风险管理建立质量策划的全新指南[13],在重点关注分析中过程以外,明确了质量教育和培训、预防性维护、统计学质量控制、室间质量评价或能力验证以及为特定检测系统建立个性化质控方案的重要性。特定检测系统的质控方案应包含特别的预防和控制机制。因此,在降低质控频率前需进行风险评估:仪器和试剂的使用是可靠和容易维护的,试剂稳定且不需要特殊处理或储存;检测技术简单,操作环节不易出现粗大误差;随着时间的推移,故障始终维持在一个较低的水平;该项目检测应该是高频率且不需要使用微量的加样技术;检测人员训练有素。就如ISO 15189中5.6.2.3质控数据条款指出的——宜尽量采用统计学和非统计学过程控制技术连续监测检验系统的性能。而在实验室进行质控的实践过程中,有些时候也确实需要使用非统计学的控制技术,包括记录、流程标准化、抽检、培训等,都可以归为此类控制技术。
综上所述,在稳定的检测环境下,微流控芯片POCT由已接受培训且操作熟练的检测人员使用相同批号/货运号的试剂检测K、Na、Cl、Glu项目时,在检测人员和环境均稳定,试剂批号相同的情况下,可采用每天进行电子质控1次和每周检测液体质控品1次的IQC方案,来保证检验结果的质量。根据POCT的特点,适当、合理地降低质控检测频率,可以在保证检测质量的前提下,既节省时间,又有效降低检测成本。
本研究尚存在一定的缺陷,一是研究的检测项目只涉及了4个生化指标,对于目前众多的POCT检测项目来说较为局限;二是研究只对2次质控评价间的时间长度进行了评估,而未涉及质控评价中的患者样本数。后续将进一步探索适用于POCT的IQC方案。

