开放性骨盆骨折软组织损伤的处置策略
李 阳,张连阳
陆军军医大学大坪医院战创伤医学中心,创伤、烧伤与复合伤国家重点实验室,重庆 400042
开放性骨盆骨折是指与外界(包括直肠、阴道、尿道)相通的骨盆骨折,占所有骨盆骨折2%~4%,病死率高达23%~57%[1]。在创伤中心建设初期,有人就提出开放性骨盆骨折只有在创伤中心才能得到有效救治[2]。事实上,开放性骨盆骨折也是最典型的严重多发伤,系高能量创伤,除骨盆、腹腔内脏器损伤外,还同时伴有严重的软组织损伤。对于创伤外科医师而言,软组织损伤往往比骨折和脏器损伤处理更加棘手,且对患者的预后影响更大。本文从开放性骨盆骨折的软组织损伤评估、早期处理、感染控制和软组织修复重建方面阐述其处置策略供同道参考。
1 开放性骨盆骨折软组织损伤的评估
骨盆骨折不同类型的致伤原因所造成的软组织损伤形式也不尽相同,具体表现为软组织挫伤或擦伤、闭合或开放性软组织脱套伤或上述损伤形式的各种组合。开放性骨盆骨折的软组织损伤存在出血多、污染重、换药难和封闭晚四个特点。首先,骨盆区具有侧枝吻合丰富血管丛,骨盆损伤后周围软组织具有填塞作用,可以限制受伤后持续出血;而开放性骨盆骨折由于软组织完整性的破坏、填塞效应消失,导致骨折断端以及创面出血无法得到有效控制。其次,开放性骨盆骨折断端与直肠、阴道、尿道等相通,使得感染风险大大增加,且其软组织创面多数位于会阴、臀部或背部,这些部位由于体位的影响,观察和换药难度大。最后,由于创面的缺损、感染、坏死等,往往造成创面封闭延迟,影响预后。
由于骨盆区解剖复杂且涉及泌尿、生殖、消化和运动多个系统,不同区域损伤面临的问题和临床处置策略也不尽相同。因此,传统的软组织损伤分型系统如Gustilo-Anderson分型和OTA分型(Orthopedic Trauma Association,OTA)无法满足对开放性骨盆骨折软组织损伤评估要求。目前,临床应用较为广泛的开放性骨盆骨折软组织损伤分型系统是Faringer等[3]1994年提出的Faringer分区(表1),其临床意义在于提供了早期肠造口的指导性原则,但未综合考虑骨盆骨折的严重程度对软组织处理的影响。在Faringer分区的基础上,Jones等[4]1997年通过对39例开放性骨盆骨折患者的回顾性研究,综合了骨盆骨折与软组织损伤的严重程度,提出了开放性骨盆骨折的Jones-Powell分型(表2),该分型在评估伤情严重程度和预测死亡风险方面具有一定意义,并在Cannada和Guo 等[5-6]的研究中得到了印证,但其对软组织处理的指导并没有实质性改进。

表1 开放性骨盆骨折软组织损伤Faringer分区
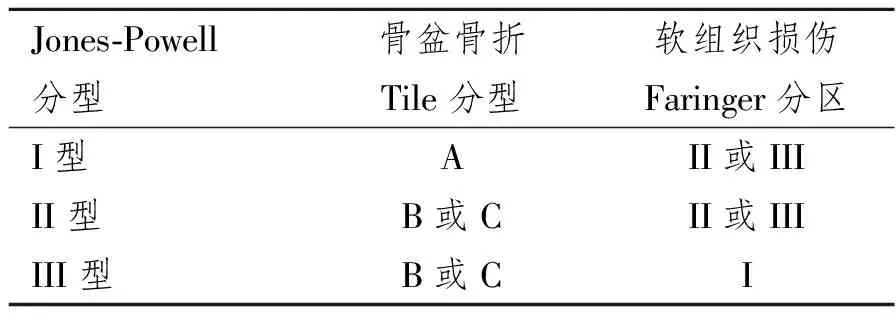
表2 开放性骨盆骨折Jones-Powell分型
此外,Fu 等[7]将会阴区分为泌尿生殖区和直肠肛门区,根据损伤缺损区域和是否合并尿道及直肠肛管损伤提出了一种开放性骨盆骨折会阴区软组织损伤改良分型(表3),并针对每种软组织损伤类型提出了相应的修复策略,但目前应用较少,未来需要更多的临床研究进一步验证其指导意义。

表3 开放性骨盆骨折会阴区软组织损伤改良分型和修复策略
2 开放性骨盆骨折软组织损伤的早期处理
2.1早期伤口处置 开放性骨盆骨折软组织损伤特点是伤口大而深、污染重,往往涉及会阴、臀部、腹股沟区,并可深达肛周、直肠前或骶前间隙。早期伤口处理的目的是止血和减少污染。需要注意的是,出血控制永远优先于清创,只有在出血得到初步控制、血流动力学稳定的情况下,才考虑对伤口进行清创手术。开放性伤口要留取深部组织行细菌涂片和培养,对于污染严重的伤口,还需考虑梭状芽孢杆菌感染,并根据患者的免疫接种史给予破伤风抗毒素或破伤风免疫球蛋白。根据创伤法则“The best solution is dilution(污染最好的解决方案就是稀释)”,清创时使用大量加温生理盐水冲洗创面,同时清除伤口内所有异物和坏死组织。为了不破坏软组织表面屏障,不建议使用碘伏、过氧化氢等杀菌剂冲洗创面[8]。如果清创后术野较为清洁,可以一期缝合伤口但必须在伤口内放置多根引流管以保证充分引流,必要时可考虑放置双腔引流管,从侧孔持续注入等渗液冲洗伤口。引流管一般于术后5d拔除。对于因需行腹膜外填塞[9]压迫止血不能一期缝合的伤口,可以在填塞纱布取出后置入双腔引流管,通过换药及冲洗使伤口逐渐缩小愈合。在早期,特别对于有盆腔填塞的患者,由于出血尚未控制,负压吸引有加重出血的可能,一般不建议使用。负压封闭一旦吸引不畅或封闭不严,反而会使局部液体积聚,加重感染[9],应密切观察确保负压有效。
2.2膀胱造瘘与结肠造口 尿液和粪便污染是造成盆底感染及难以控制的主要原因。对于合并尿道和直肠肛管损伤的患者,早期通过膀胱造瘘和结肠造口可保证盆底洁净、干燥,减少软组织感染机会,即使发生感染,处理也较为容易。开放性骨盆骨折患者往往存在尿道断裂,对于怀疑合并尿道损伤的患者,诊断性导尿、尿道造影等是诊断尿道损伤的有效办法。若尿管无法插入膀胱内或发现尿管经尿道断裂处插入周围组织,或造影有阳性发现,应尽早行膀胱穿刺造瘘(图1)。临床实践中,早期结肠造口对会阴部开放伤患者的伤口处置带来便利,有助于感染控制和早期进食。多项临床研究结果也表明,根据Faringer分区选择性行肠造口能降低开放性骨盆骨折患者的病死率[10-13],但由于其较为罕见,大宗病例研究十分困难,目前已有的临床证据等级不高,未来仍需前瞻性多中心研究来证明早期造口对此类患者的获益[14]。

图1 患者男性,13岁,卡车碾压致开放性骨盆骨折合并尿道断裂,在会阴部开放性伤口内发现导尿球囊
2.3清创节奏的把握 清创节奏的把握对感染控制具有非常重要的意义。在清创后当天,由于细菌负荷明显降低,各项感染指标会显著下降,随着时间的推移又逐渐增长。在患者血流动力学稳定的情况下,第二次清创时间应在第一次清创后24~72h。早期积极、快节奏的清创可降低患者感染风险,为后期骨盆重建手术赢得机会。然而每一次清创都是对患者脆弱机体的再次打击,都可能损害已经形成的屏障导致菌血症。如何在患者可承受感染负荷上限来临之前进行清创往往难以把握。因此,动态复查血常规、C-反应蛋白(CRP)、血沉(ESR)、降钙素原(PCT)、白细胞介素6(IL-6)、中心粒细胞CD64等感染指标综合评估患者感染负荷及免疫状态,在恰当时间果断清创才能让患者最大获益。
3 开放性骨盆骨折软组织损伤的感染控制
度过出血休克期后,由于患者的免疫平衡遭受巨大破坏,下一个问题就是感染。软组织感染是开放性骨盆骨折救治中的难点。由于伤口多在会阴部或臀部,邻近肛门、泌尿生殖道,或伴有直肠肛门或泌尿生殖道的损伤,使得开放性骨盆骨折软组织感染发生率居高不下。Jones等[4]报道开放性骨盆骨折合并会阴及直肠肛管损伤患者感染率高达77%。同时,因为忌惮再出血风险或患者本身因疼痛而导致翻身困难,更增加了感染发生的风险。开放性骨盆骨折患者早期出血控制复苏阶段大多在重症监护室进行。除了开放性创面沾染细菌外,在广谱抗生素及监护室环境中也极易感染耐药菌。根据笔者所在医院2020年重症监护室病原菌构成及药敏分析报告,排行前五位的感染细菌分别为鲍曼不动杆菌、肺炎克雷伯菌、铜绿假单胞菌、大肠埃希菌和金黄色葡萄球菌。在每次换药过程中,伤口内组织标本要留取双份深部组织标本送细菌及药敏检测以便后期指导抗生素的使用。
早期出血控制后,对于骨盆开放伤口的处理,频繁换药对医师和患者的难度和痛苦难以想象。此时,使用负压引流技术(vacuum sealing drainage,VSD)对封闭创面预防感染具有一定优势。首先,VSD的泡沫薄膜能完全封闭创面形成物理屏障屏蔽细菌,阻止细菌进入伤口,避免交叉感染;其次,VSD可通过负压作用通畅引流、减少毒素吸收同时增加创面组织血流量,促进肉芽生长加快创面修复;再者,VSD更换周期为5~7d,减少换药频率、减轻患者痛苦。然而,在VSD贴膜封闭创面的过程中也存在一定难度,特别是Faringer I区,漏气和出血是VSD常见的问题。针对漏气,在安装VSD时应选择合适的体位(如侧卧位或截石位)以充分暴露创面避免因体位影响贴膜。出血多因患者凝血功能障碍导致创面广泛渗血所致,此时可拆除VSD用普通敷料加压包扎,同时查凝血象及血栓弹力图(TEG),根据凝血障碍的具体环节输注相应血液制品。另外,要特别注意不能以更换VSD的时机作为再次清创的依据,不因VSD的使用而延迟再次清创的时机。
此外,应特别重视骨盆侧方和髋部区域的软组织潜行脱套损伤,也称Morel-Lavallee损伤。此类损伤虽然没有开放性伤口,但由于皮下组织与深筋膜之间因巨大剪切力而失去黏附,穿支血管断裂可导致皮下积血、积液和皮肤坏死引起继发性感染[15]。针对此类损伤,在早期评估中应重点关注骨盆区有无皮下淤斑,局部有无波动感和皮肤感觉异常。超声和CT可作为有效的辅助检查手段发现皮下积液积气[16]。Morel-Lavallee损伤处理原则是早期发现、有效引流并针对性使用抗生素预防感染[17-18](图2)。

图2 骨盆侧方和髋部区域的软组织潜行脱套损伤(Morel-Lavallee损伤)
4 开放性骨盆骨折软组织损伤的修复重建
部分Faringer II区和III区污染不重的软组织损伤可以清创后一期关闭。但是多数情况下,开放性骨盆骨折创面往往污染严重或软组织缺损无法做到一期关闭。对于此类患者,软组织重建主要分为两个阶段:第一阶段为出血控制后,局部清创清除感染及坏死组织并使用负压封闭引流,每5~7天为一个周期,根据实际情况重复若干个周期;第二阶段为创面感染得到有效控制,局部肉芽生长良好,可以采用游离植皮或皮瓣技术修复创面。游离皮片植皮技术难度相对较低,是目前临床应用最为广泛的皮肤缺损修复技术,取皮部位可选择头皮、腹部、大腿或小腿。电动取皮刀和拉网植皮技术的应用可使游离皮片的利用率大大提升。皮瓣技术相对显微外科技术有一定要求,目前只能在部分具有显微外科技术能力的医院开展。骨盆区软组织缺损常用皮瓣有阴股沟皮瓣、股薄肌皮瓣、腹直肌带蒂皮瓣、腹壁下动脉皮瓣、股前外侧穿支皮瓣、阔筋膜张肌皮瓣、缝匠肌皮瓣、髂腹股沟皮瓣等[19](图3、4)。此外,针对臀部等皮肤延展性较好的区域,采用皮肤牵张闭合术消灭或缩小创面是新的选择(图5)。利用皮肤的机械蠕变效应,在数个周期的循环牵张下,可有效减小创面皮肤缺损面积甚至达到无张力闭合的效果。该技术不增加供区损伤,且可缩短治疗周期,并可最大限度保留皮肤缺损处功能[20]。

图3 患者男性,65岁,开放性骨盆骨折合并会阴部皮肤软组织缺损,阴股沟旋转皮瓣修复会阴部创面

图4 患者男性,48岁,货车碾压致开放性骨盆骨折合并左髋部大面积皮肤软组织缺损,腹直肌带蒂皮瓣修复局部创面
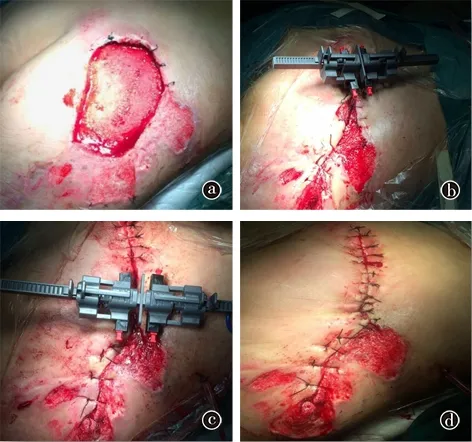
图5 患者男性,36岁。a.开放性骨盆骨折合并右臀部20cm×12cm面积皮肤缺损;b.皮肤牵张闭合器对创缘皮肤进行牵张;c.经过5个牵张循环皮肤无张力闭合;d.间断缝合关闭创面
综上所述,尽管近年来对软组织损伤的处置日益重视,其评估、诊断和治疗技术也有了长足进步,开放性骨盆骨折软组织损伤处置仍面临巨大挑战,其复杂之处在于涉及消化、泌尿、生殖和运动等多个系统,需要创伤外科医师具有丰富全面的外科知识和技能储备。早期准确的软组织损伤评估分型、及时合理的结肠造口和膀胱造瘘、稳健的清创节奏把握、有的放矢的抗生素使用和感染控制以及精妙的创面修复技术运用是开放性骨盆骨折软组织损伤成功治疗的关键。

