ABCB4基因突变相关肝硬化误诊为Wilson病1例报告
华 磊,孙 权,许文彬,张 龙,王共强
1 安徽中医药大学神经病学研究所附属医院 神经内科,合肥 230061;2 安徽中医药大学第一附属医院 感染科,合肥 230031
1 病例资料
患者男性,48岁,因“检查发现肝功能异常,肝硬化5年”于2019年8月7日入院。患者曾于2014年体检发现“谷酰转肽酶”异常升高,肝脏B超提示“肝硬化”,当时未诉不适,给予“护肝”治疗,肝酶指标未恢复正常。患者因无明显不适症状,此后未积极求诊、治疗。2019年7月初,患者出现巩膜及皮肤黄染,于当地某大学附属医院就诊,实验室检查提示:WBC 2.57×109/L,PLT 52×109/L;肝功能异常:TBil 67 μmol/L,DBil 33.2 μmol/L,ALT 58 U/L,AST 86 U/L,GGT 180 U/L,TP 54.8 g/L,Alb 31.1 g/L;血氨升高(123 μmol/L);凝血指标异常:凝血酶原时间19.5 s,国际标准化比值1.66,活化部分凝血酶时间51.9 s,纤维蛋白原1.6 g/L,凝血酶时间21.2 s;甲、乙、丙、丁、戊型肝炎病毒指标均阴性,自身免疫性肝炎抗体阴性。腹部磁共振平扫、增强及磁共振胰胆管造影示:肝硬化,门静脉高压(脾大,食管胃底静脉曲张),腹水及胆囊结石;肝细胞病理示:较符合自身免疫性肝炎(轻型)。初步诊断为自身免疫性肝炎,肝硬化失代偿期。使用糖皮质激素治疗后,肝功能各项指标无好转,进一步检查发现铜蓝蛋白轻微减低(193 mg/L,参考值220~550 mg/L),24 h尿铜升高(218 μg/24 h,参考值<100 μg/24 h)。诊断考虑为Wilson病,被推荐至本院进一步诊治。
患者入院无食欲减退、恶心、呕吐、腹胀、黑便等表现。体检:慢性肝病面容,双侧巩膜及全身皮肤黄染,面、颈部见数枚蜘蛛痣,无皮肤、黏膜瘀斑及新鲜出血点,腹部平软,未见腹壁静脉曲张,压痛(-),Murphy征(-),肝脾肋下未触及,移动性浊音(-),双下肢不肿。神经系统体检未见异常。患者无肝炎病史及血吸虫病史,否认药毒物接触史,无饮酒及吸烟史,无家族遗传病病史。入院检查,肝功能异常:TBA 117.7 μmol/L,TBil 63 μmol/L,DBil 38.3 μmol/L,ALT 69 U/L,AST 97 U/L,GGT 274 U/L,胆碱酯酶2251 U/L,TP 59.2 g/L,Alb 34.2 g/L,血氨72 μg/L。肝纤维化指标明显升高:透明质酸970.22 ng/ml,Ⅳ型胶原322.52ng/ml。铜生化各项指标均正常:铜蓝蛋白229.2 mg/L,铜氧化酶0.317 OD,血清铜12.52 μmol/L。两次检测24 h尿铜轻微升高:分别为110.43、122.98 μg/24 h;小便量为2.47 L、2.61 L。裂隙灯检查示角膜K-F环(-)。腹部彩超结果提示:肝硬化,胆囊炎,胆囊结石,脾大,腹水阴性。患者以肝硬化失代偿期表现为主,初步诊断为肝硬化失代偿期(Child-Pugh B级),病因诊断考虑遗传代谢性疾病。患者无遗传性疾病家族史,复查铜生化结果正常,角膜K-F环(-),仅24 h尿铜轻度升高,因此Wilson病诊断证据不足。治疗上暂时给予“护肝、改善胆红素循环、降血氨”等,待明确病因诊断后,进一步针对病因治疗。对症治疗10余天后,患者黄疸加深,复查肝功能结果提示胆汁淤积加重并出现“胆酶分离”倾向(TBA 338.2 μmol/L,TBil 65.7 μmol/L,DBil 43.4 μmol/L,ALT 40 U/L,AST 62 U/L,GGT 207 U/L,TP 55.7 g/L,Alb 32.0 g/L)。与患者及其亲属沟通并取得知情同意后,行肝硬化相关遗传代谢性疾病基因筛查。结果显示:ABCB4基因第6号外显子杂合突变(图1),ATP7B基因无突变。最终明确诊断为ABCB4基因突变相关肝胆病所致肝硬化。给予熊去氧胆酸治疗,患者病情仍进行性加重,2个月后患者出现大量胸腹水,拟进一步行肝移植治疗。
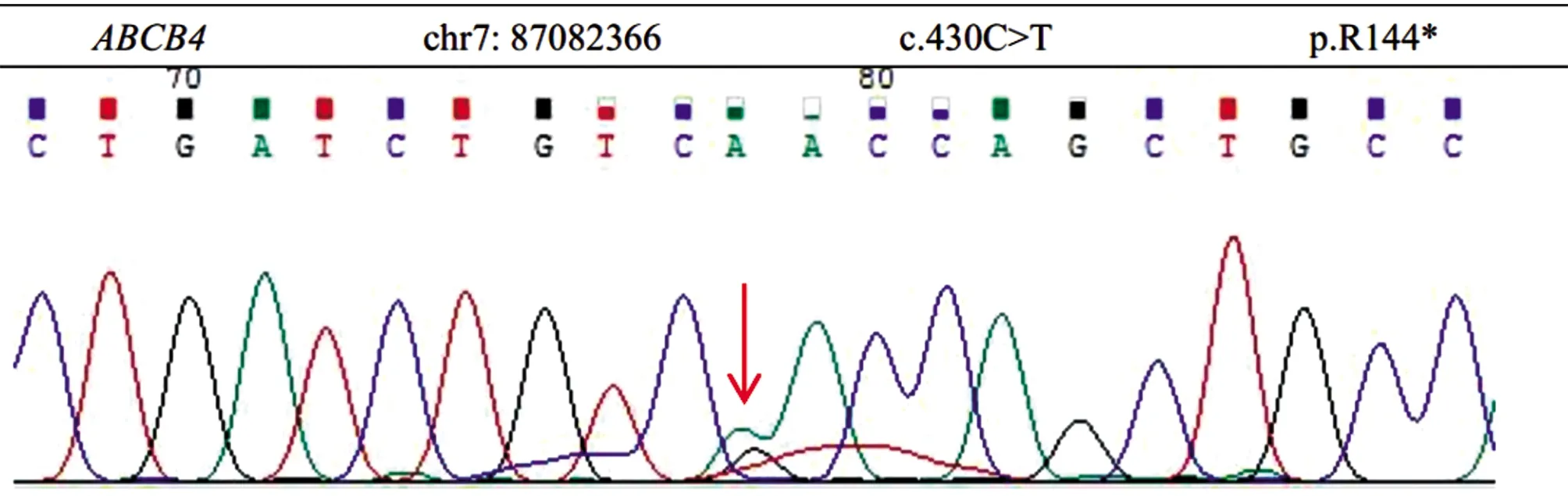
注:c.430C>T∶p.R144*,编码区第 430 号核苷酸由胞嘧啶变异为胸腺嘧啶,导致第 144 号氨基酸由精氨酸变异为终止,为无义突变。
2 讨论
ABCB4(ATP-binding cassette, sub-family B, member 4)基因位于人类第7号染色体长臂(7q21.1),分布于肝细胞毛细胆管膜,编码MDR3蛋白,MDR3蛋白可以将磷脂从毛细胆管膜双分子层内侧转运到外侧,与胆汁酸盐和胆固醇形成混合微粒,增强胆固醇的溶解,在正常胆汁排泄中起重要作用。当ABCB4基因突变时,MDR3蛋白表达减少,胆汁中磷脂减少,胆固醇溶解降低,形成结晶析出[1]。另外,由于胆汁中磷脂减少,导致肝细胞和胆管细胞长期暴露于胆盐毒性作用下而产生持续性炎症和纤维增生,从而导致纤维化[2]。ABCB4基因突变形式多变,可引起进行性家族性肝内胆汁淤积症3型、低磷脂相关性胆石症、妊娠期肝内胆汁淤积症、慢性胆管病和成人胆汁纤维化/肝硬化等疾病[3]。约34%不明原因的成人胆汁淤积患者检测到ABCB4杂合突变,并可导致明显肝纤维化,但大部分患者无胆道症状[4]。早期使用熊去氧胆酸治疗可改善胆汁淤积并延缓纤维化进程,改善预后[5]。
Wilson病为ATP7B基因突变所致的铜代谢障碍性常染色体隐性遗传疾病,以肝脏、神经系统等器官组织受累为主。ABCB4基因突变相关疾病及Wilson病均是遗传代谢性疾病导致肝硬化的重要病因。ABCB4基因突变引起铜过载及肝硬化误诊为Wilson病的病例鲜有报道。Shneider等[6]报道了1例2岁女性儿童肝硬化患者误诊为Wilson病的病例,患者铜蓝蛋白为28 mg/dl,肝脏铜含量高达248 mg/g干重,起初诊断考虑为Wilson病,基因检测确定系ABCB4突变所致胆汁淤积性肝硬化,另外该患者对熊去氧胆酸治疗反应良好也印证该病诊断。
健康人中,铜离子主要经过胆道排泄,铜蓝蛋白系铜离子排泄运载体,在Wilson病患者中,ATP7B基因突变引起铜蓝蛋白表达显著减少,导致铜离子经胆道排泄明显减少,进而肝脏中淤积的铜离子大量增加,经尿液排泄铜离子亦显著增多[7]。肝脏中铜及铜关联蛋白积聚现象在胆汁淤积性慢性肝病中可以出现[8]。27%~54%成人不明原因胆汁淤积患者中,存在已知的基因突变[9],ABCB4突变相关疾病主要导致胆汁淤积,胆盐排泄不畅,因此可以引起肝脏及尿铜含量升高。
本例患者早期仅表现转氨酶指标异常,影像学提示肝硬化,无明显胆汁淤积症状表现,待出现明显黄疸时,检查发现铜蓝蛋白减低,24 h尿铜增高,因此被误诊为Wilson病。起初胆汁淤积未引起重视,治疗过程中TBA快速上升,提示胆汁淤积加重,但由胆汁淤积引起铜代谢障碍在临床中极少被观察到,相关疾病很少引起临床医师重视,因而容易导致ABCB4突变相关疾病与Wilson病误诊。由此可见,依据铜超载相关指标,如根据肝铜质量增加,尿铜含量增加等条件诊断Wilson病存在误诊的可能。临床工作中,对于不明原因的肝脏病变,若铜蓝蛋白和/或铜氧化酶减低,24 h尿铜升高,则多提示为Wilson病。伴有神经系统锥体外系症状,角膜K-F环,相关家族史以及ATP7B基因检测等可为明确诊断提供更充分的依据。排除Wilson病诊断后,需考虑胆汁淤积性肝病的可能,排除常见的胆汁淤积病因(如原发性胆汁性胆管炎、原发性硬化性胆管炎、药物性肝损伤、酒精性肝病等)后,可进一步进行相关基因筛查,需重点关注ABCB4基因突变相关疾病,有助于明确病因诊断[10]。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:华磊负责资料收集、分析及撰写论文;孙权、许文彬、张龙参与收集资料,提供意见及修改论文;王共强负责指导撰写文章并最后定稿。

