三种全自动发光免疫分析仪检测丙型肝炎病毒抗体性能比较
刘兆宇,肖征,张自豪,程菲,周月,张晓
解放军总医院海南医院 a.检验中心;b.中心实验室,海南 三亚 572013
引言
丙型肝炎是由丙型肝炎病毒(Hepatitis C Virus,HCV)引起的一种肝脏疾病,呈全球性流行,不同性别、年龄、种族均对HCV易感[1]。研究发现80%的HCV患者因早期诊断和治疗不及时发展为慢性肝炎,约10%最终发展为肝硬化甚至肝癌[2]。针对这一严重危害人类健康的传染病,实验室诊断对丙肝的预防、诊断和疗效监测具有重要意义,早期诊断并及时治疗是防止病毒传播的有效手段[3]。抗HCV检测最常用于感染者的筛查,目前抗HCV的检测方法包括了酶联免疫吸附法、发光法、胶体金法、重组免疫印迹法等,而发光法以其自动化程度高、检测速度快、灵敏度高等特点被广泛使用[4]。
尽管用于抗HCV检测的自动化仪器争相推出,但不同品牌的仪器间往往存在较大的性能差异。全面了解检测性能,可以为临床实验室合理选购仪器和科学发布结果提供帮助。本文对Sysmex HISCOL5000、索灵LIAISON-XL、罗氏combas-E602三种全自动发光免疫分析仪的检测性能进行了全面的分析比较。为临床实验室选择合适的抗HCV检测方式提供参考依据,以便进一步提高丙肝诊断尤其是早期诊断的效率。
1 对象与方法
1.1 临床资料
收集2017年1月至2019年6月于解放军总医院海南医院就诊患者的抗HCV检测结果,统计结果分布频率。2019年1月至2019年6月于解放军总医院海南医院就诊,非丙型病毒性肝炎患者标本295例、丙型肝炎患者标本91例,诊断符合《丙型肝炎防治指南(2015年更新版)》诊断标准[3],用于性能评价。
1.2 仪器和试剂
Sysmex HISCOL5000全自动化学发光分析仪及配套试剂,结果判断以COI≥1.0为阳性,检测灰区为0.9~1.1;索灵LIAISON-XL全自动化学发光分析仪及配套试剂,结果判断以S/CO≥1.0为阳性,检测灰区为0.9~1.1;罗氏combas-E602全自动电化学发光分析仪及配套试剂,结果判断以COI≥1.0为阳性,检测灰区为0.9~1.1。抗体确证实验采用重组免疫印迹实验(Recombinant Strip Immunoblot Assay,RIBA),试剂购于北京万泰生物药业有限公司。结果判断标准为:未出现抗体特异性条带为阴性,出现一个条带判为不确定,出现两个或两个以上条带为阳性。抗-HCV标准物质(浓度2 NCU/mL)及阴性血清购自北京康彻思坦生物公司。
1.3 检测方法
参照《全国临床检验操作规程》要求,严格按照仪器的操作规程和试剂说明书操作,在室内质量控制结果允许范围内对标本进行检测。
1.4 观察与评价指标
1.4.1 精密度
通过批内和批间变异进行精密度评价,方法参考NCCLSEP5-A2[5]文件。批内精密度:选取高、低两个浓度水平临床样本(L1,L2),充分混匀,1 d内连续检测20次。批间精密度:选取各仪器配套高、低两个浓度水平质控品(L1,L2),混匀后各分装20份,-20℃保存,每天每个水平测定1次,连续检测20 d。
1.4.2 准确度
检测2019年2次卫生部感染性疾病血清学标志物系列A的EQA留样(样本编号为1911~1915和1921~1925)。结果与卫生部临检中心下发的回报结果进行比较。
1.4.3 检出限
依据CLSIEP12-A2[6]文件,用抗-HCV标准物质,浓度水平为2 NCU/mL,以阴性血清(北京康彻斯坦生物技术有限公司)进行稀释,稀释浓度分别为1、0.8、0.7、0.6、0.5、0.4、0.3、0.2、0.1、0.09、0.04 和 0.03 NCU/mL。用三种仪器分别检测不同稀释浓度的样本,以仪器可以判别阳性所对应的最低浓度为最低检测限。每个浓度重复检测3次,COI及S/CO值以均值计算。
1.4.4 临床特异性与临床灵敏度
根据《华人民共和国卫生行业标准-定性测定性能评价指南(WS/T505-2017)》[7]进行临床特异性和灵敏度评价。临床特异性:选取295例阴性样本,其中包括可能有潜在交叉反应的标本77例(乳糜标本6例、溶血标本5例、乙型肝炎病毒表面抗原阳性标本20例、类风湿因子阳性标本20例、抗核抗体阳性标本20例、抗梅毒螺旋体特异性抗体阳性6例),分别用三种仪器检测,临床特异性计算为:真阴性数/总样本数×100%。临床灵敏度:选取确诊丙型肝炎患者标本91例,分别用三种仪器检测,临床灵敏度计算为:真阳性数/总样本数×100%。
1.4.5 结果一致性比较
选取三种仪器之一检测结果COI或S/CO值在1~3之间的弱反应性标本28例,用其他两台仪器复检,最终结果用RIBA进行确认。
1.4.6 结果分布频数
统计三种仪器检测标本,其中HISCL5000共13883例、LIAISON-XL共13631例、Roche-E602共13768例,根据不同COI或S/CO值将其分为六组(0~0.5、0.5~0.9、0.9~1.1、1.1~3.0、3.0~10.0、>10.0),以各组样本数绘制结果分布图。
1.5 统计学处理
采用Excel软件进行数据整理和计算分析。Sigmaplot 12.5进行图形绘制。
2 结果
2.1 精密度
三种仪器的批内精密度、批间精密度结果,见表1。

表1 三种仪器检测丙型肝炎病毒抗体的精密度
2.2 准确度
分别用三台仪器检测2019年2次卫生部室间质评感染性疾病血清学标志物系列A(EQA)留样(样本编号为1911~1915和1921~1925),与回报结果比对,结果符合率均为100%,见表2。

表2 三种仪器检测2019年卫生部室间质评丙型肝炎病毒抗体(不同编号样本)结果
2.3 检出限
HISCOL-5000的最低检出浓度为0.4 NCU/mL;LIAISON-XL的最低检出浓度为0.7 NCU/mL;Roche-E602的最低检出浓度为0.04 NCU/mL。稀释标准血清检测结果,见表3。

表3 三种仪器对不同浓度稀释标准物质的检测结果(NCU/mL)
2.4 临床特异性与临床灵敏度
295例阴性样本(包含干扰样本77例)分别用三种仪器进行检测,HISCOL5000的临床特异性为97.96%,LIAISON-XL的临床特异性为96.94%,Roche-E602的临床特异性为98.64%。其95%置信区间,见表4。91例阳性标本检测临床灵敏度的结果均为100%,其95%置信区间为95.95~100,见表5。

表4 三种仪器检测丙型肝炎病毒抗体的临床特异性

表5 三种仪器检测丙型肝炎病毒抗体的临床灵敏度
2.5 结果一致性比较
28例结果中,RIBA确认实验阴性12例,HISCOL5000检测结果与之相符合11例、LIAISON-XL1例、Roche-E602 11例。阳性8例,HISCOL5000检测结果与之相符合8例,LIAISON-XL 7例,Roche-E602 8例。其余8例为结果不确定,见表6。

表6 28份丙型肝炎病毒抗体弱反应性标本RIBA确认结果
2.6 结果分布情况
如图1~3所示,HISCL5000测量结果中,检测结果主要集中在COI<0.5和>10的区间,灰区结果(COI:0.9~1.1)所占比例为0.10%,COI在1.1~3.0结果占比为0.16%;LIAISON-XL灰区结果(S/CO:0.9~1.1)所占比例为0.14%,S/CO值在1~3的结果所占比例为1.72%;Roche-E602灰区结果(COI:0.9~1.1)所占比例为0.07%。

图1 HISCL5000检测结果频数分布图

图2 LIAISON-XL检测结果频数分布图
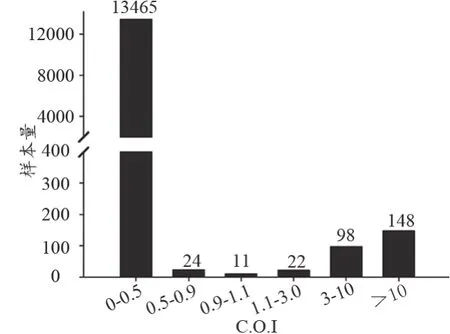
图3 Roche-E602检测结果频数分布图
3 讨论
丙型病毒性肝炎起病隐匿,多数患者症状不明显,如不加以干预,将有转归肝癌的可能[8]。值得庆幸的是,丙型肝炎的治疗已取得很大进展,绝大部分患者经8~12周的药物治疗可获得治愈且副作用极小[9]。因此早期筛查、早期诊断就成为丙型肝炎防治的重点。丙肝抗体测定是用于判断HCV是否感染的初筛试验,其结果的正确性对丙型病毒性肝炎筛查和确认具有重要意义[10]。抗HCV抗体的检测方法依次经历了ELISA、化学发光、电化学发光、时间分辨荧光等阶段[4]。而发光法检测丙肝抗体凭借可自动化、灵敏度高、快速、稳定等优点,被国内三甲医院广泛采用。然而对于不同厂家仪器的临床性能,目前还少有横向比较的研究,故本研究对Sysmex HISCOL5000、索灵LIAISON-XL、罗氏combas E602三种仪器的检测性能做了较全面的对比。
精密度是反应仪器性能最基本的指标,本研究对三种仪器检测抗HCV的精密度评价参照NCCLSEP5-A2,以定量免疫实验的评价方式为标准,此法相对严格,但结果表明,三种仪器的批内、批间精密度变异系数都较小,三种仪器的重复性较好,测定结果稳定。准确度评价中,卫生部感染性疾病血清学标志物系列A的EQA留样再测结果,三种仪器符合率均为100%,检测抗HCV的准确度符合要求。检出限是评估检验方法能检测到的分析物的最低浓度,本研究中Sysmex HISCOL5000、索灵LIAISON-XL、罗氏combas 8000 Roche-E602的检出限分别为0.4、0.7和0.04 NCU/mL。低值检出限对于HCV感染者的筛查具有重要意义,其检出阈值的降低能缩短急性丙型肝炎患者抗HCV检测的窗口期,从而达到早期诊断的目的。
在临床特异性与临床灵敏度评价中,三种仪器都表现出了较好的灵敏度(100%),这表明三种仪器可以最大程度地避免漏诊。但本研究选取的91例阳性标本均来自明确诊断的患者。受限于标本,本研究并未评估处于窗口期患者标本的检出灵敏度,这也是本研究的一点不足。三种仪器的临床特异性分别为97.96%、96.94%、98.64%。临床特异性与假阳性息息相关,假阳性结果可能导致误诊并使患者产生不必要的心理压力,更严重者有可能导致医疗事故,所以对于这类结果,在临床工作中必须加以重视。造成假阳性的原因可能与骨髓瘤、类风湿因子阳性、肝病(如肝硬化和癌症)、自身免疫性疾病(如自身免疫性肝炎)或其他病毒感染(如艾滋病或乙型肝炎)所造成的非特异性免疫球蛋白发生交叉反应有关[11-12]。本研究选取的295例阴性样本中,包含了可能存在干扰样本77例,但具体何种物质会造成干扰反应以及反应程度如何还需进一步探究。
将“弱反应性(COI或S/CO值为1~3)”结果与RIBA确认实验比较,Sysmex HISCOL5000和Roche-E602的一致率较高(67.9%),索灵LIAISON-XL较低,仅为28.6%。不一致的结果主要体现为假阳性,这可能与抗-HCV检测试剂采用重组抗原包被有关,重组抗原在提高检测灵敏性的同时,也更容易出现假阳性[13]。三种仪器间比较,Sysmex HISCOL5000和Roche-E602有较高的一致率。同时,我们也分析了三种仪器检测结果出现“弱反应性”的频率,实际工作中,弱反应性结果给检验人员造成极大困扰[14],建议当结果出现弱反应时,应采取不同厂家的两种方法进行复检,对于有条件的单位,可以采用RIBA实验进行确认。但需要指出的是,RIBA实验并不能反映感染是否处于活动期[15],且试剂的费用昂贵,因此对于此类标本,进一步进行丙型肝炎病毒核算定量检测是较科学的评估手段[16]。
此外,经济成本、检测时间、可操作性等也是评价仪器时需要综合考虑的因素,本研究的三种仪器中,Sysmex HISCOL5000的检测时间最短(17 min),标本用量最少(20 μL),更适于急诊标本检测。总之,本研究对三种全自动发光仪检测抗HCV的性能做了全面的比较分析,为临床实验室选择仪器和复检流程的制定提供参考策略,进一步为提高丙型病毒性肝炎诊断效率提供一定帮助。

