交联木薯淀粉的干法制备及其性能研究
玉琼广,陈江枫,梁露锋,陈 渊
(1.非粮生物质酶解国家重点实验室,广西农垦明阳生化股份有限公司,广西南宁 530226; 2.广西农产资源化学与生物技术重点实验室,玉林师范学院化学与食品科学学院,广西玉林 537000)
淀粉的交联变性是交联剂与淀粉分子中羟基发生反应,淀粉分子通过醚键或酯键形成具有空间网状结构的高聚物[1-2]。交联变性淀粉与原淀粉相比,淀粉糊化温度高、黏度下降、热稳定性好,同时具有抗剪切性能及耐酸性等性质[3-4],广泛应用于食品[3]、制药[5]、纺织[6]、造纸[7]、化工[8]等领域。目前,交联淀粉制备工艺主要有湿法和干法,工业上一般采用湿法生产。湿法工艺是将淀粉分散于水或其他溶剂中调成淀粉乳,在碱性体系中与交联剂反应得到交联变性淀粉[9]。该法反应均匀,但存在反应时间过长、产生废水、反应效率低、工艺复杂、生产成本高等不足[10]。干法工艺生产变性淀粉是在淀粉含水量较少的条件下(20%以下),将反应原料混合溶液喷洒于干淀粉上,混合均匀后,在一定温度下反应得到产品。制备工艺简单、反应效率高、能耗低、污染小。但需要较高的反应温度(140~180 ℃),且传统加热法升温速度慢、物料受热面积小、交联反应不均匀[10]。
机械活化改性法是利用机械力作用,使固体颗粒在机械力作用下获得能量,增多、增强化学反应点的一种新型干法技术[11]。具有反应效率高、操作简单、生产成本低、废水排放少的特点[12]。课题组前期采用机械活化干法进行制备性能较好的酯化淀粉[13-14]、羧甲基淀粉[15]等。本试验以自制球磨机作为反应器,以木薯淀粉为原料,干法制备了交联木薯淀粉,考察了各因素对交联反应的影响,采用正交试验优化了工艺条件。在测定交联淀粉的理化特性的基础上,采用红外光谱(FTIR)、X-射线衍射(XRD)、扫描电镜(SEM)对木薯淀粉交联的结构进行表征,以便为干法生产交联淀粉及其应用提供理论依据。
1 材料与方法
1.1 材料与仪器
木薯淀粉(工业级) 广西农垦明阳生化股份有限公司;三偏磷酸钠(AR) 上海晶纯试剂有限公司;氢氧化钠(AR) 广东光华化学厂有限公司;无水乙醇(AR) 广东光华化学厂有限公司。
自制球磨机(内径为115 mm,高度为170 mm,容积1200 mL,不锈钢磨球);BS224S型电子分析天平 赛多利斯科学仪器(北京)有限公司;DHG-9076A型电热恒温鼓风干燥箱 上海精宏实验设备有限公司;SHZ-88型水浴恒温振荡器 江苏金坛市医疗仪器厂;SHB-III型循环水式多用真空泵 郑州长城科工贸有限公司;FW100型高速万能粉碎机 天津市泰斯特仪器有限公司;80-2型离心机离心机 金坛市医疗仪器厂;722SP型可见分光光度计 上海光学仪器五厂;Spectrum100傅立叶变换红外光谱仪 美国铂金埃尔默仪器有限公司;D8 ADVANCEX-RD粉末衍射仪 德国BRUKER。
1.2 实验方法
1.2.1 交联木薯淀粉制备 称取1 g三偏磷酸钠(占淀粉干基质量分数2%),加入50 g木薯淀粉(干基),不断搅拌,再加入1.25 g氢氧化钠(占淀粉干基质量分数2.5%),使体系呈弱碱性(pH=8~9),混合物密封放置24 h,安装好球磨机和恒温水箱管路,加入磨球和混合物,在球磨介质堆体积500 mL、搅拌速度380 r·min-1、水浴温度50 ℃条件下,反应60 min,分离样品与磨球,用75%的乙醇洗涤产品呈至中性,烘箱50 ℃烘干,再经粉碎、过筛,得交联木薯淀粉,备用[16]。
1.2.2 淀粉交联的单因素和正交试验
1.2.2.1 单因素实验 固定木薯淀粉为50 g(干基)、氢氧化钠用量2.5%(占淀粉干基质量分数)、反应时间为60 min、反应温度为50 ℃、搅拌桨转速为380 r·min-1、球磨介质堆体积为500 mL,分别考察三偏磷酸钠用量1%、2%、3%、4%、5%对淀粉交联反应的影响。
固定木薯淀粉为50 g(干基)、三偏磷酸钠4%、反应时间为60 min、反应温度为50 ℃、搅拌桨转速为380 r·min-1、球料比为500 mL,分别考察氢氧化钠用量0.5%、1.5%、2.5%、3.5%、4.5%对淀粉交联反应的影响。
固定木薯淀粉为50 g(干基)、三偏磷酸钠4%、氢氧化钠用量2.5%、反应时间为60 min、搅拌桨转速为380 r·min-1、球磨介质堆体积为500 mL,分别考察反应温度30、40、50、60、70 ℃对淀粉交联反应的影响;
固定木薯淀粉为50 g(干基)、三偏磷酸钠4%、氢氧化钠用量2.5%、反应温度为50 ℃、搅拌桨转速为380 r·min-1、球磨介质堆体积为500 mL,分别考察反应时间15、30、60、90、120 min对淀粉交联反应的影响;
固定木薯淀粉为50 g(干基)、三偏磷酸钠4%、氢氧化钠用量2.5%、反应温度为50 ℃、反应时间60 min、球磨介质堆体积为500 mL,分别考察转速为220、300、380、450、520 r·min-1对淀粉交联反应的影响;
固定木薯淀粉为50 g(干基)、三偏磷酸钠4%、氢氧化钠用量2.5%、反应温度为50 ℃、反应时间60 min、转速380 r·min-1,分别考察球磨介质堆体积为300、400、500、600、700 mL对淀粉交联反应的影响。
1.2.2.2 正交试验 在单因素实验的基础上,以沉降积为试验指标,选取反应温度(A)、反应时间(B)、搅拌桨转速(C)、三偏磷酸钠用量(D)、氢氧化钠用量(E)五个因素安排L16(45)正交试验,优化干法制备交联木薯淀粉工艺条件,并对结果进行验证,正交因素与水平设计见表1。
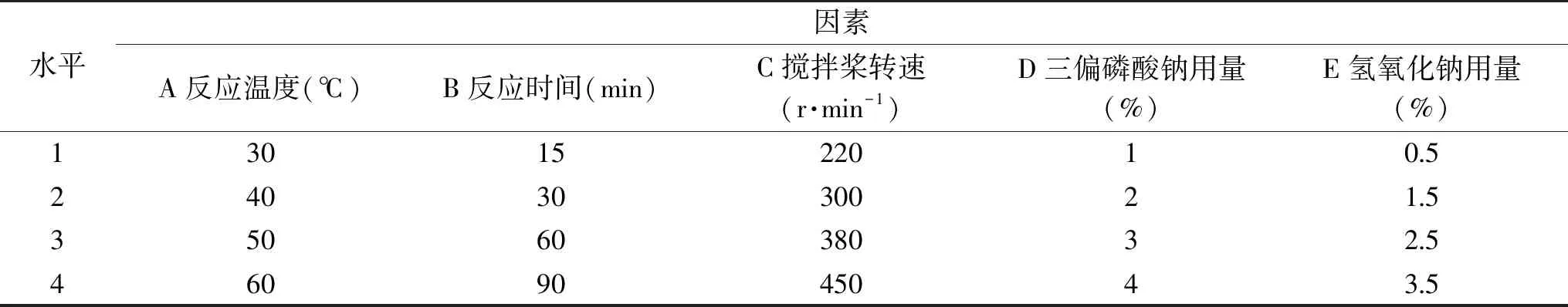
表1 正交试验因素与水平Table 1 Factors and levels of orthogonal experiments
1.2.3 交联度测定 参考文献[17]采用沉降积法测定淀粉交联度。沉降积越小,交联度越大。准确称取1.0 g淀粉样品置于100 mL的烧杯中,用移液管移取50 mL蒸馏水,与样品混合均匀后制成质量分数为2%的乳液。将乳液于82~85 ℃的水浴中,略加搅拌,保温2 min,取出自然冷却至室温。用2支10 mL刻度离心管分别装入10 mL的糊液,在转速为4000 r·min-1离心4 min,将上层清液移入另一支同样体积的离心管中,读取上清液的毫升数,同一样品平行测定两次,取其平均值。沉降积计算公式如下:
Vs=10-V
式中,V-上清液的体积,mL;Vs-沉降积,mL。
1.2.4 透明度、凝沉性、膨胀度的测定
1.2.4.1 透明度测定 用蒸馏水为空白,在25 ℃室温下,测定波长为620 mm处淀粉糊(质量浓度为2%)的透光率[18]。
1.2.4.2 凝沉性测定 配制质量分数为1%的淀粉乳100 mL,在沸水浴中加热搅拌20 min,取出冷却至室温,移入量筒内,加入水调糊液至100 mL,混匀,放置24 h,记录上清部分所占体积[18]。
1.2.4.3 溶解度和膨胀度的测定 将淀粉液于85 ℃恒温水浴中加热搅拌30 min,离心15 min,糊下沉部分为膨胀淀粉。将上清液分离、干燥、衡重,所得即为水溶淀粉的量,计算出溶解度,根据溶解度和膨胀淀粉的量计算交联淀粉的膨胀度[18]。溶解度和膨胀度的计算公式如下:

式中,S-溶解度,%;A-上清液蒸干后恒重的质量,g;W-绝干样品质量,g;P-离心后沉淀物的质量,g。
1.2.5 交联淀粉表征 采用美国Spectrum100型傅立叶红外光谱仪(FTIR)对样品进行FTIR测定。2 mg试样和200 mg KBr混合压片,扫描范围:4000~500 cm-1;采用德国D8 ADVANCE型X射线粉末衍射仪(XRD)对样品的XRD测定。操作条件为:特征射线Cukα,Ni片滤波,电压为40 kV,电流30 mA,测量范围(2θ):5°~70°。对样品粉末进行喷金处理,S-4800型电子扫描电镜对样品进行形貌测试。
1.3 数据处理
以沉降积为试验指标进行单因素试验。试验中独立样本t检验(显著性检验为t检验)采用SPSS 18.0统计软件进行统计学分析处理。
2 结果与讨论
2.1 三偏磷酸钠用量对交联木薯淀粉沉降积的影响
不同三偏磷酸钠用量对交联木薯淀粉沉降积的影响如图1所示。

图1 三偏磷酸钠用量对交联木薯淀粉交联度的影响 Fig.1 Effect of sodium phosphate dosage on the cross linking degree of cross-linked cassava starch
从图1可以看出,三偏磷酸钠用量在4%的范围内,交联木薯淀粉的沉降积随着三偏磷酸钠用量的增加而降低。当三偏磷酸钠用量为4%时,交联木薯淀粉的交联度达到最大,沉降积为1.45 mL。之后随着三偏磷酸钠用量的增加,沉降积增大,交联度下降。在适当范围内,增加交联剂的用量,增大了淀粉分子链上羟基交联的机会,提高反应效率,交联度增大[2]。随着交联剂用量的增加,淀粉的分子链增长,分子量增加,空间位阻增大,交联反应达到饱和状态,交联反应进行缓慢[19]。因此,三偏磷酸钠用量为4%(占淀粉干基质量分数)比较适宜。
2.2氢氧化钠用量对木薯交联度的影响
不同氢氧化钠用量对淀粉交联反应的影响如图2所示。
从图2中可以看出,氢氧化钠用量在2.5%范围内,交联淀粉的沉降积随着氢氧化钠用量不断增加而减小,用量达到2.5%时沉降积为1.45 mL,交联度最大。氢氧化钠用量超过2.5%后沉降积增大,交联度下降。氢氧化钠作为催化剂,可活化淀粉分子中的羟基,随着用量的增加,反应活性得到提高,交联剂更容易与淀粉发生交联反应[19]。但是催化剂用量进一步增加时,也增加了副反应发生的几率,导致淀粉交联度降低。因此,氢氧化钠催化剂用量为2.5%(占淀粉干基质量分数)比较适宜。

图2 氢氧化钠用量对交联木薯淀粉交联度的影响Fig.2 Effect of sodium hydroxide dosage on cross linking degree of cross-linked cassava starch
2.3 反应温度对木薯淀粉交联度的影响
不同反应温度对淀粉交联反应的影响如图3所示。

图3 反应温度对木薯交联淀粉交联度的影响Fig.3 Effect of reaction temperature on cross linking degree of cassava cross-linked starch
从图3中可以看出,反应温度为50 ℃时交联淀粉沉降积最小,交联度最大。温度升高有利于淀粉颗粒的膨胀,增加淀粉的平均能量,提高淀粉分子的活化能,有利于交联剂的渗透反应[2]。当温度超过50 ℃后,部分淀粉分子发生糊化,同时也增加副反应。因此,反应温度50 ℃为宜。
2.4 反应时间对木薯交联淀粉交联度的影响
不同反应时间对淀粉交联反应的影响如图4所示。
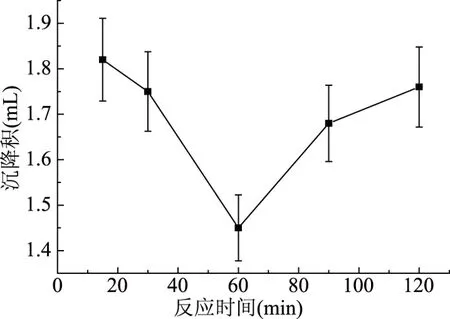
图4 反应时间对木薯交联淀粉交联度的影响Fig.4 Effect of reaction time on cross linking degree of cassava cross-linked starch
从图4中可以看出,反应时间在60 min范围内,交联淀粉的交联度随时间的增大而增大,反应时间超过60 min后交联木薯淀粉的交联度随时间的增大而减小。反应时间延长,可以使用反应原料接触机会增大,淀粉羟基与交联剂反应充分,增大交联木薯淀粉交联度[20]。在机械力的作用下,淀粉结晶结构更易受到破坏,加快反应速度,缩短了交联时间。故反应时间60 min为宜。
2.5 搅拌速度对木薯淀粉交联度的影响
不同搅拌桨转速对淀粉交联反应的影响如图5所示。

图5 转速对交联木薯淀粉交联度的影响Fig.5 Effect of rotational speed on cross linking degree of cross-linked cassava starch
从图5中可以看出,在转速为380 r·min-1以内,交联淀粉的交联度随转速的增大而增大,转速超过380 r·min-1后,淀粉交联度有所减小。主要原因是转速越快,淀粉分子的表面保护膜和其晶型结构破坏更加彻底,更有利于交联剂与催化剂的渗透反应,提高交联反应效率。随着转速的进一步增加,原料接触时间缩短,吸收热量减少,影响淀粉进行交联反应[14]。故转速380 r·min-1为宜。
2.6 球磨介质堆体积对木薯交联淀粉交联度的影响
不同球磨介质堆体积对淀粉交联反应的影响如图6所示。
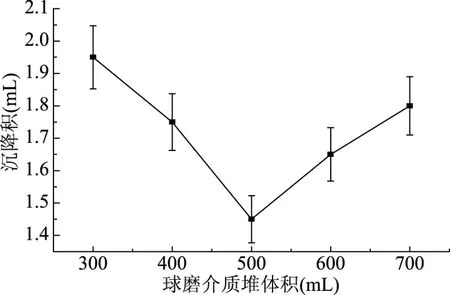
图6 球磨介质堆体积对交联木薯淀粉交联度的影响Fig.6 Effect of heap volume of ball milling media on cross linking degree of cross-linked
从图6中可以看出,在球磨介质堆体积为500 mL时,沉降积为1.45 mL,交联度最大。主要因为是随着球磨介质的体积增大,物料在球磨筒中的混合更加均匀,淀粉与交联剂和催化剂受到更大的摩擦力、剪切力,反应更加充分。但球磨介质过大会使物料的接触面积变小,不利于淀粉交联反应的进行[14]。采用球磨介质堆体积500 mL为宜。
2.7 交联工艺条件优化
根据单因素实验结果,采用三偏磷酸钠用量、氢氧化钠用量、反应温度、反应时间、搅拌桨转速五个因素进行正交试验,每个因素取4水平L16(45)安排正交试验,试验设计与结果如表2所示。
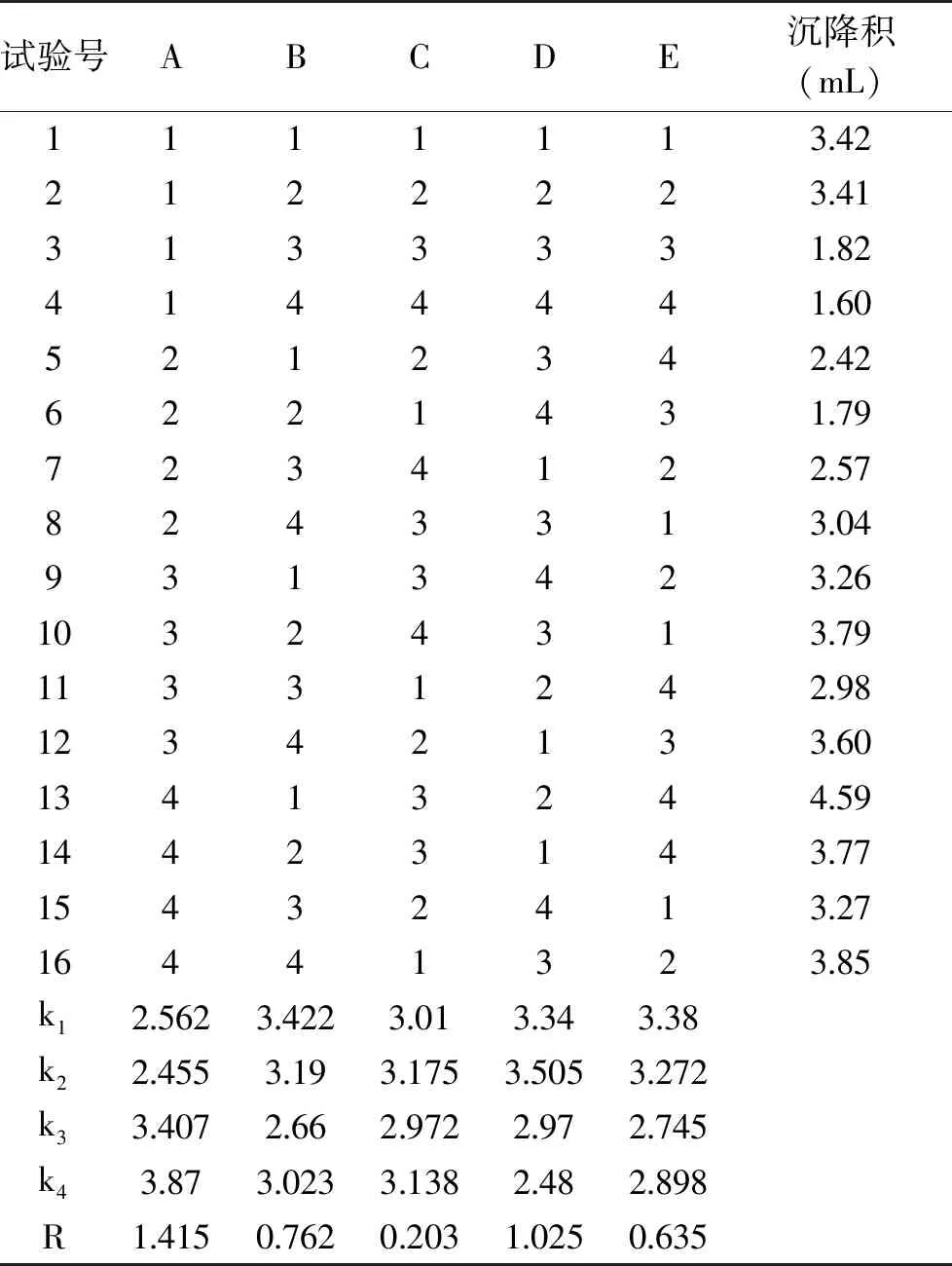
表2 正交试验设计与结果Table 2 Design and analyses of orthogonale test
由表2 和表3 可知,反应温度(A)的变化对实验结果的影响最为显著,影响交联木薯淀粉交联度因素的先后顺序为:反应温度>三偏磷酸钠用量>反应时间>氢氧化钠用量>搅拌桨转速。最终确定制备交联木薯淀粉工艺的最佳条件为A2B3C3D4E3,即:反应温度40 ℃,反应时间60 min,搅拌桨转速380 r·min-1,三偏磷酸钠用量4%,氢氧化钠用量2.5%。在最佳条件下,固定球磨介质堆体积为500 mL,进行两次平行试验,交联木薯淀粉沉降积为1.52 mL。
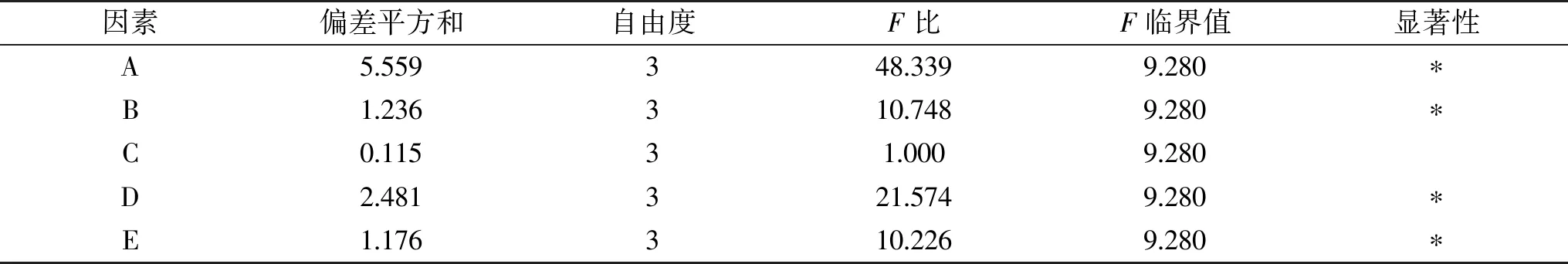
表3 正交试验方差分析Table 3 Variation analysis of orthogonal tests
2.8 交联木薯淀粉理化特性
不同沉降积交联木薯淀粉的透光率、凝沉性、膨胀度、溶解度如表4所示。

表4 木薯交联淀粉理化特性Table 4 Physicochemical properties of cross-linked cassava starch
由表4可看出,随着淀粉交联度的增大,透光率、膨胀度、溶解度下降,凝沉性增强。主要原因是,淀粉交联度增大,淀粉分子量增大,阻碍了光的透射,淀粉透光度下降。同时,交联度淀粉引入了交联键,键强度大于氢键强度,淀粉颗粒强度提高,淀粉糊化及溶胀困难,膨胀度和溶解度下降。此外,直链淀粉分子间的氢键在交联反应中受到了破坏,重新排列、缔合趋势下降,减弱了淀粉糊的分层倾向[21]。
2.9 红外光谱分析
不同沉降积交联淀粉的红外光谱如图7所示。从图7可以看出,交联淀粉红外光谱吸收在吸收峰波数方面与原淀粉相差不大。根据淀粉与三偏磷酸钠的反应原理,两者反应后会在995~1050 cm-1处形成P-O-C键,但是从图7中看到交联淀粉峰的强度很小,这可能是淀粉的交联度较小,反应生成的淀粉磷酸酯含量较少,与木薯原淀粉中磷酸酯基团产生了重叠[22]。但与原淀粉相比,交联淀粉中波数为3400 cm-1的-OH伸缩振动峰强度大而且宽,在3200~3600 cm-1范围内的平缓宽峰。表明-OH键发生了缔合,淀粉颗粒的羟基伸缩振动减少,即发生了交联反应,-OH键正逐渐以交联键取代,淀粉颗粒之间的交联是一个氢键不断受到破坏,氢键被交联键取代的过程[23]。
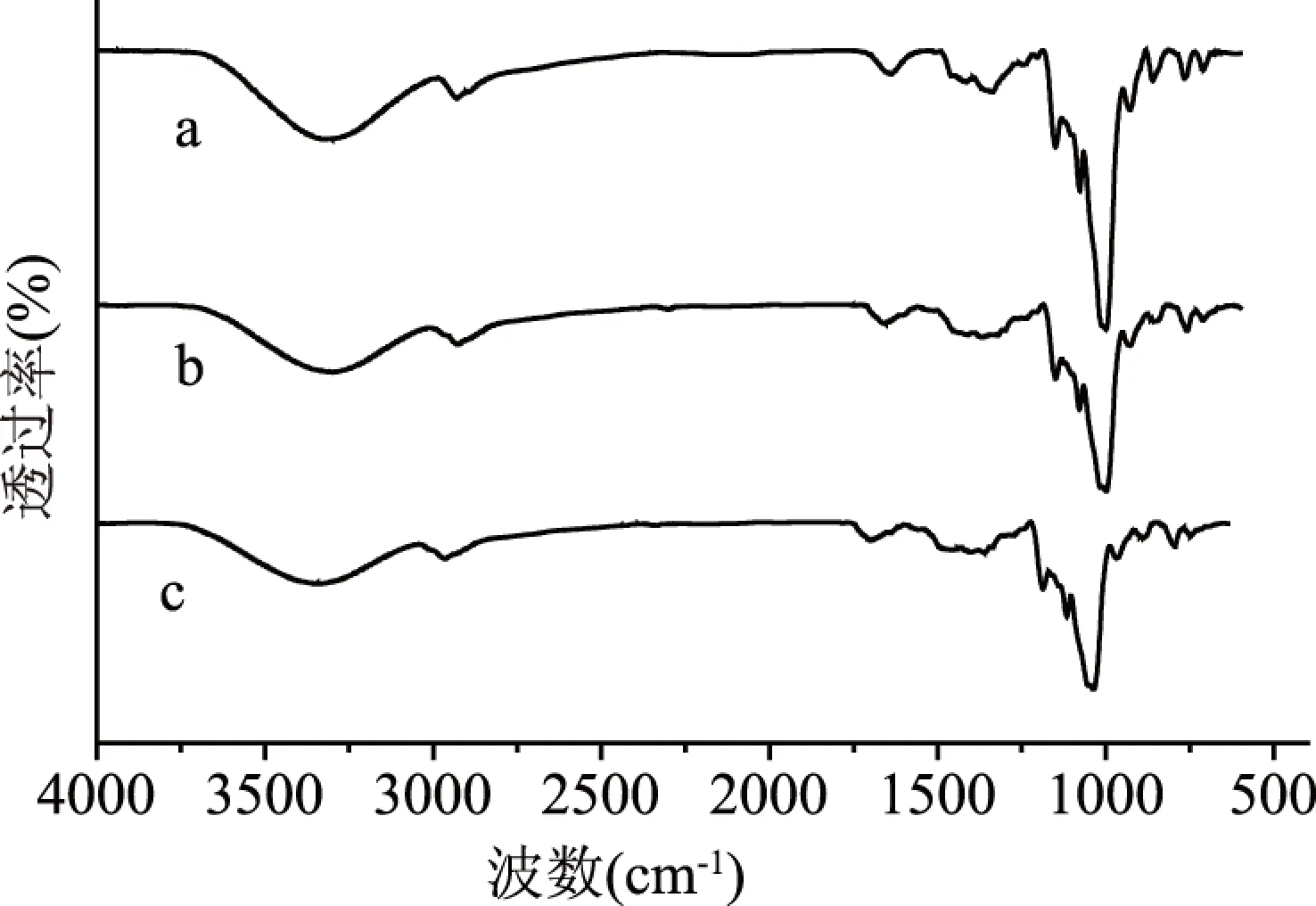
图7 木薯淀粉与不同交联度交联木薯淀粉的红外光谱Fig.7 FTIR of cassava starch and cross-linked cassava starch注:a:木薯淀粉;b:交联红薯淀粉(沉降积=1.82 mL); c:交联红薯淀粉(沉降积=1.52 mL);图8、图9同。
2.10 X-射线衍射分析
不同沉降积交联淀粉的X-射线衍射图如图8所示。由图8可以看出,木薯原淀粉衍射曲线有尖峰和弥漫峰,存在结晶结构和非结晶结构,在2θ=15.3、17.3、18.3、23.5 °处出现强衍射峰,表明木薯淀粉的晶型结构为 C 型[24]。随着产物交联度逐渐增加,曲线尖峰衍射特征逐渐减弱,弥散衍射特征逐渐增强。表明交联反应不但发生在无定形区,也发生在结晶区。随着交联度的增加,淀粉结晶区受破坏程度增大,但未明显改变淀粉晶型,这是产物交联度比较低的缘故。

图8 木薯淀粉与不同交联度交联木薯淀粉的XRD曲线Fig.8 XRD patterns of cassava starch and cross-linking cassava starch
2.11 交联淀粉扫描电镜分析
不同沉降积交联淀粉的X-射线衍射图如图9所示。从图9a可以看到,木薯淀粉颗粒部分呈球状,表面光滑,颗粒间紧密;淀粉经交联变性后,部分颗粒表面变粗糙,松散(图9b);当沉降积=1.52 mL时,颗粒表面更加粗糙,出现小孔洞,部分颗粒被破坏(图9c),这可能是交联反应和机械活化共同影响所致。

图9 木薯淀粉与不同交联度交联淀粉的扫描电镜照片Fig.9 SEM microscopy of cassava starch and cross-linking cassava starch
3 结论
机械活化干法可制备不同交联度的交联木薯淀粉,最佳工艺条件为:反应温度40 ℃,反应时间60 min,搅拌桨转速380 r·min-1,三偏磷酸钠用量4%,氢氧化钠用量2.5%,球料比500 mL。在此条件下制备的交联木薯淀粉的沉降积为1.52 mL。经过三偏磷酸钠交联改性的木薯淀粉随着交联度的增大,其透光率、膨胀度、溶解度下降,凝沉性增强。淀粉经交联变性后,结晶度下降,淀粉颗粒表面与原淀粉有明显差别,交联度大的样品表面粗糙,出现小孔洞,颗粒被破坏。

