高温下含缺陷CL-20 初始化学反应的分子动力学模拟
胡靖伟,甘 强,冯长根,李昌霖,朱双飞,程年寿
(北京理工大学爆炸科学与技术国家重点实验室,北京 100081)
1 引言
六硝基六氮杂异伍兹烷(简称HNIW,或CL-20)是已应用能量密度最高的单质炸药,1986 年由美国Nielsen[1]首次合成,其热安定性较好,最大爆速、爆压、密度等均高于奥克托今(HMX),能量输出比HMX高10%~15%[2]。为深入研究CL-20 爆轰机理,近年来许多理论模拟和实验研究CL-20 的初始化学反应,较少考虑缺陷的影响。研究含缺陷CL-20 的初始化学反应,对于了解其复杂的微观反应机理以及安全应用均具有重要意义。
1993 年Patil 等[3]首先采用光谱法研究了CL-20 热分解,计算出CL-20的热分解动力学参数。Tureotte等[4]通过热重分析研究了CL-20 的热分解过程,并对热分解产生的气体进行表征。陈松林等[5]采用布氏压力计法研究了CL-20 在真空条件下的热分解,并估算出70 ℃下的贮存寿命为43.8 年。许丽娟等[6]发现CL-20 热分解后的气体产物主要有NO、CO、CO2和H2O,计算了CL-20 的热力学参数和动力学参数,确定了活化焓、活化熵和活化自由能。目前关于CL-20热分解实验研究已取得较大进展,但只局限于宏观性质如分解温度、活化能等研究,缺少热分解反应中分子结构的变化、化学键的生成和断裂以及反应路径等信息。
近年来理论模拟方法在CL-20 单分子热解、极端高温热解研究中得以广泛应用。2005年Okovytyy等[7]采用量化计算研究了CL-20 单分子热分解反应,认为其初始反应是N—NO2断键形成NO2自由基,之后骨架上C—N 键断裂,导致开环以及H 原子转移。Isayev 等[8]发现CL-20 分解过程主要包括N—N 键断裂并伴有NO2生成、C—C 和C—N 键断裂导致开环反应。张力等[9]采用ReaxFF 力场研究发现,ε-CL-20 超晶胞发生N—N 键断裂,导致硝基官能团脱离,形成NO2分子。对α-CL-20 及其水合物在1000~3000 K 的分解研究发现,含水分子体系反应速率常数增大,水分子促进了CL-20 第二阶段的分解[10]。Wang 等[11]研究了2000~3500 K 下CL-20 热分解初始反应路径,发现温度不影响CL-20 的分解路径,随着温度升高,CL-20的分解速率增加并且笼状结构更早被破坏,温度会极大地提高H2O 和N2的生成速率。Ren 等[12]研究了800~3000 K 温度下CL-20 的热分解过程,同样发现CL-20 初始分解路径主要是N—NO2键断裂反应和C—N 键断裂引起的开环反应,高温下N—NO2键断裂反应显著增多,而C—N 键断裂开环反应随温度升高变化不大。Wang 等[13]采用ReaxFF-lg 力场研究不同压缩密度下ε-CL-20 超晶胞热分解,发现密度越大热分解反应释放的能量越小,反应速率越快,但反应活化能不随密度变化而改变。
含能材料中普遍存在杂质、空位、孔隙等缺陷,会降低黑索今(RDX)、奥克托今(HMX)等含能材料反应活化能,加快发生热分解,同时有助于热点的生成和演化,导致含能材料感度提高[14-16]。2000 年Kuklja等[14-15,17]研究了位错对RDX 热分解反应的影响,发现缺陷会激发其周围的电子,促进RDX 的N—NO2键的解离,从而促进RDX 发生分解。2003 年黄亨建等[18]采用急速重结晶方法研究发现晶体缺陷使HMX 热分解起始温度及相应表观活化能明显降低,热感度增加,热安定性降低。Zhou 等[16]发现分子空位缺陷会大大改变HMX 的N—NO2键断裂、HONO 离解以及分子主环断裂等分子内反应的频次,增大了HMX 的反应速率常数、降低了其反应活化能。含能晶体内部的微观缺陷将在外界能量作用下形成高温“热点”,使含能晶体对外界感度显著增大,从而对热稳定性产生较大影响。当前晶体缺陷对CL-20 热分解反应影响报道较少,有必要展开相关研究。
为探讨晶体缺陷对CL-20 热分解机理和反应动力学的影响,采用分子动力学方法和ReaxFF-lg 力场,研究在不同温度(1500~3500 K)下含空位缺陷CL-20 的热分解反应过程,获得了CL-20 势能的演变规律和反应动力学参数,分析不同高温下初始反应路径和产物演变,讨论了空位浓度对CL-20 热分解反应的影响,期望对CL-20 热分解研究提供参考。
2 计算方法
2.1 ReaxFF-lg 力场势函数
ReaxFF-lg 反应力场通过键级判定原子间距离,并用于描述化学键断裂和生成。当化学键断裂时,与价键相关的能量和力变为零,采用该反应力场计算得到系统的总能量为[19]:

式中,Elp、Eover、Eunder、Ebond为与化学键伸缩有关的势能项,Eval、Epen、Ecoa为与键角弯曲有关的势能项;Etors、Econj为与二面角扭转有关的势能项,EH-bond为氢键能、EvdW、ECoulomb为非价键作用力,最后是描述分子间长程作用的修正项,各项单位均为kJ·mol-1。
2.2 模型的构建
从剑桥数据库中获得ε-CL-20 单晶数据[20],将单胞沿a、b和c方向分别扩展4倍、3倍和3倍,构建4×3×3的ε-CL-20 超晶胞模型,包含36 个单胞,144 个CL-20 分子,共5184 个原子,记为CL-20 完美晶体。参考已报道含空位缺陷的HMX 模型[16,21-22],从CL-20 超晶胞中分别剪切移除2 行、4 行、6 行CL-20 分子,即8、16、24个分子,构建空位浓度分别为5.56%、11.2%、16.7%的CL-20 超晶胞模型,分别含有4896、4608、4320 个原子,如图1 所示,任意两组空位的距离较远,以消除空位间的相互作用。
2.3 分子动力学模拟
分子动力学计算均使用大规模原子分子并行模拟程序(Large-scale Atomic/Molecular Massively Parallel Simulator,LAMMPS)[23]和ReaxFF-lg 反应性力场。采用共轭梯度算法[24],根据麦克斯韦-玻尔兹曼分布[25]给原子分配初始速度。采用等温等压系综(isothermal-isobaric ensemble,NPT),在300 K 和一个大气压条件下驰豫10 ps 得到超晶胞的平衡结构。采用正则系综(canonical ensemble,NVT)和Berendsen控温方法[26],将弛豫后的体系分别在1500~3500 K 下进行分子动力学计算。整个计算过程采用周期性边界条件,时间步长为0.1 fs。采用C++语言自编程进行产物分析。
2.4 反应速率分析
采用Arrhenius 方程[27]描述分析含缺陷CL-20 晶体热分解动力学参数:

式中,t 为时间,ps;T 为温度,K;α 为反应进度;f(α)为反应模型;k(t)为与温度相关的反应速率常数,ps-1;A为指前因子,s-1;E 为反应活化能,kJ·mol-1;R 为理想气体常数,8.314 J·mol-1·K-1。
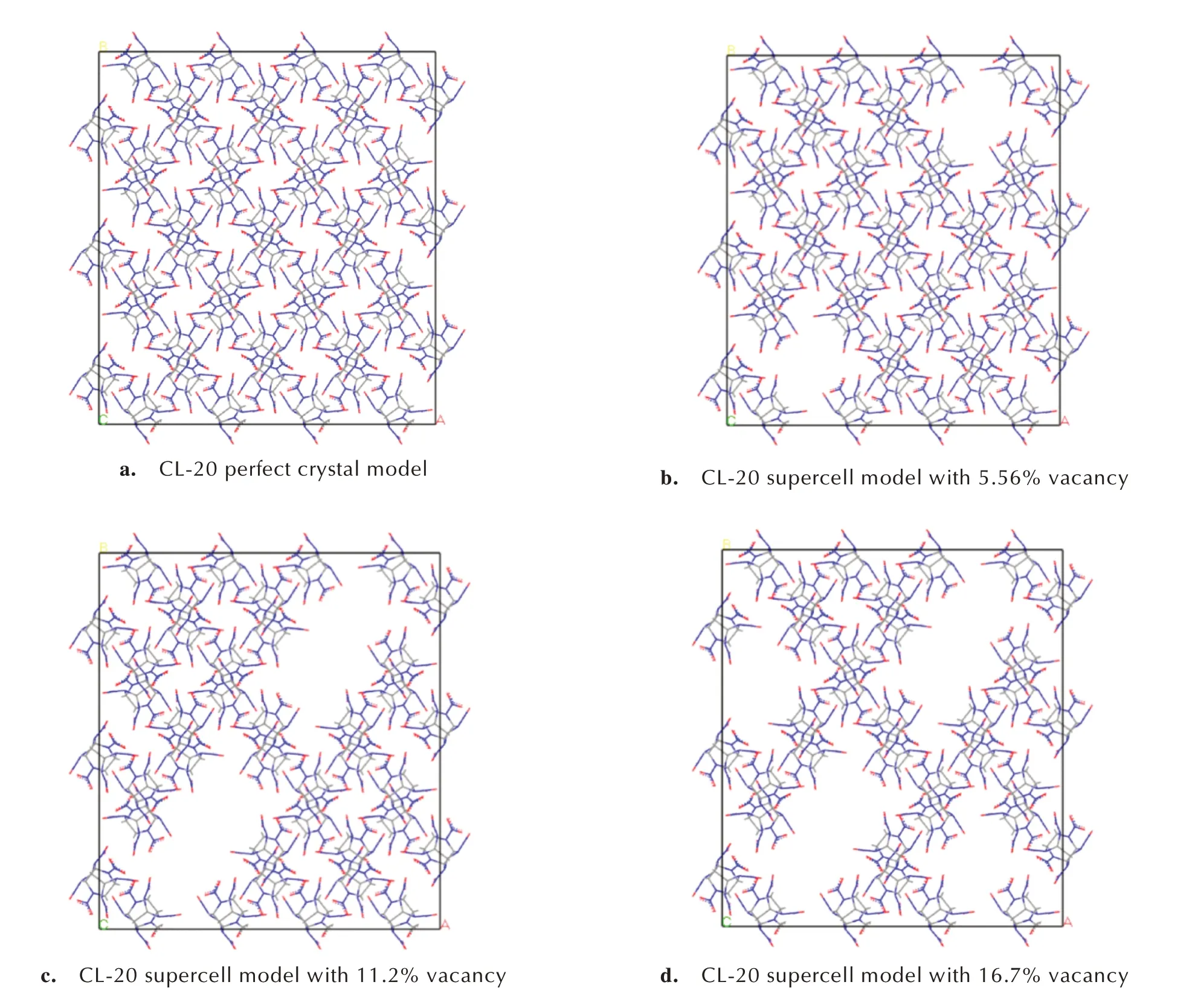
图1 CL-20 完美晶体和不同空位浓度CL-20 超晶胞模型Fig.1 CL-20 perfect crystal and its supercell models with different vacancy concentrations
根据Arrhenius 定律将反应速率常数与反应活化能联系起来:

根据Rom 等[21]提出的反应速率的分析方法,将不同温度下CL-20 的热分解过程分为吸热反应、放热反应和终态产物生成三个阶段进行分析。在吸热反应阶段,将CL-20 分子数量随时间的变化按照一阶衰减指数式进行拟合:
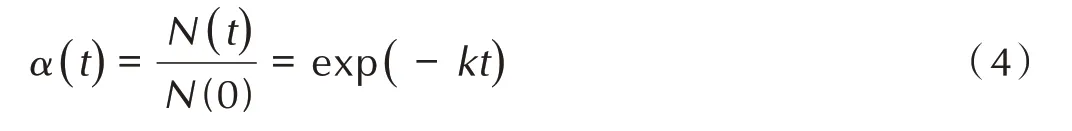
式中,t 为反应时间,ps;α(t)为t 时刻的反应进度;N(0)和N(t)分别是为初始时刻和t 时刻CL-20 的分子数量;k 为吸热阶段的反应速率,ps-1。将式(4)得到的反应速率常数k 代入式(3)并进行线性拟合,得到反应活化能E 和指前因子A。
3 结果与分析
3.1 空位缺陷对CL-20 热分解反应动力学的影响
考察1500~3500 K 下空位缺陷对CL-20 热分解反应速率常数、活化能和指前因子的影响,CL-20 完美晶体和缺陷模型反应速率常数见表1,反应速率常数的对数与温度的倒数关系见图2,线性拟合得到反应活化能E 和指前因子A 见表2。
已有研究表明CL-20 初始化学反应为N—NO2键的断裂,该反应遵循一级化学反应速率方程[10-11,28]。由图2 可见,在反应初始阶段,完美和空位缺陷模型ln(k)与1000/T 的关系符合一阶衰减指数规律。从表1 可见,在1500~3500 K 温度下,反应速率常数k 均随着空位浓度的增加而增大,这说明空位缺陷加速了CL-20 的初始化学反应速率。在相对较低温度(1500、2000 K)下,缺陷对反应速率的促进作用更加明显,其中1500 K 时含16.7%空位缺陷CL-20 反应速率常数是完美晶体的2 倍以上。

表1 不同温度下含空位缺陷CL-20 反应速率常数Table 1 Reaction rate constant of CL-20 with different vacancy concentrations at different temperatures

图2 含空位缺陷CL-20 热分解反应速率常数的对数与温度倒数的对数拟合关系Fig.2 The fitting curve between the logarithm of the thermal decomposition rate constant of CL-20 with vacancy defectsand the logarithm of the reciprocal temperature

表2 含空位缺陷CL-20 晶体热分解的反应动力学参数Table 2 Reaction kinetic parameters of thermal decomposition of CL-20 crystal with vacancy defects
由表2 可见,空位浓度越大,CL-20 热分解反应的活化能越低,其中含16.7%空位CL-20 的热分解活化能比完美晶体低11.80 kJ·mol-1,这表明空位降低了CL-20 热分解反应能垒,促进CL-20 发生分解。本研究得出的CL-20 完美晶体热分解的活化能,与Wang 等[11]的ReaxFF-lg 分子动力学计算和Isayev 等[8]的量化计算结果接近。许丽娟等[6]测定了CL-20 热分解的活化能,由于实验通常低于1000 ℃,且与外界有温度和压力交换,导致与模拟结果存在一定差异。空位缺陷的引入降低了CL-20 的热分解反应活化能,使CL-20 热分解速率显著增大,与含位错、空位RDX、HMX 热分解规律[14,16]类似。
3.2 含空位CL-20 势能和产物种类演化规律
1500~3500 K 热分解过程中CL-20 分子平均势能随时间变化曲线见图3,相对产物种类随时间的变化曲线见图4。为了消除CL-20 初始体系中分子数不同的影响,分别对各体系CL-20 分子数进行归一化处理。
由图3 可见,在各温度下,不同空位浓度下CL-20分子平均势能迅速升高后缓慢下降,表明初始分解反应以吸热反应开始,势能达到最大值后初始分解产物发生次级反应,体系的势能逐渐降低,与已报道CL-20势能变化规律一致[11-12]。温度显著影响CL-20 平均分子势能达到平衡的时间,在3000~3500 K 温度下势能曲线在40~60 ps 后平衡,1500~2500 K 时势能100 ps内分子势能未完全达到平衡,可见在100 ps 时间尺度内,反应温度为3000 K 及以上时含空位CL-20 充分反应,而3000 K 以下温度梯度未完全反应。选取势能变化趋势差异较大的两个温度(2000 K 和3000 K),进行热分解深入分析。对比CL-20 完美晶体可见,空位缺陷浓度越高,CL-20 势能降低速度越快,这说明空位缺陷降低了分解反应的能垒,促进了CL-20 的热分解,温度较低时势能差异更显著。
由图4a 可见,反应温度为2000 K 时,在20 ps 产物种类达到最大值,之后略有下降,说明反应还停留在中间产物阶段,没有大规模生成终态产物。100 ps 时含16.7%空位CL-20 分子平均产物种类约为1.5 个,而完美晶体只有1.2 个,这说明空位缺陷使CL-20 热分解产物种类增加,增大了晶体的破碎程度,促进了CL-20 热分解。由图4b 可见,反应温度为3000K 时,产物种类到达峰值在4.7 ps,相比于2000 K 产物种类增大;100 ps 时产物种类趋向平衡,CL-20 分子平均分解产物为0.8 个左右,这比2000 K 时产物种类减少。是因为3000 K 时CL-20 完美晶体和缺陷体系产物更接近于终态产物,反应比2000 K 时更加完全,因而物质种类更少,与Wang[11]对CL-20 完美晶体热分解研究结果一致。
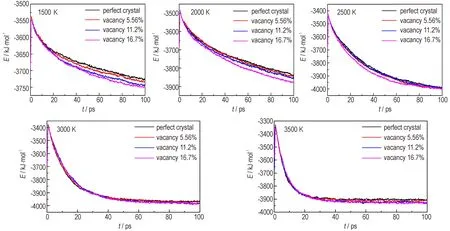
图3 1500~3500 K 时含空位缺陷CL-20 平均分子势能随时间变化曲线Fig.3 Curve of average molecular potential energy of vacancy defect CL-20 with time at 1500-3500 K
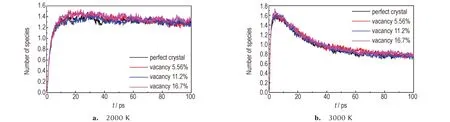
图4 含空位缺陷CL-20 分子产物种类随时间变化曲线Fig.4 Curves of products species of vacancy defect CL-20 with time
3.3 空位缺陷对CL-20 初始反应路径的影响
对含缺陷CL-20 初始化学反应进行统计分析,2000 K 和3000 K 时CL-20 发生初始化学反应时高频基元反应式、持续时间和反应频次见附表S1、S2,表4、图5~图7 是根据附表统计的结果。其中,表4 为统计出的CL-20 主要初始化学反应类型及其反应式,图5是CL-20 两种脱硝基反应示意图,图6 和图7 分别是2000 K 和3000 K 下CL-20 热分解反应类型分布图(扣除逆反应)。
由表4 可见,CL-20 初始化学反应主要有脱硝基反应(包括步步脱硝基和连续脱硝基两种类型反应)、CL-20 与小分子反应、CL-20 与大基团的反应。CL-20热分解初始化学反应主要是CL-20 分子环上发生N—NO2断裂、脱去一个硝基,其次发生其余硝基脱落或者主环的裂解反应,少部分CL-20 发生多重脱硝基反应。 随着硝基脱离CL-20 分子,生成NO2和C6H6N10O8、C6H6N9O6等中间体,会发生CL-20 与NO2、CL-20 以及中间体的反应,但后者发生频次不高。表S1 和表S2 的统计结果也表明,脱硝基反应是频次最高的热分解反应,CL-20 与小分子或大基团的反应频次很低,随着空位浓度增大,反应频次有一定提高。
由图5 可以看出,2000 K 时CL-20 初始分解反应主要为步步脱硝基反应,CL-20 依次脱去一个硝基分别生成化合物Ⅰ(C6H6N11O10)、化合物Ⅱ(C6H6N10O8)和化合物Ⅲ(C6H6N9O6)。这与Isayev 等[8]得到的单分子CL-20 分解路径相同。3000 K 时出现一定频次连续脱硝基反应,即CL-20 连续脱落两个硝基生成化合物Ⅱ,连续脱落三个硝基生成化合物Ⅲ。

表4 CL-20 初始化学反应类型及其主要反应Table 4 Initial chemical reaction types and main reactions of CL-20

图5 2000 K(a)和3000 K(b)时CL-20 分子脱硝基反应Fig 5 Denitration reaction of CL-20 at 2000 K(a)and 3000 K(b)
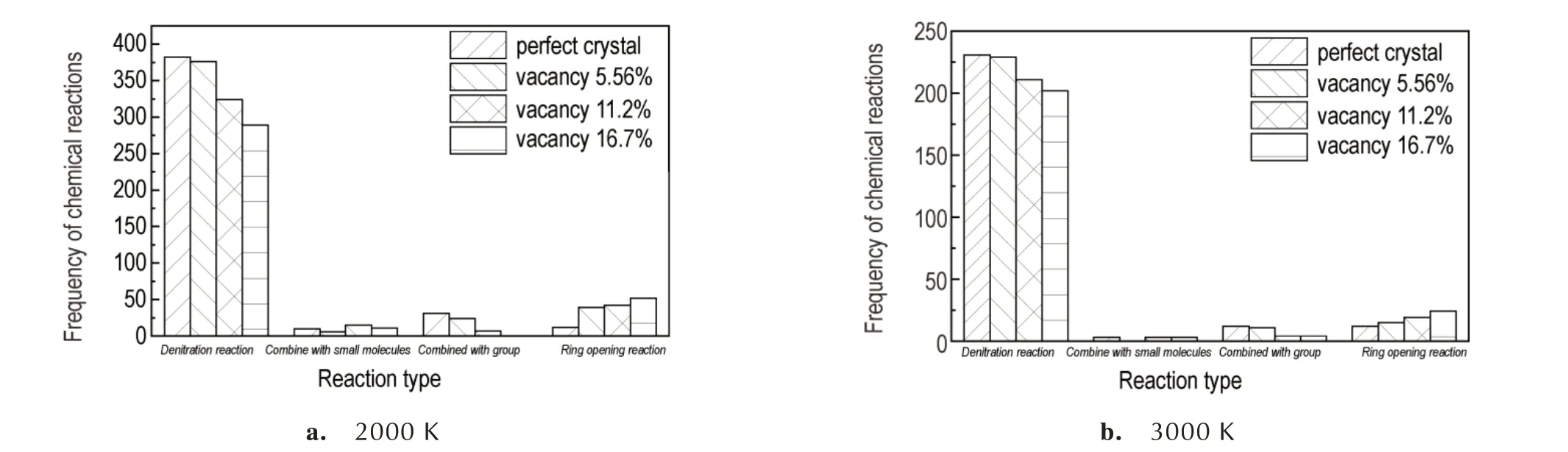
图6 含空位缺陷CL-20 热分解反应类型分布Fig.6 Thermal decomposition reaction distributions of CL-20 with vacancy defects
由图6 可以看出,空位缺陷对CL-20 各类反应频次产生显著影响。2000 K 和3000 K 下主要发生脱硝基反应,随着空位缺陷浓度增大,反应频次略有下降。另一种重要反应是CL-20 及较大中间产物的开环反应,反应频次随着空位浓度增大逐渐增加。说明空位缺陷加速了CL-20 体系的裂解,使CL-20 开环反应频次增加,促进了CL-20 分解反应。相比于2000 K,3000 K 下各类分解反应及其逆反应频次减少,CL-20热分解进程提前。
Zhou 等[16]研究表明,在高温下HMX 主要分解路径为N—NO2键断裂、HONO 离解以及分子主环断裂,空位缺陷促进N—N 键裂解和开环反应,但阻碍了HONO 的形成。本文结果表明空位的引入并不改变CL-20 主要初始反应路径,含空位CL-20 热分解仍以N—NO2键断为主,其他反应比例有一定增加。凝聚态含能材料热分解时,外界压力也会产生重大影响。文献[29-30]显示,硝基甲烷和HMX 在低压下的初始分解以分子内反应为主,而高压下以分子间反应为主。Wang 等[13]指出高压下CL-20 热分解以分子内反应为主,本研究表明常压下CL-20 完美晶体和缺陷模型仍主要发生分子内反应,高压下反应则需进一步研究。
3.4 空位缺陷对CL-20 小分子产物的影响
图7 和图8 分别是2000 K 和3000 K 时,完美和含空位CL-20 主要小分子产物含量随时间变化曲线。从分解产物变化可见,完美晶体和含空位CL-20 初始分解反应是N—NO2键的断裂生成NO2,这与文献报道一致[7-8]。
空位缺陷不会改变CL-20 主要初始热分解反应类型,但会对产物分布产生一定影响。如图7 所示,2000 K 时,完美CL-20 最主要的初始分解产物是NO2,次级反应消耗掉大量的NO2,生成N2、NO3等中间产物。其中NO3是仅次于NO2的产物,进一步分解生成N2、H2O 等终态产物,与Wang 等[11]、Ren 等[12]以及Isayev 等[8]的模拟结果基本一致。CL-20 分子骨架上C—N 键断裂,发生开环反应,主要小分子产物为CO2,该反应在CL-20 的热分解初期不占主导地位,20 ps 以后CO2数量剧增,说明骨架上C 原子在快速脱离,这与Xiang 等[31]的研究结果一致。随着CL-20 中缺陷浓度的增大,NO2峰值逐渐增大,其他小分子产物无显著变化。相比之下,如图8 所示,3000 K 时初始产物NO2峰值较2000 K 显著增大,由2 上升到2.5,N2、H2O、CO2、H2等终态产物含量增加,其中N2最大值由3 增加到4.5 左右、CO2最大值由0.5~1 增加到2.5 左右、H2O 最大值由1 增加到1.5 左右且提前达到平衡,中间产物NO3峰值急剧减小。相比于2000 K 时NO、N2O 等含量极少。说明在较高的温度下CL-20的分解程度更高,副产物也更少。该温度下空位缺陷未见明显影响,不同空位浓度CL-20 热分解小分子产物差异不显著。
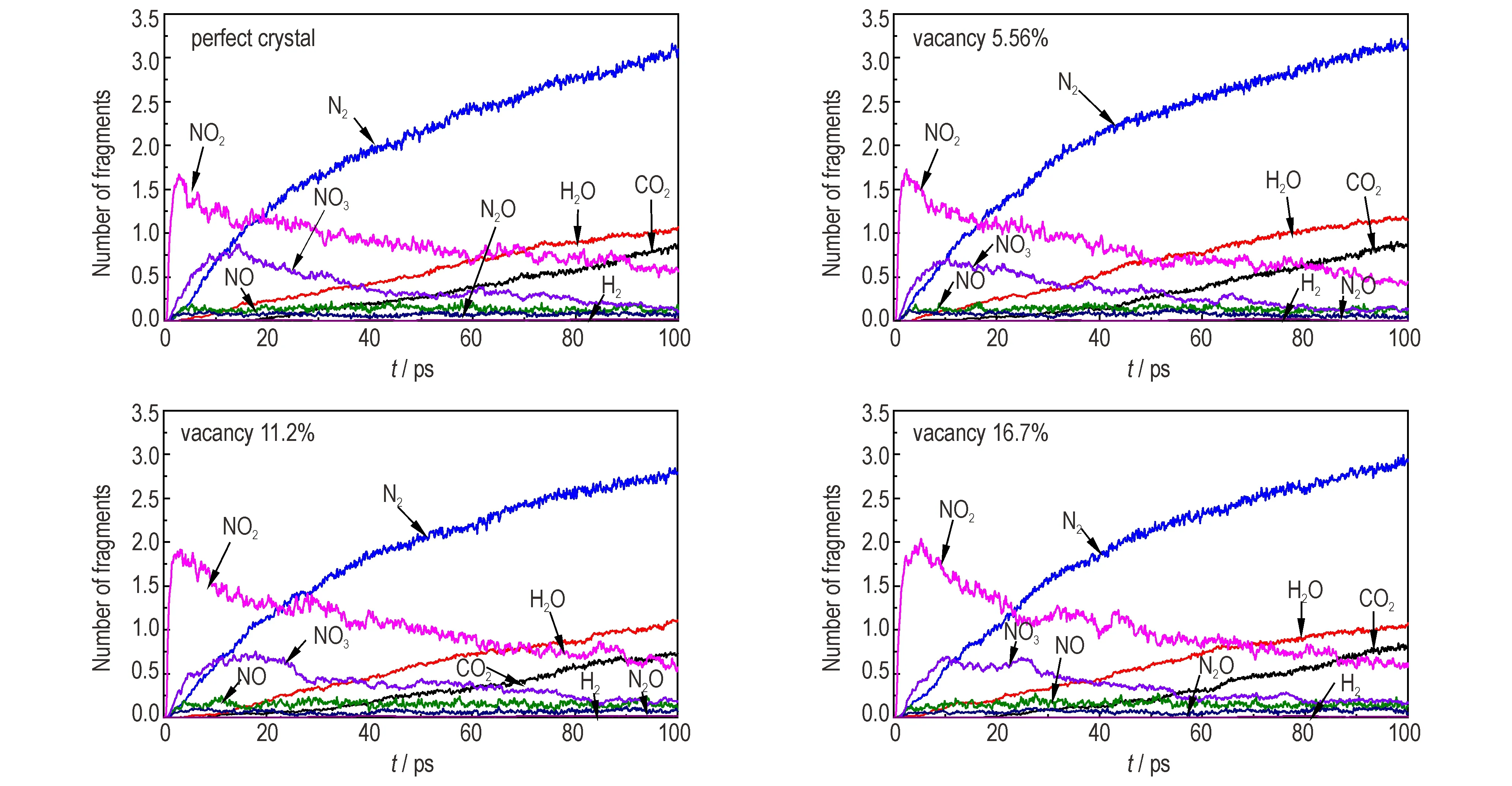
图7 2000 K 时含空位缺陷CL-20 分子主要分解产物相对含量随时间变化曲线Fig.7 Curve of relative content of the main decomposition products of vacancy defect CL-20 with time at 2000 K

图8 3000 K 时含空位缺陷CL-20 分子主要分解产物相对含量随时间变化曲线Fig.8 The curve of relative content of the main decomposition products of vacancy defect CL-20 with time at 3000 K
4 结论
采用ReaxFF-lg 力场和分子动力学方法,研究了1500~3500 K 下空位缺陷对CL-20 初始热分解反应、反应动力学和热分解产物的影响规律,得出以下结论:
(1)高温下CL-20 的初始化学反应以硝基脱落为主,引入空位缺陷后,脱硝基反应比例略有下降,开环反应比例增大,反应首先发生在空位缺陷周围,在CL-20 中可能形成热点。
(2)空位缺陷降低了CL-20 热分解活化能,增大了反应速率常数,温度升高和空位浓度的增加,都会使热分解反应加快。空位浓度越大对热分解促进作用越显著,且随着温度升高影响逐渐减小,2000 K 和3000 K时含16.7% 空位CL-20 反应速率常数分别是完美CL-20 的1.7 倍和1.4 倍,说明较低温度下空位缺陷的促进作用更为明显。
(3)高温下CL-20 主要发生分子内反应,当温度从2000 K 上升到3000 K 时,小分子产物NO2、N2、H2O、CO2等产物峰值显著增加,但中间产物NO3等的含量降幅较大。2000 K 时空位提升了NO2峰值,其他小分子产物无显著变化,3000 K 时空位对CL-20 热分解小分子产物影响不显著。
——《势能》

