卡博替尼与血清白蛋白的相互作用研究
王晓芳,孙 亮,王 雷,梁 栋,鄂诗瑀,徐诚炜,王家欢,刘 彬
(辽宁大学 药学院,辽宁 沈阳 110036)
0 引言
卡博替尼(CBZ)是一种小分子多靶点酪氨酸梅抑制剂,广谱抗肿瘤药,用于治疗甲状腺髓样癌、肾细胞癌、前列腺癌、晚期肝癌等疾病.但是,使用不当可引起出血、胃肠穿孔、高血压、血栓栓塞、腹泻、呕吐等不良反应[1].血清白蛋白是人与动物血浆中含量最丰富的蛋白质,它在生物体中起着血液缓冲剂、维持血液渗透压、载运等作用,药物吸收后最先会与其结合.因此,研究药物与血清白蛋白的相互作用,对于了解药物在生物体内的存在状态、运输、吸收、代谢及药理作用具有重要意义.而牛血清白蛋白(BSA)与人血清白蛋白有70%以上的同源性,因此BSA常被用来代替人血清白蛋白被选作模型蛋白[2].
1 实验部分
1.1 仪器与试剂
紫外-可见分光光度计(UV-2550型,日本岛津公司);荧光光谱仪(F-7000型,日本日立公司);CBZ(辽宁大学药学院药物化学研究室自制);BSA(上海麦克林生化科技有限公司);三羟甲基氨基甲烷(Tris:生化试剂,国药集团化学试剂有限公司);氯化钠(沈阳新化试剂厂);其他试剂均为市售分析纯,实验用水为双蒸水.
1.2 实验方法
首先,用pH=7.4的NaCl-Tris-HCl缓冲液配制实验中所需的各种溶液.室温下,在200~600 nm范围内,分别扫描浓度为1.0×10-5mol·L-1的CBZ溶液、BSA溶液和上述溶液等体积混合后生成的CBZ-BSA混合溶液紫外光谱.然后,采用荧光滴定法考察CBZ与BSA间相互作用.将不同体积1.0×10-3mol·L-1的CBZ溶液逐步滴加到装有2.5 mL 1.0×10-5mol·L-1BSA溶液的1 cm石英比色皿中(滴定剂累加体积不大于0.05 mL),每次加入CBZ溶液后混合均匀,静置5 min后,于278 nm激发波长下进行荧光扫描.发射与激发狭缝宽度均为5 nm,扫描波段范围200~800 nm,扫描速度1 200 nm·min-1.
2 结果与讨论
2.1 CBZ与BSA相互作用的紫外光谱

图1 BSA、CBZ及CBZ-BSA混合体系的紫外光谱1.CBZ;2.BSA;3.BSA+CBZ;4.CBZ-BSA混合溶液([BSA]=[CBZ]=1.0×10-5 mol·L-1)
有文献报道[3],动态淬灭只影响到荧光体分子的激发态,并不改变荧光体的吸收光谱;相反在静态淬灭中,基态配合物的生成往往会导致荧光体的吸收光谱的改变.图1为CBZ、BSA及CBZ-BSA体系的紫外吸收光谱图.
由图1可见,CBZ的加入不仅使BSA在278 nm处的吸收峰强度升高,而且CBZ-BSA复合体系的吸收光谱与单独CBZ和BSA吸收光谱的数学加和不一致(图中虚线),说明该现象的发生不是CBZ与BSA简单混合导致的,而是CBZ的确与BSA的基态分子发生了相互作用,形成了基态配合物,从而初步推断CBZ很可能使BSA发生静态淬灭[4].
2.2 CBZ与BSA相互作用的荧光光谱
BSA分子中含有色氨酸、酪氨酸和苯丙氨酸等内源性荧光的物质,因此荧光光谱经常用来研究药物与BSA分子之间的相互作用.由图2可见,随着CBZ浓度增大,BSA的最大发射荧光峰强度逐步降低,称为荧光淬灭,同时也表明CBZ与BSA之间存在相互作用.荧光淬灭过程一般分为静态淬灭和动态淬灭,通常可借助动态淬灭常数的大小及温度对淬灭过程的影响判断其淬灭类型.应用Stern-Volmer方程对CBZ引起BSA荧光淬灭的数据进行处理[5]:
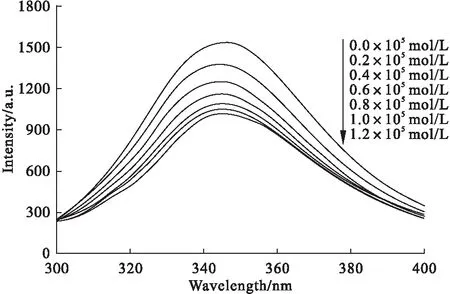
图2 CBZ与BSA相互作用的荧光光谱([BSA]=1.0×10-5 mol·L-1)
F0/F=1+KSV[Q]
(1)
其中,F和F0分别代表加入和不加CBZ时BSA的荧光强度,KSV为动态淬灭常数,[Q]为CBZ浓度.根据图2中343 nm处的荧光强度变化值,由式(1)作出BSA荧光淬灭的Stern-Volmer曲线,再根据直线斜率及截距可求出不同温度CBZ与BSA相互作用的KSV,5.2×104L·mol-1(293K);5.4×104L·mol-1(303K);5.7×104L·mol-1(310K).数值均在104数量级,说明CBZ对BSA有极强的淬灭作用.随着反应体系温度的升高,KSV略有升高,表明CBZ与BSA的激发态分子间发生相互作用,并且在相互碰撞过程中会发生能量转移或电子转移,从而引起BSA荧光发生动态淬灭.综上,CBZ与BSA间相互作用很可能是一个联合淬灭过程.一般讲,对于联合淬灭过程,可以用修正Stern-Volmer方程来验证[6].
F0/F=(1+KD[Q])(1+KS[Q])=1+(KD+KS)[Q]+KDKS[Q]2
(2)
式中KD为动态淬灭常数,KS静态淬灭常数,其它参数含义同公式(1),绘制修正Stern-Volmer曲线,见图3.如图所示,可看到三条微向下弯曲的曲线,进一步确证BSA的荧光淬灭机理为联合淬灭[6-7].
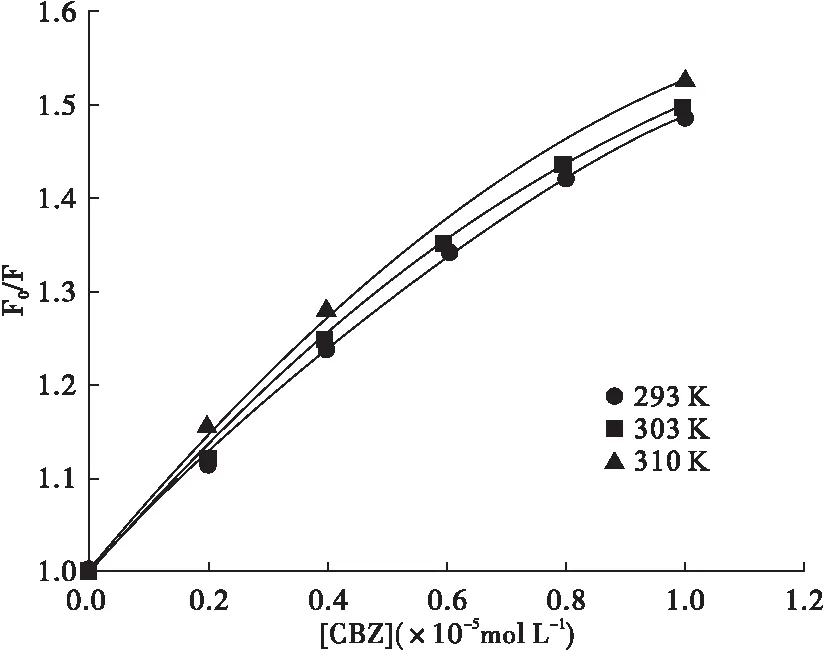
图3 修正的Stern-Volmer曲线
2.3 CBZ与BSA的相互作用模式
结合常数和结合位点数通常用来描述分子之间相互作用模式,该项参数可由公式(3)修正的双对数方程获得.
lg[(F0-F)/F]=nlgKa+nlg{[Q]-n[P](F0-F)/F0}
(3)
式中的[Q]、[P]分别为CBZ和BSA的总浓度,n为结合位点数,由式(3)作lg[(F0-F)/F]-lg[Q]图,可根据图中直线的斜率及截距计算不同温度下CBZ与BSA表观结合常数Ka和结合位点数n.计算结果为T=293 K,Ka=5.06×104L·mol-1,n=0.913 7;T=310 K,Ka=4.34×104L·mol-1,n=0.730 1,表明CBZ和BSA分子之间具有较强的相互作用,且形成1∶1形式的配合物.进一步,根据热力学公式(4)和(5)可以求得结合反应的热力学参数ΔG=-26.39 kJ mol-1、ΔH=0.945 kJ·mol-1、ΔS=92.28 J·mol-1·K-1.
lnKa=-ΔH/RT+ΔS/R
(4)
ΔG=-RTlnKa=ΔH-TΔS
(5)
ΔG<0表明CBZ与BSA的相互结合是自发的,同时,ΔH和ΔS均为正值,这表明CBZ与BSA之间的主要作用力是疏水作用[7].
3 结论
本研究借助紫外光谱法、荧光光谱法和热力学理论等手段,考察了CBZ与BSA之间的相互作用.结果发现,CBZ可以使BSA内源性荧光发生淬灭,其淬灭类型属于动、静态联合方式.此外,在CBZ分子与BSA间存在较大相互作用,且其主要依靠疏水作用力生成1∶1形式的配合物,该研究对于从分子水平上研究CBZ合理应用具有重要意义.

