不同浓度和给药频次的低浓度阿托品滴眼液控制儿童近视进展疗效比较
覃建 吕勇 魏丽 张俊杰 赵兵新 符爱存
1河南省人民医院眼科 河南省立眼科医院 河南省眼科研究所 郑州大学人民医院,郑州 450003;2郑州大学第一附属医院眼科 450052
近视是全球范围内严峻的公共卫生问题,预计2050年全球近视患病人口将达到47.58亿[1]。2018年全国近视调查数据显示我国儿童青少年总体近视率为53.6%,且呈现发病低龄化、重度化、进展快的趋势[2]。近视已是影响中国儿童青少年眼健康的主要原因,造成沉重的经济负担和社会问题,高度近视所致眼底病变也日益成为中国不可逆性致盲眼病的主要原因[3-4]。因此采取有效措施降低近视发病率、减缓其发展速度、预防相关并发症,已成为儿童眼保健工作的重要内容。循证医学证据支持的控制儿童近视进展的主要方式有不同浓度阿托品滴眼液、角膜塑形术、周边离焦框架眼镜或角膜接触镜、双光棱镜等[5-13]。新加坡、美国、中国等国家和地区不同浓度的阿托品滴眼液控制儿童近视进展的研究结果显示,阿托品滴眼液浓度越高,近视控制效果越好,但同时畏光、视近模糊等不良反应也更明显[5-10,14]。Chia等[5]观察不同浓度的阿托品滴眼液连续点眼2年后的停药反弹效应,结果显示0.01%组停药反弹率明显低于0.1%组和0.5%组。目前临床上多采用0.01%阿托品滴眼液控制儿童近视进展[14],但最新研究显示质量分数低于0.05%的阿托品滴眼液所产生的不适症状程度均在可接受范围内[8]。本课题组前期研究显示,0.02%阿托品滴眼液每日点眼1次控制儿童近视进展的效果优于0.01%阿托品滴眼液,且2种浓度的不良反应基本一致[15]。阿托品滴眼液用于控制儿童近视进展需要长期持续使用,用药依从性直接影响药物的疗效,目前临床上普遍采用每日1次的给药频次。研究显示,约有35%的近视儿童缺乏良好的阿托品用药依从性[16]。如果能降低阿托品使用频次,同时维持其疗效,将对临床用药指导产生积极意义。本研究比较0.02%阿托品滴眼液隔日点眼1次和0.01%阿托品滴眼液每日点眼1次对儿童近视的控制效果和不良反应的差异,以期为其临床应用提供参考。
1 资料与方法
1.1 一般资料
采用随机对照临床试验方法,纳入2016年6月至2017年6月在郑州大学第一附属医院和河南省立眼科医院就诊的汉族近视性屈光不正儿童231例,受试者均配戴近视全矫正单光框架眼镜。纳入标准:(1)年龄6~14岁;(2)双眼近视等效球镜度(spherical equivalent refraction,SER)为-0.75~-6.0 D,散光度<2.00 D;(3)最佳矫正视力(LogMAR)≦0.1;(4)双眼SER差值<1.00 D;(5)眼压为10~21 mmHg(1 mmHg=0.133 kPa)。排除标准:(1)对阿托品滴眼液有变态反应或不耐受者;(2)曾因防控近视长期使用过低浓度阿托品滴眼液、硬性透气角膜接触镜或角膜塑形镜者;(3)无法保证定期随访者;(4)有其他眼病、眼部手术史和外伤史者;(5)有其他全身系统性疾病者。采用随机数表法将受试者随机分为0.02%阿托品组110例和0.01%阿托品组121例。研究过程中0.02%阿托品组舍弃18例,占16.4%,其中6例失访,7例因担心不良反应自行停药,4例未按时复查,1例因畏光不适自行停药,最终92例完成1年随访。0.01%阿托品组舍弃20例,占16.5%,其中9例失访,7例因担心副作用自行停药,2例未按时复查,2例因畏光不适自行停药,最终101例完成1年随访。所有受试者均取右眼数据纳入分析。2个组受试者的基线资料比较差异均无统计学意义(均P>0.05)(表1)。本研究遵循《赫尔辛基宣言》,经郑州大学第一附属医院伦理委员会批准(批文号:2016-35),并在国家临床试验注册中心注册(注册号码:ChiCTR-IPD-16008844)。所有受试者及其监护人均了解研究目的并签署知情同意书。
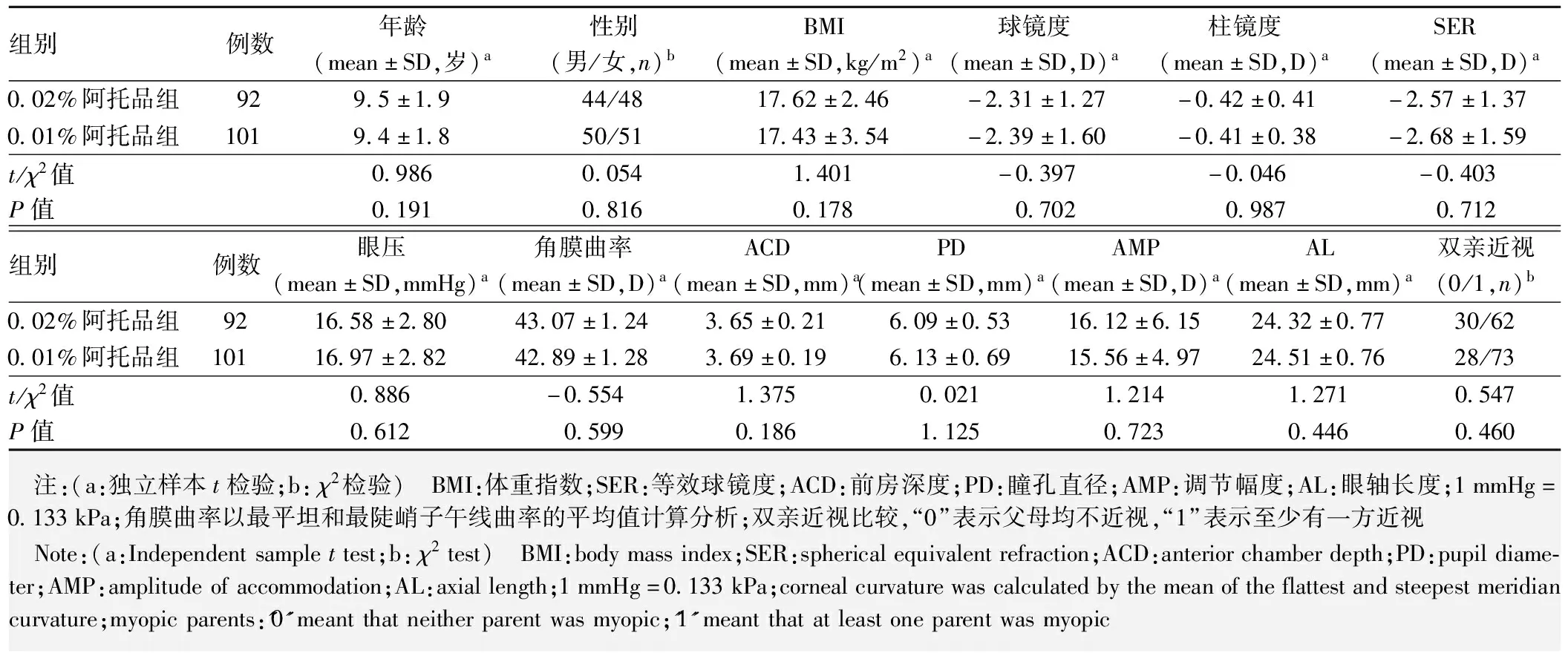
表1 0.02%阿托品组和0.01%阿托品组干预前基线特征比较
1.2 方法
1.2.1试验药物配制 不同质量分数的阿托品滴眼液由河南省立眼科医院药物研究室专业药师配制。将硫酸阿托品粉末置于超净工作台,用生理盐水将硫酸阿托品配制成0.01%和0.02%阿托品滴眼液,调节pH值为5.4~5.6,添加羟苯乙酯防腐剂,装入3 ml滴眼液瓶中,于15~25 ℃避光保存,开瓶后1个月丢弃。
1.2.2受试者用药前眼科检查 采用IOL-Master 500(德国Carl Zeiss公司)测量眼轴长度(axial length,AL)、前房深度(anterior chamber depth,ACD)、角膜曲率。采用AR-1电脑验光仪(日本NIDEK公司)测量瞳孔直径(pupil diameter,PD),测量时受试者完全放松,裸眼状态下室内适应5 min,受检眼平面的光照度值在300~310 lx;采用TX-10非接触眼压计(日本Canon公司)测量眼压;采用移近法测量单眼调节幅度(amplitude of accommodation,AMP)。采用复方托吡卡胺滴眼液每10 min点眼1次,共4次,麻痹睫状肌40 min后,采用AR-1自动电脑验光仪进行客观验光,再行检影验光和主觉验光,遵循最佳视力的最高正镜原则获得球镜度和柱镜度,计算SER=球镜+柱镜/2。以上检查均由同一固定的相应技术人员完成。
1.2.3不同质量分数阿托品滴眼液用药方法 所有滴眼液由同一位不参与辅助检查的药师保管和发放。受试者由监护人领取滴眼液。0.02%阿托品组采用隔日点眼方案,0.01%阿托品组采用每日点眼方案。2个组均为晚上睡前双眼点眼1次,1滴/次,共持续点眼1年。
1.2.4评价指标及随访 分别于用药1、4、8、12个月复查,观察指标包括视力、眼压、PD、AMP、SER和AL。SER、AL、PD和AMP的变化量为用药后1年与用药前数值的差值。所有随访检查均在上午进行。每次复查后发放新配制的供下一阶段使用的滴眼液。
1.2.5不良反应观察和评估 在签署知情同意书时,向受试儿童及其监护人详细解释可能出现的局部或全身不良反应,并告知应对措施。每次随访时以问卷调查表的形式询问受试者(监护人协助)自上一次复查期间总的不良反应情况并记录。眼部不良反应问卷调查表包括以下3个方面:(1)有无畏光(从不、偶尔、经常、总是)及哪种情况下畏光(无、室内正常光、日常户外光、明亮太阳光)和持续时间;(2)有无视近阅读模糊(从不、偶尔、经常、总是)及严重程度(无、轻度、中度、重度)及持续时间;(3)有无眼痒、眼胀或其他不适(从不、偶尔、经常、总是)及严重程度(无、轻度、中度、重度)和持续时间。全身不良反应观察内容包括有无心动过速、口鼻咽喉干燥、发热、面部潮红等。
1.3 统计学方法
采用易侕统计软件(http://www.empowerstats.com)进行统计分析。计量资料经Kolmogorov-Smirnov检验证实呈正态分布,以mean±SD表示。2个组受试者用药前后不同时间点SER和AL等参数差异比较采用重复测量两因素方差分析,组间多重比较采用LSD-t检验。计数资料用百分比表示,2个组间性别构成、双亲近视率差异比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 2个组受试者用药前后SER变化比较
用药前后SER总体比较差异有统计学意义(F时间=252.125,P<0.001),各组用药1年SER均高于用药前,差异均有统计学意义(均P<0.05),0.02%阿托品组和0.01%阿托品组SER变化量分别为(-0.46±0.49)D和(-0.48±0.46)D,差异无统计学意义(t=-0.875,P=0.383)(表2)。
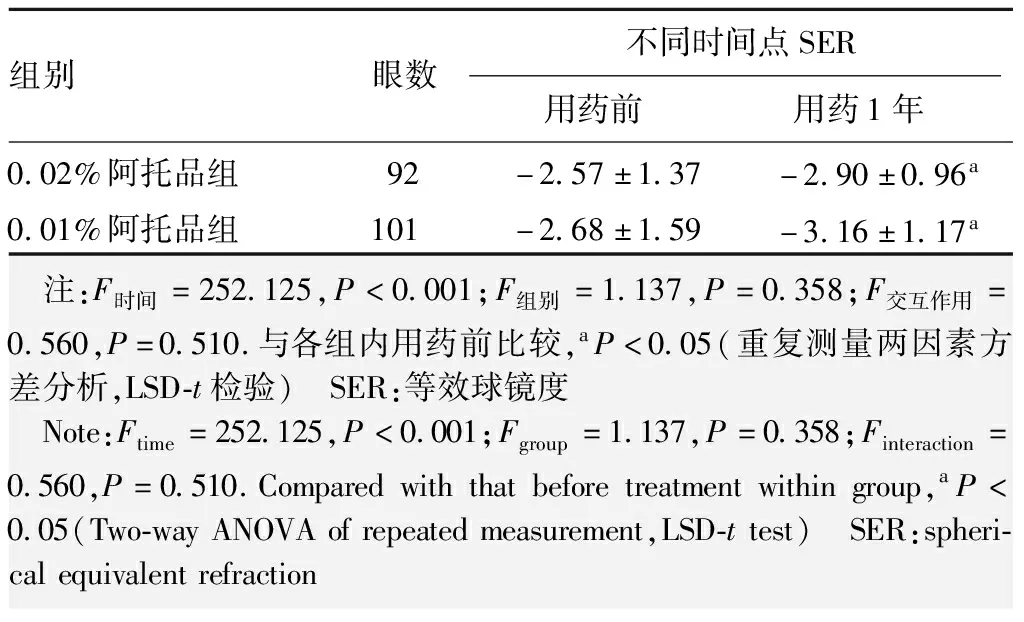
表2 0.02%阿托品组和0.01%阿托品组用药前后SER比较(mean±SD,D)
2.2 2个组受试者用药前后AL变化比较
用药前后AL总体比较差异有统计学意义(F时间=630.173,P<0.001),2个组用药后AL均较用药前增长,差异均有统计学意义(均P<0.05),0.02%阿托品组和0.01%阿托品组AL变化量分别为(0.38±0.21)mm和(0.39±0.19)mm,差异无统计学意义(t=-1.472,P=0.143)(表3)。

表3 0.02%阿托品组和0.01%阿托品组用药前后AL比较(mean±SD,mm)
2.3 2个组受试者用药前后眼压、ACD、AMP及PD比较
0.02%阿托品组与0.01%阿托品组用药前后眼压及ACD总体比较,差异均无统计学意义(均P>0.05)(表4)。用药前后AMP和PD比较,差异均有统计学意义(AMP:F时间=9.898,P=0.007;PD:F时间=312.573,P<0.001),各组用药1年AMP均较用药前下降,PD均较用药前扩大,差异均有统计学意义(均P<0.05);各组间AMP和PD比较,差异均无统计学意义(AMP:F组别=0.634,P=0.472;PD:F组别=3.431,P=0.088)(表5,6)。0.02%阿托品组与0.01%阿托品组AMP变化量分别为(-1.49±0.29)D和(-1.61±0.26)D;PD变化量分别为(0.72±0.44)mm和(0.70±0.40)mm,差异均无统计学意义(均P>0.05)。
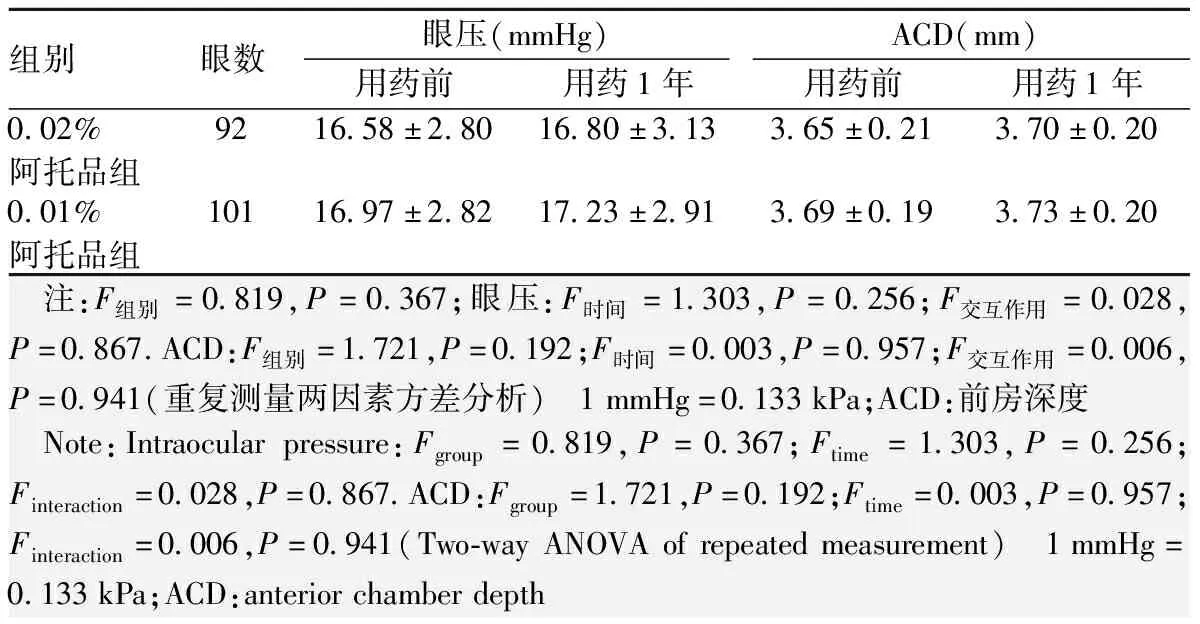
表4 0.02%阿托品组和0.01%阿托品组用药前后眼压及ACD比较(mean±SD)

表5 0.02%阿托品组和0.01%阿托品组用药后1年AMP比较(mean±SD,D)
2.4 各组用药后相关不良反应
用药后1个月,0.02%阿托品组和0.01%阿托品组分别有19.1%(21/110)和20.7%(25/121)的患眼表现出畏强光,但在室内正常光和日常户外光下无不适,在户外活动时配戴太阳镜或遮阳帽均能缓解。0.02%阿托品组在用药后1、4、5个月分别有7、4和1眼畏光症状消失;0.01%阿托品组在用药后1、4、6个月分别有4、6和3眼畏强光症状消失;其余患眼畏强光症状在后续随访过程中稍有缓解,但并未完全消失。在用药后1个月的随访过程中无新的受试者出现畏光症状。0.02%阿托品组和0.01%阿托品组患眼在用药1个月内分别有4.5%(5/110)和5.0%(6/121)的患眼出现轻度的视近阅读模糊,持续2~4周后症状逐渐消失。0.01%阿托品组中1例受试者在用药后1个月出现轻微变态反应,表现为晨起眼痒、眼肿,停药后2 d自行消失。无受试者出现其他眼部及全身不适症状。

表6 0.02%阿托品组和0.01%阿托品组用药前后PD比较(mean±SD,mm)
3 讨论
阿托品为非选择性毒蕈碱受体拮抗剂,是控制近视进展的有效药物[12]。研究认为阿托品主要通过作用于视网膜、脉络膜上的M1和M4受体来减缓眼球的生长速度从而抑制近视增长[17]。阿托品滴眼液控制近视进展的疗效和不良反应与其浓度有关[5,8,18-19]。Chia等[20]使用不同质量分数的阿托品滴眼液每日点眼,随访5年结果显示,0.5%、0.1%和0.01%阿托品用药组受试者SER分别进展-1.98、-1.83和-1.38 D,而安慰剂对照组(ATOM1[6])近视受试者在2.5年时SER已经进展达-1.40 D;其研究显示0.01%阿托品滴眼液控制近视进展的效果最佳,停药反弹效应和不良反应最弱,由此奠定了0.01%阿托品滴眼液每日1次控制近视进展的临床基础。Yam等[8]和Fang等[9]研究显示,0.025%阿托品滴眼液每日点眼1次能显著减缓近视进展和AL增长。Cooper等[19]观察12例年龄8~16岁SER为+0.75~+1.75 D的儿童使用0.012%、0.025%和0.05%阿托品滴眼液的不良反应,以用药后AMP不低于5 D、瞳孔扩张小于3 mm、仅出现轻微视近模糊和畏光为可接受的舒适度判断标准,发现阿托品滴眼液适宜浓度为0.012%~0.025%,推测0.02%阿托品滴眼液是不引起明显调节麻痹和瞳孔扩大的最高浓度。本课题组前期的研究发现,0.02%阿托品滴眼液每日点眼1次,SER进展速度为-0.44 D/年,AL增长速度为0.35 mm/年[15]。综合各方面的研究成果,本研究观察0.02%阿托品滴眼液改变给药频次后的临床疗效和不良反应。
本研究结果显示,0.02%阿托品组和0.01%阿托品组1年SER分别平均进展-0.46 D和-0.48 D,AL分别增加0.38 mm和0.39 mm,2个组控制儿童近视进展的效果一致;与ATOM2[5]研究中0.01%阿托品滴眼液每日点眼1次,SER每年进展-0.43 D、AL每年增加0.24 mm的结果较为接近;明显低于本课题组前期与本研究基线数据匹配的仅配戴单光框架眼镜近视儿童SER进展程度(-0.70 D/年)和AL增加量(0.62 mm/年)[10];同时也低于中国台湾地区[21]和新加坡[22]配戴框架眼镜近视儿童的SER进展程度(-0.93 D/年和-0.76 D/年)。Clark等[7]对美国6~15岁近视儿童进行研究发现,0.01%阿托品滴眼液每日点眼1次的近视儿童每年SER平均进展-0.10 D,与本研究存在较大差异。分析差异较大的原因可能为其主要采用非睫状肌麻痹验光,屈光度测量可能存在误差;同时纳入样本量较小,仅28例,且71%(20/28)为非亚裔人群;纳入儿童的SER范围为-0.25~-0.75 D,用药后部分儿童产生“远视漂移”[9,23]。本研究结果显示,0.02%阿托品滴眼液隔日点眼1次与0.01%阿托品滴眼液每日点眼1次控制儿童近视进展的效果和不良反应一致,但0.02%阿托品组的用药次数减少了一半。
给药时间和频次是影响患者依从性的重要因素[24]。李维娜等[25]对青光眼患者的研究显示,简化用药方案,减少点药频次,能有效提高患者的依从性。在保证有效治疗效果,同时不引起更多不良反应的前提下,本研究尝试性探索了0.02%阿托品滴眼液隔日点眼1次的用药方式,具有积极的临床意义。
低浓度阿托品滴眼液的眼部不良反应主要是对虹膜括约肌和睫状肌的麻痹作用所致的PD增大和AMP降低,表现为畏光、视近困难等,偶尔可能出现眼部变态反应和其他刺激症状,不良反应的发生率和严重程度呈剂量依赖性[5,8,26]。LAMP研究显示0.05%阿托品滴眼液不良反应发生率与0.01%阿托品滴眼液无明显差异,且AMP、PD仅在用药早期变化明显,后期趋于稳定[8]。钟梅等[27]对近视儿童分别采用0.02%和0.01%阿托品滴眼液每日点眼1次,2个组AMP在用药4个月时略下降,8个月和12个月时呈轻微回升趋势,但仍低于初始状态;PD在用药4个月时增大,之后保持稳定,2个组不良反应的发生率一致。本研究2个组复查时间均是阿托品滴眼液点眼的次日上午,以了解不良反应的最大程度,2个组受试者用药后1年AMP和PD的变化趋势基本一致且程度较轻。由于AMP和PD变化引起的眼部不适症状在用药初期(1个月内)即表现出来。2个组出现畏光症状的比例接近,仅在户外明亮的阳光下畏光,通过配戴太阳镜或遮阳帽均能有效缓解。随着用药时间延长,部分患者畏光症状消失,其余患者畏光症状均不同程度缓解。推测是由于后期PD趋向稳定,机体对药物的耐受和自身代偿机制[28]而表现出症状减轻。本研究中2个组分别有4.5%和5.0%的受试者出现持续时间不超过1个月的轻度视近阅读模糊,均能自然缓解,提示研究所用的低浓度阿托品滴眼液不会对受试者的生活和学习造成显著影响。
本研究结果显示,0.02%阿托品滴眼液隔日1次和0.01%阿托品滴眼液每日1次的干预方式对于中国大陆近视儿童近视进展控制方面能达到基本一致的效果,长期使用均未发生明显不良反应。当前仍缺乏在眼部的药理学试验证据指导下的用药剂量和频次个性化的循证依据,本研究能为临床实践中根据儿童和家庭情况个性化选择有效的药物浓度和相对应给药频次提供科学参考。
利益冲突所有作者均声明不存在利益冲突
志谢感谢河南省人民医院 河南省眼科研究所明帅老师为本文提供部分统计学指导

