基于变化观念与平衡思想核心素养下的数字化实验教学设计
吕旭东

摘要:以数字化实验为手段,温度为变量,在敞开体系与封闭体系中,探究碳酸氢钠溶液pH的变化规律。从“变化观念与平衡思想”的视角,帮助学生深度学习电离、水解等知识,以提升学生化学学科核心素养。
关键词:变化观念与平衡思想;数字化实验;碳酸氢钠溶液;实验探究
文章编号:1008-0546(2021)02-0089-04 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.02.022
近年来,随着课程改革的力度不断加大和认知水平的逐步提高,学生核心素养的培育成为教育工作者研究的热点。“变化观念与平衡思想”作为化学学科核心素养的五个维度之一,具有典型的学科特征和思维特征,在培育的过程中教师不仅应立足于知识性的教学,更应注重学生在学习过程中的能力培养、观念建构和思维提升。同时要求学生能在微观角度认识物质,动态方式分析变化和理论层面揭示本质,逐步形成化学学科的思想和方法。
以培养学生核心素养为本,笔者设计了“探究温度对碳酸氢钠溶液pH的影响”一节数字化实验探究课,参加了2019年11月7日在芜湖举行的安徽省高中化学优质课评选活动,并获一等奖。对课堂中如何培育学生“变化观念与平衡思想”核心素养进行了探索和反思。
一、教学内容和学情分析
1.教学内容分析
人教版选修4《化学反应原理》第三章介绍了“水溶液中的离子平衡”,其主要内容包括弱电解质的电离平衡、盐类的水解平衡和难溶电解质的溶解平衡。从内容特点来看,该章知识比较抽象、理论性强,难度较大;从功能地位来看,它承接了第二章化学平衡的相关知识,同时又为下一章的电化学学习奠定了基础,更是学生形成微粒观、平衡观和变化观的核心章节。基于此,本课例将利用传统实验和数字实验相结合的手段,重构教学内容,引导学生进行探究式学习,旨在巩固和提升第三章的内容,落实“变化观念与平衡思想”核心素养。
2.学情分析
学生已经学习了水溶液中的离子平衡相关知识,对电离平衡、水解平衡、溶解平衡的建立和平衡移动有了一定的认识,学生也能熟练地掌握化学平衡常数相关的定量计算,但在处理实际问题时,对微观粒子在水溶液中的变化规律还缺乏较为全面的理解。特别在深度学习水溶液中的离子平衡方面,学生由于缺乏综合分析问题的能力,处理复杂问题时,常常举手无措,不知如何应对。
二、教学流程
基于以上学情,教师精心设置情境,鼓励学生提出问题,师生共同设计实验方案并开展探究,在活动中形成知识,达成学科核心素养。教学流程如图1所示。
三、教学过程分析
1.复习旧知,导入新课
[教师]回顾必修一教材中有关碳酸氢钠固体的相关性质,投放到大屏幕(见表1)。
[学生]观看投影,回忆知识
设计意图:通过回忆碳酸氢钠固体的性质,创设情境,明确思维方向,为探究碳酸氢钠溶液是否分解做好铺垫。
[教师]设问:碳酸氢钠溶液会分解吗?如果分解,在什么温度下分解呢?
2.查阅资料,提出质疑
[教师]查阅资料:碳酸氢钠水溶液呈极弱碱性,在50℃开始分解放出CO2。常温下,NaHCO3溶液会分解吗?如果分解,有哪些方法可以证明呢?
[学生]小组讨论,设计方案(见表2)。
设计意图:激励学生敢于质疑,勇于探索的科学态度。引导学生从基于物质特性的角度设计实验方案,培养证据意识和宏观辨识的能力。
3.设计实验,合作探究
探究1:常温下,饱和NaHCO3溶液是否分解
[学生]根据表2设计的方案,组装实验装置,分组同时进行实验。
[实驗一]气球套在盛有饱和NaHCO3溶液的锥形瓶口,用磁力搅拌器不断搅拌,如图2所示。
[实验二]用二氧化碳传感器测封闭体系中饱和NaHCO3溶液上方CO2的含量,如图3所示。
[实验三]常温下,利用pH传感器测敞开体系饱和NaHC03溶液的pH变化,如图4所示。
[学生]各组汇报实验现象。
实验一:短时间无明显现象,一段时间后气球鼓胀,如图2;
实验二:CO2的含量不断增大,一段时间后保持不变,如图5;
实验三:溶液的pH不断增大,如图6。
实验收获:常温下,饱和NaHCO3溶液就可以发生分解,打破了部分老师和学生原有的认知一NaHCO3溶液不易分解。
设计意图:学生自主实验探究,激发了学习化学的兴趣,在实践的过程中获取了最直接的经验,学会合作、交流和表达。传统实验和数字化实验同时进行,充分体现了数字化实验在探究微观变化方面的优势。
探究2:常温下,封闭体系中饱和NaHCO3溶液的pH变化
[教师]设问:常温下,在封闭体系中饱和NaHCO3溶液的pH将如何变化?
[学生]根据探究1中的图5和图6实验曲线进行预测。
[实验四]常温下,用磁力加热搅拌器不断搅拌饱和NaHCO3溶液,利用传感器测封闭体系中溶液的pH变化,实验曲线如图7所示。
实验结果:常温下,敞开体系中饱和NaHCO3溶液的pH不断缓慢增大;封闭体系中溶液pH先增大,一段时间后保持不变。
[学生]主动提出问题:溶液pH的变化是否和液面上方CO2的含量存在关系呢?
[实验五]常温下,用磁力加热搅拌器对盛有饱和NaHCO3溶液的三口烧瓶进行搅拌,同时用传感器测封闭条件下溶面上方CO2的含量和溶液pH的变化,如图8所示。
实验收获:NaHCO3溶液分解为可逆反应,随着液面上方CO2含量的增大,会抑制NaHCO3溶液的分解。建议碳酸氢钠溶液最好密封保存。
设计意图:本环节从学生现有的认知水平出发,精心设置问题,并鼓励学生自己提出问题,由浅入深,层层递进。学生先预测实验现象,再进行实验探究,最后通过对比数字化实验曲线,得出实验结论,提升了实验求证,推理论证的能力。
探究3:升温下,敞开体系饱和NaHCO3溶液的pH变化情况
[教师]以上研究了常温下饱和NaHCO3溶液的pH变化情况,如果升温,溶液pH将如何变化呢?
[学生]各小组讨论后猜想:溶液pH增大,或减小,或不变。
[实验六]用磁力加热搅拌器加热并搅拌烧杯中的饱和NaHCO3溶液,同时利用传感器测溶液的温度和pH的变化,实验结果如图9所示。
注:受pH传感器适用条件的限制,温度升高到约80℃开始降温。
[学生]分析图9得出pH变化特点:升温过程中,溶液的pH先基本不变(略有降低),后增大明显;降温过程中,pH仍缓慢增大。
[师生]把曲线分成a、b、c三段进行分析(见表3)。
分析原因:a段温度升高,NaHCO3溶液分解导致溶液碱性增强,即c(OH-)增大,但同时溶剂水的电离程度也增大,Kw增大,由于两者增大的幅度相近,故pH基本不变.b段因为在该温度范围内,NaHCO3溶液分解产生的CO2迅速逸出,加速了分解反应的平衡正向移动;c段在降温的过程中,NaHCO3溶液持续的分解,所以pH仍缓慢增大。
实验收获:升温过程中,体系中不仅仅是HCO3-简单的发生电离和水解变化,同时溶剂水以及液相和气相之间都出现了平衡的移动,溶液pH的变化是综合作用的结果。
设计意图:分析加热饱和碳酸氢钠溶液pH的变化情况,增强了学生归纳整理数据的能力,有助于提升学生思维的有序性、系统性。由于体系中存在多种平衡相互影响,增加了问题的复杂性,学生需要从微观粒子的相互作用视角分析物质的电离、水解和分解,从而增强了变化的观念。
4.微观分析,深度思考
[教师]反应①产生的H+和反应②产生的OH-相结合生成水,从而进一步促进了HCO3-的电离和水解。因此,反应⑤实质上是HCO3-的电离和水解共同作用的结果。反应⑤的平衡常数远大于HCO3-的电离和水解常数,当外界条件(如压强、温度)发生变化时,用反应⑤解释溶液pH的变化更令人信服。
设计意图:要求学生写出体系中存在的平衡反应式,以符号和数据进行表征,由定性到定量,提升了学生分析问题,解决问题的能力,实现了高阶思维的发展。
四、课后反思
1.在探究碳酸氫钠溶液pH的变化时,采用了数字化实验。与传统实验相比,数字化实验呈现出来的实时的、动态的、可视化的曲线充分激发了学生实验探究的兴趣和学习的热情,课堂上,教师只是引导者和组织者,让学生真正成为了探究活动中的践行者和体验者。另外,数字化实验由于操作简便、快速,并可精确测查数据和处理数据,所以提高了实验探究的效率,保证了课堂内容的完整性及实验数据的可靠性。2017年版课程标准提出了“注重发挥现代信息技术的作用,积极探索现代信息技术与化学实验的深度融合”。随着课程改革的不断深入,数字化实验在中学化学日常教学中将会有更广泛的应用。
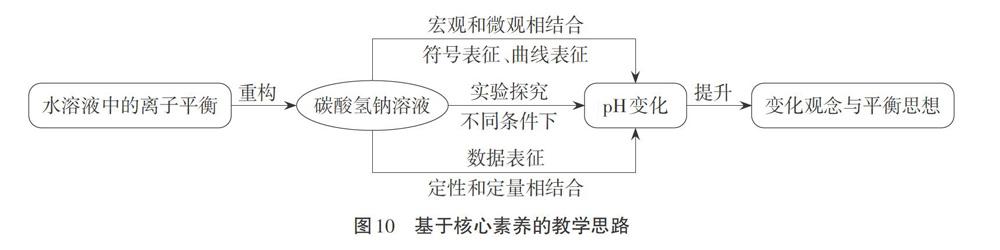
2.本节课的教学以碳酸氢钠溶液为载体,以实验探究为手段,深度学习水溶液中的离子平衡,以提升学生“变化观念与平衡思想”核心素养(具体见图10)。在整个教学过程中,融合了符号表征、曲线表征和数据表征等多重表征,引导学生由宏观到微观、由定性到定量、由变化到平衡的认识过程,实现了知识、能力和素养的协同发展。
3.基于核心素养培育为目标的课堂教学,应是一个主动协作的课堂、一个高效运转的课堂、一个具有探究精神的课堂,在活动中不断实现知识的内化和观念的形成。当然,学生核心素养的培育并非一朝一夕就能实现的,需要教师紧跟教育改革的步伐,及时更新教育教学理念,认真研读教材甚至创造性地使用教材,在日常教学中不断促进和强化。

