小针刀预防骨质疏松性椎体压缩性骨折椎体成形术后残余痛临床观察
张芬,王怀泽,孙奎,刘德春,宋阳春
安徽中医药大学第二附属医院,安徽省中医药科学院针灸临床研究所 安徽合肥 230061
随着老龄化社会的来临,骨质疏松性椎体压缩骨 折(Osteoporotic Vertebral Compression Fractures,OVCF)的发病率逐年升高。传统的保守治疗,患者长期卧床会加剧骨质疏松,并且容易并发褥疮、肺部感染及下肢深静脉血栓等相关并发症。目前针对OVCF骨折的治疗主要指为经皮椎体成形术(PVP)或经皮椎体后凸成形术(PKP)[1-3],该手术创伤小,效果显著且术后恢复快,国内外已有文献报道[4-5]。可在临床上却有部位患者椎体成形术后疼痛缓解不佳,据Liliang、Yan等报道[6-7]相当一 部分患者椎体成形术后疼痛缓解不明显,尤其是术后腰骶部疼痛,这种残余痛[8](residual back pain)极大的影响患者对治疗方案的满意程度。 本研究通过观察PKP术时加用小针刀疗法预防术后残余痛,并与单纯PKP手术治疗进行对照观察探讨此法临床应用价值,现报道如下。
资料与方法
1 入组标准
1.1 纳入标准 经实验室、体格、影像学等检查确诊符合该病诊断标准[9]。
1.2 排除标准 存在手术禁忌症;非骨质疏松原因导致的椎体压缩性骨折(如胸腰椎爆裂骨折、肿瘤导致的椎体压缩性骨折等);不能完成试验,中途退出者。
2 一般资料
选择安徽中医药大学第二附属医院2018年7月-2019年7月在骨科收治骨质疏松性椎体压缩骨折(OVCF)患者60例,所有入选病例均为单节段新鲜性椎体压缩性骨折,椎体CT平扫见椎体后缘完整,且均无脊髓和神经根受损症状。所选患者随机顺序法分入对照组、治疗组各30例。对照组中,男11例,女19例;年龄65~88岁,平均(74.84±6.18)岁;治疗组中,男 8 例,女 22 例;(χ2=0.693,P=0.045),年龄 65~86 岁,平均(76.00±4.95)岁(t=-0.800,P=0.427);2组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准。
3 治疗方法
3.1 对照组 患者俯卧位,采用经皮单侧椎弓根穿刺球囊扩张技术,配套器械为常州百隆医疗科技有限公司生产。C臂机正位透视下标记伤椎椎弓根外侧缘穿刺点,常规消毒铺巾,用1%利多卡因局部浸润麻醉至骨膜,尖刀片于穿刺点作长约1cm切口正位透视下确定穿刺针位于椎弓根投影“猫眼征”的外侧缘,一般选取左侧2点钟,右侧10点钟位置,C臂机侧位透视下穿刺针顺椎弓根方向并于矢状面约25°~30°方向骨锤徐徐敲击进针,透视下不断调整穿刺针方向,正位透视再次确认穿刺针未穿破椎弓根内侧缘,侧位透视穿刺针尖及工作通道到达椎体后缘约8~ 10mm,取出穿刺针芯,植入骨钻侧位透视下转入约2cm达到椎体前缘的1/3,且正位透视下超过椎体的中线,取出骨钻,置入可扩张球囊。透视下缓慢扩张球囊加压复位,当椎体复位满意,停止加压(扩张压力的最大值不超过300Psi),维持球囊加压复位约30s后,回抽造影剂拔出球囊。调配骨水泥即聚甲基丙烯酸甲脂(PMMA),连续透视低压下推杆缓慢注入拉丝期骨水泥,一旦见骨水泥渗漏或接近椎体后缘的趋势时应立即停止注射,一般每个椎体注入骨水泥3~5ml。待骨水泥凝固后拔出工作通道,伤口无菌敷料加压包扎。
3.2 治疗组 同对照组PKP术后,患者俯卧位,首先于伤椎附近寻找压痛点,如胸腰椎关节突关节、横突、棘突间隙、臀上皮神经卡压点等。标记后常规消毒铺巾,进针点皮下注射1% 利多卡因局部浸润麻醉,选择合适长度针刀,按针刀治疗规范垂直四步法快速刺入皮肤后逐层刺入,刀口线与该处肌纤维、神经、血管走行方向一致,以刀口下有沉紧感或清脆响来确定治疗深度,此时患者诉局部有酸胀痛,提示针刀已到达病理反应点,纵向剥离2~3刀,横向铲剥2~3刀,感觉手下有松动感取出小针刀;棉球压迫止血,进针点贴无菌敷料。
2组均术后24h腰围保护下床活动,适当腰背肌功能锻炼,均继续行抗骨质疏松治疗。
4 观察指标
2组在术前、术后3天、术后1月及术后3月分别记录其VSA评分、ODI评分及JOA量表评分。VSA评分越高,表示疼痛越剧烈,JOA评分越高,表示腰椎功能障碍程度越低。鉴于老年人性功能减退,删除ODI量表中关于性生活的评价,ODI评分越高,表示腰椎功能障碍越严重。
5 统计学方法
数据采用SPSS20.0统计软件处理,计量资料以均数±标准差()表示,同组术前术后比较采用配对t检验,2组间比较采用独立样本t检验;若资料不服从正态分布且方差不齐,则采用秩和检验,P<0.05判断为差异有统计学意义。
结 果
1 2组患者治疗结果比较
2组所有患者均完成手术,术中均无一例出现骨水泥渗漏,所有患者均术后24h腰围保护下床活动,术后均复查X线见骨水泥弥散满意。
2 2组患者治疗前后VAS评分比较
2组术后3天、术后1月及术后6月VAS评分分别与术前比较,差异具有统计学意义(P<0.05);治疗组术后3天、术后1月VAS评分分别与对照组比较,差异具有统计学意义(P<0.05);术后6月治疗组与对照组比较,差异无统计学意义(P>0.05)。见表1 。
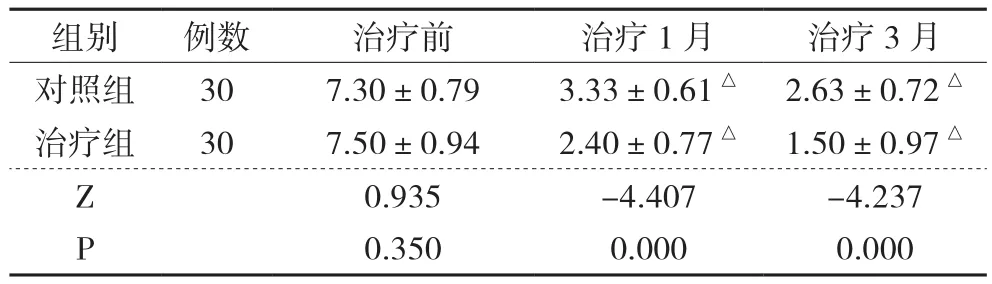
表1 2组患者治疗前后VAS评分比较
3 2组患者治疗前后JOA评分比较
2组术后3天、术后1月及术后6月JOA评分分别与术前比较,差异具有统计学意义(P<0.05);治疗组术后3天、术后1月JOA评分分别与对照组比较,差异具有统计学意义(P<0.05);术后6月,治疗组与对照组比较差异无统计学意义(P>0.05)。见表2。
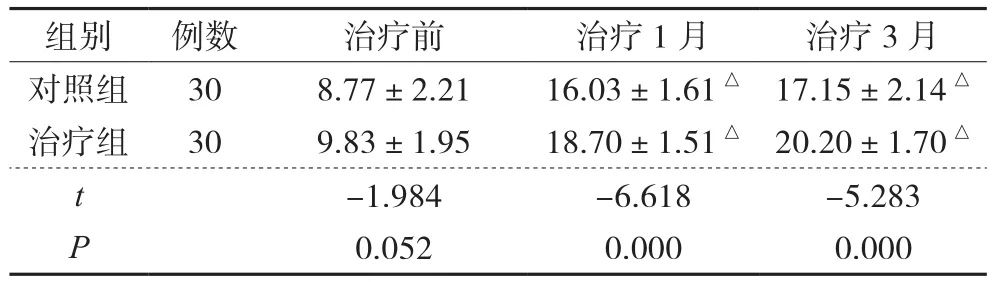
表2 2组患者治疗前后JOA评分比较
4 2组患者治疗前后ODI评分比较
2组术后3天、术后1月及术后6月ODI评分分别与术前比较,差异具有统计学意义(P<0.05);治疗组术后3天、术后1月ODI评分分别与对照组比较,差异具有统计学意义(P<0.05);术后6月,治疗组与对照组比较差异无统计学意义(P>0.05)。见表3。
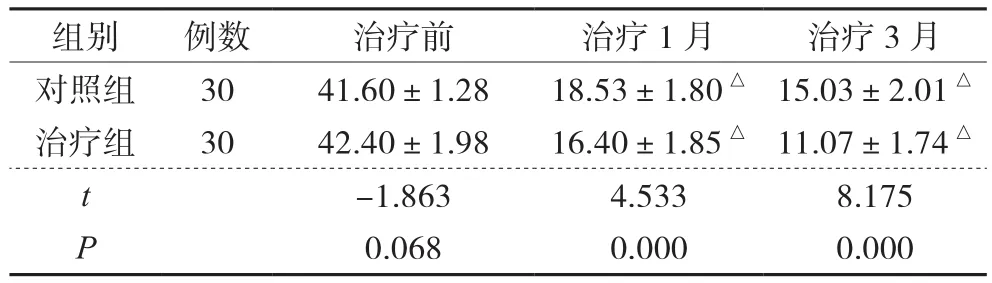
表3 2组患者治疗前后ODI评分比较
讨 论
骨质疏松症发病年龄高是一种全身性疾病,针刀医学认为[10],骨质疏松的同时也导致了脊柱椎体关节突关节囊、韧带、肌肉、周围的筋膜等软组织存在不同程度的退变,当发生OVCF时必然导致椎体周围筋膜、韧带、肌肉等软组织损伤,引起软组织充血、水肿,释放炎症物质,导致局部软组织的粘连、挛缩、瘢痕,正常的机体能自我代偿,但是由于该处软组织退变严重,常会超过了人体自身代偿能力,导致局部软组织动态平衡失调,使局部组织内张力增高,刺激周围神经,引起疼痛。且痛点通常位于应力较高的关节突、横突、棘突的肌肉止点以及肌肉与筋膜交汇处。 早期软组织的疼痛容易被椎体骨折所致疼痛掩盖,在PKP术后才能表现出来。术后术椎的强度增加,导致与邻椎的刚性梯度发生变化,必然会导致椎体周围生物力学的改变,导致动态平衡的失调,造成术后的疼痛。而对于椎体成形术的止痛机理尚未十分明确,目前公认的是观点:①骨水泥凝固后可以锚定骨质疏松椎体的微骨折,大大减少了骨折的微动,减少对椎体内痛觉末梢神经的刺激[11]。②PKP术能恢复骨折椎体高度,减轻了脊神经后支的牵拉作用,从而缓解了腰背部的疼痛[12]。③骨水泥即聚甲基丙烯酸甲脂(PMMA)的毒性及聚合反应时发热反应,可降低椎体内部和椎体周围的痛觉神经末梢的敏感性,从而达到缓解疼痛的目的[13]。有研究认为[15-16]PKP术仅解决椎体骨折导致的疼痛,并没有解决病椎周围筋膜、韧带、肌肉等软组织损伤所引起的疼痛。
小针刀治疗根据慢性软组织损伤、骨质增生以及闭合性手术理论,通过调节术后软组织损伤,重建动态平衡出发,通过对软组织损伤形成的粘连、挛缩和疤痕进行切割、松解,解除卡压,消除异常应力,恢复脊柱关节软组织的力学平衡;针刀直接作用于痛点,可以切断敏感神经末梢的伤害性传导,提高疼痛阈值,同时能改善局部软组织的血液循环,加速水肿消除及炎性致痛物质的吸收从而达到止痛的目的[17-20]。
小针刀疗法联合经皮椎体后凸成形术(PKP术)治疗骨质疏松性椎体压缩骨折可很好预防术后残余痛的发生,巩固临床疗效,大大提高患者满意度,充分发挥了祖国医学“简、便、廉、验”的优势,值得临床推广应用。

