离子键形成过程实验的改进
王春阳 王蓝蓝 王后雄

摘要:分析钠单质和氯气反应演示实验的不足和研究现状,设计利用石英坩埚进行钠单质和碘单质反应的新实验装置,可以持续动态观察反应现象。经过多次探索和改进,该实验具有试剂用量小、操作简便化、密封可控、环保安全、易推广等优点,适合课堂演示实验和学生分组实验。
关键词:离子键形成过程;实验装置设计;实验探究;石英坩埚;钠单质和碘单质
文章编号:1005-6629(2021)04-0064-02 中图分类号:G633.8 文献标识码:B
1问题的提出
1.1教材实验分析
人教版必修2第一章第3节“化学键”中,离子键形成过程的演示实验是钠单质和氯气反应,以此说明氯原子失去一个电子给钠原子,形成相互吸引的阴阳离子,即离子键形成过程。但在实际教学中,制备氯气装置复杂、耗时较长,且氯气容易逸散,对于通风条件较差,特别是某些农村高中的教室里做演示实验,显然会造成环境污染,更别说学生分组实验或探究实验对环境造成的影响;实验过程中,实验操作比较麻烦,特别是集气瓶倒置于加热的石棉网上时,集气瓶倒置过程和玻璃片移出过程都会有氯气的逸出;尾气处理也很难控制,实验结束后,在集气瓶移出过程中会导致未反应的氯气大部分逸出。多数教师鉴于制备麻烦、易造成污染,干脆以视频代替演示实验,显然不能给学生形成深刻印象和引發深度思考,大大影响学生学习的积极性。所以寻找更易操作、取材方便、污染较小、现象明显的替代实验就势在必行。
1.2研究现状及分析
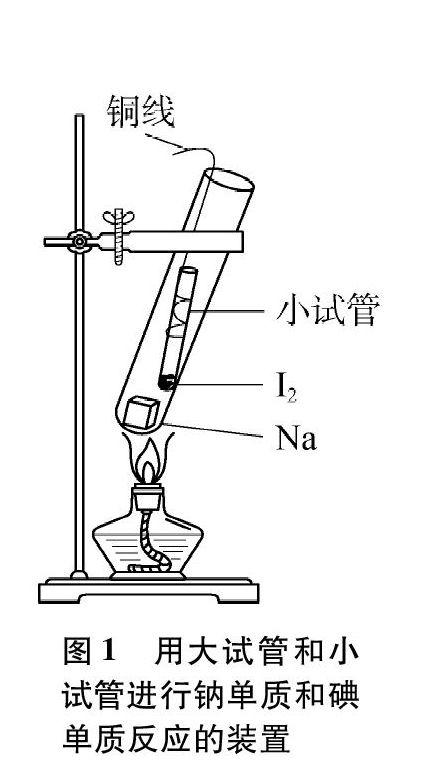
近年来,一线教师不断对该实验进行改进和优化,取得了一定的成效,如有教师把钠单质粉碎为非常细小的颗粒直接和氯气反应,无需加热,可观察到钠单质在氯气中剧烈燃烧,现象比较明显,但这也无法排除氯气的制备麻烦和漏气污染等弊端。也有教师改用钠单质和碘单质反应,如图1所示。此实验利用碘单质易升华、熔沸点较低等性质,与钠单质反应现象明显,排除了氯气泄漏的弊端,但按照作者的实验及说明进行实验,发现大试管中加入钠单质直接加热很容易被炸裂。实验刚开始时,钠单质容易和空气中氧气反应,有黄色固体生成,大约1分钟左右碘单质才升华,紫色的碘蒸气从小试管中移出并下沉与钠单质反应,试管上部内壁有大量碘单质凝华,造成浪费;大试管口上盖的小烧杯(为防止碘蒸气逸出大试管)也有碘凝华造成浪费。因此该实验钠单质和碘单质用量都比较大,且只有大试管底部可以观察到稍许现象,甚至需要关掉实验室或教室里的灯才可以看到有明显的现象。上述实验虽然有不少缺陷,但其设计思路和发散性思维,为后续的设计和研究提供了学习资源和借鉴。
1.3装置的改进
针对教材实验和有关文献实验的不足,确定本次实验创新的主要原则是:装置需要密封、药品用量少、操作方便、现象明显、对环境无污染、反应时间更短、便于学生观察,适合于课堂演示和学生分组实验。
经过多次实验,选用20 mL石英坩埚,采用直接加热方式,可观察到钠单质和碘蒸气的动态反应过程,由紫色蒸气逐渐变为白色的烟,现象明显,效果极好。
2实验过程和机理分析
2.1实验过程及现象
在20 mL石英坩埚中加入2粒绿豆大小的金属钠单质和1粒绿豆大小的碘单质,盖上盖子,用酒精灯加热,观察现象。
碘单质迅速充满整个石英坩埚,石英坩埚底部先出现白烟,然后白烟由底部向上升,最后出现在盖子上,紫色物质逐渐变为白色物质,当盖子上紫色物质全部变为白色物质时,停止加热,整个过程持续大约1.5min,是动态的变化过程。
2.2反应过程和机理分析
查资料可知,碘单质易升华,熔点113.5℃,沸点184.35℃。实验时,碘单质来不及熔化就迅速升华为气体并充满整个石英坩埚,呈现紫色。钠单质熔点为97.72℃,沸点为883℃,刚开始熔化的钠单质的表面与碘蒸气反应,随着温度的升高,钠单质开始变为钠蒸气,与坩埚中的碘蒸气发生反应生成白色的碘化钠,然后钠蒸气继续上升,与石英坩埚上面紫色的碘单质继续发生反应,直至石英坩埚的紫色碘蒸气全部变为白色的碘化钠。实验现象非常明显。观察发现,整个实验过程没有碘蒸气逸出,也没有白色固体移出,因为盖子周边环境温度较低,碘单质、碘化钠乃至钠蒸气不可能以气体的形式逸出到空气中污染空气。为了确保坩埚和盖子接触严密,可以在坩埚和盖子接触处涂抹少量凡士林。
计算表明,该反应在室温下熵变比较小,焓变比较大,因此不是熵驱动,主要是由焓变驱动,在室温下,反应从热力学角度分析能自发进行。从实验结果看,该反应室温下反应非常慢,需要加热至高温以达到缩短反应时间、现象明显、高温产生钠蒸气与碘充分反应的目的,满足课堂演示实验和学生分组实验的需求。
3实验优点和后续处理
自主设计使用石英坩埚作装置,利用碘单质的独特性质(易升华),避免使用氯气、制备过程复杂、装置移动不便等弊端。利用钠单质熔沸点低,加热易使钠单质熔化和生成钠蒸气,使整个实验现象非常明显,且有生成白色固体的动态过程,便于学生进行观察和思考。改进后的实验既可以方便教师演示实验,又可以让学生进行分组实验,钠单质和碘单质取材都比较方便,20mL的石英坩埚,网上购买非常方便,价格也很便宜。
停止实验后,可以打开石英坩埚盖子,让学生观察碘化钠在空气中的变化过程:碘化钠迅速由白色变为无色,进而潮解变成粘稠状,说明碘化钠具有易潮解的性质。待碘化钠完全潮解后,在石英坩埚中加入10 mL无水乙醇,以除去未反应的钠单质。

